- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Вода з точки зору хімії презентация
Содержание
- 1. Вода з точки зору хімії
- 2. У молекулі води є
- 3. Між молекулами води існують водневі
- 4. Розглянемо на малюнку утворення зв'язків в молекулі
- 5. Вода одночасно і проста, і
- 6. Молекули води з’єднані між собою
- 7. Вода — єдина речовина
- 8. При переході від рідкого
- 9. Жесткость воды Общая Некарбонатная (постоянная) Карбонатная (временная)
- 10. Оксиди Основні Амфотерні Кислотні Тверді речовини Частіше
- 13. Дякуємо за увагу
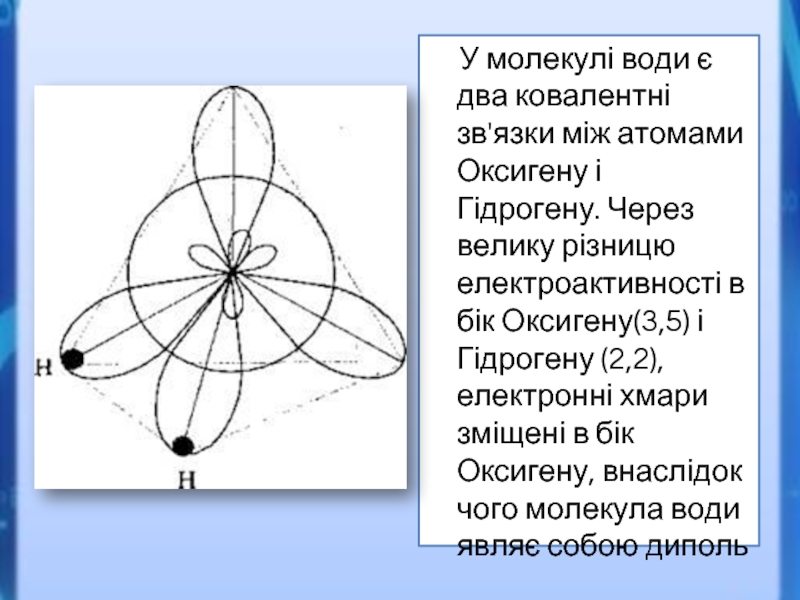
Слайд 2 У молекулі води є два ковалентні зв'язки між
атомами Оксигену і Гідрогену. Через велику різницю електроактивності в бік Оксигену(3,5) і Гідрогену (2,2), електронні хмари зміщені в бік Оксигену, внаслідок чого молекула води являє собою диполь
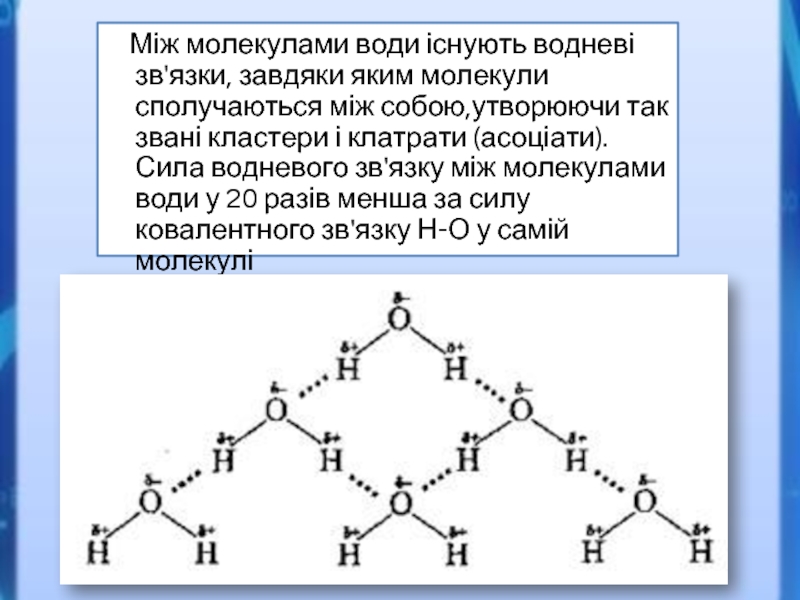
Слайд 3 Між молекулами води існують водневі зв'язки, завдяки яким молекули
сполучаються між собою,утворюючи так звані кластери і клатрати (асоціати). Сила водневого зв'язку між молекулами води у 20 разів менша за силу ковалентного зв'язку Н-О у самій молекулі
Слайд 4Розглянемо на малюнку утворення зв'язків в молекулі води між атомами Гідрогену
та Оксигеном, елементами неметалами. Спільна електронна пара зміщена до більш електронегативного елементу Оксигену, тому тип ковалентного зв'язку – ковалентний полярний. Але дана схема не передає просторове розміщення атомів. Молекула води має кутову будову і кут зв'язку між атомами 104,5 градусів
Слайд 5 Вода одночасно і проста, і складна речовина. Її молекула
складається з трьох атомів — двох атомів водню та одного атому кисню. Водночас, вода має такі особливості будови, які зумовлюють ряд її незвичайних, майже магічних властивостей
Слайд 6 Молекули води з’єднані між собою водневими зв’язками. Ці слабкі
зв’язки між позитивно зарядженими атомами водню та від’ємним зарядом атомів кисню іншої молекули визначають фізичні, а також деякі хімічні властивості води.
Слайд 7 Вода — єдина речовина на Землі, яка зустрічається
у трьох агрегатних станах: твердому, рідкому та газоподібному. За нормальних умов, температура замерзання чистої води дорівнює 0 градусів Цельсія, а кипіння - відповідно 100 градусів Цельсія, що покладено в основу температурної шкали Цельсія. В залежності від атмосферного тиску, наприклад, на висоті, де тиск нижчий, температура кипіння води теж знижується. Розчинення різних речовин у воді знижує її температуру замерзання
Слайд 8 При переході від рідкого до твердого стану густина
і вага майже всіх речовин збільшується. На відміну від них, вода збільшує свій об’єм і стає легшою при замерзанні. Ця властивість має велике значення для збереження життя у водних об’єктах узимку. Лід утворюється на поверхні водойми і захищає її від повного промерзання. Падаюча крапля дощу розчиняє різні гази
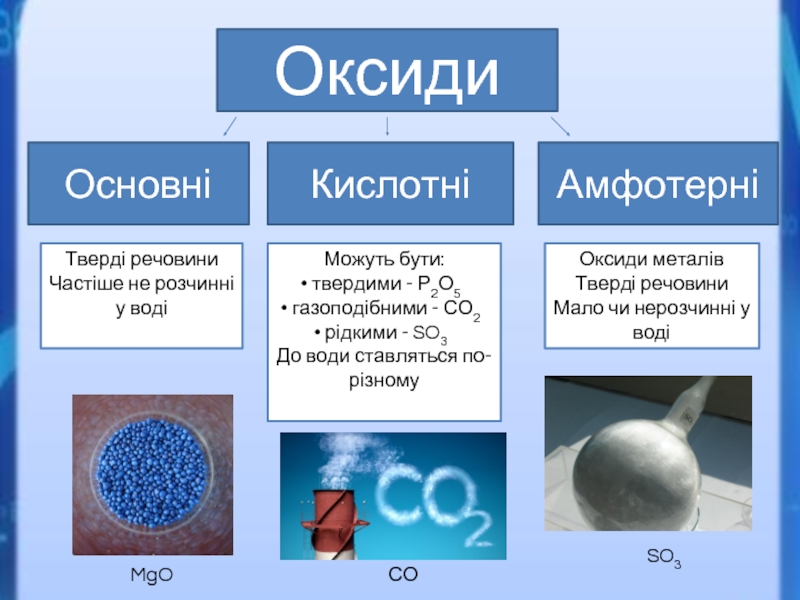
Слайд 10Оксиди
Основні
Амфотерні
Кислотні
Тверді речовини
Частіше не розчинні у воді
Можуть бути:
твердими - Р2О5
газоподібними
- СО2
рідкими - SO3
До води ставляться по-різному
рідкими - SO3
До води ставляться по-різному
Оксиди металів
Тверді речовини
Мало чи нерозчинні у воді
MgO
СО2
SO3