- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Валентность и степень окисления презентация
Содержание
- 1. Валентность и степень окисления
- 3. Из атомов мир создавала Природа.
- 4. Н2О Почему такой состав имеет молекула воды?
- 5. Задачи урока: 1. выяснить, от чего зависит
- 6. Степень окисления Степень окисления (с.о.)- это условный
- 7. Правила определения степеней окисления У свободных
- 8. Определение степени окисления элементов в соединениях +3
- 9. Определите валентность элементов по структурной формуле.
- 10. Сравнение понятий валентность и степень окисления
- 11. Как правило, в записи степени окисления знаки
Слайд 3
Из атомов мир создавала Природа.
Два атома лёгких взяла водорода.
Прибавила атом
один кислорода.
И получилась частица …
И получилась частица …
Слайд 5Задачи урока:
1. выяснить, от чего зависит состав сложных веществ;
2.что необходимо знать,
чтобы составить формулы веществ.
Слайд 6Степень окисления
Степень окисления (с.о.)- это условный заряд, который мог бы возникнуть
на атоме при условии, что все общие электронные пары смещены к более электроотрицательному элементу.
Слайд 7Правила определения степеней окисления
У свободных атомов и у простых веществ
СТЕПЕНЬ ОКИСЛЕНИЯ равна 0
Металлы во всех соединениях имеют ПОЛОЖИТЕЛЬНУЮ С.О.
В соединениях кислород имеет С.О.-2
(кроме Н2О2 , К2О2, ОF2 )
В соединениях с неметаллами у водорода С.О.+1, а с металлами -1
В соединениях сумма всех С.О. равна 0
Металлы во всех соединениях имеют ПОЛОЖИТЕЛЬНУЮ С.О.
В соединениях кислород имеет С.О.-2
(кроме Н2О2 , К2О2, ОF2 )
В соединениях с неметаллами у водорода С.О.+1, а с металлами -1
В соединениях сумма всех С.О. равна 0
Слайд 8Определение степени окисления элементов в соединениях
+3 х
АlСl 3
(+3)*1 + х *3 = 0;
+3 = - 3х
Х = -1
+3 -1
АlСl 3
(+3)*1 + х *3 = 0;
+3 = - 3х
Х = -1
+3 -1
АlСl 3
Слайд 9
Определите валентность элементов по структурной формуле.
Внесите значение валентности элементов в таблицу.
Валентность Степень окисления
Н
О
Са
Аl
С
Н
О
Са
Аl
С
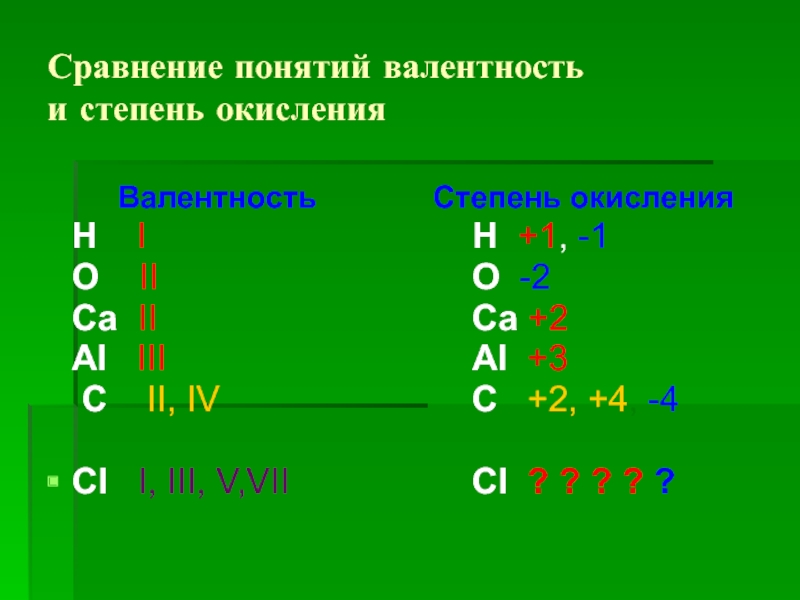
Слайд 10Сравнение понятий валентность
и степень окисления
Валентность
Н I
О II
Са II
Аl III
С II, IV
CI I, III, V,VII
Степень окисления
Н +1, -1
О -2
Са +2
Аl +3
С +2, +4, -4
CI ? ? ? ? ?
Слайд 11Как правило, в записи степени окисления знаки «+» и «-» ставятся
перед цифрой, указывающей величину заряда. Например, Ca+2O-2, Al+3I-13.
Ионы – положительно или отрицательно заряженные частицы. Заряд иона в отличие от степени окисления существует, например, в растворах. Если в воде растворить всем нам известную соль — хлорид натрия, то в результате произойдет его диссоциация, с образованием ионов Na+ и Cl-. Единичный заряд иона обозначается только знаками «+» или «-», а при записи многозарядного иона цифры стоят перед знаками (в отличие от степени окисления). Например, Ba2+S2-. Кроме этого, ионы могут состоять из группы атомов, например, NO3-, CH3COO-.
Примеры: степени окисления атомов в серной кислоте H2+1S+6O4-2, а заряды ионов H2+SO42-; степени окисления атомов в карбонате кальция Ca+2C+4O3-2, а заряды ионов Ca2+CO32-.
Ионы – положительно или отрицательно заряженные частицы. Заряд иона в отличие от степени окисления существует, например, в растворах. Если в воде растворить всем нам известную соль — хлорид натрия, то в результате произойдет его диссоциация, с образованием ионов Na+ и Cl-. Единичный заряд иона обозначается только знаками «+» или «-», а при записи многозарядного иона цифры стоят перед знаками (в отличие от степени окисления). Например, Ba2+S2-. Кроме этого, ионы могут состоять из группы атомов, например, NO3-, CH3COO-.
Примеры: степени окисления атомов в серной кислоте H2+1S+6O4-2, а заряды ионов H2+SO42-; степени окисления атомов в карбонате кальция Ca+2C+4O3-2, а заряды ионов Ca2+CO32-.