- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Углеводы. Моно- и дисахариды. Хроматографические методы исследования презентация
Содержание
- 1. Углеводы. Моно- и дисахариды. Хроматографические методы исследования
- 2. Углево́ды — органические вещества, содержащие карбонильную группу
- 3. - альдозы - кетозы
- 4. Стереоизомерия УВ Первый член
- 5. В
- 6. Реакции, протекающие в живом организме приводят к
- 8. Абсолютная конфигурация — это истинное расположение в
- 9. Определить пространственное расположение атомов в молекуле относительно
- 10. Если абсолютную конфигурацию молекулы узнать трудно,
- 12. Для изображения строения мнсх. используют проекционные формулы
- 14. N = 23 = 8 УВ такого
- 15. Рибоза входит в состав РНК .Может быть
- 17. Дезоксирибоза входит в состав ДНК . Получают
- 19. 2) Гексозы - C6H12O6 8 пар энантиомеров
- 20. N = 24 = 16, 8
- 22. Используют глюкозу в пищевой промышленности,
- 23. D (-) фру
- 24. Фруктоза Фруктоза фруктовый или плодовый, сахар, левулёза,
- 25. Н Н -δ +δ п/а Схема образования циклических форм.
- 26. α – D глюкопираноза β– D глюкопираноза
- 27. Фураноза (от фурана) Пираноза (от пирана)
- 28. α-D-глюкопираноза α-D-фруктофураноза Более наглядными
- 30. Таутомерия. Мутаротация Сосуществование в динамическом равновесии
- 31. C C H 2 - O
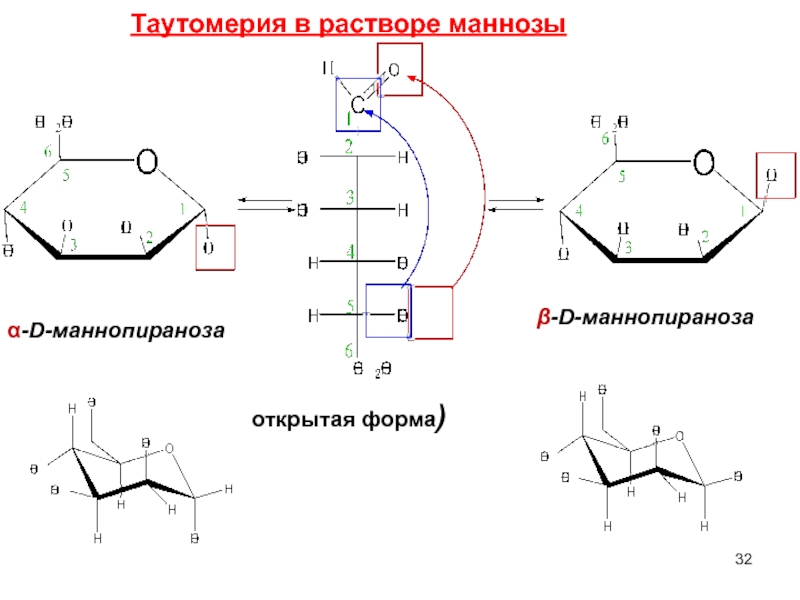
- 32. α-D-маннопираноза β-D-маннопираноза открытая форма) Таутомерия в растворе маннозы
- 33. Манноза Манноза – компонент многих полисахаридов
- 34. Превращения маннозы в организме происходят с
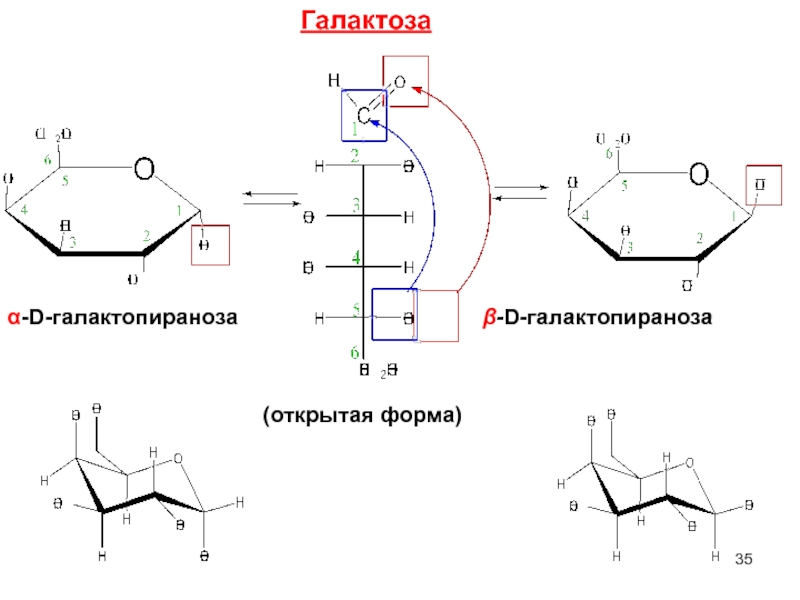
- 35. α-D-галактопираноза β-D-галактопираноза (открытая форма) Галактоза
- 36. Галактоза Встречается в природе в свободном виде,
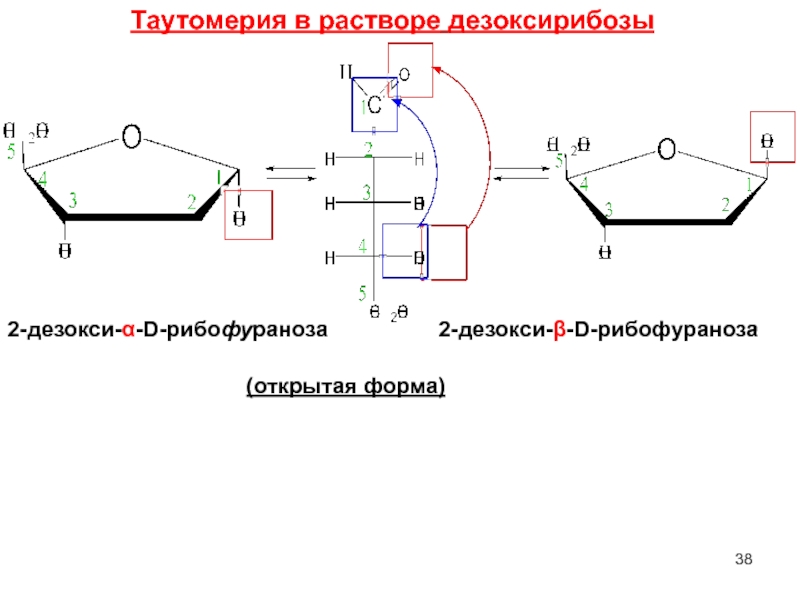
- 38. 2-дезокси-α-D-рибофураноза 2-дезокси-β-D-рибофураноза (открытая форма) Таутомерия в растворе дезоксирибозы
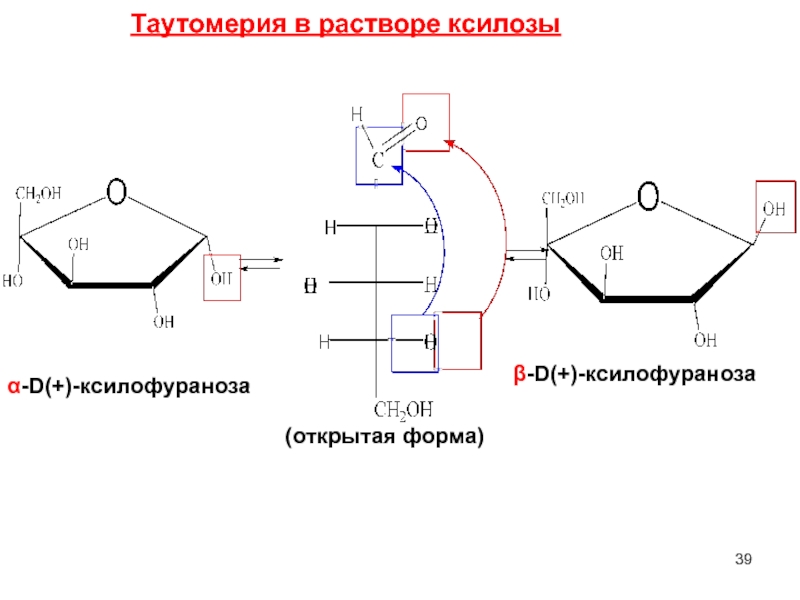
- 39. α-D(+)-ксилофураноза β-D(+)-ксилофураноза (открытая форма) Таутомерия в растворе ксилозы
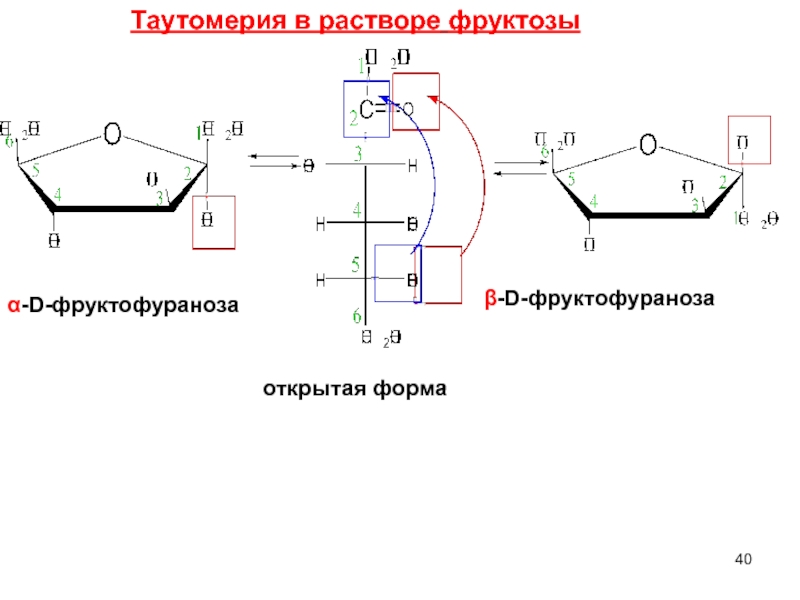
- 40. β-D-фруктофураноза α-D-фруктофураноза открытая форма Таутомерия в растворе фруктозы
- 41. Эпимеры –диастереомеры,отличающиеся конфигурацией только одного асимметрического атома
- 42. C C H 2 - O
- 43. Эпимеризация углеводов связана с изменением конфигурации первого
- 44. Химические свойства УВ Общие реакции для
- 45. высокая реакционная способность D -глюкопираноза
- 46. Особенности гликозидов Легко гидролизуются
- 47. В природе наиболее распространены O-
- 48. амигдалин амигдалин в косточках горького миндаля,
- 49. Витамины К, Р – это О -
- 50. N-гликозиды Тимидин (только в составе ДНК) цитидин
- 51. нуклеозиды: аденозин гуанозин N-гликозиды -
- 52. + 5CH3I + 5KOH -5KI -5H2O
- 53. + H2O, H+ + CH3OH 2,3,4,6-тетраметилглюкопираноза (метилированная
- 54. D гал + 5 (CH3CO)2O H+ CH3CO
- 55. + H2O, H+ 5NaOH 5 CH3COOH 5
- 56. Большое значение имеют эфиры H3PO4 –
- 57. Фосфаты моносахаридов (эфиры неорганических кислот) 6-фосфат α-D-глюкопиранозы 1-фосфат α-D-глюкопиранозы 1,6-дифосфат α-D-фруктофуранозы
- 58. + АДФ + АДФ α-
- 59. Этот процесс происходит на первойстадии гликолиза, а
- 60. 1 2 3 4 А этот дифосфат
- 61. Фруктоза-1,6-дифосфат, фруктозо-6-фосфат промежуточные соединения в темновой
- 62. + NH3 D гал 2-D-галактозамин (производные 2-галактозамина
- 63. D-глюкозамин (2-амино-2-дезокси- -D-глюкопираноза) N-ацетил--D-глюкозамин Аминосахара
- 64. Ацилирование аминосахаров Ацилирование происходит, как правило, ацетильным
- 65. Аминосахара входят в состав: хитина, который
- 66. β(1→3) D-глюкуроновая кислота N-ацетил-D-галактозамин Аминосахара входят в
- 67. … … β(1→3) Аминосахара входят в состав:
- 68. D-ксилоза + Н2
- 69. Окисление моносахаридов Реакции окисления используют в структурных
- 70. A g ( N H 3 )
- 71. Окисление в щелочной среде (качественная реакция на
- 72. Кирпично-красный осадок Продукты реакции Окисление в
- 73. б) окисление в кислых средах Окисление может
- 74. В форме глюкуронидов из организма с мочой
- 75. + HCN OH HO D-фруктоза OH
- 76. 7.Качественные реакции на
- 77. на ОН- спиртовой: действие
- 78. C C H 2 - O H
- 79. Дисахариды
- 80. Сложные углеводы (подвергающиеся гидролизу). (полисахариды) олигосахариды
- 81. Дисахариды. Это олигосахариды, состоящие их двух моносахаридов.
- 82. Дисахариды могут быть образованы двумя типами связей:
- 83. in vitro (H+) in vivo
- 84. α - D- глюкопираноза β - D-
- 85. В названии невосстанавливающих дисахаридов отражено отсутствие полуацетальных
- 87. Присутствуют свойства: 1. Гидролиз сахарозы – (инверсия)
- 88. При гидролизе сахарозы в кислой среде образуются
- 89. Поэтому процесс гидролиза иногда называется инверсией, а
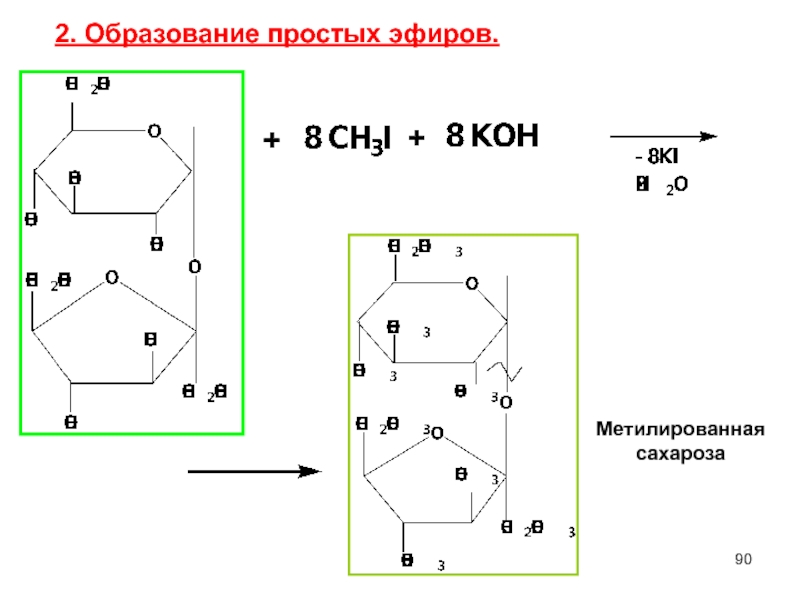
- 90. + Метилированная сахароза 2. Образование простых эфиров. +
- 91. образуются метилированные исходные моносахариды б). При щелочном
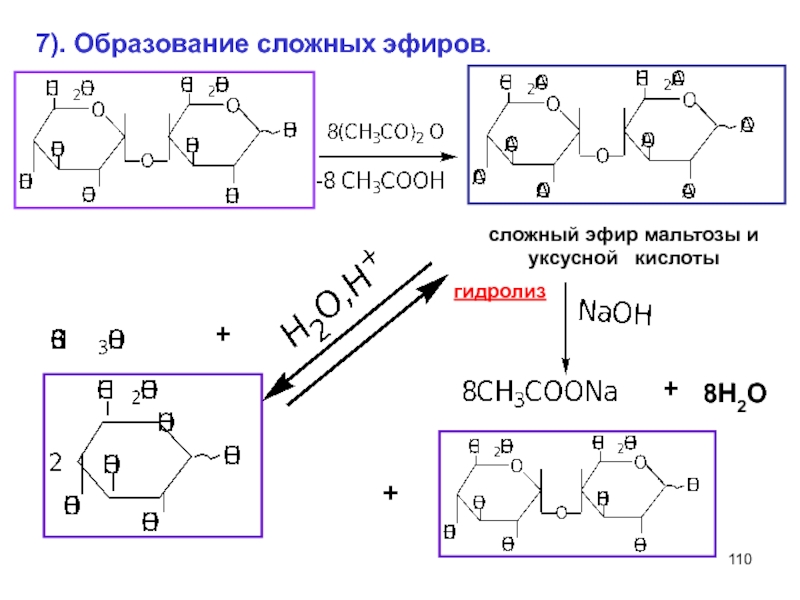
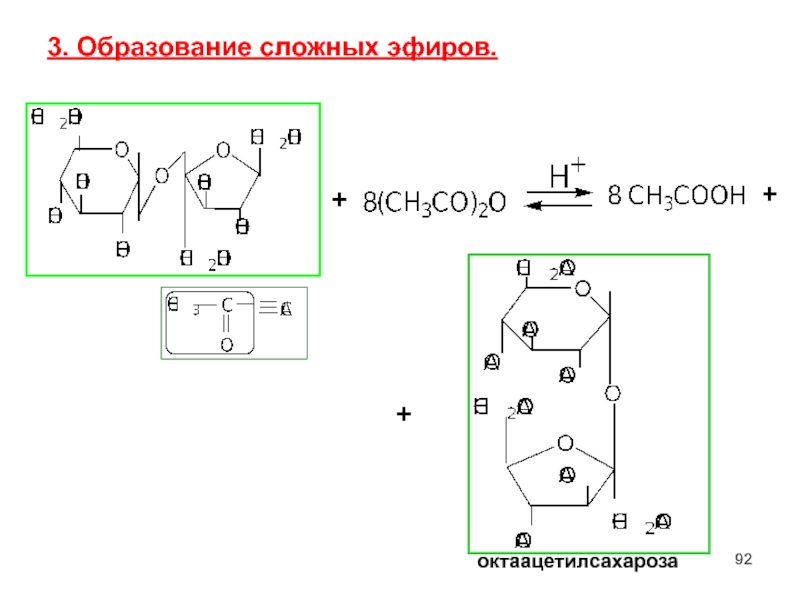
- 92. 3. Образование сложных эфиров. + + + октaацетилсахароза
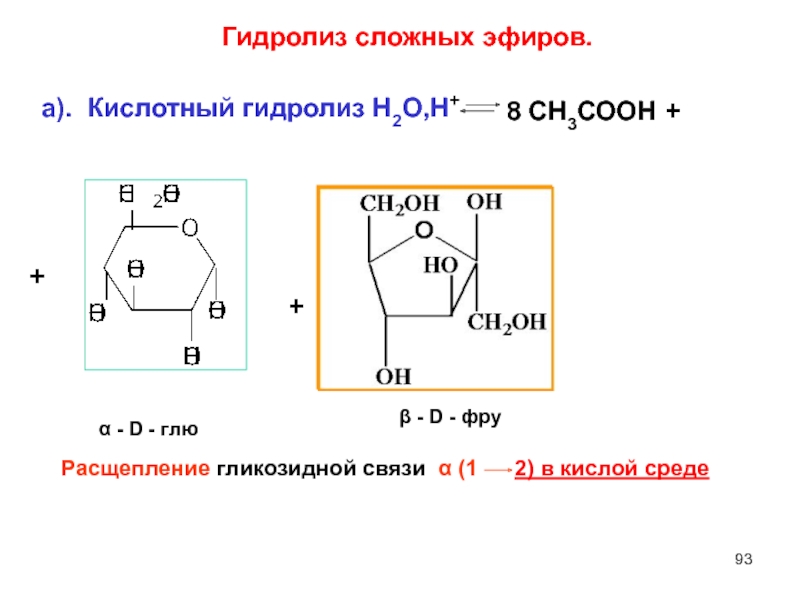
- 93. Гидролиз сложных эфиров. а). Кислотный гидролиз Н2О,Н+
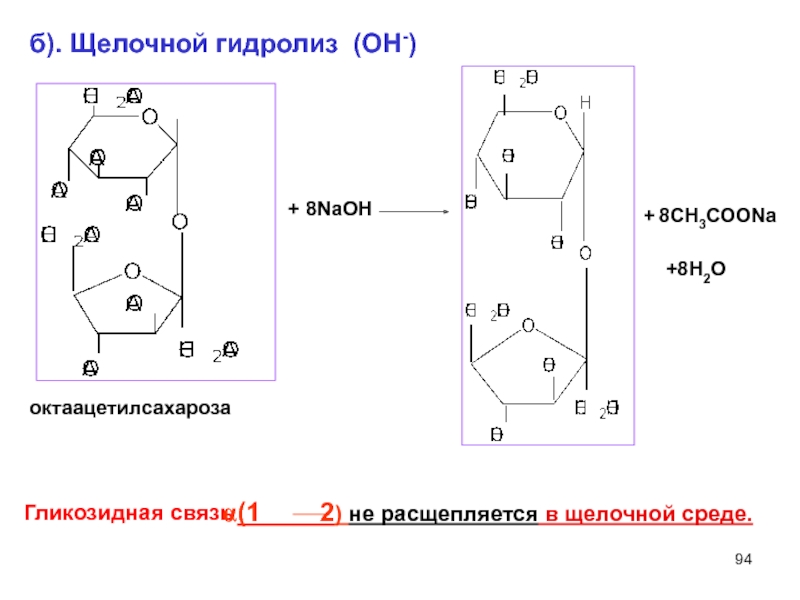
- 94. б). Щелочной гидролиз (ОН-) Гликозидная связь
- 95. [O] 4. Жесткое окисление сахароза трикарбоновая кислота – 3 СООН
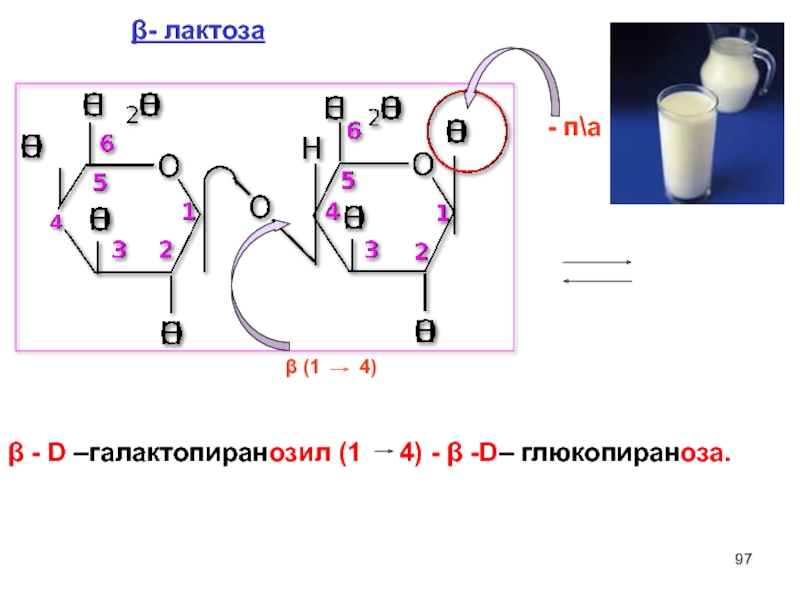
- 97. β - D –галaктопиранозил (1
- 98. β - лактоза содержится в материнском молоке,
- 99. Лактоза содержит полуацетальный гидроксил, а значит, имеет
- 100. Мальтоза – (солодовой сахар). Основной продукт расщепления
- 101. Мальтоза – структурная единица, биозный фрагмент крахмала
- 102. Целлобиоза β (1 4) гликозидная связь
- 103. 1). Мутаротация: есть свободный ОН – полуацетальный,
- 104. 2) Окисление >C = O ,
- 105. [O] Жесткое окисление Свободная группа с защитой полуцетального гидроксила
- 106. 3). Восстановление Качественная реакция восстанавливающих дисахаридов –
- 107. 4). Присоединение: (AN) HCN гидроксинитрил мальтозы α
- 108. 5). Образование гликозидов. а ) O-
- 109. 6). Образование простых эфиров метиловый эфир α(β)
- 110. 7). Образование сложных эфиров. сложный эфир мальтозы
- 111. Выделенное и очищенное соединение идентифицируют путем сравнения
- 112. Физико-химические и химические методы исследования и идентификации
- 113. Распределительная хроматография была впервые применена для разделения
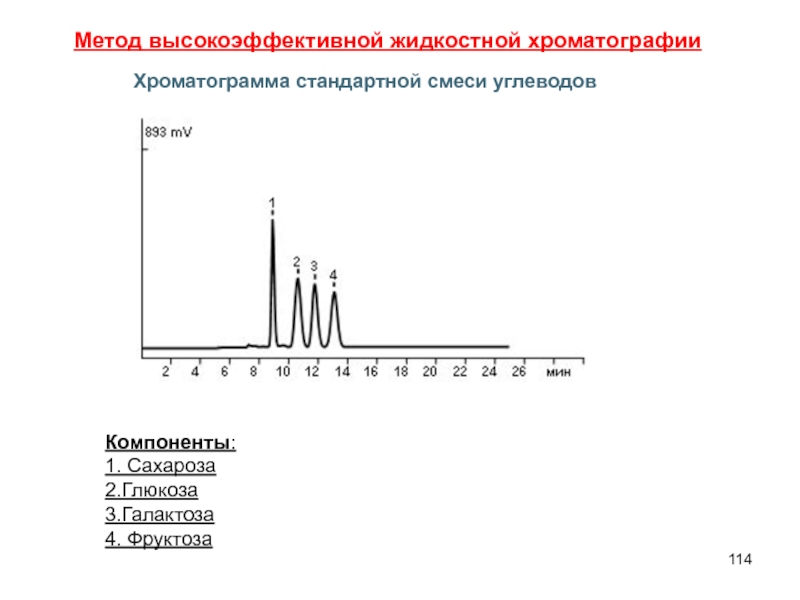
- 114. Компоненты: 1. Сахароза 2.Глюкоза 3.Галактоза 4. Фруктоза Метод высокоэффективной жидкостной хроматографии
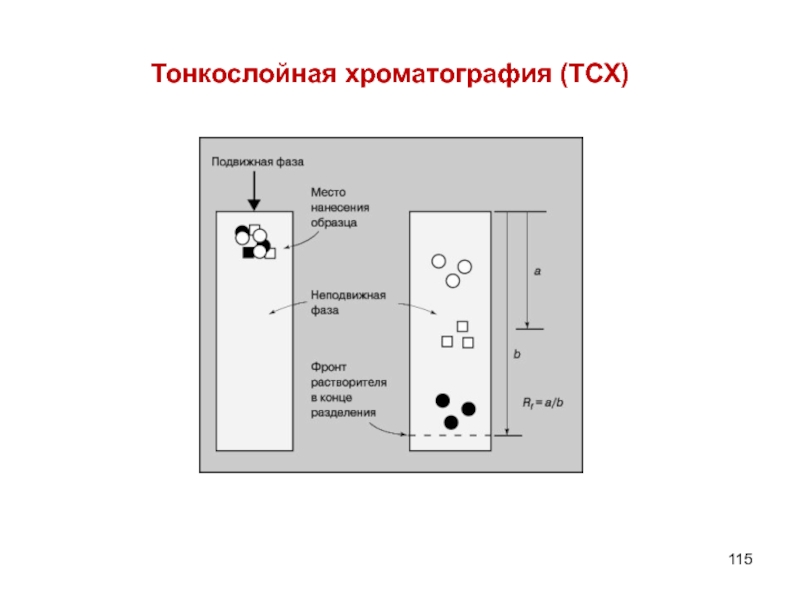
- 115. Тонкослойная хроматография (ТСХ)
- 118. Хроматографические методы исследования Тонкослойная хроматография находит все
- 119. Спасибо за внимание!
Слайд 1Кафедра общей и медицинской химии
Углеводы. Моно- и дисахариды
Хроматографические методы исследования.
Лекция
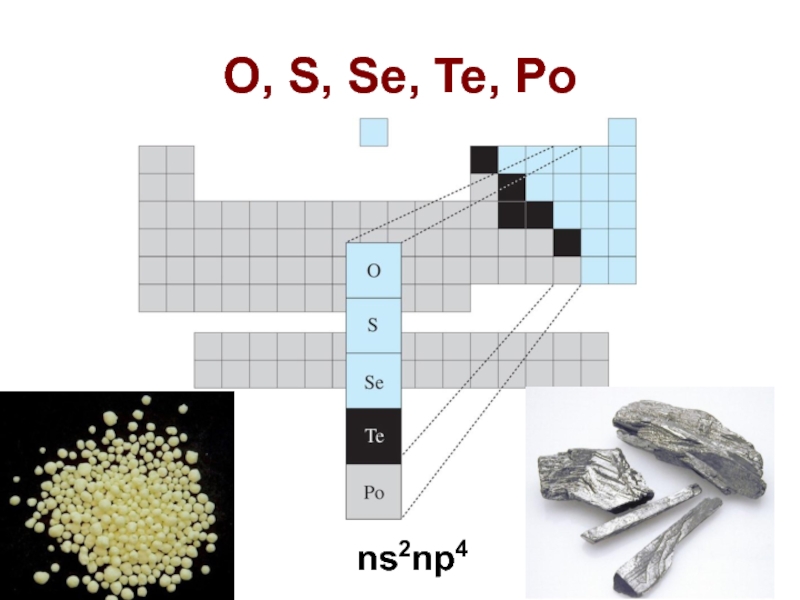
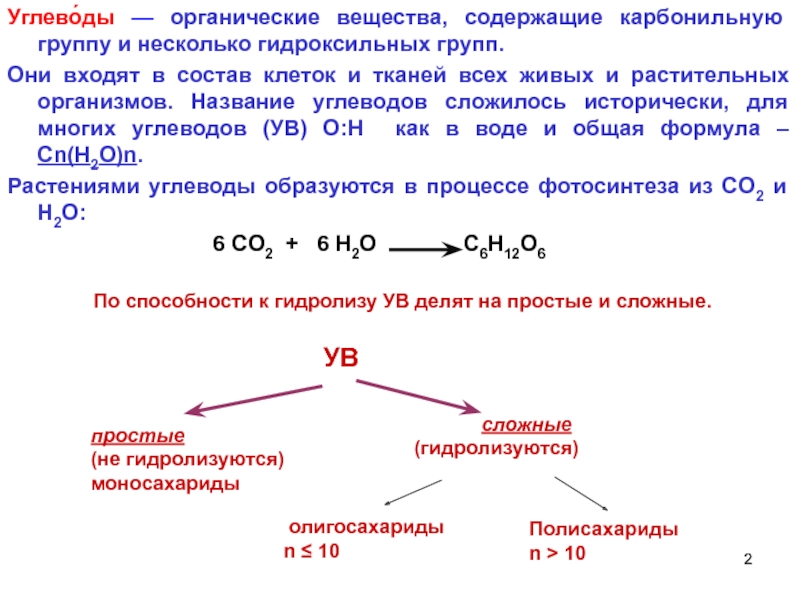
Слайд 2Углево́ды — органические вещества, содержащие карбонильную группу и несколько гидроксильных групп.
Они входят в состав клеток и тканей всех живых и растительных организмов. Название углеводов сложилось исторически, для многих углеводов (УВ) О:H как в воде и общая формула – Сn(H2O)n.
Растениями углеводы образуются в процессе фотосинтеза из CO2 и Н2О:
6 CO2 + 6 Н2О C6H12O6
По способности к гидролизу УВ делят на простые и сложные.
сложные
(гидролизуются)
УВ
простые
(не гидролизуются)
моносахариды
олигосахариды
n ≤ 10
Полисахариды
n > 10
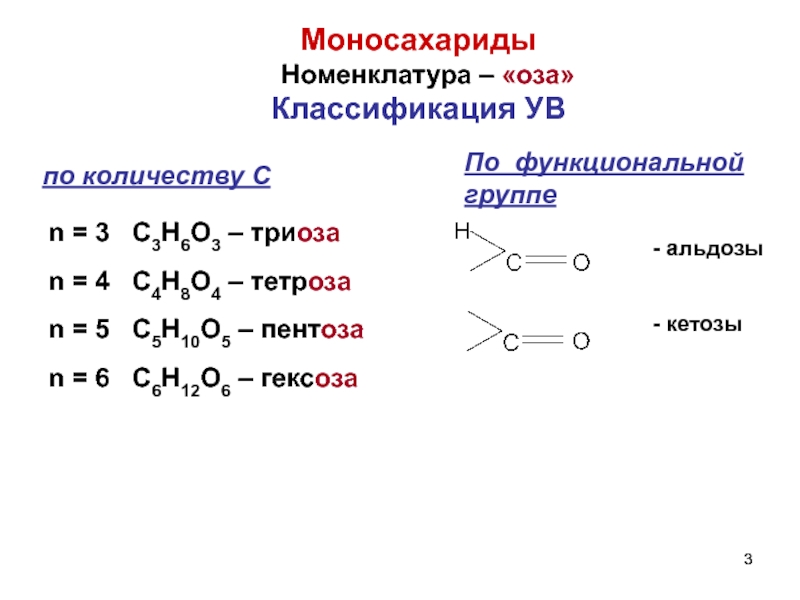
Слайд 3 - альдозы
- кетозы
n = 3
n = 4 C4H8O4 – тетроза
n = 5 C5H10O5 – пентоза
n = 6 C6H12O6 – гексоза
Моносахариды
Номенклатура – «оза»
Классификация УВ
по количеству С
По функциональной группе
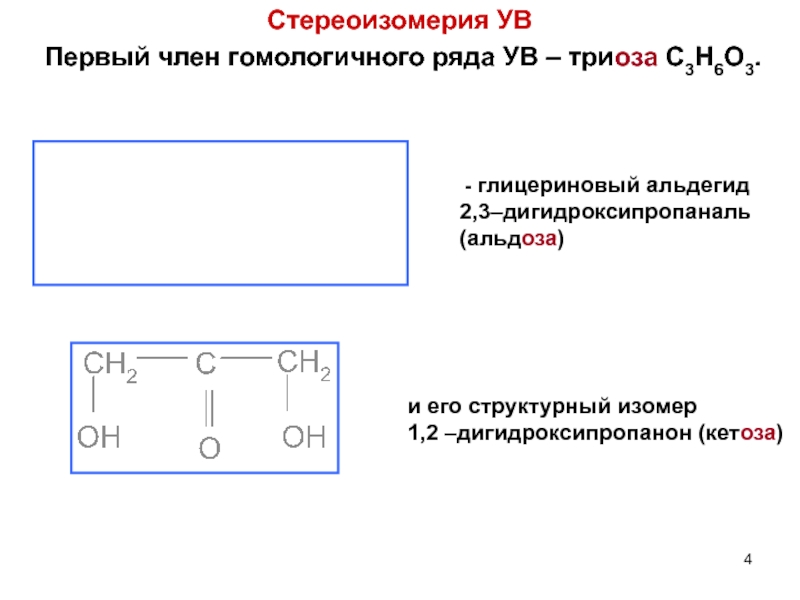
Слайд 4Стереоизомерия УВ
Первый член гомологичного ряда УВ – триоза
- глицериновый альдегид
2,3–дигидроксипропаналь (альдоза)
и его структурный изомер
1,2 –дигидроксипропанон (кетоза)
Слайд 5
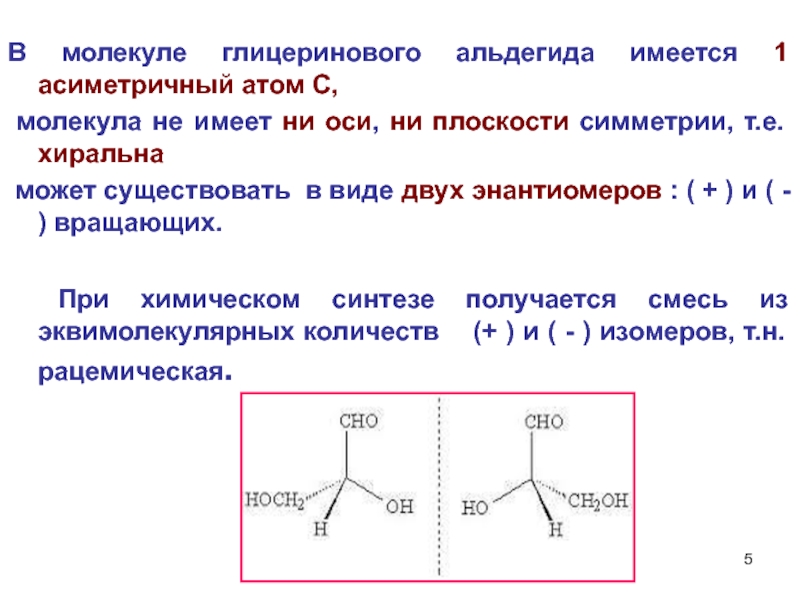
В молекуле глицеринового альдегида имеется 1
молекула не имеет ни оси, ни плоскости симметрии, т.е. хиральна
может существовать в виде двух энантиомеров : ( + ) и ( - ) вращающих.
При химическом синтезе получается смесь из эквимолекулярных количеств (+ ) и ( - ) изомеров, т.н. рацемическая.
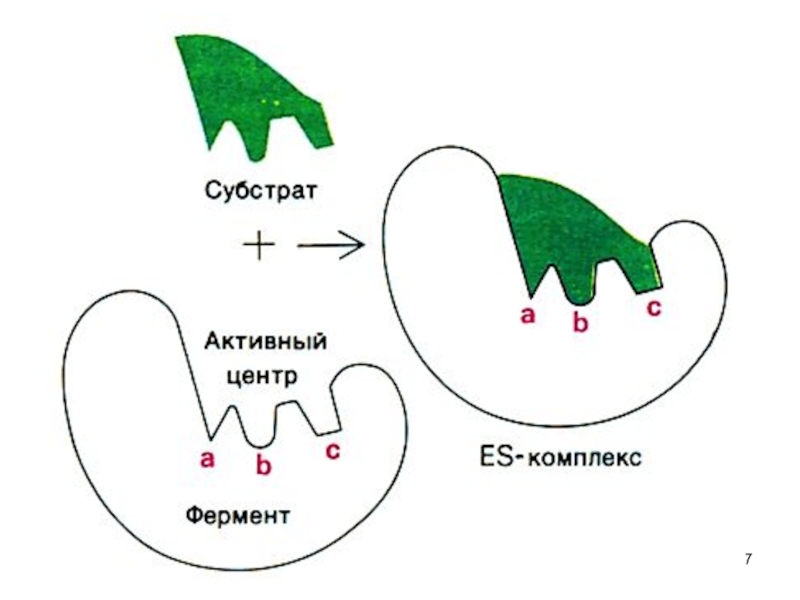
Слайд 6Реакции, протекающие в живом организме приводят к одному энантиомеру, т.е. стереоселективны.
Необходимо
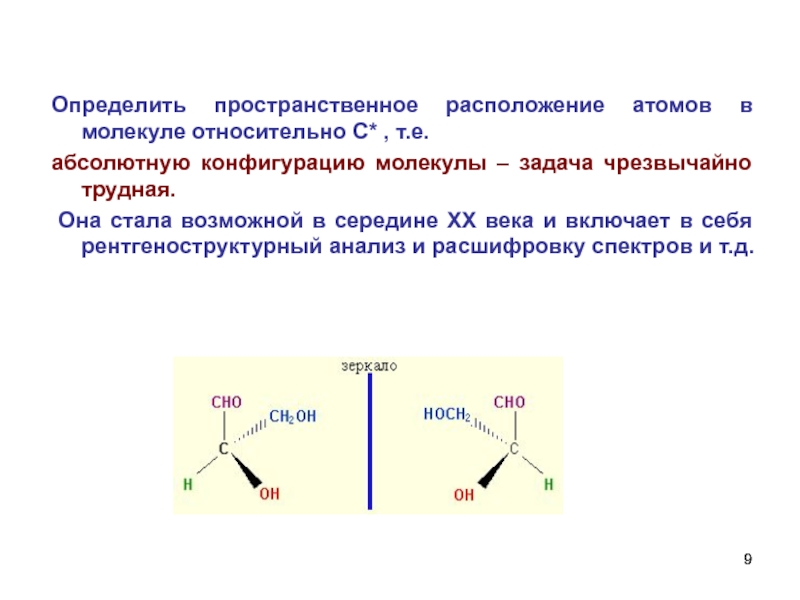
Слайд 8Абсолютная конфигурация — это истинное расположение в пространстве заместителей при каждом
Относительная конфигурация — это взаимное расположение заместителей при разных асимметрических атомах по отношению друг к другу; обычно ее обозначают приставками к основному названию вещества (цис- и транс-, трео- и эритро-, мезо-, алло- и др.)
Слайд 9Определить пространственное расположение атомов в молекуле относительно С* , т.е.
абсолютную
Она стала возможной в середине ХХ века и включает в себя рентгеноструктурный анализ и расшифровку спектров и т.д.
Слайд 10
Если абсолютную конфигурацию молекулы узнать трудно, то можно определить относительную.
Химики
1)выбрали конфигурационный стандарт
2) стали определять относительную конфигурацию изучаемого стереоизомера, сравнивая его со стандартом,
3) относить соединения к D и L стереохимическим рядам.
За конфигурационный эталон в 1906 году Розанов А. принял глицериновый альдегид.
Слайд 11
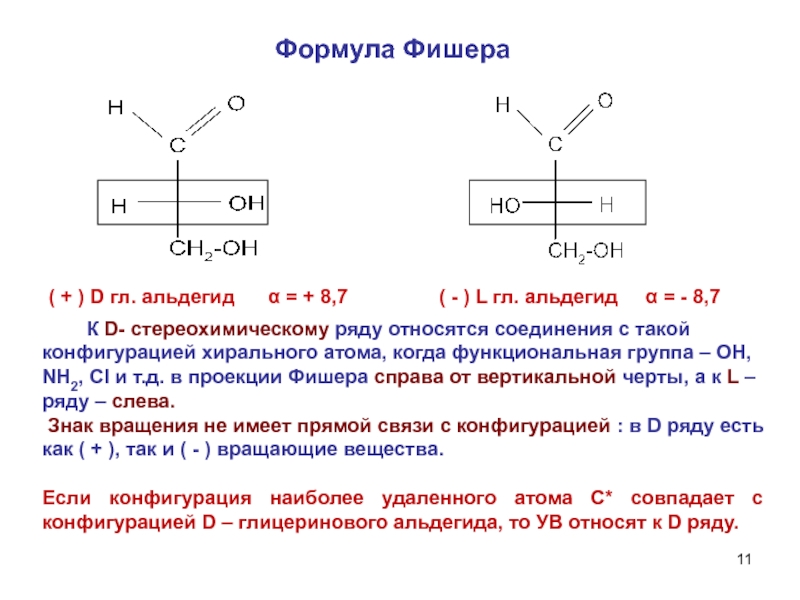
( + ) D гл. альдегид α = +
( - ) L гл. альдегид α = - 8,7
Формула Фишера
К D- стереохимическому ряду относятся соединения с такой конфигурацией хирального атома, когда функциональная группа – OH, NH2, Cl и т.д. в проекции Фишера справа от вертикальной черты, а к L – ряду – слева.
Знак вращения не имеет прямой связи с конфигурацией : в D ряду есть как ( + ), так и ( - ) вращающие вещества.
Если конфигурация наиболее удаленного атома С* совпадает с конфигурацией D – глицеринового альдегида, то УВ относят к D ряду.
Слайд 12Для изображения строения мнсх. используют проекционные формулы Фишера.
Фишер Эмиль Герман (1852-1919),
1. Исследовал строение и синтезировал ряд производных пурина: кофеин, гуанин, аденин и др.
2. Ввел номенклатуру, создал рациональную классификацию и осуществил синтез многих углеводов.
3. Открыл специфичность действия ферментов. Основополагающие исследования по химии белков. Нобелевская премия (1902).
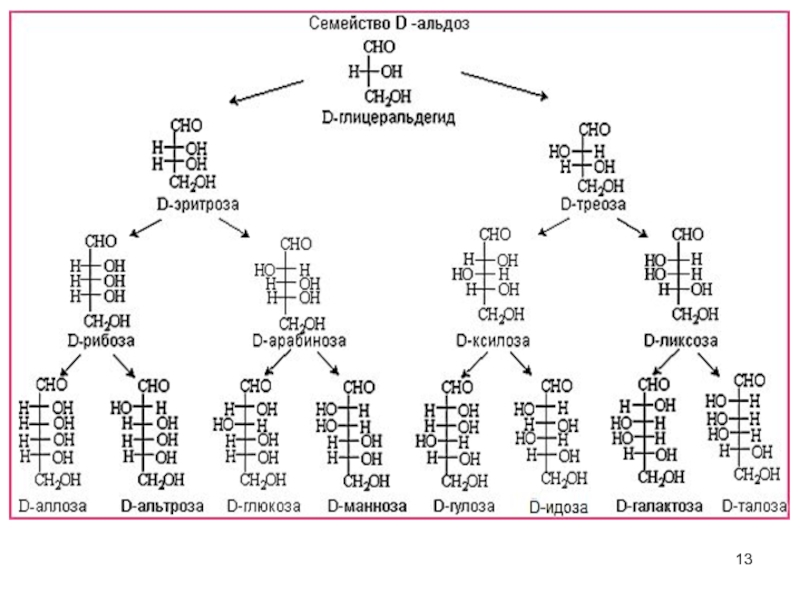
Слайд 14N = 23 = 8
УВ такого состава - 4 пары (
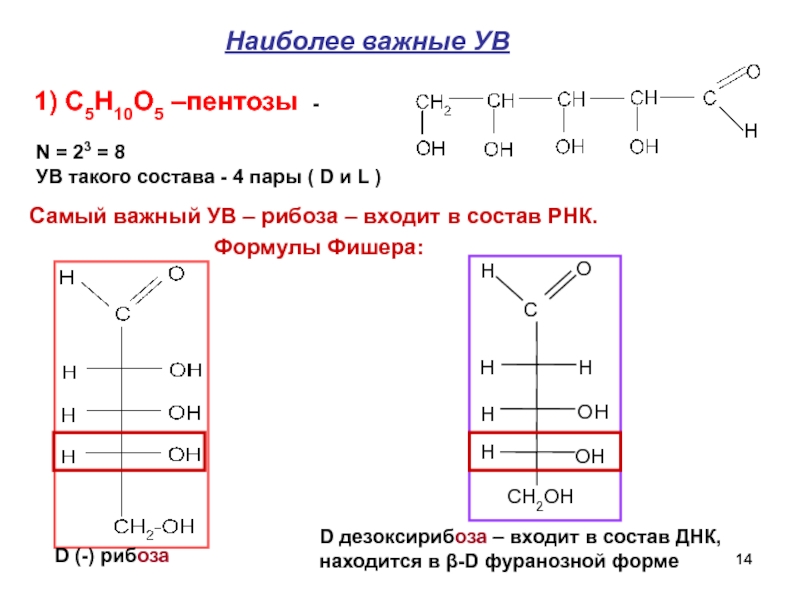
D (-) рибоза
D дезоксирибоза – входит в состав ДНК,
находится в β-D фуранозной форме
Наиболее важные УВ
Самый важный УВ – рибоза – входит в состав РНК.
Формулы Фишера:
1) C5H10O5 –пентозы -
C
H
H
H
O
H
O
H
ОH
H
СН2ОН
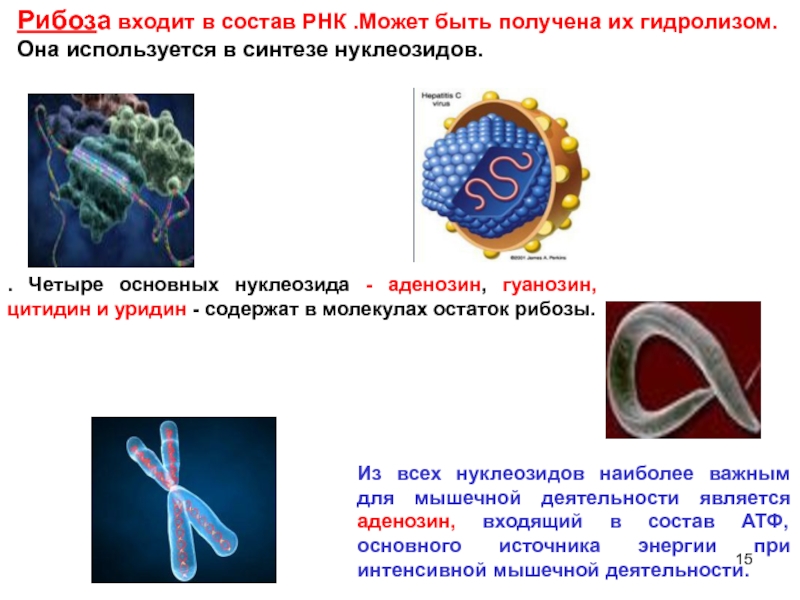
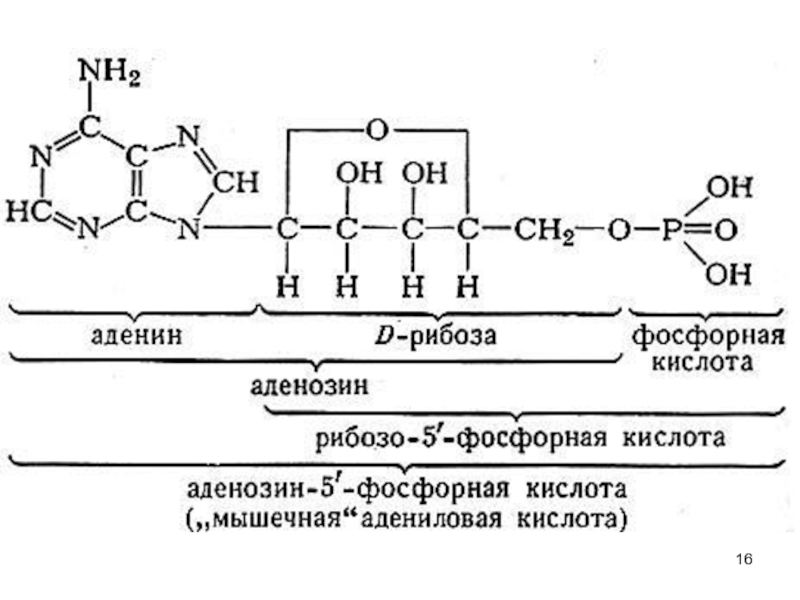
Слайд 15Рибоза входит в состав РНК .Может быть получена их гидролизом. Она
. Четыре основных нуклеозида - аденозин, гуанозин, цитидин и уридин - содержат в молекулах остаток рибозы.
Из всех нуклеозидов наиболее важным для мышечной деятельности является аденозин, входящий в состав АТФ, основного источника энергии при интенсивной мышечной деятельности.
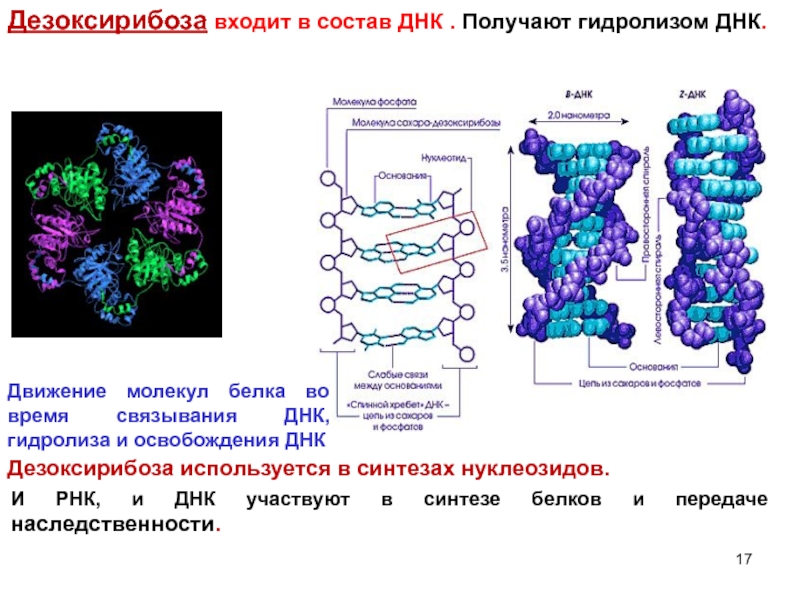
Слайд 17Дезоксирибоза входит в состав ДНК . Получают гидролизом ДНК.
Дезоксирибоза используется в
Движение молекул белка во время связывания ДНК, гидролиза и освобождения ДНК
И РНК, и ДНК участвуют в синтезе белков и передаче наследственности.
Слайд 18
C
ОH
H
O
НO
OН
D ( +
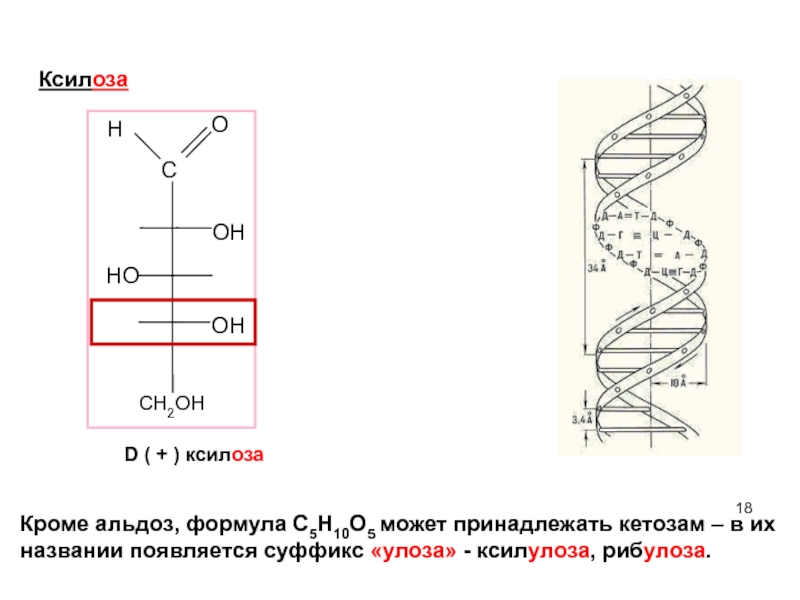
Кроме альдоз, формула C5H10O5 может принадлежать кетозам – в их названии появляется суффикс «улоза» - ксилулоза, рибулоза.
Ксилоза
СН2ОН
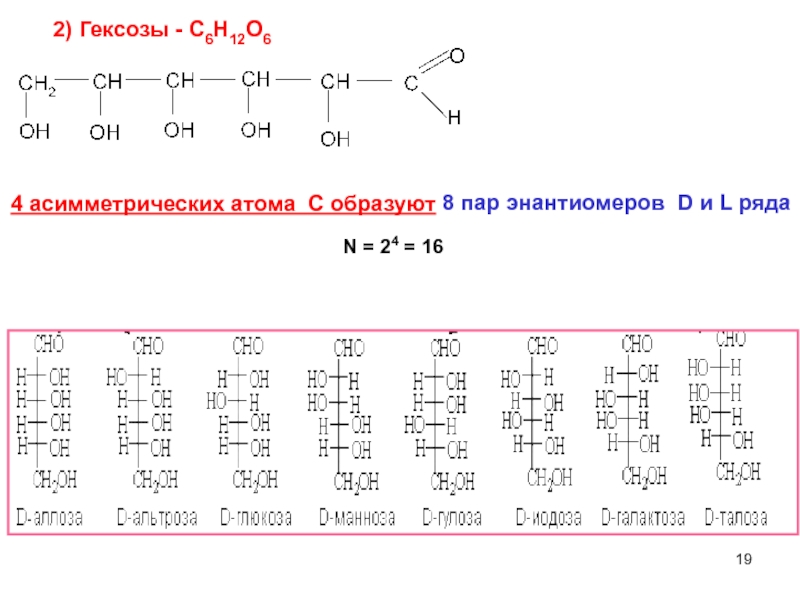
Слайд 192) Гексозы - C6H12O6
8 пар энантиомеров D и L ряда
4 асимметрических
N = 24 = 16
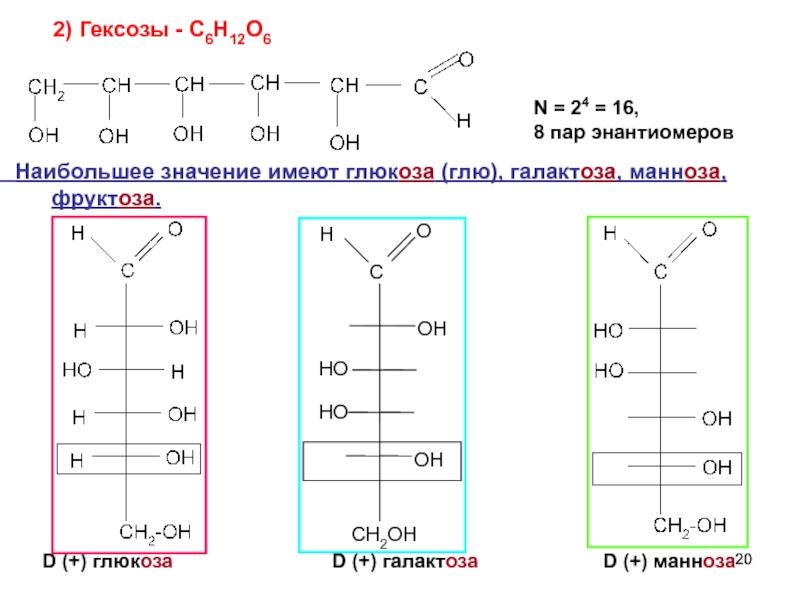
Слайд 20N = 24 = 16,
8 пар энантиомеров
D (+) глюкоза
D
D (+) манноза
2) Гексозы - C6H12O6
HО
C
OН
H
O
OН
НO
СН2ОН
Наибольшее значение имеют глюкоза (глю), галактоза, манноза, фруктоза.
Слайд 21
Глюкоза - самый распространенный моносахарид
В свободном виде содержится
во фруктовых соках,
в качестве составной части входит в молекулы дисахаридов (сахарозы, мальтозы, лактозы, целлобиозы
и полисахаридов (крахмал, гликогена, целлюлозы, декстринов
Слайд 22Используют глюкозу
в пищевой промышленности,
медицине , для синтеза глюконовой и
в качестве восстановителя в текстильной промышленности,
для получения этилового спирта.
Глюкоза
Слайд 23
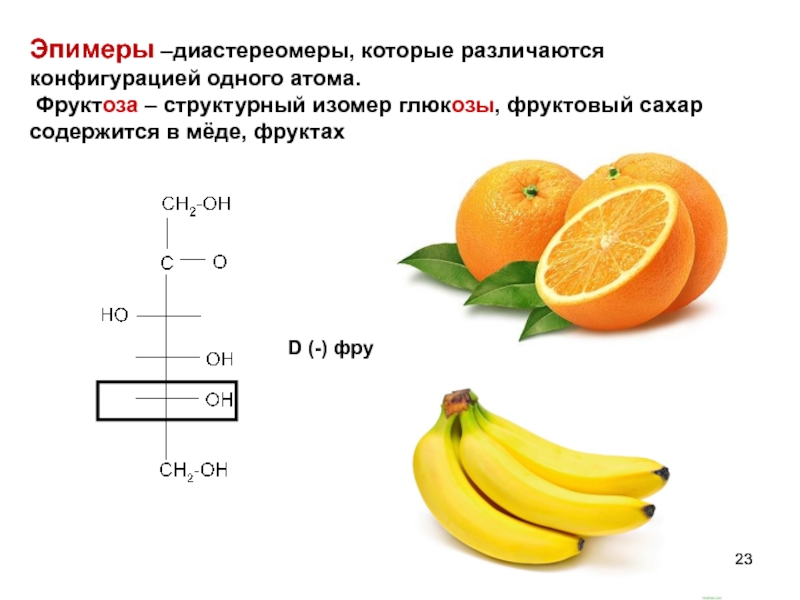
D (-) фру
Эпимеры –диастереомеры, которые различаются конфигурацией одного атома.
Фруктоза
Слайд 24Фруктоза
Фруктоза фруктовый или плодовый, сахар, левулёза, β-D-фруктофураноза, бесцветные кристаллы сладкого вкуса
Встречается в свободном виде во многих фруктах и плодах: в яблоках, помидорах, пчелином мёде (около 50% ), входит в состав олиго- и полисахаридов.
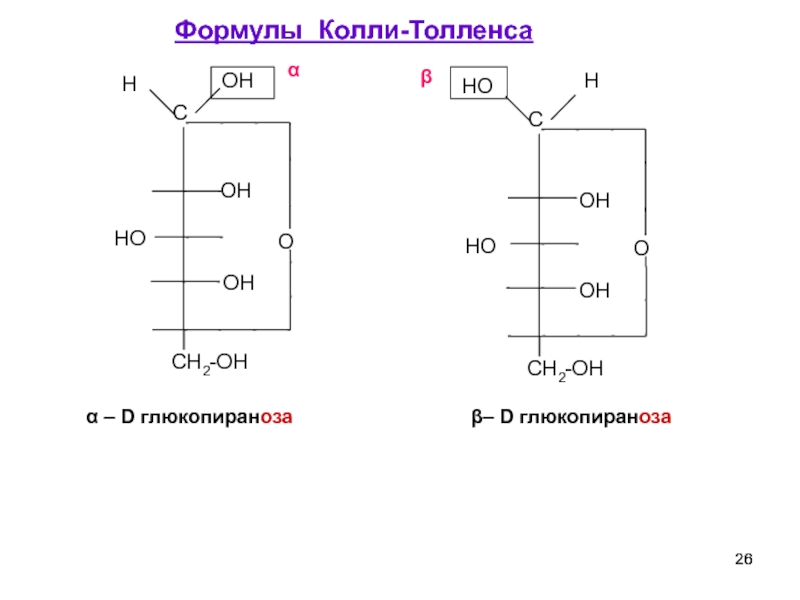
Слайд 26α – D глюкопираноза
β– D глюкопираноза
C
H
2
-
O
H
O
H
H
O
H
O
H
O
C
C
H
2
-
O
H
O
H
H
O
H
O
H
O
C
H
O
H
O
α
Формулы Колли-Толленса
β
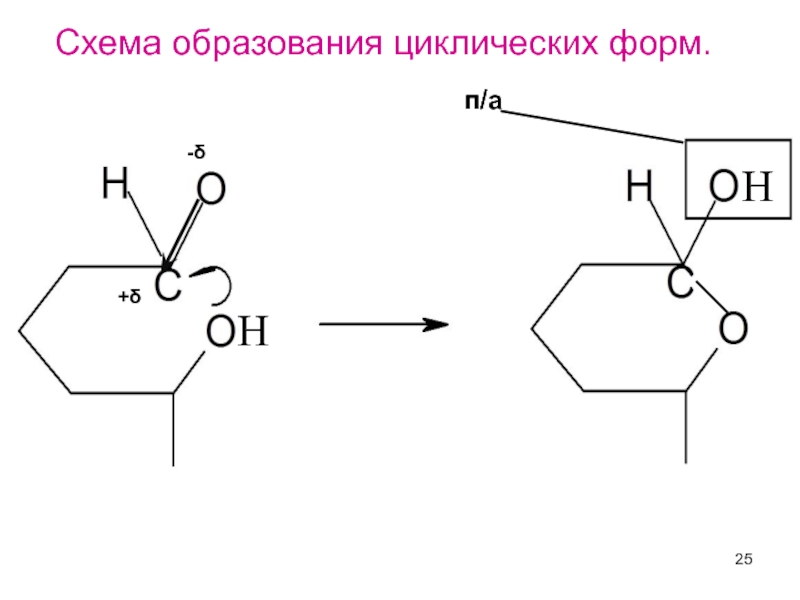
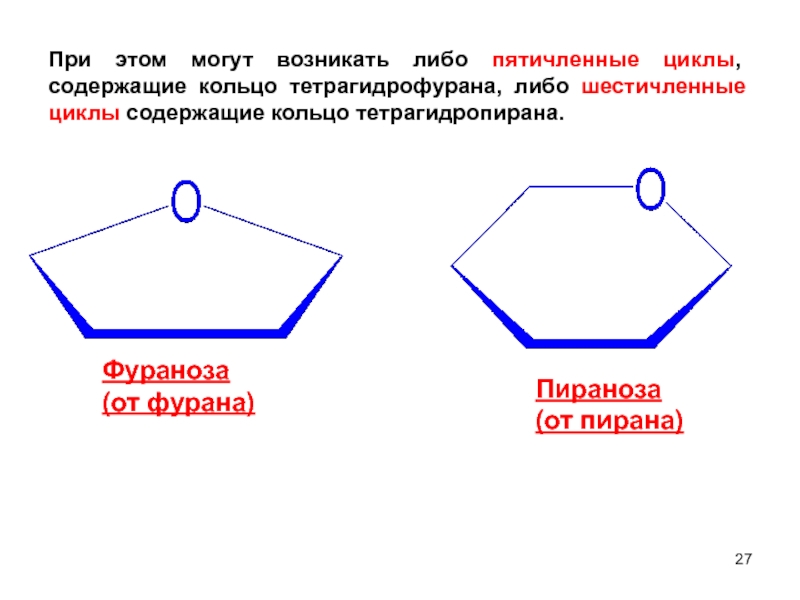
Слайд 27Фураноза
(от фурана)
Пираноза
(от пирана)
При этом могут возникать либо пятичленные циклы, содержащие
Слайд 28
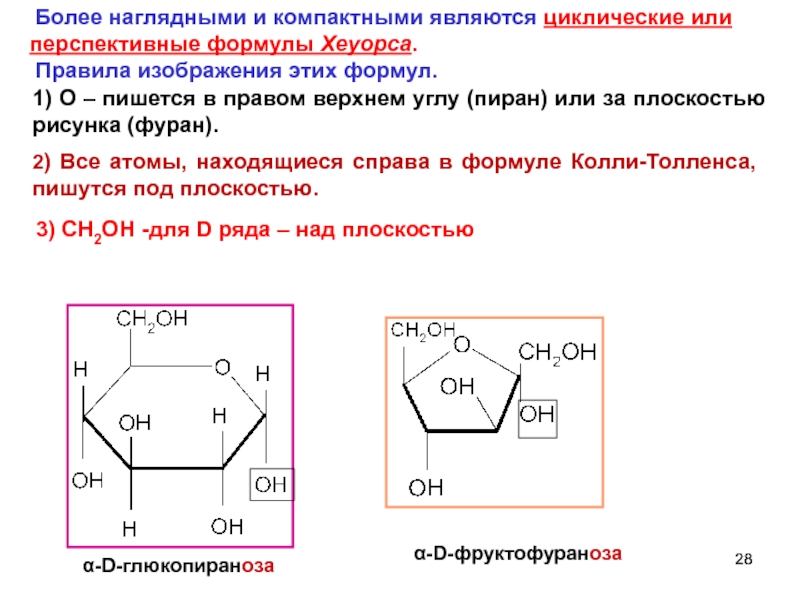
α-D-глюкопираноза
α-D-фруктофураноза
Более наглядными и компактными являются циклические или перспективные формулы Хеуорса.
1) О – пишется в правом верхнем углу (пиран) или за плоскостью рисунка (фуран).
2) Все атомы, находящиеся справа в формуле Колли-Толленса, пишутся под плоскостью.
3) CH2OH -для D ряда – над плоскостью
Слайд 29
Доказательством существования циклической формы может быть
В твердом состоянии моносахариды имеют циклическое строение.
При растворении моносахаридов первоначальное значение [α] меняется, со временем достигнув определенного значения, которое остается постоянным.
Таутомерия. Мутаротация
Сахариметр-поляриметр СУ-5 предназначен для измерения концентрации сахарозы в растворах по углу вращения плоскости поляризации
Мутаротация – изменение удельного вращения растворов УВ
во времени.
Слайд 30Таутомерия. Мутаротация
Сосуществование в динамическом равновесии двух и более изомерных форм
Таутомерия УВ - окси-оксо, цикло-оксо, или кольчато-цепная.
При растворении моносахарид из одной циклической формы может перейти в другую, но только через открытую.
β-D- глюкопираноза D – глю α-D- глюкопираноза
α = + 19° равнов. α = 52.5° α = + 112°
Автоматический цифровой поляриметр
Слайд 31
C
C
H
2
-
O
H
O
H
H
O
O
H
O
H
O
H
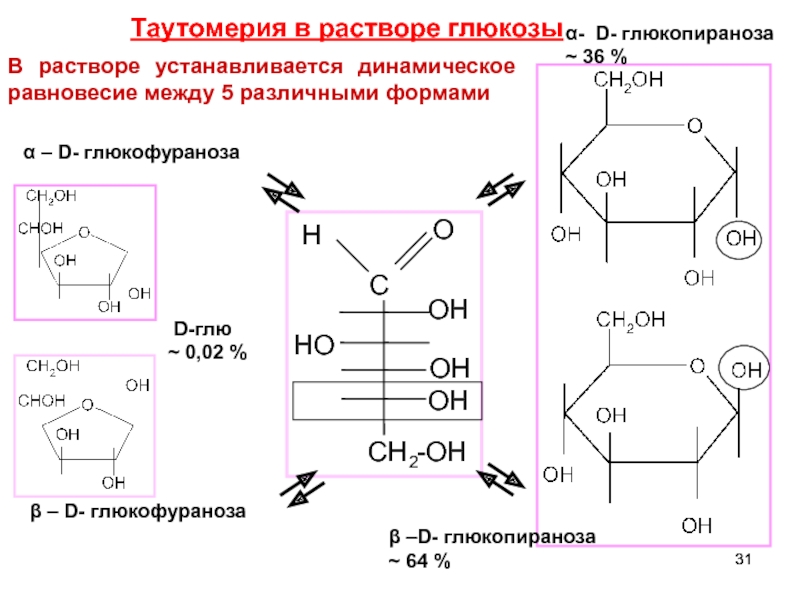
α – D- глюкофураноза
β – D- глюкофураноза
D-глю
~ 0,02 %
α- D-
~ 36 %
β –D- глюкопираноза
~ 64 %
Таутомерия в растворе глюкозы
В растворе устанавливается динамическое равновесие между 5 различными формами
Слайд 33Манноза
Манноза – компонент
многих полисахаридов и смешанных биополимеров растительного, животного и
В природе встречается только D-форма. Существует в виде двух аномеров: α- и β- формы.
В свободном виде обнаружена в плодах многих цитрусовых, анакардиевых и коринокарповых
Слайд 34
Превращения маннозы в организме происходят с помощью активированной формы маннозы –
Манноза
Слайд 36Галактоза
Встречается в природе в свободном виде, в виде гликозидов, дисахаридов (лактозы),
Агар-агар
Слайд 38
2-дезокси-α-D-рибофураноза
2-дезокси-β-D-рибофураноза
(открытая форма)
Таутомерия в растворе дезоксирибозы
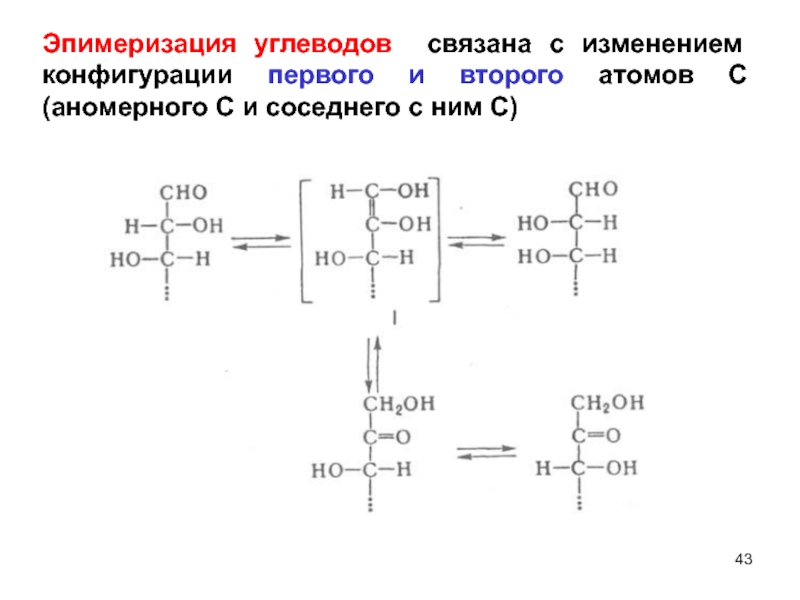
Слайд 41Эпимеры –диастереомеры,отличающиеся конфигурацией только одного асимметрического атома С.
В организме эпимеризация
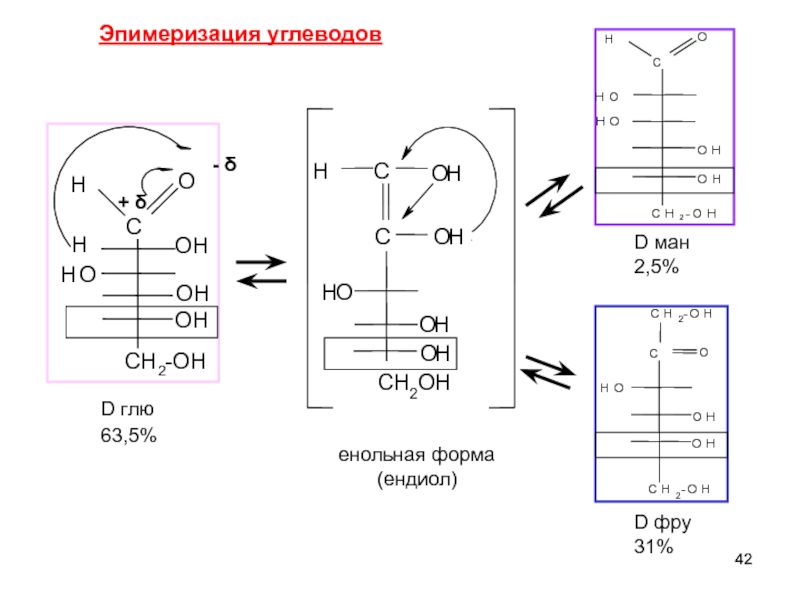
В слабощелочном растворе D-глюкоза находится в равновесии с кетогексозой, D-фруктозой, и альдогексозой, D-маннозой. Глюкоза и манноза различаются конфигурацией при С-2
Связана с открытой формой УВ .
Причина – в кислотном характере Н при α.С атоме.
Эпимеризация углеводов
ЭПИМЕРИЗАЦИЯ - изменение конфигурации одного из хиральных центров молекулы на противоположную
Dглю
Dман
Dфру
Слайд 42
C
C
H
2
-
O
H
O
H
H
O
O
H
O
H
O
H
H
+ δ
- δ
C
C
H
O
H
O
H
O
H
O
H
O
H
CH2OH
C
C
H
2
-
O
H
H
O
O
H
O
H
H
O
O
H
C
C
H
2
-
O
H
O
H
C
H
2
-
O
H
O
O
H
O
H
D ман
2,5%
D глю
63,5%
енольная форма
(ендиол)
D
31%
Эпимеризация углеводов
Слайд 43Эпимеризация углеводов связана с изменением конфигурации первого и второго атомов С
Слайд 44Химические свойства УВ
Общие реакции для всех углеводордов
на ОН- спирт
на п/а ОН
на > C = O
ОВР
Специфические реакции (различают пентозы и гексозы)
брожение
действ. кт. конц.
реакция Селиванова
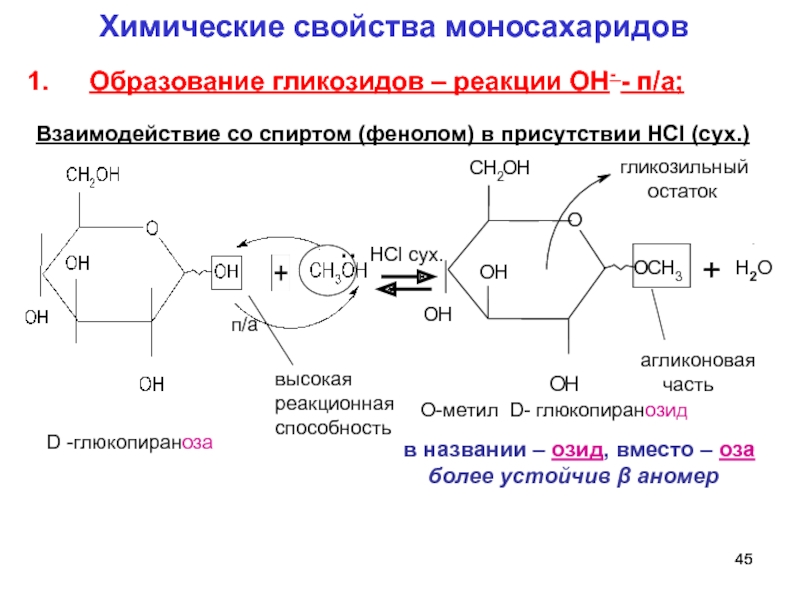
Слайд 45высокая
реакционная
способность
D -глюкопираноза
О-метил D- глюкопиранозид
гликозильный
остаток
агликоновая
часть
в
более устойчив β аномер
Химические свойства моносахаридов
Образование гликозидов – реакции ОН- - п/а;
Взаимодействие со спиртом (фенолом) в присутствии HCl (сух.)
Слайд 46
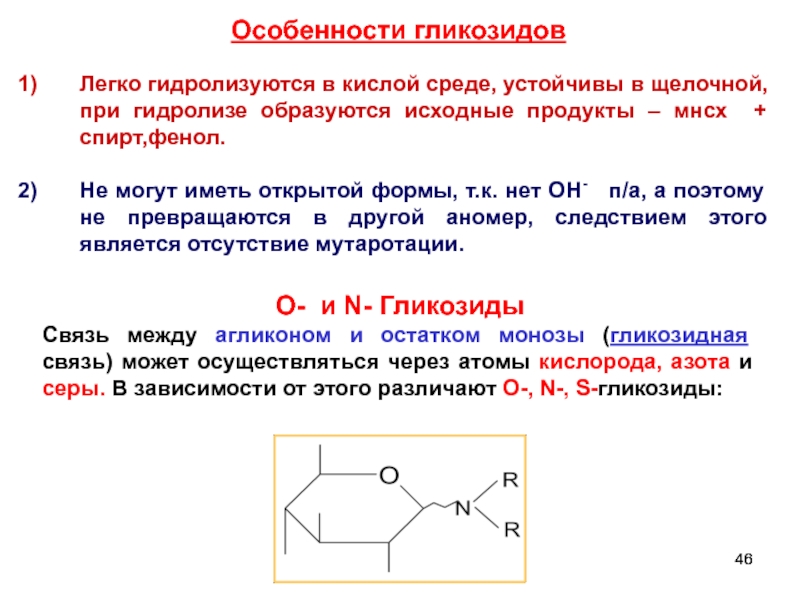
Особенности гликозидов
Легко гидролизуются в кислой среде, устойчивы в щелочной, при гидролизе
Не могут иметь открытой формы, т.к. нет ОН- п/а, а поэтому не превращаются в другой аномер, следствием этого является отсутствие мутаротации.
O- и N- Гликозиды
Связь между агликоном и остатком монозы (гликозидная связь) может осуществляться через атомы кислорода, азота и серы. В зависимости от этого различают O-, N-, S-гликозиды:
Слайд 47
В природе наиболее распространены O- и N-гликозиды. Большое количество О –
ванилил-β-D-глюкопиранозид в стручках ванили
кониферин в составе лигнина
О-гликозиды
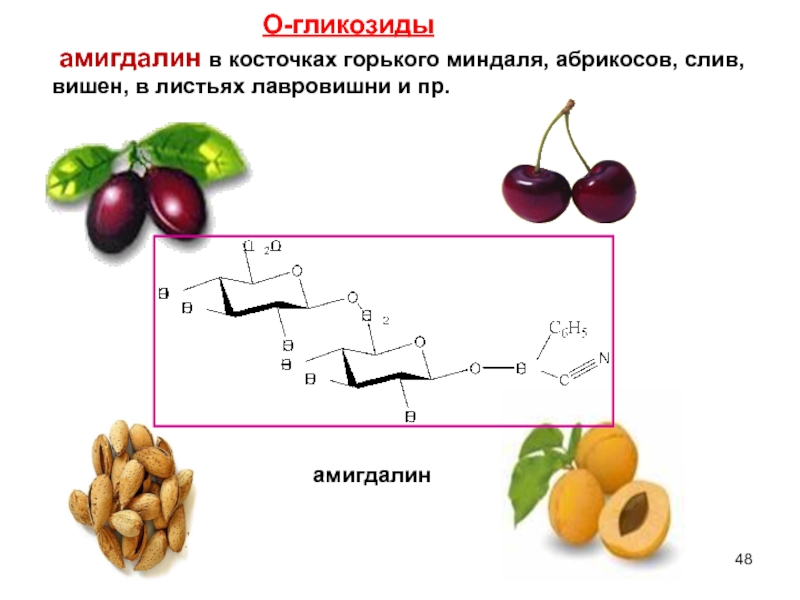
Слайд 48амигдалин
амигдалин в косточках горького миндаля, абрикосов, слив, вишен, в листьях
О-гликозиды
Слайд 49Витамины К, Р – это О - гликозиды, некоторые лекарственные препараты
О-гликозиды
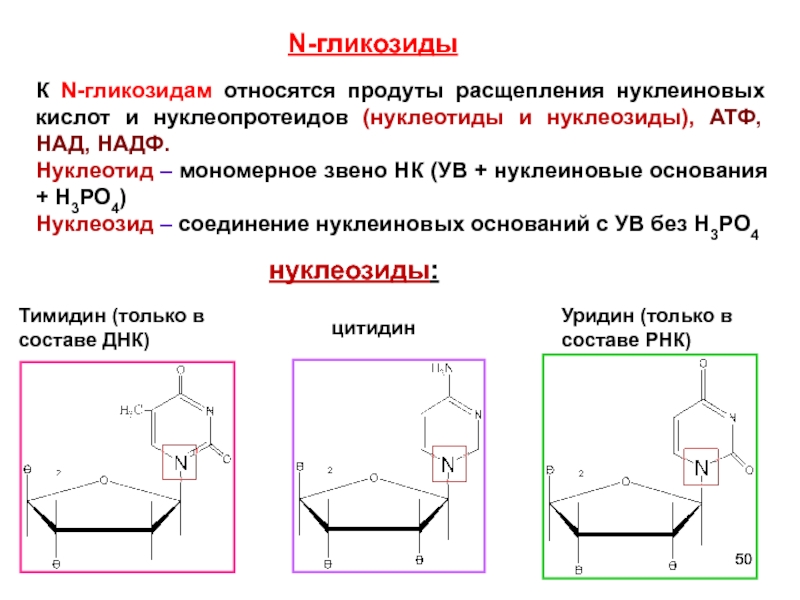
Слайд 50N-гликозиды
Тимидин (только в составе ДНК)
цитидин
К N-гликозидам относятся продуты расщепления нуклеиновых кислот
Нуклеотид – мономерное звено НК (УВ + нуклеиновые основания + H3PO4)
Нуклеозид – соединение нуклеиновых оснований с УВ без H3PO4
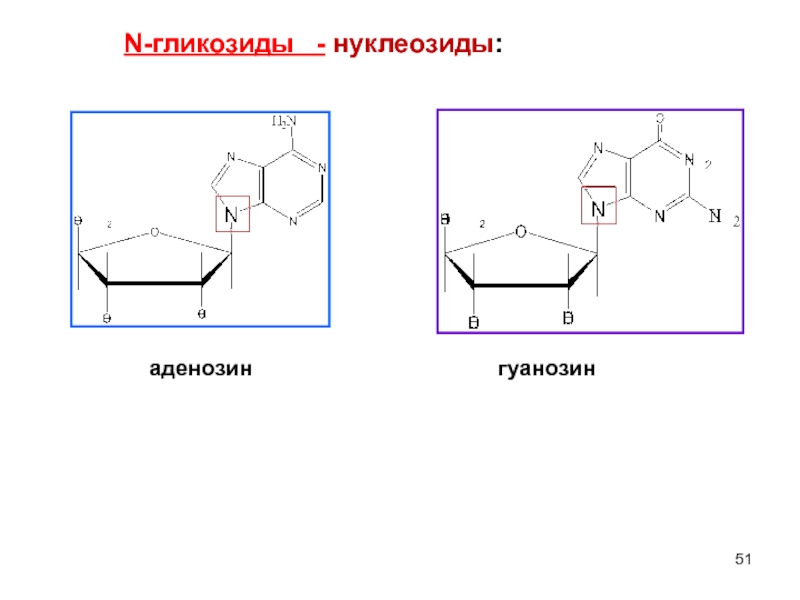
нуклеозиды:
Уридин (только в составе РНК)
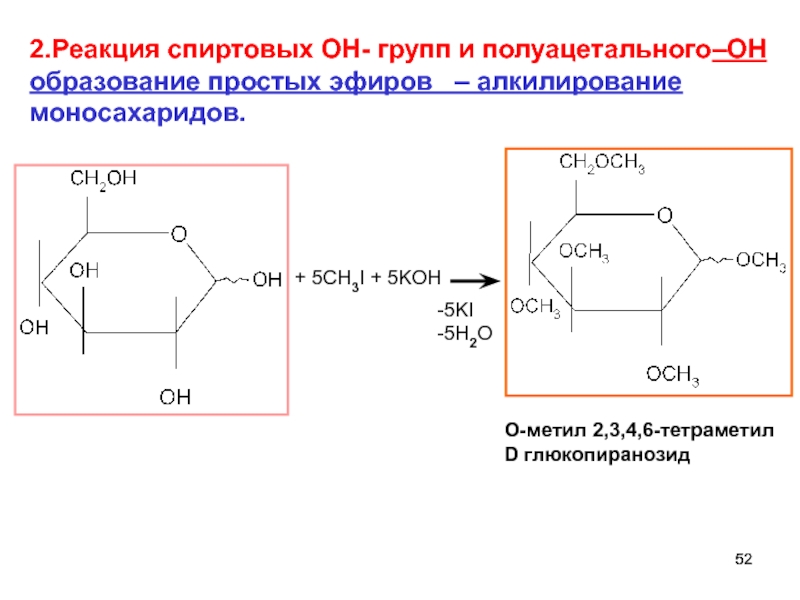
Слайд 52+ 5CH3I + 5KOH
-5KI
-5H2O
O-метил 2,3,4,6-тетраметил
D глюкопиранозид
2.Реакция спиртовых ОН- групп и
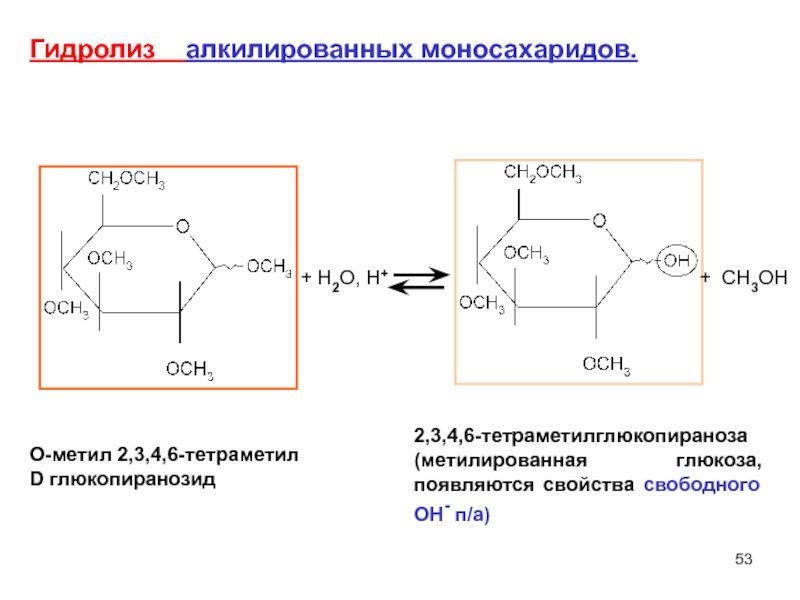
Слайд 53+ H2O, H+
+ CH3OH
2,3,4,6-тетраметилглюкопираноза
(метилированная глюкоза, появляются свойства свободного ОН- п/а)
Гидролиз
O-метил 2,3,4,6-тетраметил
D глюкопиранозид
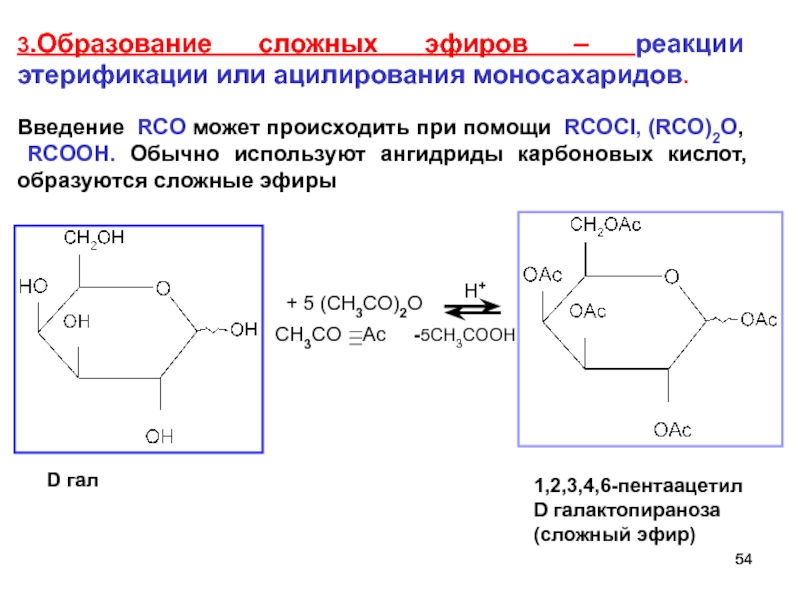
Слайд 54D гал
+ 5 (CH3CO)2O
H+
CH3CO Ac
1,2,3,4,6-пентаацетил
D галактопираноза
(сложный эфир)
3.Образование сложных эфиров
Введение RCO может происходить при помощи RCOCI, (RCO)2О,
RCOOH. Обычно используют ангидриды карбоновых кислот,образуются сложные эфиры
-5CH3COOH
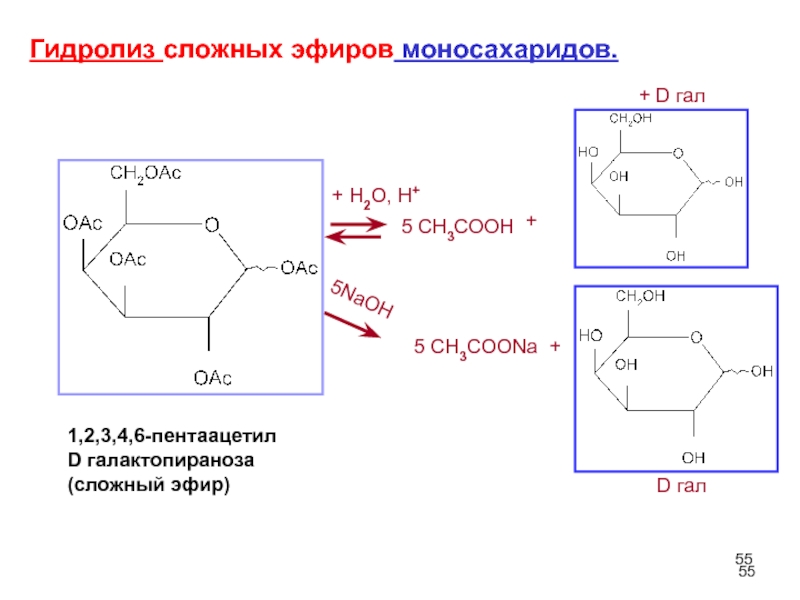
Слайд 55+ H2O, H+
5NaOH
5 CH3COOH
5 CH3COONa
Гидролиз сложных эфиров моносахаридов.
1,2,3,4,6-пентаацетил
D галактопираноза
(сложный эфир)
+
+
D
+ D гал
Слайд 56
Большое значение имеют эфиры H3PO4 – фосфаты. Это - наиболее метаболически
3.Образование сложных эфиров- фосфатов
Фосфаты содержатся во всех растительных и животных организмах
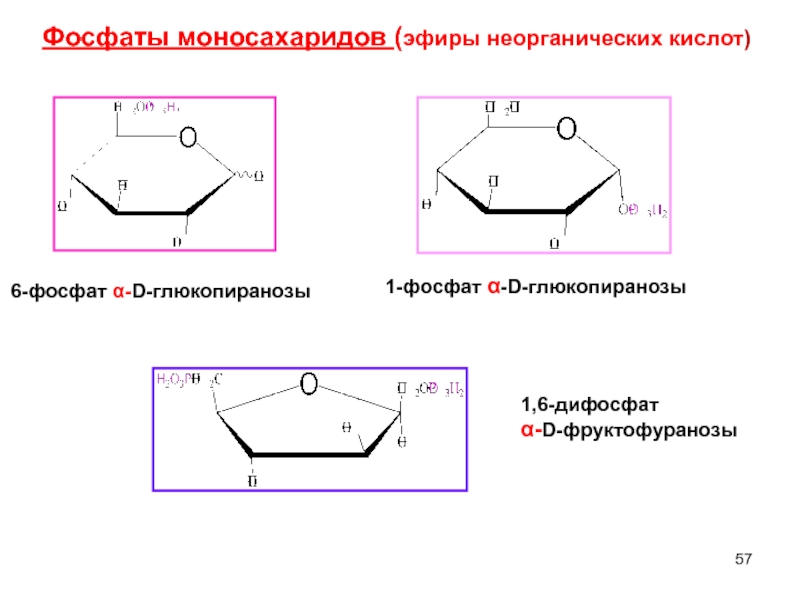
Слайд 57Фосфаты моносахаридов (эфиры неорганических кислот)
6-фосфат α-D-глюкопиранозы
1-фосфат α-D-глюкопиранозы
1,6-дифосфат
α-D-фруктофуранозы
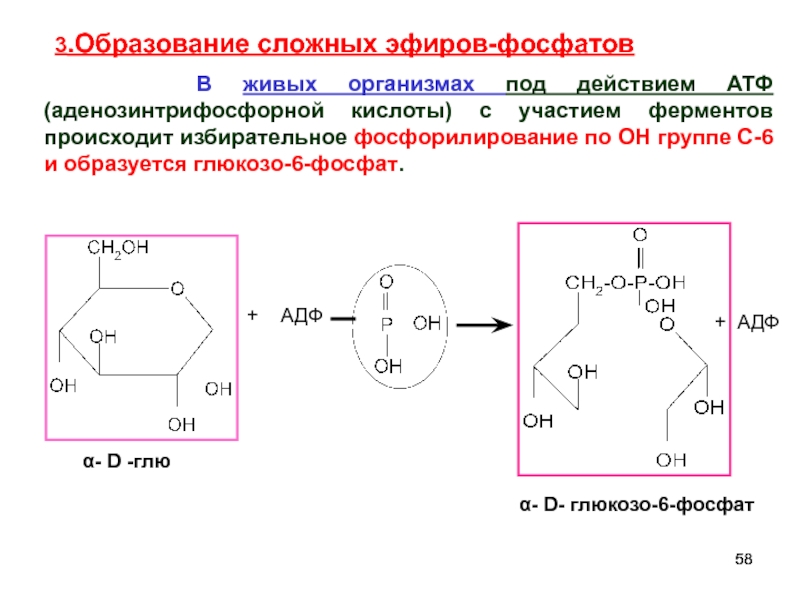
Слайд 58 + АДФ
+ АДФ
α- D -глю
α- D- глюкозо-6-фосфат
3.Образование сложных эфиров-фосфатов
В живых организмах под действием АТФ (аденозинтрифосфорной кислоты) с участием ферментов происходит избирательное фосфорилирование по ОН группе С-6 и образуется глюкозо-6-фосфат.
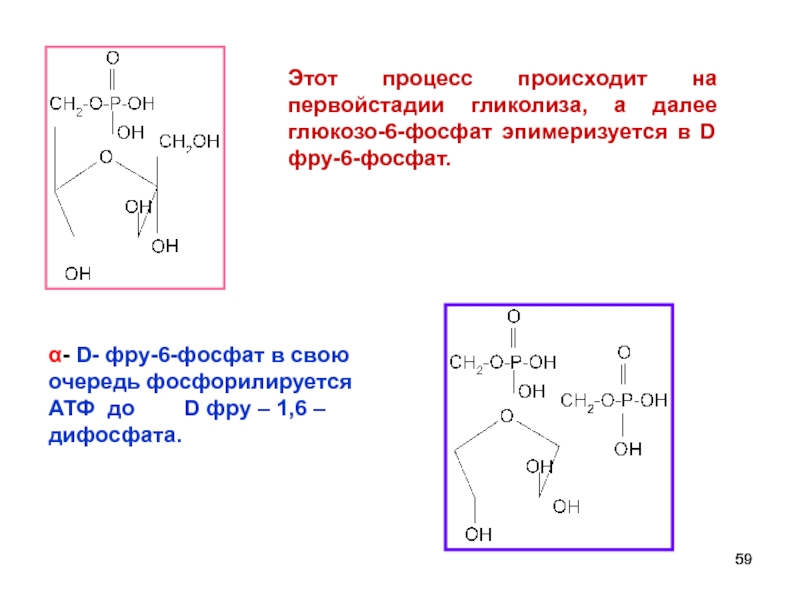
Слайд 59Этот процесс происходит на первойстадии гликолиза, а далее глюкозо-6-фосфат эпимеризуется в
α- D- фру-6-фосфат в свою очередь фосфорилируется АТФ до D фру – 1,6 – дифосфата.
Слайд 601
2
3
4
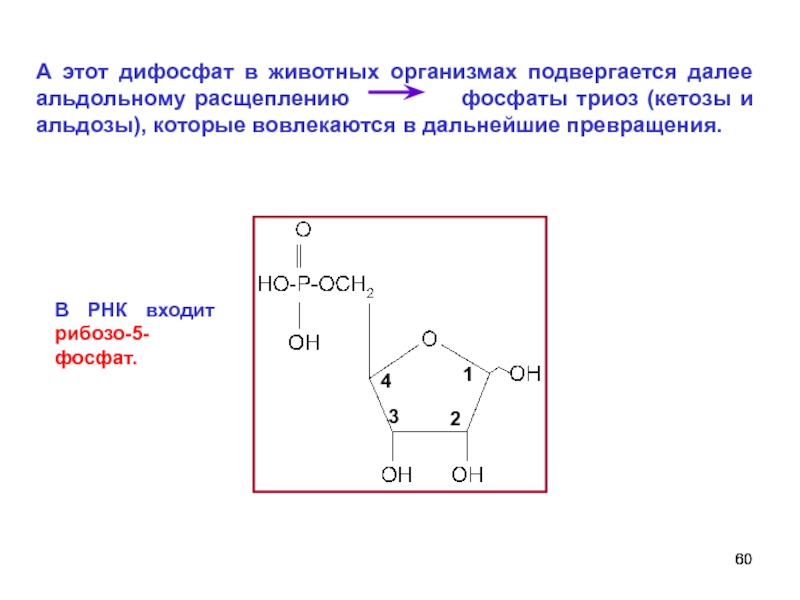
А этот дифосфат в животных организмах подвергается далее альдольному расщеплению
В РНК входит рибозо-5-фосфат.
Слайд 61Фруктоза-1,6-дифосфат, фруктозо-6-фосфат
промежуточные соединения в темновой фазе фотосинтеза (цикл Кельвина),
участники спиртового брожения и
биосинтеза углеводов.
Кроме того,
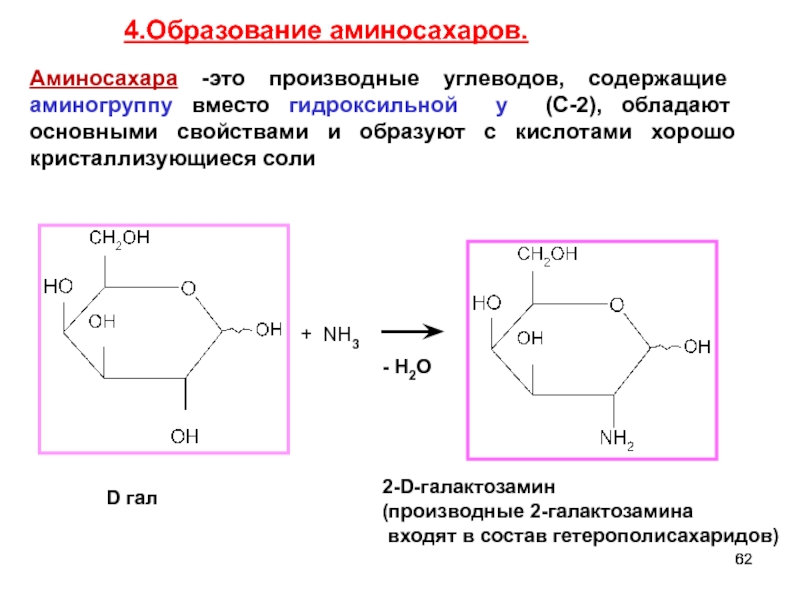
Слайд 62+ NH3
D гал
2-D-галактозамин
(производные 2-галактозамина
входят в состав гетерополисахаридов)
- Н2О
4.Образование аминосахаров.
Аминосахара -это
Слайд 63D-глюкозамин
(2-амино-2-дезокси-
-D-глюкопираноза)
N-ацетил--D-глюкозамин
Аминосахара
Важнейшими представителями аминосахаров служат 2-аминоаналоги D-глюкозы и D-галактозы.
D-галактозамин
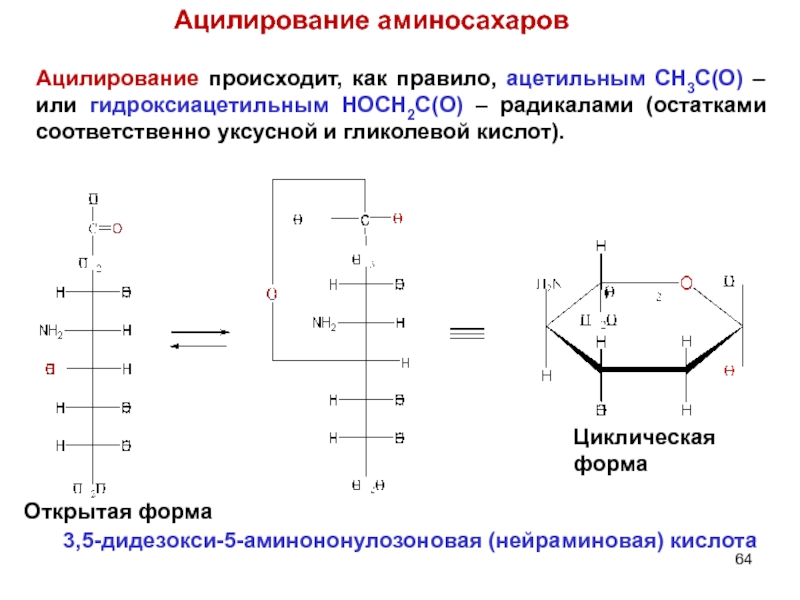
Слайд 64Ацилирование аминосахаров
Ацилирование происходит, как правило, ацетильным CH3C(O) – или гидроксиацетильным HOCH2C(O)
Открытая форма
Циклическая форма
3,5-дидезокси-5-аминононулозоновая (нейраминовая) кислота
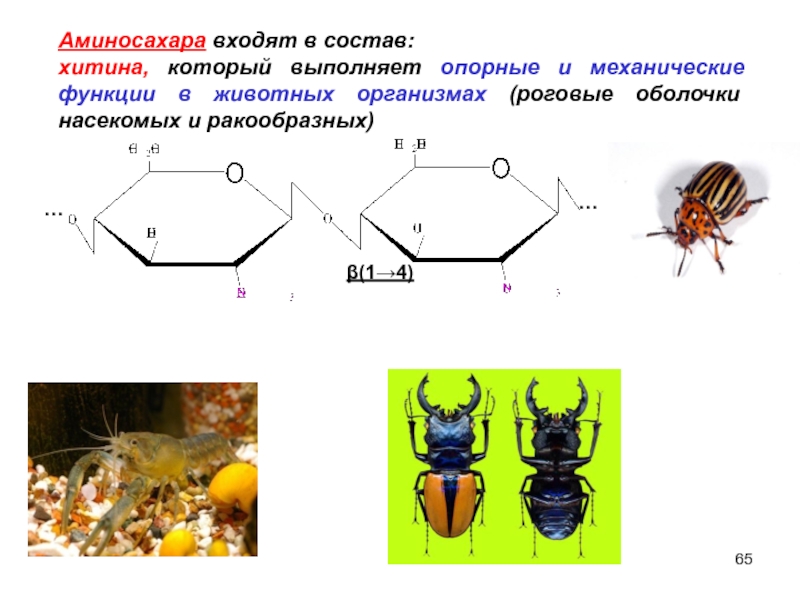
Слайд 65Аминосахара входят в состав:
хитина, который выполняет опорные и механические функции
…
…
β(1→4)
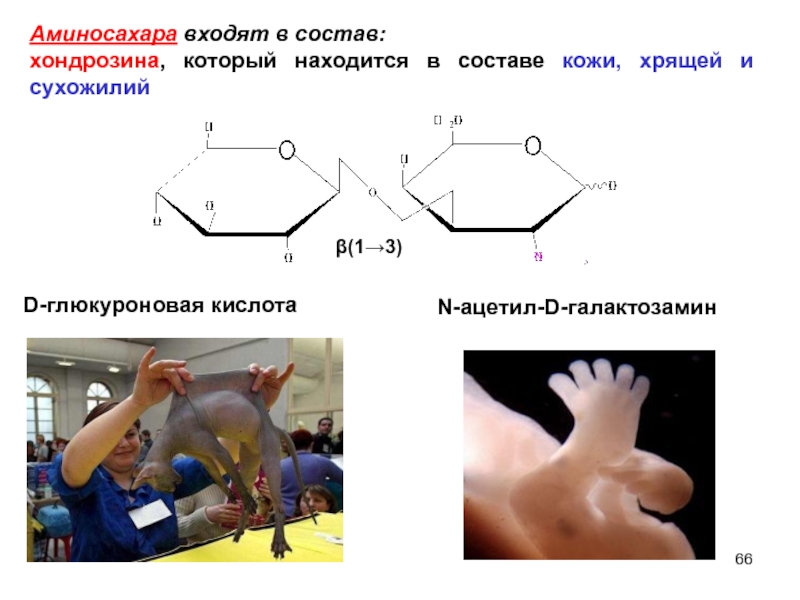
Слайд 66β(1→3)
D-глюкуроновая кислота
N-ацетил-D-галактозамин
Аминосахара входят в состав:
хондрозина, который находится в составе кожи,
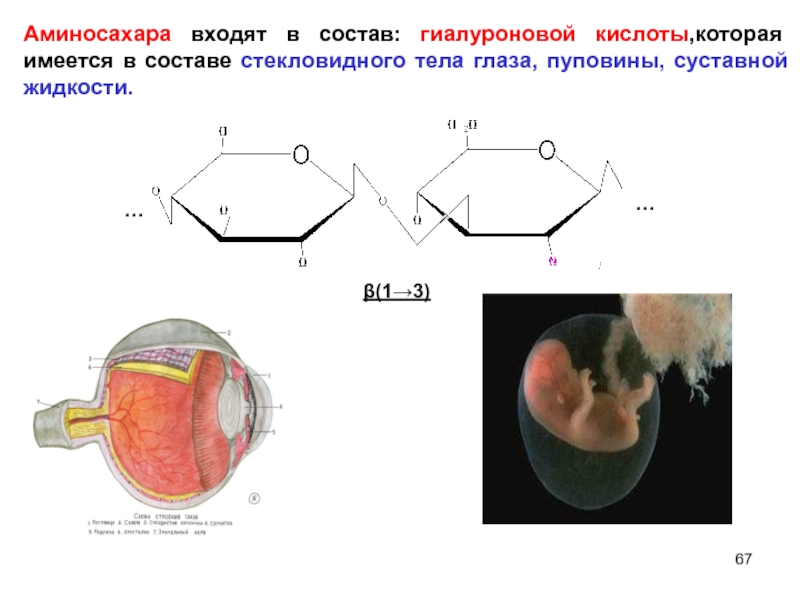
Слайд 67…
…
β(1→3)
Аминосахара входят в состав: гиалуроновой кислоты,которая имеется в составе стекловидного тела
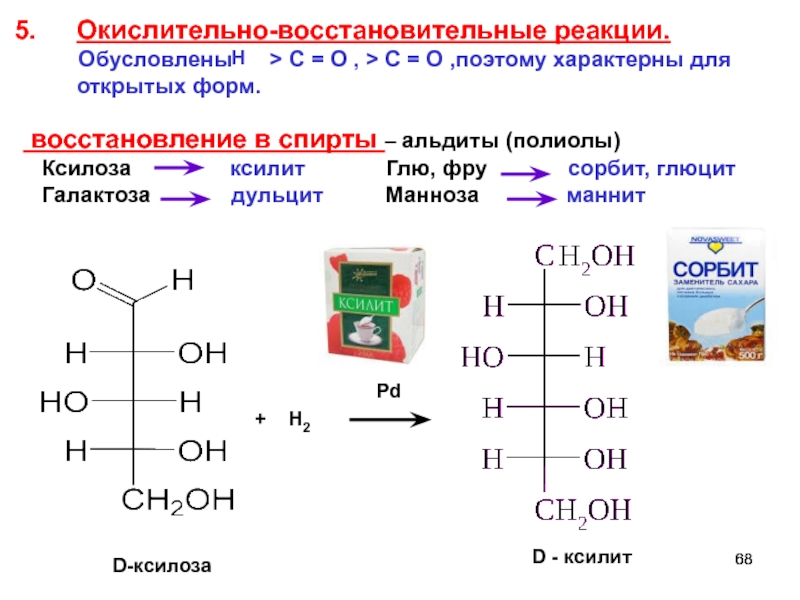
Слайд 68D-ксилоза
+ Н2
Pd
D - ксилит
Окислительно-восстановительные реакции.
восстановление в спирты – альдиты (полиолы)
Ксилоза ксилит Глю, фру сорбит, глюцит
Галактоза дульцит Манноза маннит
Н
Слайд 69Окисление моносахаридов
Реакции окисления используют в структурных исследованиях и биохимических анализах для
В зависимости от условий окисления образуются различные продукты.
Слайд 70A
g
(
N
H
3
)
2
O
H
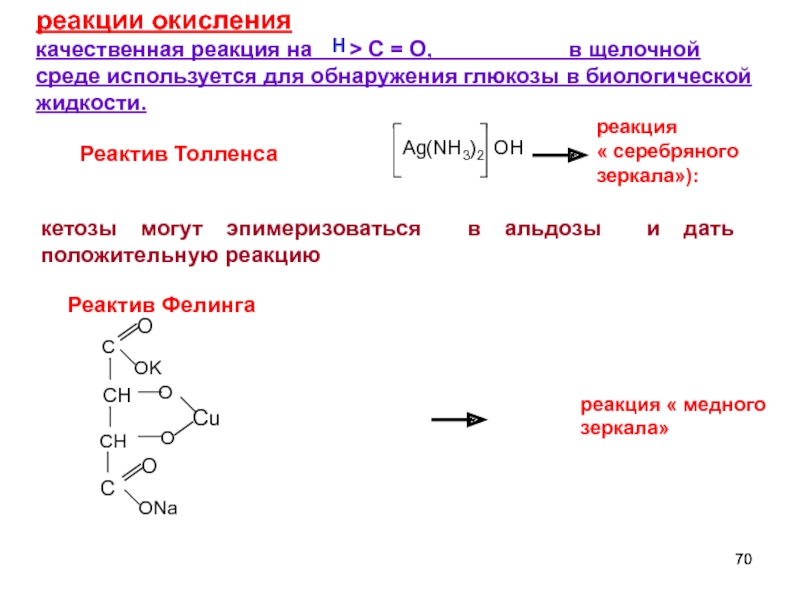
кетозы могут эпимеризоваться в альдозы и дать положительную реакцию
Реактив Толленса
C
O
K
O
C
H
O
C
H
Cu
C
O
N
a
O
O
реакции
качественная реакция на > C = O, в щелочной среде используется для обнаружения глюкозы в биологической жидкости.
Н
Реактив Фелинга
реакция
« серебряного зеркала»):
реакция « медного зеркала»
Слайд 71Окисление в щелочной среде (качественная реакция на альдозу)
реактивом Толленса (реакция
Ag(NH3)2 OH
Продукты окисления
D-Глюкоза
(глюконовая кислота)
Слайд 72Кирпично-красный
осадок
Продукты реакции
Окисление в щелочной среде (качественная реакция на альдозу)
Реактивом
(глюконовая кислота)
D-Глюкоза
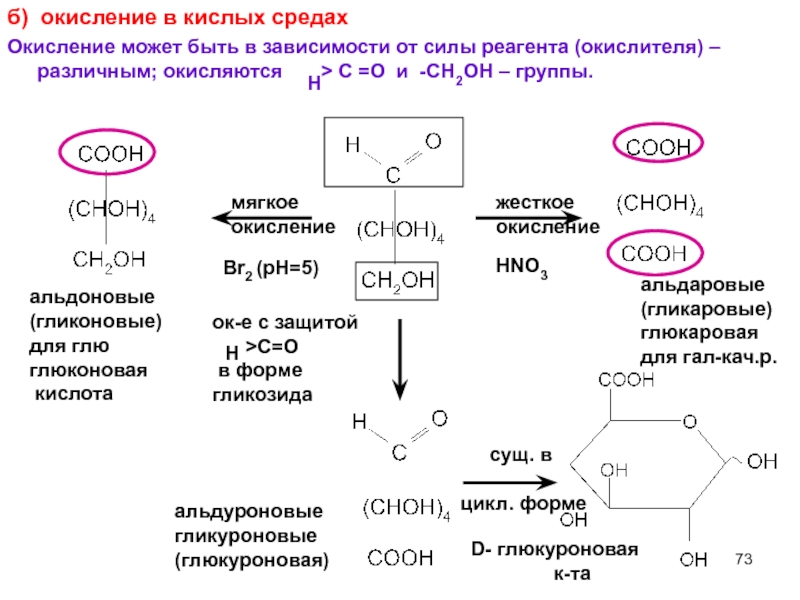
Слайд 73б) окисление в кислых средах
Окисление может быть в зависимости от силы
альдоновые
(гликоновые)
для глю
глюконовая
кислота
мягкое
окисление
Br2 (pH=5)
жесткое
окисление
HNO3
альдаровые
(гликаровые)
глюкаровая
для гал-кач.р.
ок-е с защитой
>C=O
в форме гликозида
Н
сущ. в
цикл. форме
альдуроновые
гликуроновые
(глюкуроновая)
D- глюкуроновая
к-та
Н
Слайд 74В форме глюкуронидов из организма с мочой выводятся многие яды (фенол,
Из D глюкуроновой кислоты в организме образуется при декарбоксилировании – ксилоза.
- СО2
D кси
Слайд 75+ HCN
OH
HO
D-фруктоза
OH
OH
OH
HO
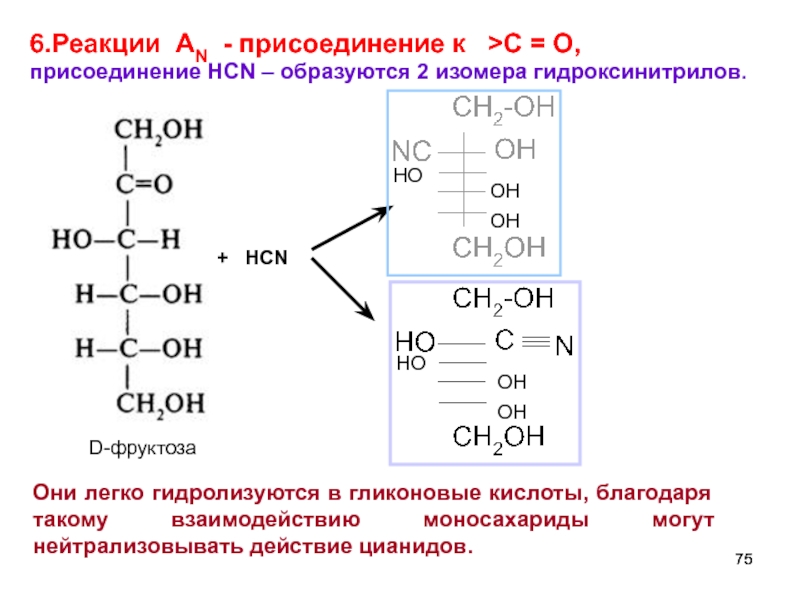
6.Реакции AN - присоединение к >C = O,
присоединение HCN – образуются 2 изомера гидроксинитрилов.
Они легко гидролизуются в гликоновые кислоты, благодаря такому взаимодействию моносахариды могут нейтрализовывать действие цианидов.
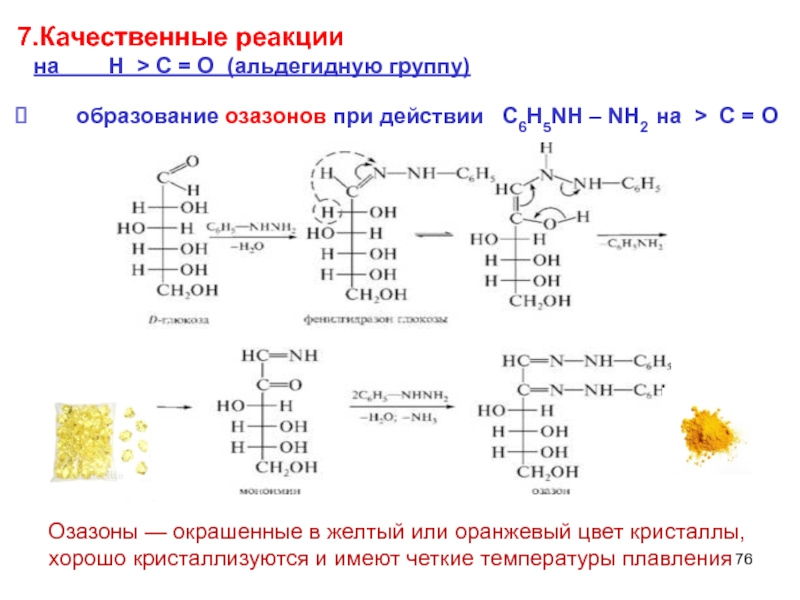
Слайд 767.Качественные реакции
на Н > C =
образование озазонов при действии С6H5NH – NH2 на > C = O
Озазоны — окрашенные в желтый или оранжевый цвет кристаллы, хорошо кристаллизуются и имеют четкие температуры плавления
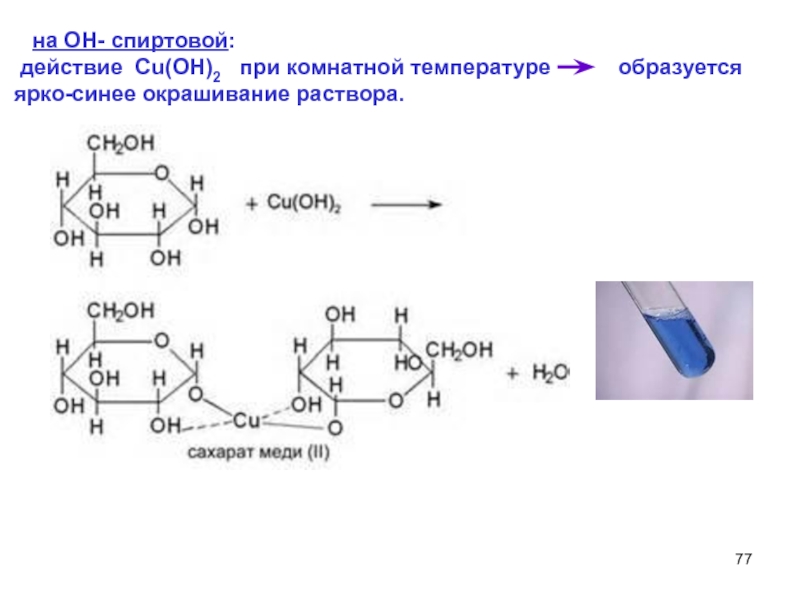
Слайд 77 на ОН- спиртовой:
действие Cu(OH)2 при комнатной температуре
Слайд 78C
C
H
2
-
O
H
O
H
C
H
2
-
OН
O
O
H
O
H
фру
HCl, t
- 3 H2O
+ резорцин
гидроксиметил-
фурфурол
HOH2C
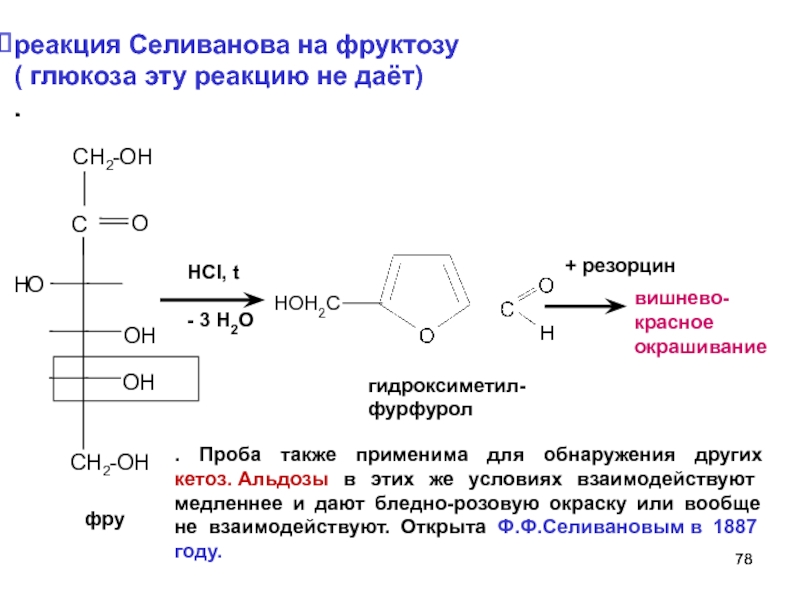
реакция Селиванова на фруктозу
( глюкоза эту реакцию
.
. Проба также применима для обнаружения других кетоз. Альдозы в этих же условиях взаимодействуют медленнее и дают бледно-розовую окраску или вообще не взаимодействуют. Открыта Ф.Ф.Селивановым в 1887 году.
вишнево-красное окрашивание
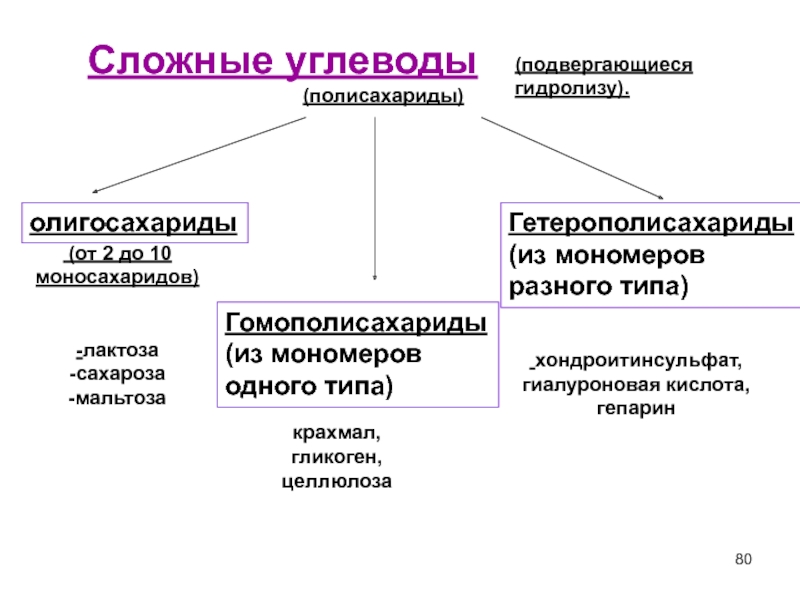
Слайд 80Сложные углеводы
(подвергающиеся гидролизу).
(полисахариды)
олигосахариды
(от 2 до 10 моносахаридов)
-лактоза
-сахароза
-мальтоза
Гомополисахариды
(из мономеров
одного типа)
крахмал,
Гетерополисахариды
(из мономеров
разного типа)
хондроитинсульфат, гиалуроновая кислота, гепарин
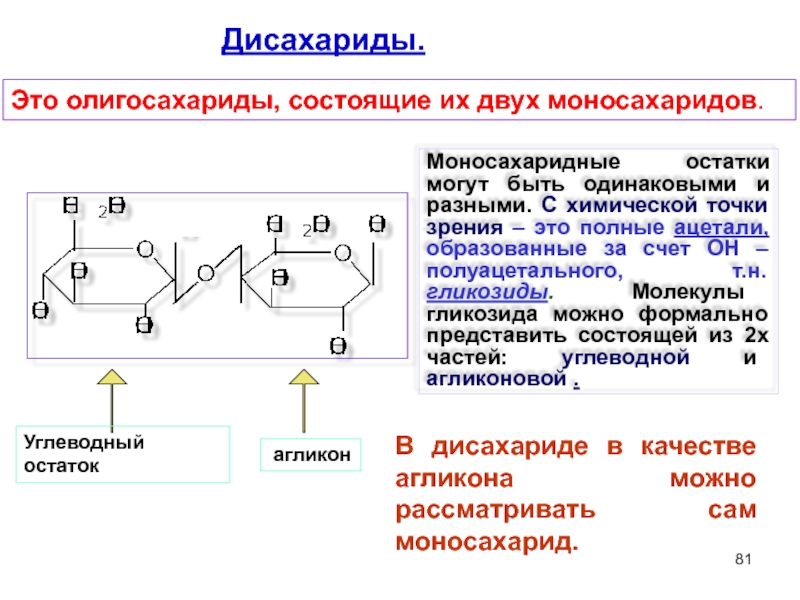
Слайд 81Дисахариды.
Это олигосахариды, состоящие их двух моносахаридов.
Моносахаридные остатки могут быть одинаковыми и
Углеводный остаток
агликон
В дисахариде в качестве агликона можно рассматривать сам моносахарид.
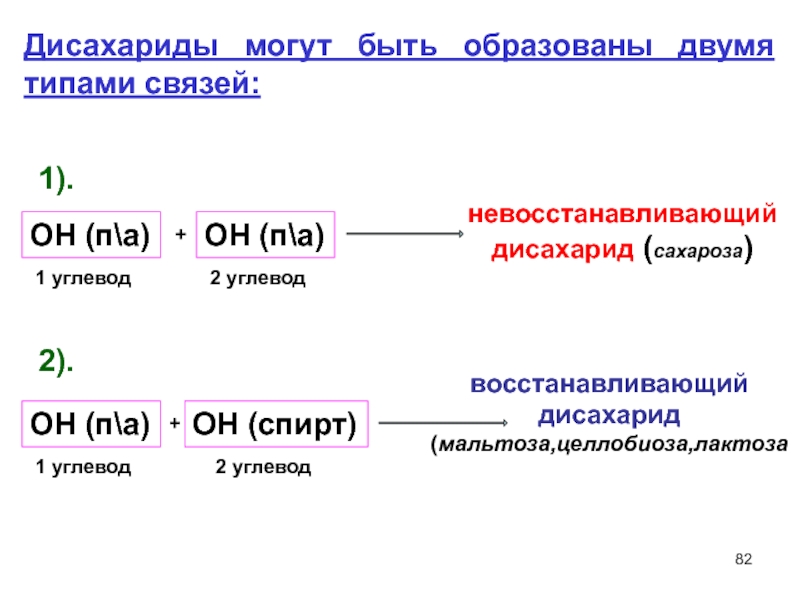
Слайд 82Дисахариды могут быть образованы двумя типами связей:
1).
2).
ОН
+
ОН (п\а)
невосстанавливающий дисахарид (сахароза)
1 углевод
2 углевод
ОН (п\а)
+
ОН (спирт)
восстанавливающий дисахарид
(мальтоза,целлобиоза,лактоза
1 углевод
2 углевод
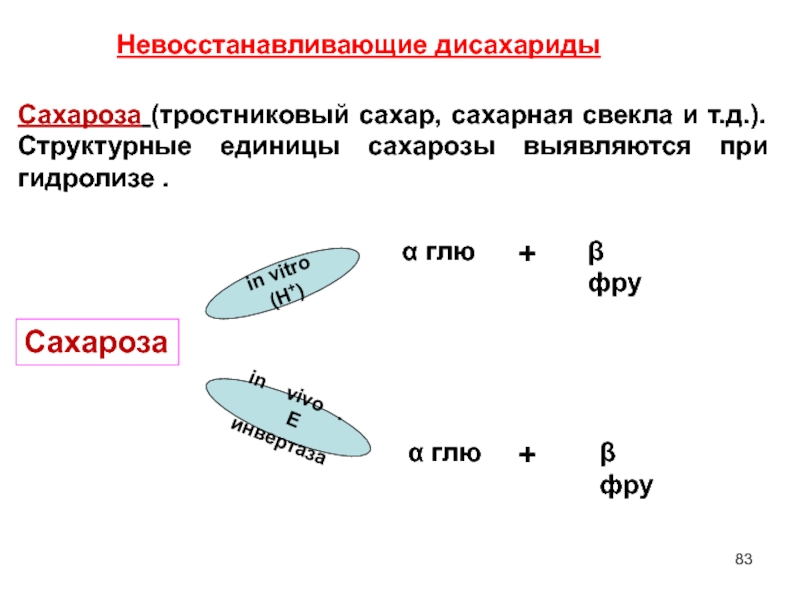
Слайд 83in vitro (H+)
in vivo .
E инвертаза
Невосстанавливающие дисахариды
Сахароза (тростниковый
Сахароза
β фру
β фру
α глю
α глю
+
+
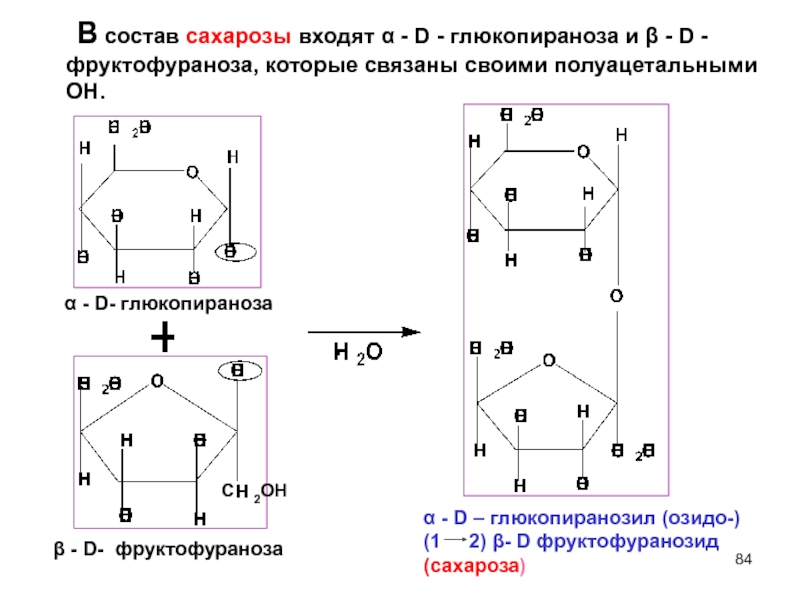
Слайд 84α - D- глюкопираноза
β - D- фруктофураноза
α - D – глюкопиранозил
(1 2) β- D фруктофуранозид (сахароза)
С 2ОН
В состав сахарозы входят α - D - глюкопираноза и β - D - фруктофураноза, которые связаны своими полуацетальными ОН.
Слайд 85В названии невосстанавливающих дисахаридов отражено отсутствие полуацетальных ОН, суффикс оза заменен
Правомерны оба названия:
α- D - глюкопиранозил - (1 2) - β- D – фруктофуранозид.
β- D - фруктофуранозил - (2 1) - α- D - глюкопиранозид.
Слайд 86
Свойства сахарозы.
В невосстанавливающем дисахариде нет свободного
1). Мутаротация
2). Восстанавливающие способности. Не реагирует с реактивом Толленса (Ag (NH3)2OH) с реактивом Фелинга, так как нет открытой формы, содержащей альдегидной группы
3). Отсутствуют реакции AN, например с HCN, с фенилгидразином C6Н5-NH-NH2.
отсутствуют:
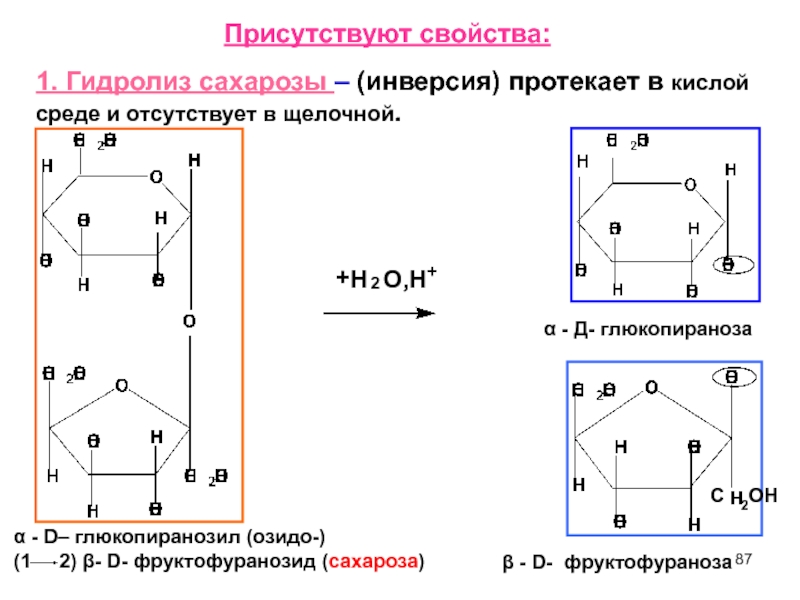
Слайд 87Присутствуют свойства:
1. Гидролиз сахарозы – (инверсия) протекает в кислой среде и
α - Д- глюкопираноза
β - D- фруктофураноза
α - D– глюкопиранозил (озидо-)
(1 2) β- D- фруктофуранозид (сахароза)
С 2ОН
Слайд 88При гидролизе сахарозы в кислой среде образуются исходные моносахариды.
Гидролиз сахарозы идет
Раствор сахарозы правовращающий (+), а при гидролизе образуется α-D- глю (+) и β-D- фру (-) – левовращающая. В результате будет преобладать левое вращение.
Автоматический поляриметр
Слайд 89Поэтому процесс гидролиза иногда называется инверсией, а смесь образующихся α глю
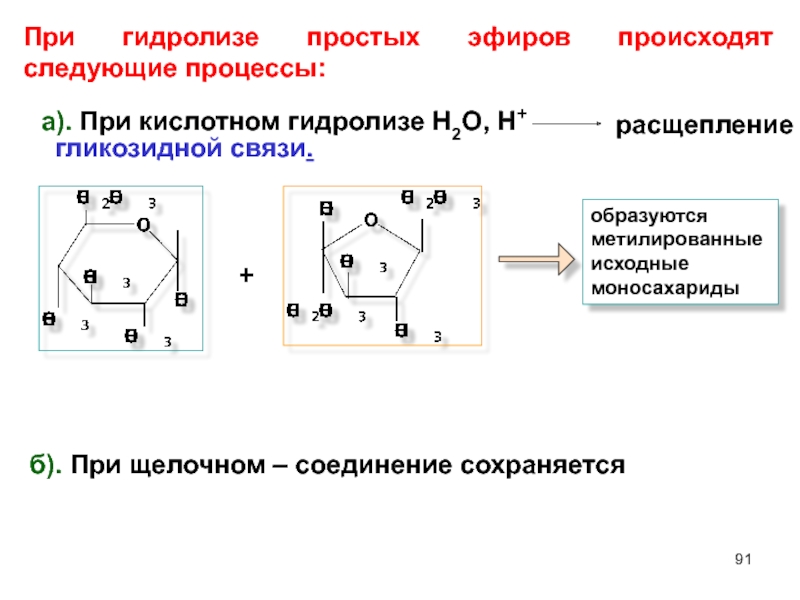
Слайд 91образуются метилированные исходные моносахариды
б). При щелочном – соединение сохраняется
При гидролизе простых
+
а). При кислотном гидролизе Н2О, Н+
гликозидной связи.
расщепление
Слайд 93Гидролиз сложных эфиров.
а). Кислотный гидролиз Н2О,Н+
8 СН3СООН
+
+
+
α - D - глю
β
Расщепление гликозидной связи α (1
2) в кислой среде
+
Слайд 94б). Щелочной гидролиз (ОН-)
Гликозидная связь
(1 2) не
8NaОН
+
+
8СН3СООNa
октaацетилсахароза
+8H2O
Слайд 96
Восстанавливающие дисахариды.
ОН(п/а)
+
ОН (спиртовой)
1 УВ
2 УВ
-озил
-оза
1). Лактоза.
2). Мальтоза.
3). Целлобиоза.
Лактоза - молочный
образованы
Слайд 98β - лактоза содержится в материнском молоке,
является основным углеводом пищи для
α - лактоза (α - глю) – в коровьем.
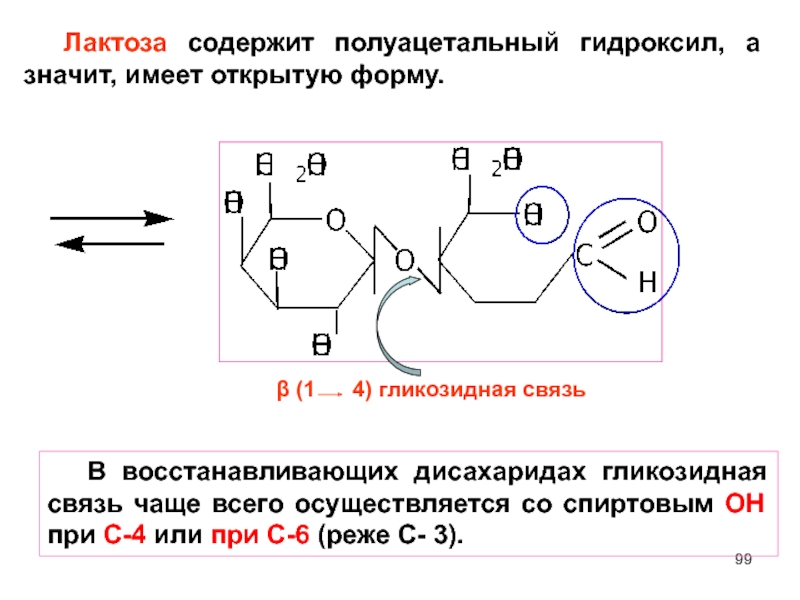
Слайд 99 Лактоза содержит полуацетальный гидроксил, а значит, имеет открытую форму.
β (1
В восстанавливающих дисахаридах гликозидная связь чаще всего осуществляется со спиртовым ОН при С-4 или при С-6 (реже C- 3).
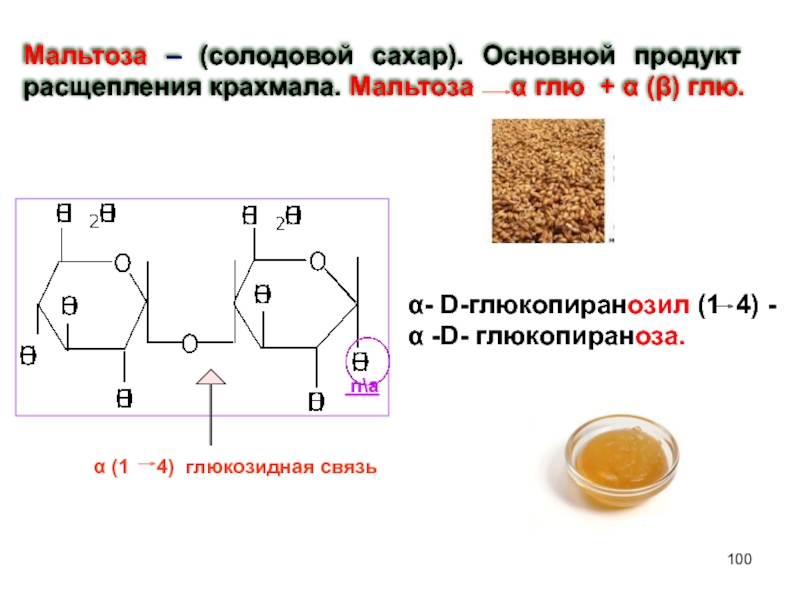
Слайд 100Мальтоза – (солодовой сахар). Основной продукт расщепления крахмала. Мальтоза
α- D-глюкопиранозил (1 4) - α -D- глюкопираноза.
п\а
α (1 4) глюкозидная связь
Слайд 101Мальтоза – структурная единица, биозный фрагмент крахмала и гликогена
α-гликозидная связь расположена
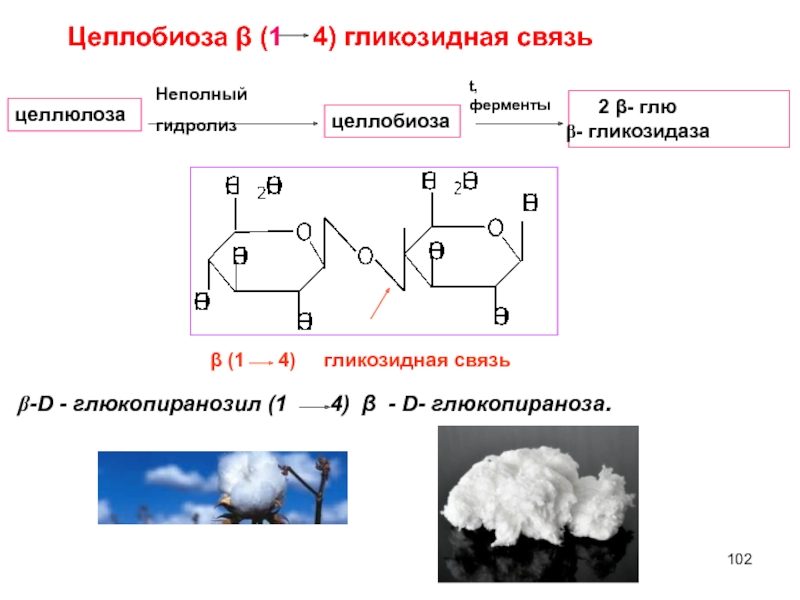
Слайд 102Целлобиоза β (1 4) гликозидная связь
2 β- глю
-
целлобиоза
Неполный гидролиз
β (1 4) гликозидная связь
-D - глюкопиранозил (1 4) β - D- глюкопираноза.
целлюлоза
t, ферменты
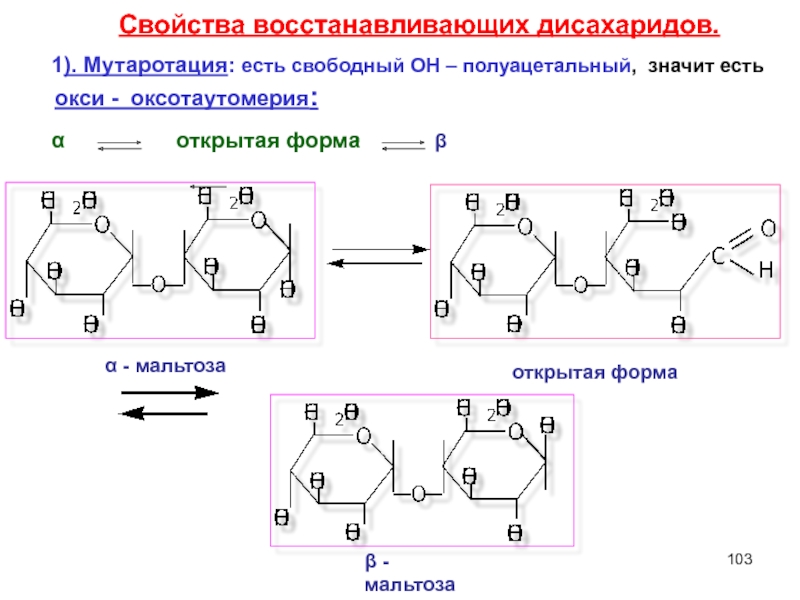
Слайд 1031). Мутаротация: есть свободный ОН – полуацетальный, значит есть
α
Свойства восстанaвливающих дисахаридов.
окси - оксотаутомерия:
α - мальтоза
открытая форма
β - мальтоза
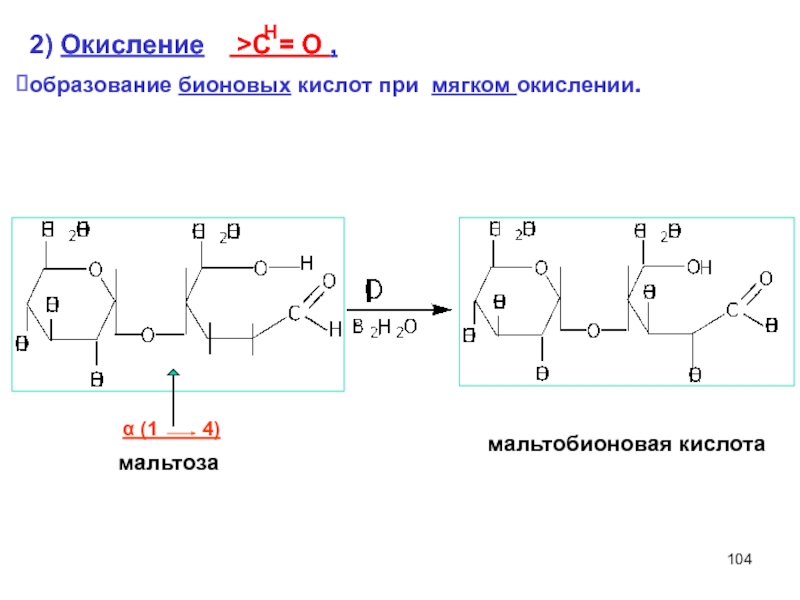
Слайд 1042) Окисление >C = O ,
образование бионовых кислот при мягком
α (1 4)
мальтобионовая кислота
мальтоза
Н
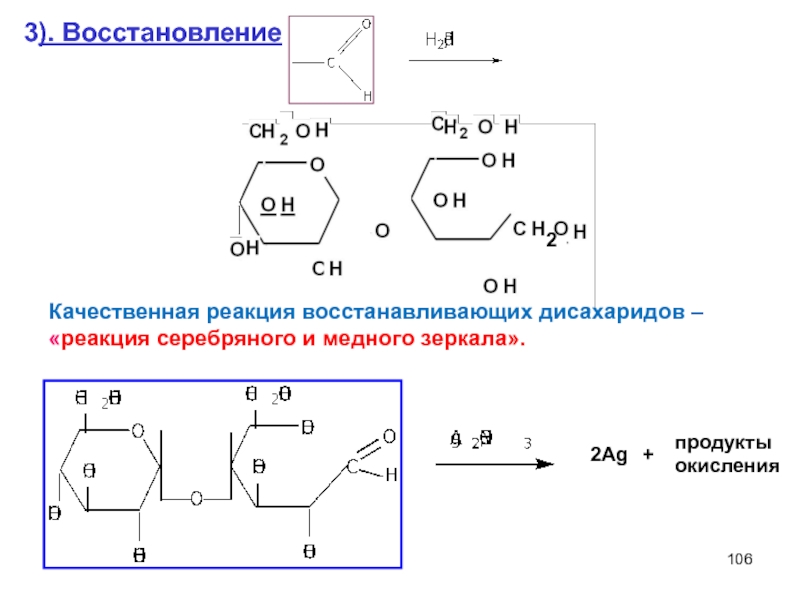
Слайд 1063). Восстановление
Качественная реакция восстанавливающих дисахаридов – «реакция серебряного и медного зеркала».
продукты
+
2
2Ag
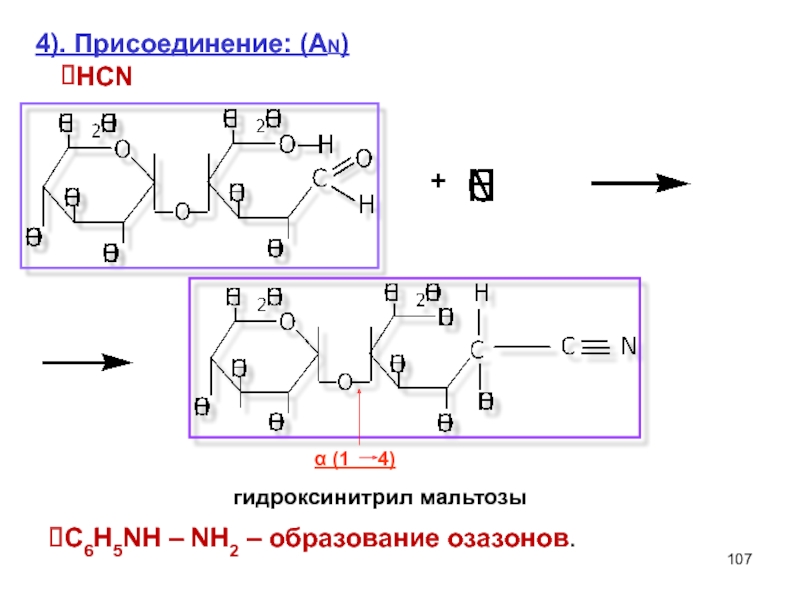
Слайд 1074). Присоединение: (AN)
HCN
гидроксинитрил мальтозы
α (1 4)
C6H5NH – NH2
+
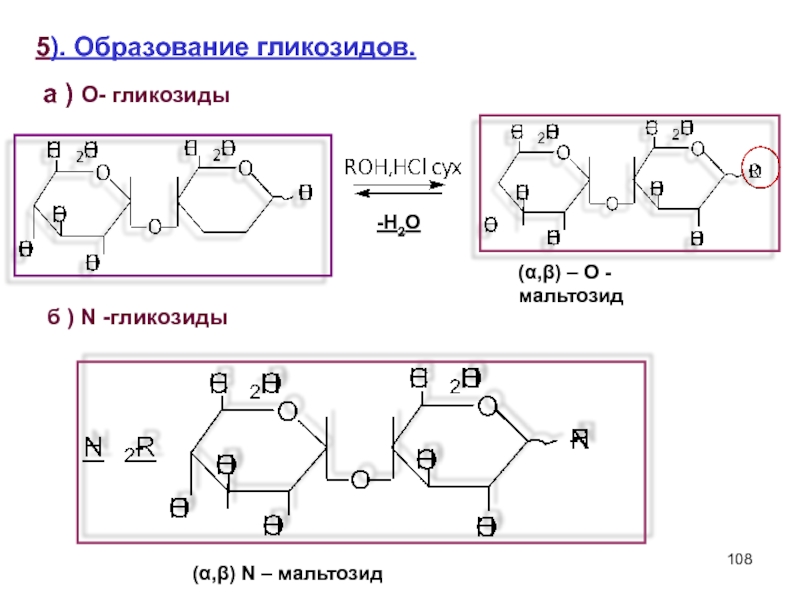
Слайд 1085). Образование гликозидов.
а ) O- гликозиды
(α,β) – О - мальтозид
б
(α,β) N – мальтозид
-H2O
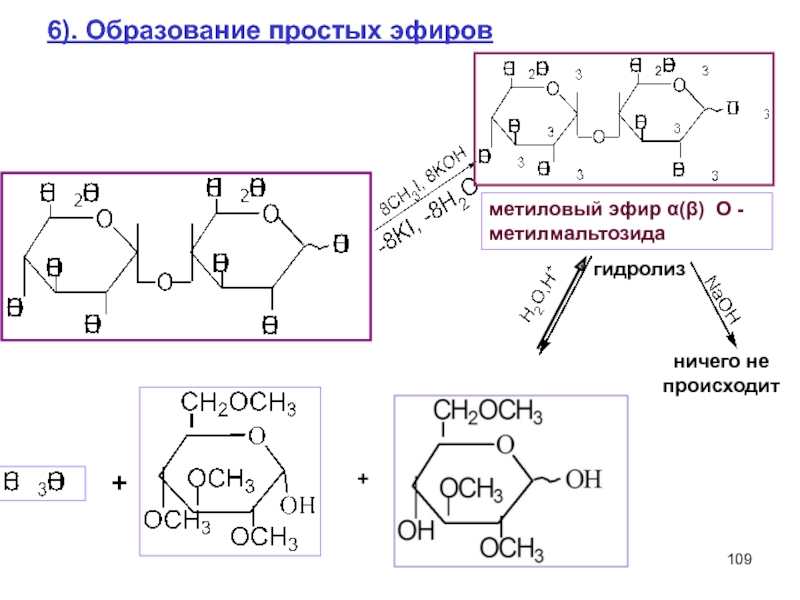
Слайд 1096). Образование простых эфиров
метиловый эфир α(β) О - метилмальтозида
гидролиз
ничего не
+
+
Слайд 111Выделенное и очищенное соединение идентифицируют путем сравнения его физических констант с
1.Температуры плавления и кипения
2.Плотность
3.Показатель преломления
4.Удельное вращение
5.Хроматографические и
6.Спектральные характеристики
Анализ органических соединений
Физико-химические и химические методы исследования и идентификации углеводов
Слайд 112Физико-химические и химические методы исследования и идентификации углеводов
Качественный функциональный анализ
Для установления
1.Для доказательства существования альдегидной группы используют её отличительную способность восстанавливать амммиачный раствор серебра (реактив Толленса) и щелочной раствор тартратного комплекса меди (II) (реактив Фелинга) :
2.Присутствие диольного рагмента определяют свежеосажденным гидроксидом меди (II) при комнатной температуре.
3.Присутствие енольного фрагмента подтверждается цветной реакцией с раствором хлорида железа (III).
Слайд 113Распределительная хроматография была впервые применена для разделения углеводов в 1949 г.
Тонкослойная хроматография (ТСХ) в том виде, в каком она известна сейчас впервые была описана Шталем 1958 г., а в 1961 г. появилось первое сообщение о применении ТСХ для разделения углеводов.
Начиная с этого времени ТСХ широко используется для идентификации углеводов, в том числе незамещенных моно- и олигосахаридов и различных производных сахаров и сложных эфиров, циклических ацеталей и других производных.
Хроматографические методы исследования
Слайд 114Компоненты:
1. Сахароза
2.Глюкоза
3.Галактоза
4. Фруктоза
Метод высокоэффективной жидкостной хроматографии
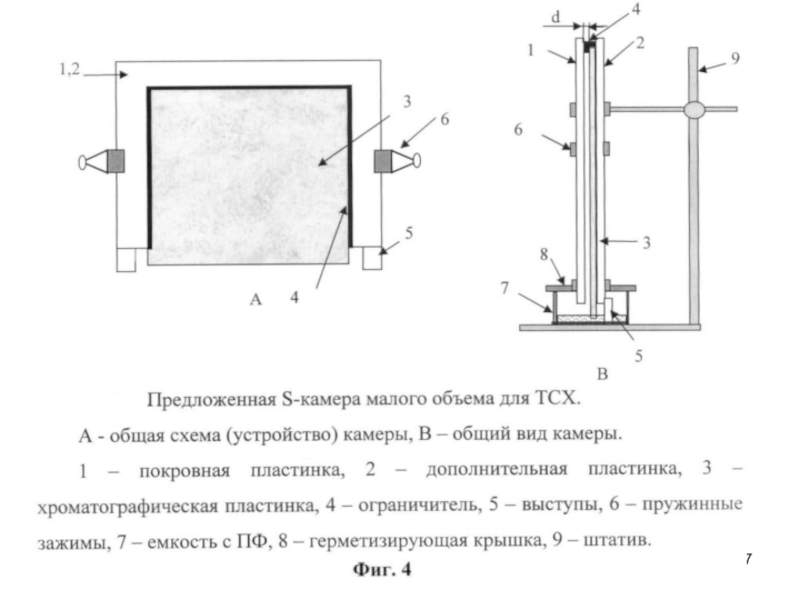
Слайд 118Хроматографические методы исследования
Тонкослойная хроматография находит все большее применение для количественного определения
Способы количественного определения делят на две большие группы:
а) прямое определение (установление количества вещества непосредственно на пластинке);
б) косвенное определение (элюирование пятен вещества с последующим анализом элюата физическими методами).





























![[O]4. Жесткое окислениесахарозатрикарбоновая кислота – 3 СООН](/img/tmb/3/276200/66d0b360ba39786deddf67b7eb80cf3f-800x.jpg)


![[O]Жесткое окислениеСвободная группас защитой полуцетального гидроксила](/img/tmb/3/276200/99d7c3a08a90d7b6faeef8357f95f3e3-800x.jpg)