- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Углеводороды. Свойства алканов презентация
Содержание
- 1. Углеводороды. Свойства алканов
- 2. Химические свойства алканов определяются его строением,
- 3. Химические свойства алканов 1. предельная насыщенность
- 4. Химические свойства алканов 2. симметричность неполярных
- 5. Крекинг алканов реакции расщепления углеродного скелета крупных
- 6. Крекинг алканов Распад связей происходит гомолитически с образованием свободных радикалов: 01.04.2016
- 7. Крекинг алканов Свободные радикалы очень активны. Один
- 8. Крекинг алканов 01.04.2016 Разрыв С–С–связи возможен в любом случайном месте молекулы.
- 9. Крекинг алканов образуется смесь алканов и алкенов
- 10. Крекинг алканов В общем виде этот процесс можно выразить схемой: 01.04.2016
- 11. Крекинг алканов При более высокой температуре (свыше
- 12. Галогенопроизводные алканов (галогеналканы) имеют очень важное значение
- 13. Галогенопроизводные алканов (галогеналканы) Галогенопроизводные алканов широко применяются
- 14. Галогенопроизводные алканов (галогеналканы) Чтобы получить алкан с
- 15. Нуклеофильное замещение (SN) 01.04.2016 положительно заряженный
- 16. Механизм-1 (SN1) - двухстадийный 01.04.2016 Cтадия 1.
- 17. Механизм-1 (SN1) - двухстадийный 01.04.2016 Cтадия 2.
- 18. Механизм-2 (SN2) - одностадийный 01.04.2016 заключается в
- 19. Получение алканов 01.04.2016 Алканы выделяют из
- 20. Получение алканов 1. Крекинг нефти (промышленный
- 21. Получение алканов 2. Гидpиpование непpедельных углеводоpодов: 01.04.2016
- 22. Получение алканов 3. Газификация твердого топлива
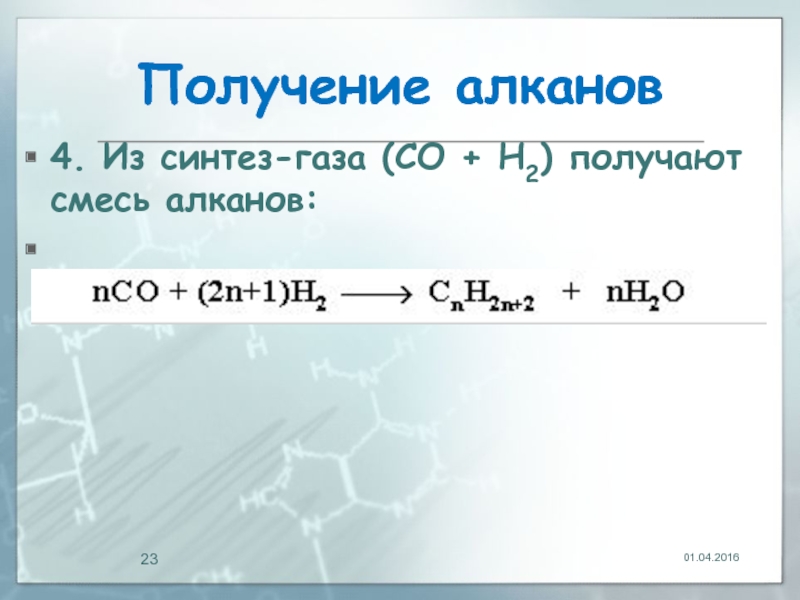
- 23. Получение алканов 4. Из синтез-газа (СО + Н2) получают смесь алканов: 01.04.2016
- 24. Получение алканов 5. Синтез более сложных
- 25. Получение алканов 6. Из солей карбоновых
- 26. Получение алканов 7. Разложение карбидов металлов (метанидов) водой: 01.04.2016
- 27. Применение алканов Алканы – основной источник
- 28. Применение алканов Газообразные алканы (метан и
- 29. Применение алканов Вазелиновое масло (смесь жидких
- 30. Применение алканов Паpафин (смесь твеpдых углеводоpодов
- 31. Применение алканов В современной нефтехимической промышленности
- 32. Применение алканов Алканы – основной источник
- 33. 1.Контрольная работа 01.04.2016 Напишите полные структурные и
- 34. 2. Контрольная работа 01.04.2016 Дайте названия радикалам
- 35. 3.Контрольная работа 01.04.2016 Напишите процесс расщепления для
- 36. 4. Контрольная работа 01.04.2016 Написать уравнение реакции
Слайд 1Основы органической химии
Семинар-7. Углеводороды.
Свойства алканов.
E-mail: irkrav66@gmail.com
лектор:
проф. Рохин Александр
Слайд 2Химические свойства алканов
определяются его строением, т.е. природой входящих в его
Исходя из справочных данных о связях С–С и С–Н, можно предсказать, какие реакции характерны для алканов
01.04.2016
Слайд 3Химические свойства алканов
1. предельная насыщенность алканов не допускает реакций присоединения,
01.04.2016
Слайд 4Химические свойства алканов
2. симметричность неполярных С–С и слабополярных С–Н ковалентных
01.04.2016
Слайд 5Крекинг алканов
реакции расщепления углеродного скелета крупных молекул при нагревании и в
Два вида крекинга:
- термический (без доступа воздуха)
- каталитический
01.04.2016
Слайд 6Крекинг алканов
Распад связей происходит гомолитически с образованием свободных радикалов:
01.04.2016
Слайд 7Крекинг алканов
Свободные радикалы очень активны.
Один из них (например, этил) отщепляет атомарный
Другой радикал, став двухвалентным, превращается в алкен (бутен-1) за счет образования p–связи при спаривании двух электронов у соседних атомов:
01.04.2016
Слайд 9Крекинг алканов
образуется смесь алканов и алкенов с меньшей, чем у исходного
01.04.2016
Слайд 11Крекинг алканов
При более высокой температуре (свыше 1000°С) происходит разрыв не только
термический крекинг метана используется для получения сажи (чистый углерод) и водорода:
01.04.2016
Слайд 12Галогенопроизводные алканов (галогеналканы)
имеют очень важное значение для синтеза многих соединений. Замена
Общий вид – СnH2n+2-xHalx.
01.04.2016
Слайд 13Галогенопроизводные алканов (галогеналканы)
Галогенопроизводные алканов широко применяются для синтеза алканов с заданным
Для этого используется реакция взаимодействия их с активными металлами (реакция Вюрца-получение чётных алканов):
01.04.2016
Слайд 14Галогенопроизводные алканов (галогеналканы)
Чтобы получить алкан с нечётным количеством атомов углерода потребуется
01.04.2016
Слайд 15Нуклеофильное
замещение (SN)
01.04.2016
положительно заряженный углеродный атом, связанный с галогеном, является центром
Слайд 16Механизм-1 (SN1) - двухстадийный
01.04.2016
Cтадия 1. Алкилгалогенид, отщепляя галоген (электролитическая диссоциация), превращается
Стадия 1 является лимитирующей. Поскольку в ней участвует только одна частица
Слайд 17Механизм-1 (SN1) - двухстадийный
01.04.2016
Cтадия 2. Карбокатион взаимодействует с нуклеофилом (донором пары
Слайд 18Механизм-2 (SN2) - одностадийный
01.04.2016
заключается в практически одновременном отщеплении галогенид-иона и присоединении
Слайд 19Получение алканов
01.04.2016
Алканы выделяют из природных источников:
- природный и попутный газы,
- нефть,
- каменный уголь.
Используются также синтетические методы.
Слайд 20Получение алканов
1. Крекинг нефти (промышленный способ):
При крекинге алканы получаются
при разрыве молекул высших алканов получается очень ценное сырье для органического синтеза: пропан, бутан, изобутан, изопентан
01.04.2016
Слайд 22Получение алканов
3. Газификация твердого топлива (при повышенной температуре и давлении,
01.04.2016
Слайд 24Получение алканов
5. Синтез более сложных алканов из галогенопpоизводных с меньшим
01.04.2016
Слайд 25Получение алканов
6. Из солей карбоновых кислот:
а) сплавление со щелочью
б) электролиз по Кольбе:
01.04.2016
Слайд 27Применение алканов
Алканы – основной источник природного углеводородного сырья.
Предельные углеводороды находят
01.04.2016
Слайд 28Применение алканов
Газообразные алканы (метан и пpопан-бутановая смесь) используются в качестве
Жидкие углеводоpоды составляют значительную долю в моторных и ракетных топливах и используются в качестве растворителей.
01.04.2016
Слайд 29Применение алканов
Вазелиновое масло (смесь жидких углеводоpодов с числом атомов углерода
Вазелин (смесь жидких и твеpдых пpедельных углеводоpодов с числом углеpодных атомов до 25) пpименяется для пpиготовления мазей, используемых в медицине
01.04.2016
Слайд 30Применение алканов
Паpафин (смесь твеpдых углеводоpодов С19-С35) - белая твеpдая масса
пpименяется для изготовления свечей, пpопитки спичек и упаковочной бумаги, для тепловых пpоцедуp в медицине и салонах красоты
01.04.2016
Слайд 31Применение алканов
В современной нефтехимической промышленности предельные улеводороды являются базой для
01.04.2016
Слайд 32Применение алканов
Алканы – основной источник природного углеводородного сырья.
Предельные углеводороды находят
01.04.2016
Слайд 331.Контрольная работа
01.04.2016
Напишите полные структурные и электронные формулы;
- пропана
- октана
Слайд 342. Контрольная работа
01.04.2016
Дайте названия радикалам следующих алканов:
- пропан
- декан
- этан
- пентан
- гексан
Слайд 353.Контрольная работа
01.04.2016
Напишите процесс расщепления для следующих алканов, используя общую формулу крекинга
- декан
- гептан
Слайд 364. Контрольная работа
01.04.2016
Написать уравнение реакции 9по какому механизму оно протекает –
Alk-Hal + OH- —>