- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Типы кристаллических решеток, cингонии. (Лекция 2) презентация
Содержание
- 1. Типы кристаллических решеток, cингонии. (Лекция 2)
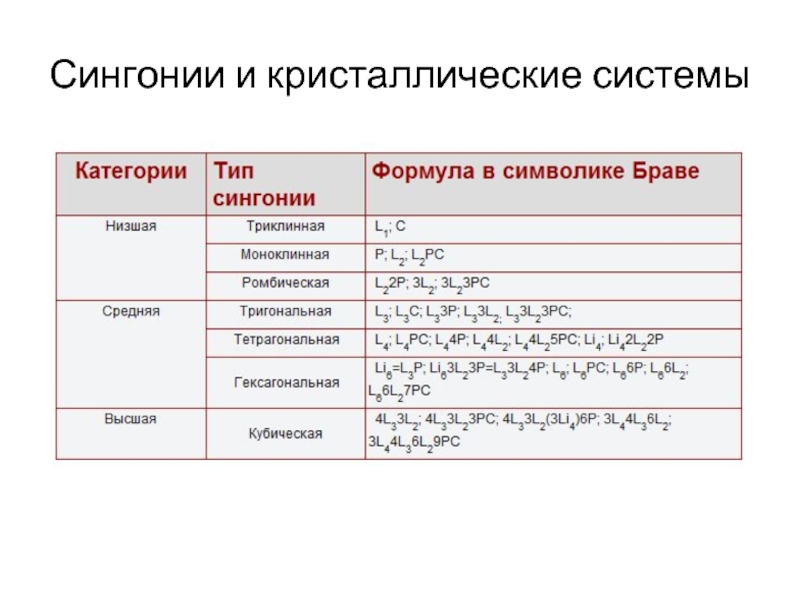
- 2. Сингонии и кристаллические системы
- 3. Типы кристаллических решеток Примитивная Объемно-центрированная (ОЦК) Гранецентрированная (ГЦК) Гексагональная плотноупакованная (ГПУ)
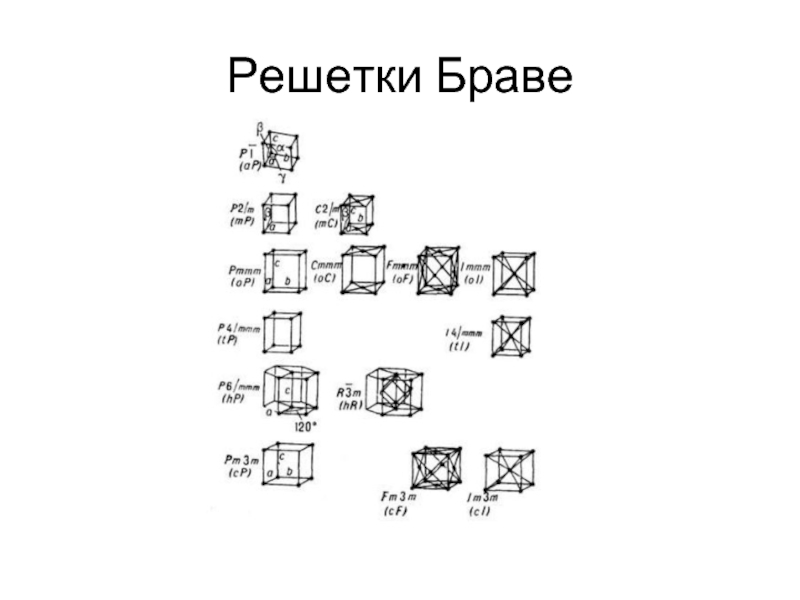
- 4. Решетки Браве
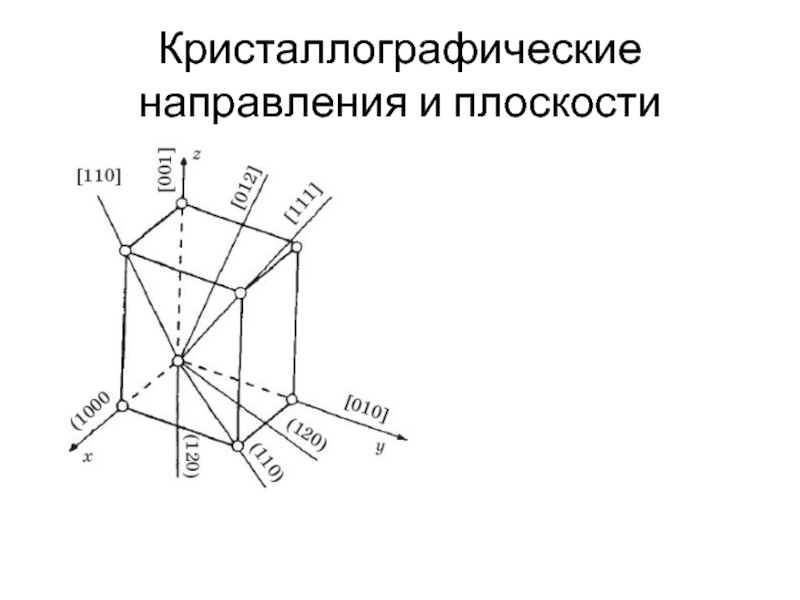
- 5. Кристаллографические направления и плоскости
- 6. Обозначение кристаллографических плоскостей
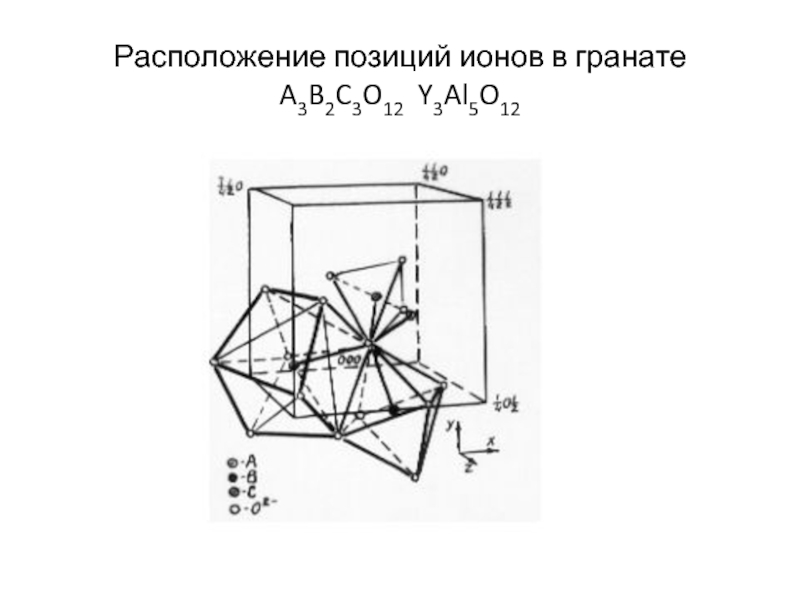
- 7. Расположение позиций ионов в гранате A3B2C3O12 Y3Al5O12
- 8. А – элементы; В – соединения
- 9. Основные структурные типы Структура Меди Au,
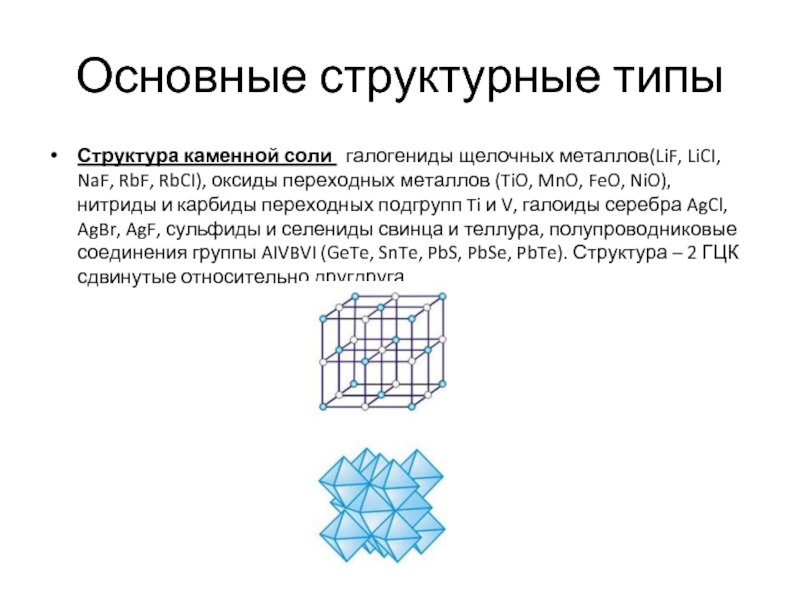
- 10. Основные структурные типы Структура каменной соли
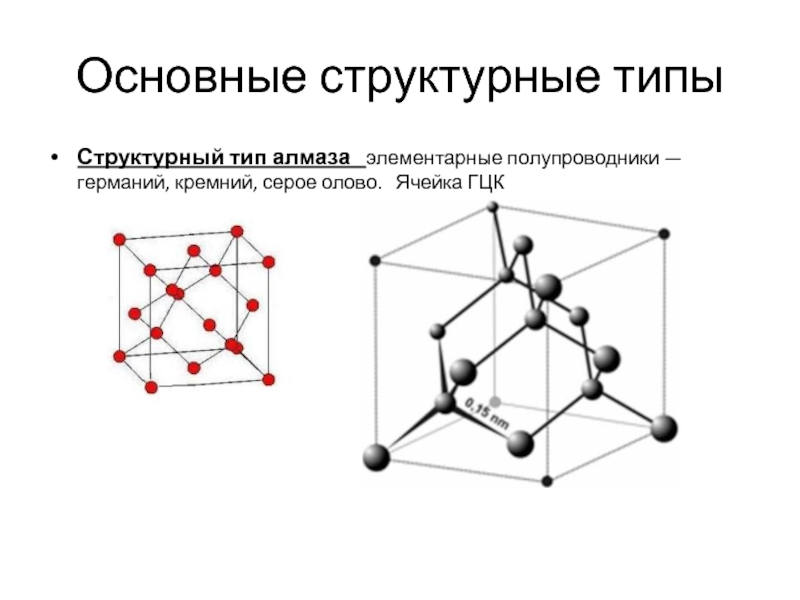
- 11. Основные структурные типы Структурный тип алмаза
- 12. Основные структурные типы Структурный тип сфалерита и
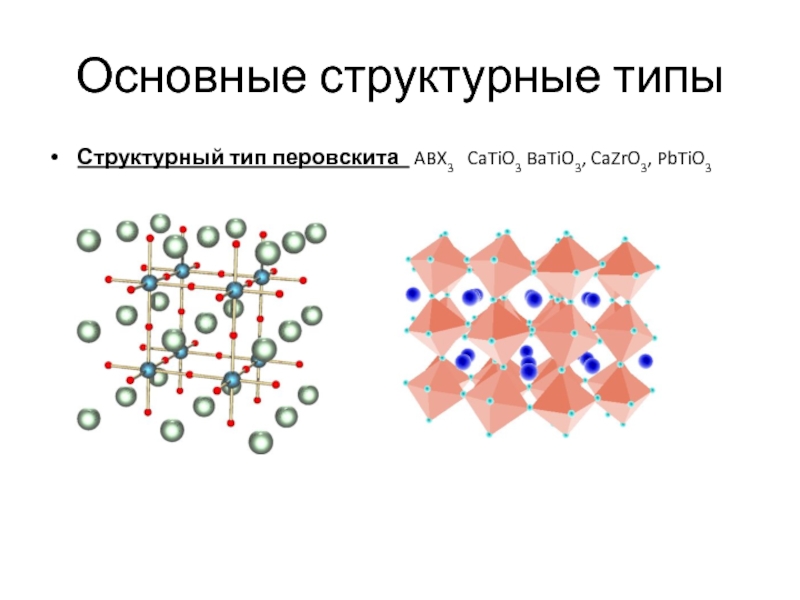
- 13. Основные структурные типы Структурный тип перовскита ABX3 CaTiO3 BaTiO3, CaZrO3, PbTiO3
- 14. Основные структурные типы Структурный тип шпинели X
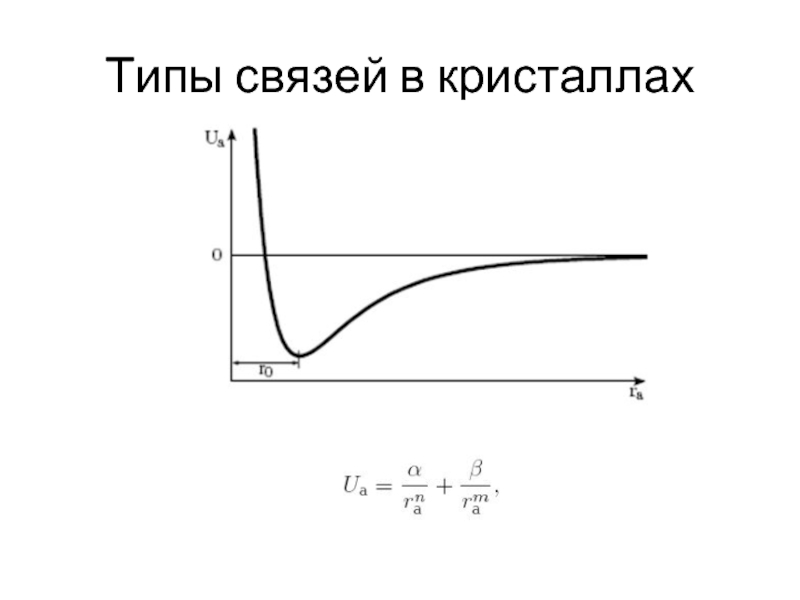
- 15. Типы связей в кристаллах
- 16. Типы связей в кристаллах. Ионная Ковалентная Ван-дер-вальсова металлическая
- 17. Дефекты в кристаллах Дефект – это
- 18. Точечные дефекты в кристаллах По Шотки
- 19. Обозначения дефектов по Крегеру-Винку V′А V′′А V·Х
- 21. Дефекты
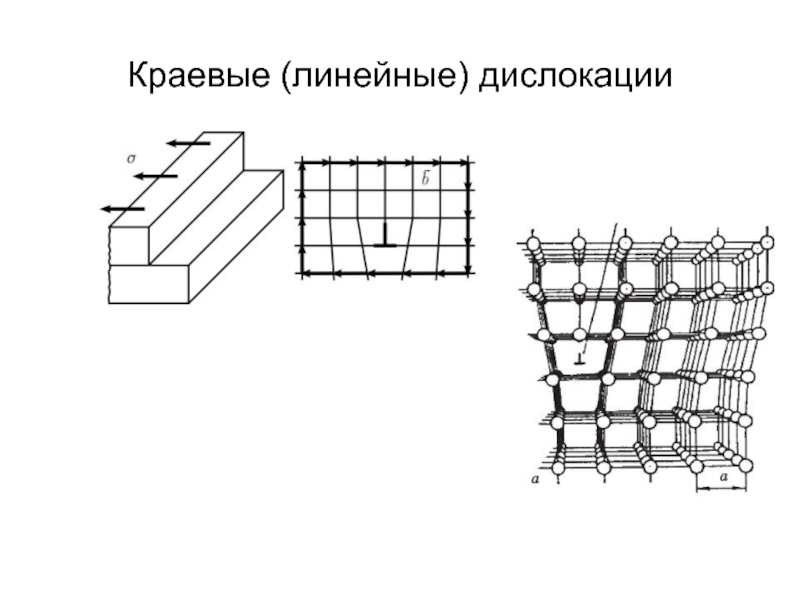
- 22. Краевые (линейные) дислокации
- 23. Винтовые дислокации ? = ½ ??2, где
- 24. Поверхностные дефекты Блоки Двойники Дефекты упаковки Границы зерен
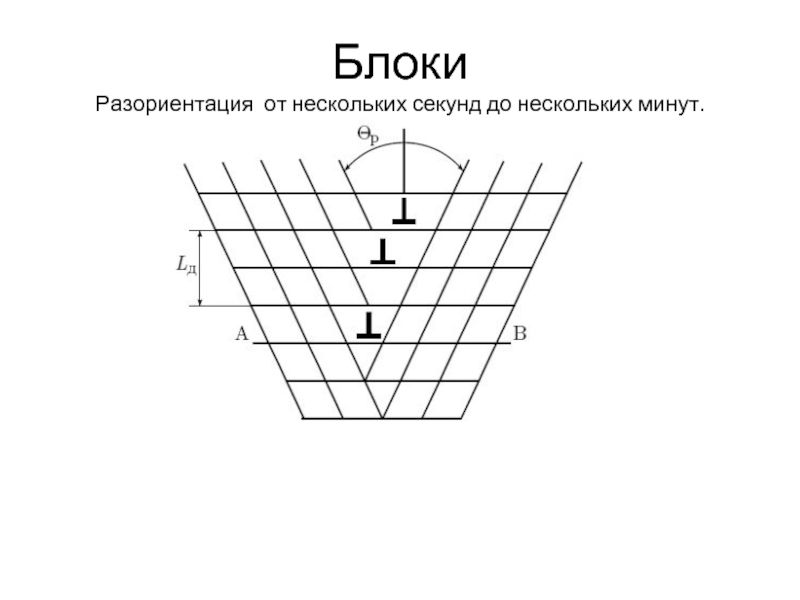
- 25. Блоки Разориентация от нескольких секунд до нескольких минут.
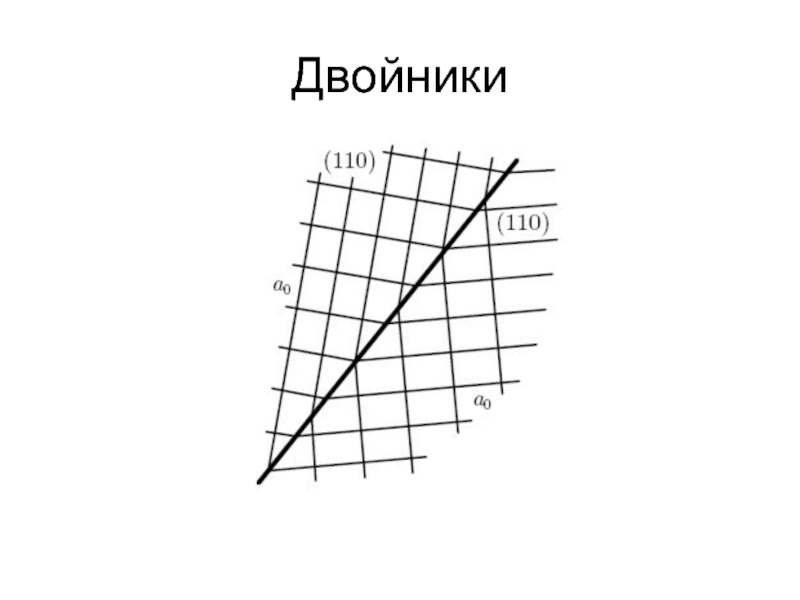
- 26. Двойники
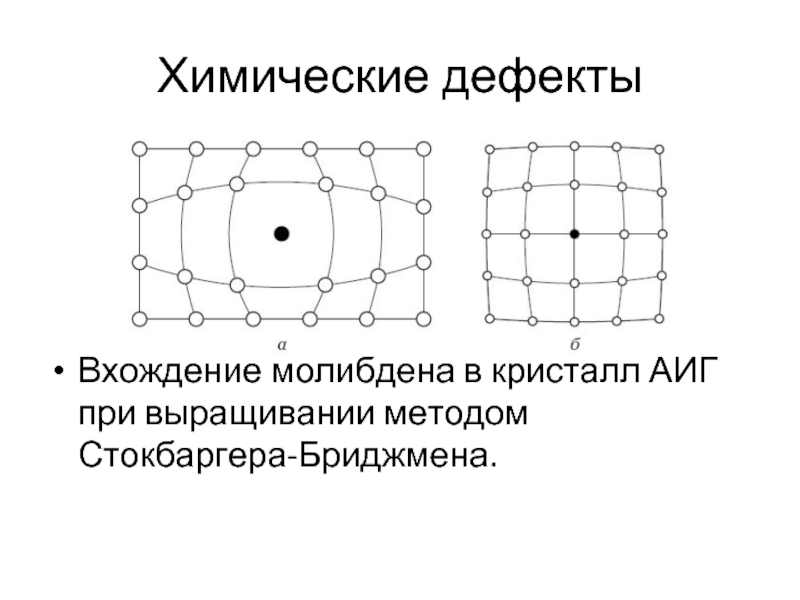
- 27. Химические дефекты Вхождение молибдена в кристалл АИГ при выращивании методом Стокбаргера-Бриджмена.
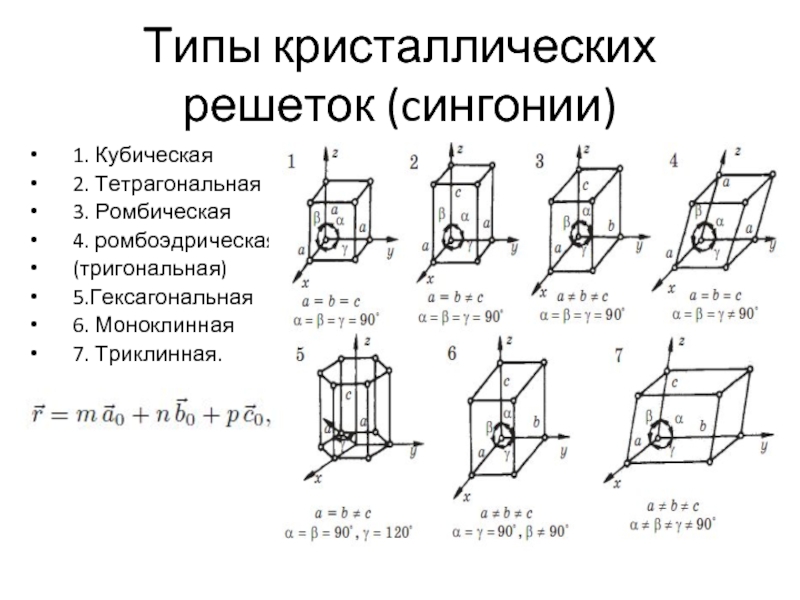
Слайд 1Типы кристаллических решеток (cингонии)
1. Кубическая
2. Тетрагональная
3. Ромбическая
4. ромбоэдрическая
(тригональная)
5.Гексагональная
6. Моноклинная
7. Триклинная.
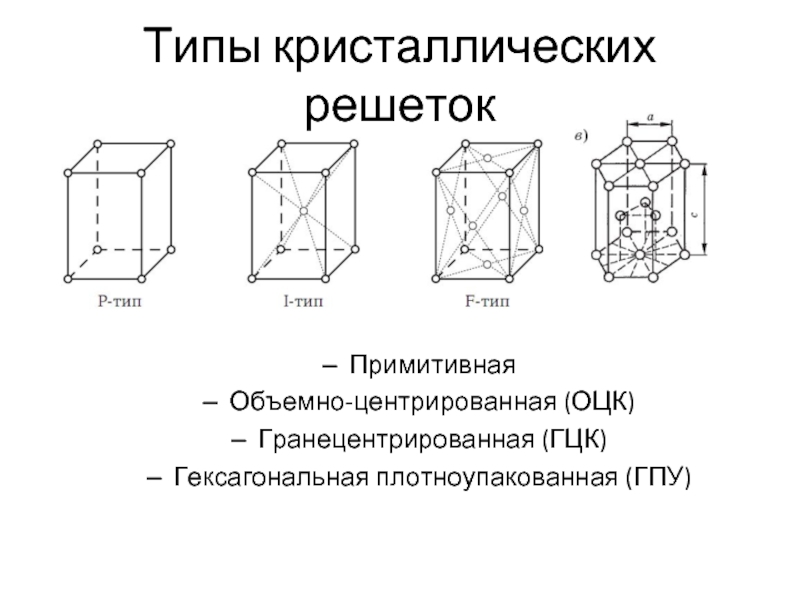
Слайд 3Типы кристаллических решеток
Примитивная
Объемно-центрированная (ОЦК)
Гранецентрированная (ГЦК)
Гексагональная плотноупакованная (ГПУ)
Слайд 8А – элементы;
В – соединения типа АВ (например, NaCl, CsI);
С –
D - соединения типа AnBm (Al2O3);
E – соединения, образованные больше, чем двумя сортами атомов без радикалов или комплексных ионов (например, CuFeS);
F –структуры соединений с двух- или трехатомными ионами (KCNS, NaHF2);
G – соединения с четырехатомными ионами (CaCO3, NaClO3);
H – соединения с пятиатомными ионами (CaSО4.2H2O, CaWO4);
L – сплавы;
S –силикаты. (гранаты A3B2(SiO4)3
Группы структурных типов
Слайд 9Основные структурные типы
Структура Меди Au, Ag, Ni, Al, Pb. Твердые
Структура Вольфрама хром, ванадий, молибден, ниобий, тантал, -кобальт, -железо, титан, цирконий, гафний, щелочные элементы — литий, натрий, калий, рубидий, цезий, щелочноземельные — кальций, стронций, барий, актиниды — уран, нептуний, плутоний. Ячейка ОЦК , 2 атома на ячейку.
Слайд 10Основные структурные типы
Структура каменной соли галогениды щелочных металлов(LiF, LiCI, NaF,
Слайд 11Основные структурные типы
Структурный тип алмаза элементарные полупроводники — германий, кремний,
Слайд 12Основные структурные типы
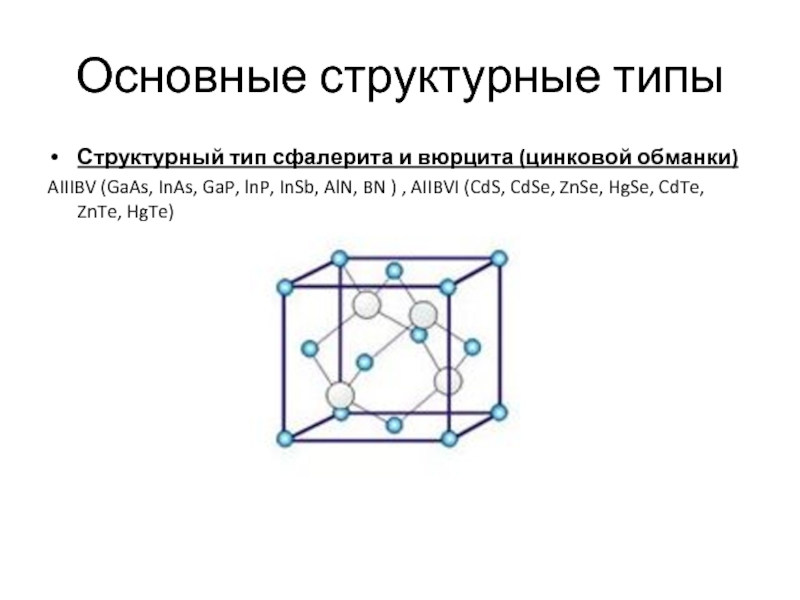
Структурный тип сфалерита и вюрцита (цинковой обманки)
AIIIBV (GaAs, InAs,
Слайд 14Основные структурные типы
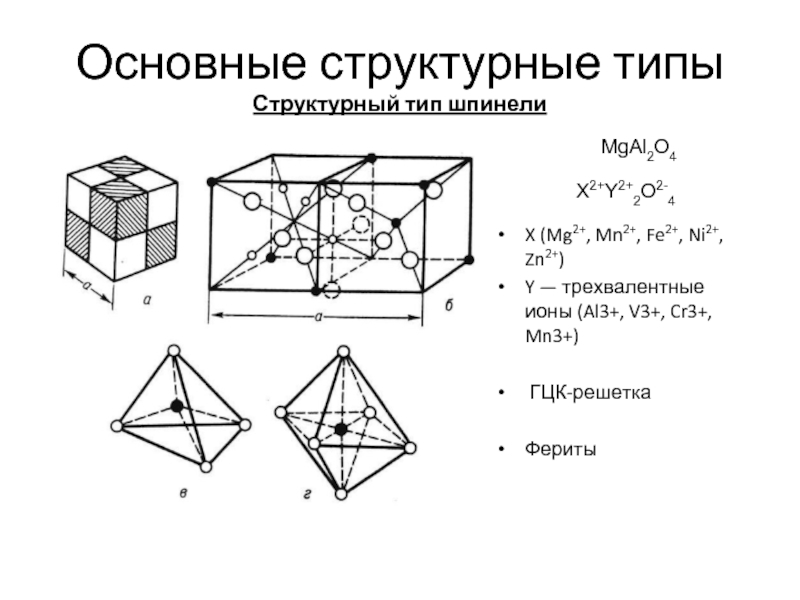
Структурный тип шпинели
X (Mg2+, Mn2+, Fe2+, Ni2+, Zn2+)
Y —
ГЦК-решетка
Фериты
MgAl2O4
X2+Y2+2O2-4
Слайд 17Дефекты в кристаллах
Дефект – это нарушение идеальной структуры кристалла.
Классификация дефектов
· Нульмерные (точечные) дефекты – вакансии, межузельные атомы, примесные атомы, антиструктурные дефекты и т.д.
· Одномерные (линейные) дефекты – цепочки точечных дефектов, дислокации, дисклинации.
· Двумерные (поверхностные) дефекты – дефекты упаковки, границы
блоков мозаики, двойников, зерен, межфазные границы, поверхность
кристалла.
· Трёхмерные (объёмные) дефекты – поры, включения второй фазы.
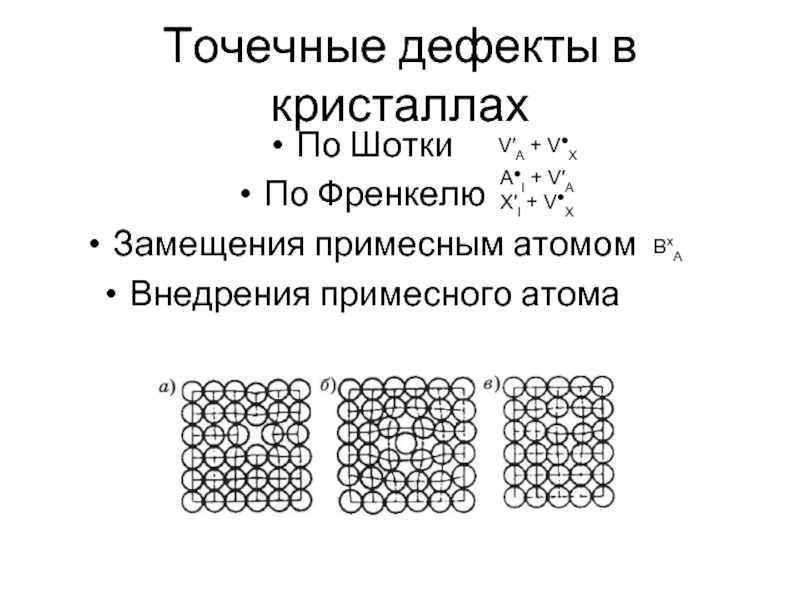
Слайд 18Точечные дефекты в кристаллах
По Шотки
По Френкелю
Замещения примесным атомом
Внедрения примесного
V′А + V●Х
А●I + V′А
X′I + V●Х
ВxA
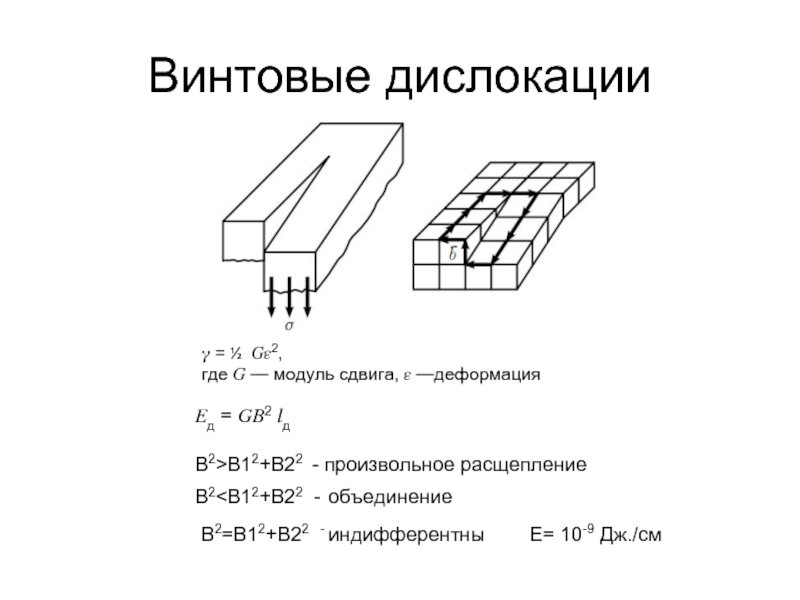
Слайд 23Винтовые дислокации
? = ½ ??2,
где ? — модуль сдвига, ? —деформация
?д = ??2 ?д
B2>B12+B22 - произвольное расщепление
B2 B2=B12+B22 - индифферентны E= 10-9 Дж./см