- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Типы химических реакций на примере свойств воды презентация
Содержание
- 1. Типы химических реакций на примере свойств воды
- 2. Н2О Мr(Н2О)=18 Физические свойства Нахождение в природе Химические свойства Применение
- 3. Н2О Мr(Н2О)=18 Физические свойства
- 4. Физические свойства Нахождение в природе Химические
- 5. 1) Реакции разложения: Электролиз воды: 2 H2O
- 6. Реакции соединения: А) С оксидами металлов: С
- 7. Реакции соединения: А) С оксидами металлов: С
- 8. Реакции соединения: Б) С оксидами неметаллов: НеМеО
- 9. Правило: Вода реагирует с оксидами металлов и
- 10. Реакции замещения: Щелочные и щелочноземельные металлы реагируют
- 11. Реакции обмена: Обменное взаимодействие веществ с
- 12. Реакции обмена: Обменное взаимодействие веществ с
- 13. Реакции обмена: Обменное взаимодействие веществ с
- 14. Реакции обмена: Обменное взаимодействие веществ с
- 15. Физические свойства Нахождение в природе Химические
- 16. Вариант № 1 1) 2) Напишите
- 17. Домашнее задание: § 33, № 1 (б - д), 2, 4, с. 173
Слайд 3
Н2О
Мr(Н2О)=18
Физические свойства
Нахождение в природе
Химические свойства
Применение
Атмосфера
2. Гидросфера
3. Литосфера
4. Биосфера
5. Космос
Нахождение в природе
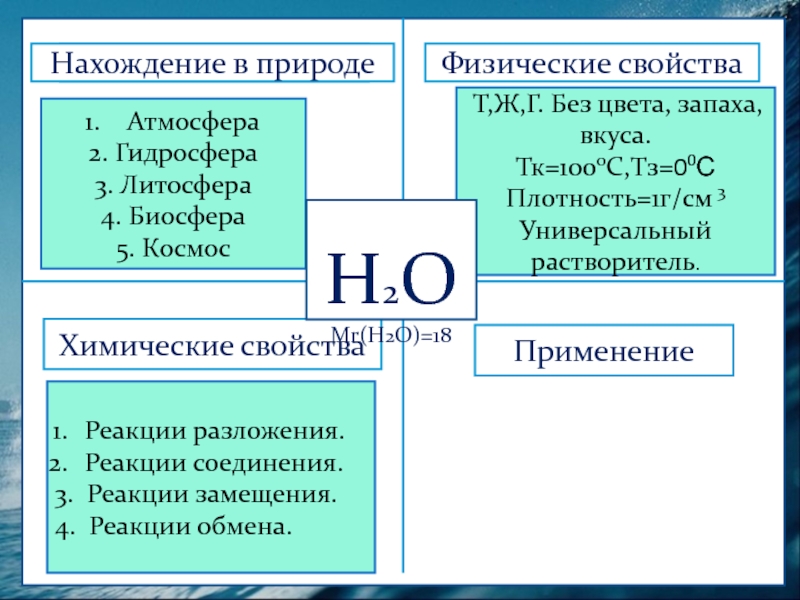
Слайд 4
Физические свойства
Нахождение в природе
Химические свойства
Применение
Атмосфера
2. Гидросфера
3. Литосфера
4. Биосфера
5. Космос
Нахождение в природе
Т,Ж,Г. Без цвета, запаха, вкуса.
Тк=1000С,Тз=00С Плотность=1г/см 3
Универсальный растворитель.
Н2О
Мr(Н2О)=18
Реакции разложения.
Реакции соединения.
3. Реакции замещения.
4. Реакции обмена.
Слайд 6Реакции соединения:
А) С оксидами металлов:
С оксидами щелочных металлов ( Li ,
C оксидами щелочноземельных металлов (Ca, Sr, Ba)
MeO + H2O → Me+n(OH)n
Пример: СаО + H2O → Са+2(OH)2
негашеная известь гашеная известь
Na2O + H2O → Na+1OH
Слайд 7Реакции соединения:
А) С оксидами металлов:
С оксидами щелочных металлов ( Li ,
C оксидами щелочноземельных металлов (Ca, Sr, Ba)
MeO + H2O → Me+n(OH)n
Пример: СаО + H2O → Са+2(OH)2
негашеная известь гашеная известь
Na2O + H2O → 2Na+1OH
Слайд 8Реакции соединения:
Б) С оксидами неметаллов:
НеМеО + Н2О → Нn(КО)-n
N2O3 + H2O → 2HNO2
N2O5 + H2O → 2HNO3
Ст. ок. элемента, образующего оксид остается неизменной.
Основания и кислородсодержащие кислоты называются общим словом – гидроксиды.
Слайд 9Правило:
Вода реагирует с оксидами металлов и оксидами неметаллов в том случае,
Слайд 10Реакции замещения:
Щелочные и щелочноземельные металлы реагируют с водой по схеме:
Me +
K + H2O → K+OH+ H2↑
Ca + H2O → Ca+2(OH)2+ H2↑
Слайд 11Реакции обмена:
Обменное взаимодействие веществ с водой, приводящее к их разложению,
Al2S3 + HOH → Al(OH)3↓ + H2S↑
СаС2 + Н2О → Са(ОН)2 + С2Н2
Слайд 12Реакции обмена:
Обменное взаимодействие веществ с водой, приводящее к их разложению,
Al2S3 + HOH → 2Al(OH)3 + H2S
СаС2 + Н2О → Са(ОН)2 + С2Н2
Слайд 13Реакции обмена:
Обменное взаимодействие веществ с водой, приводящее к их разложению,
Al2S3 + HOH → 2Al(OH)3 + 3H2S
СаС2 + Н2О → Са(ОН)2 + С2Н2
Слайд 14Реакции обмена:
Обменное взаимодействие веществ с водой, приводящее к их разложению,
Al2S3 + 6HOH → 2Al(OH)3 + 3H2S
СаС2 + Н2О → Са(ОН)2 + С2Н2
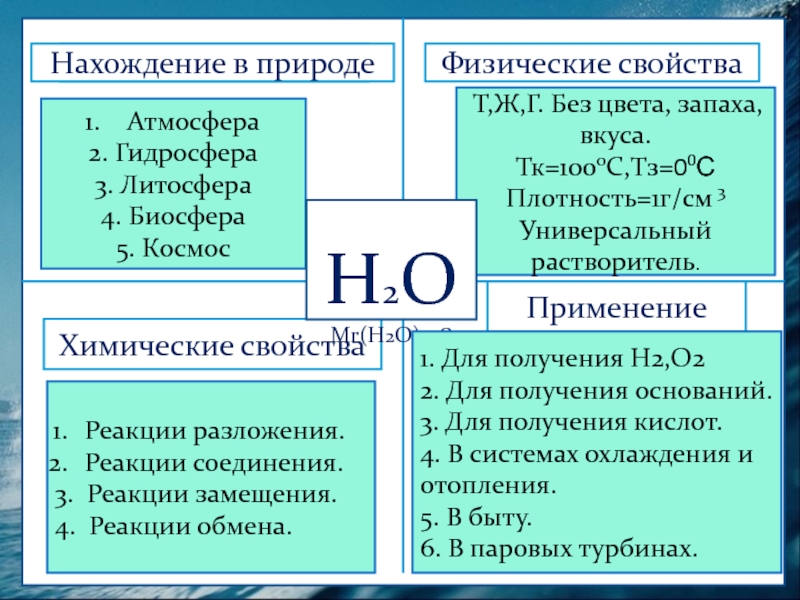
Слайд 15
Физические свойства
Нахождение в природе
Химические свойства
Применение
Атмосфера
2. Гидросфера
3. Литосфера
4. Биосфера
5. Космос
Нахождение в природе
Т,Ж,Г. Без цвета, запаха, вкуса.
Тк=1000С,Тз=00С Плотность=1г/см 3
Универсальный растворитель.
Н2О
Мr(Н2О)=18
Реакции разложения.
Реакции соединения.
3. Реакции замещения.
4. Реакции обмена.
1. Для получения Н2,О2
2. Для получения оснований.
3. Для получения кислот.
4. В системах охлаждения и отопления.
5. В быту.
6. В паровых турбинах.
Слайд 16Вариант № 1
1)
2) Напишите уравнение реакции взаимодействия кальция с кислородом и
3)
Вариант № 2
1)
2) Напишите уравнение реакции взаимодействия железа с хлором и лития с водой.
3)