величина зависит только от природы реагирующих веществ и температуры.
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Термодинамическое равновесие презентация
Содержание
- 1. Термодинамическое равновесие
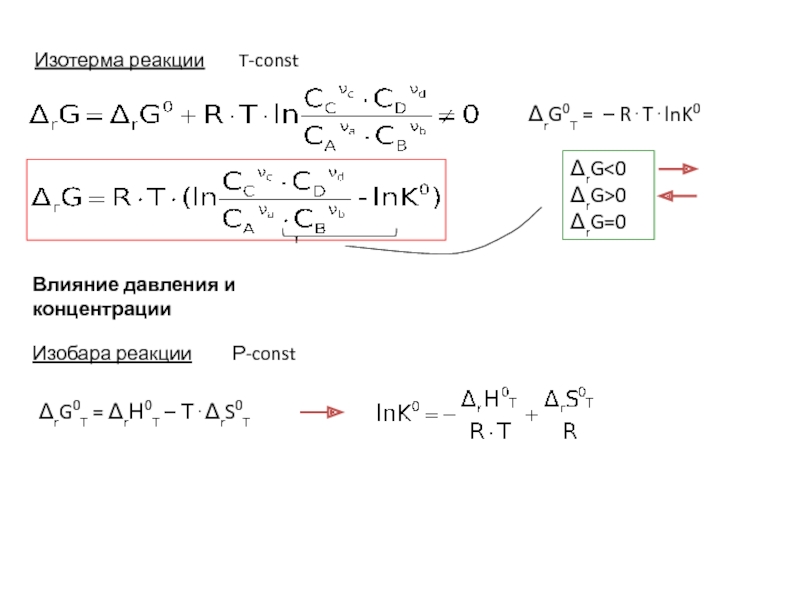
- 2. Изобара реакции Р-const ΔrG0T = ΔrН0T – Т⋅ΔrS0T Влияние давления и концентрации
- 3. Сдвиг равновесия Изобара реакции Р-const ΔrН00 – K(T)
- 4. Химическое равновесие Термодинамические параметры: T; P; νi;
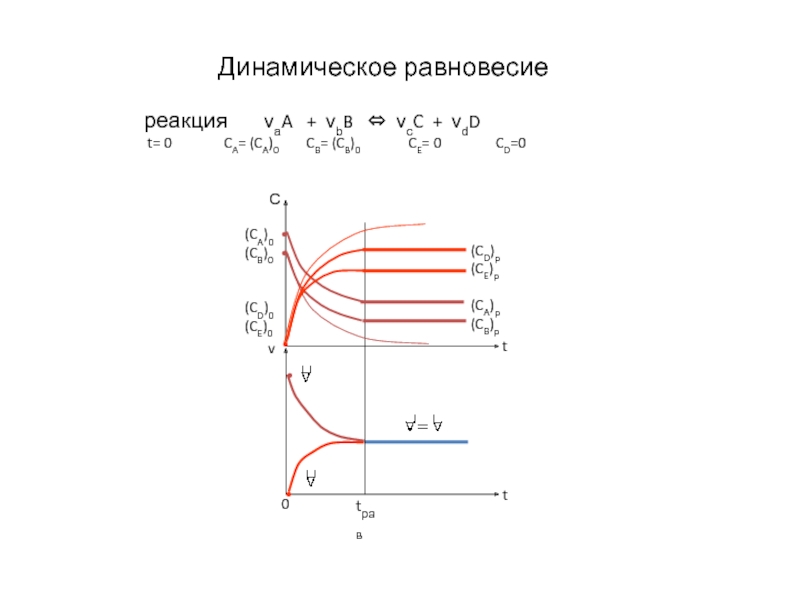
- 5. Динамическое равновесие реакция νаA + νbB
- 6. Константа равновесия KX - концентрации задаются мольными
- 7. Равновесие в растворах
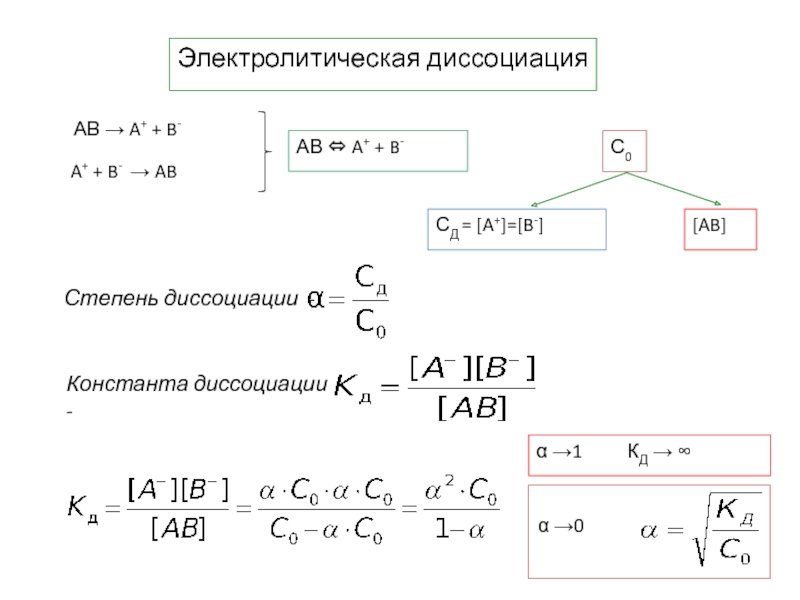
- 8. Электролитическая диссоциация С0 α →1 КД → ∞
- 10. Диссоциация воды H2O ⇔ H+ + OH-
- 11. Водородный показатель pH = –lg[H+] Нейтральная среда
- 12. Произведение растворимости [Kat+]= x·C [моль/л] [An-]= y·C [моль/л]
- 13. Число компонентов - К Компонент –
- 14. Число степеней свободы равновесной термодинамической системы С
- 15. Диаграмма состояния однокомпонентной системы (К=1) Н2О Ф=2
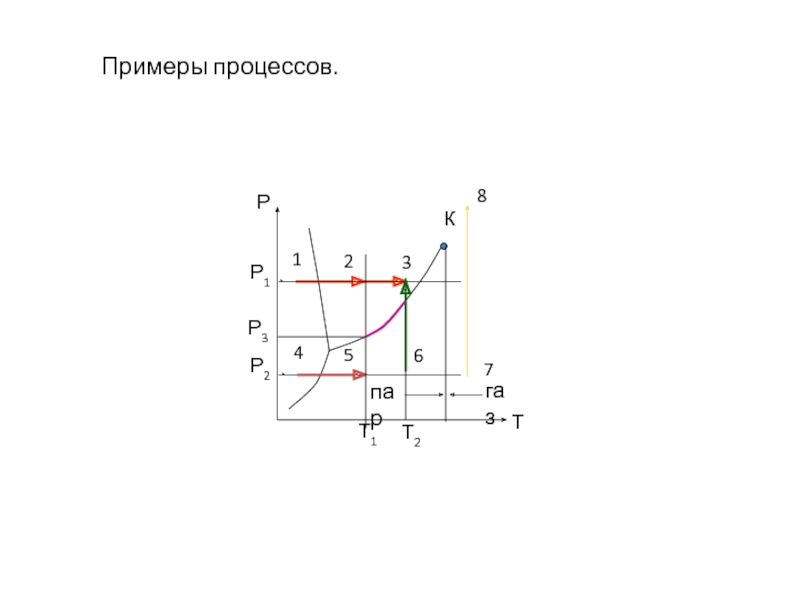
- 16. Примеры процессов.
- 17. Двухкомпонентная система (К=2) α→0 Двухфазное равновесие
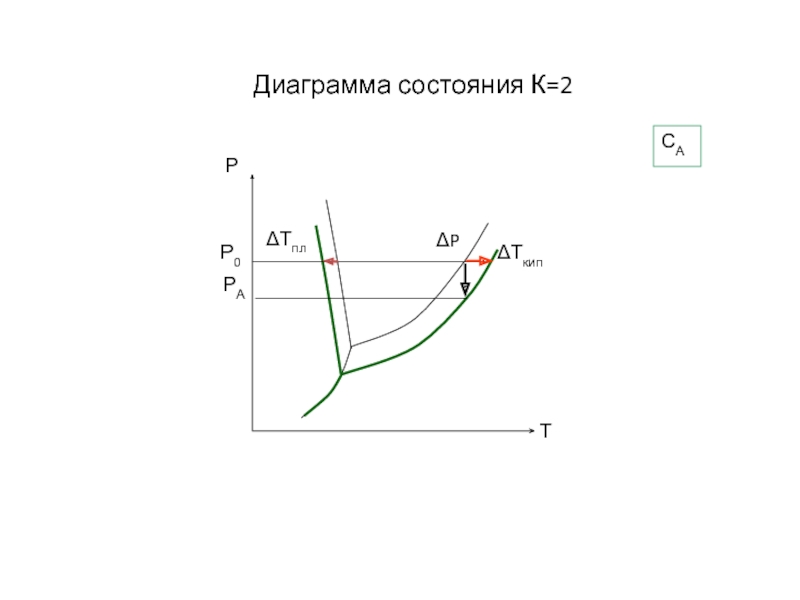
- 18. Диаграмма состояния К=2 СА
- 19. Кипение и кристаллизация растворов Повышение температуры
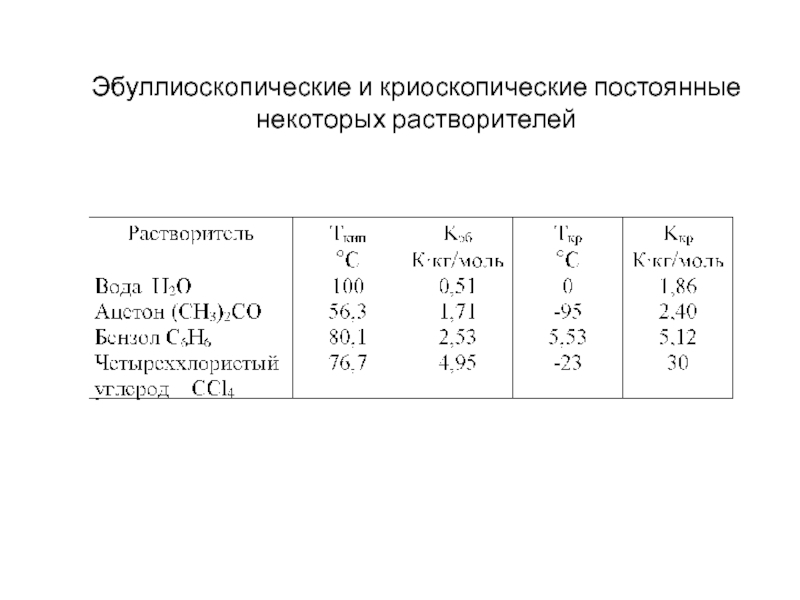
- 20. Эбуллиоскопические и криоскопические постоянные некоторых растворителей
- 21. Изотонический коэффициент - i - показывает
Слайд 1 Равновесие
Термодинамическим равновесием называется такое термодинамическое состояние системы, которое при постоянстве
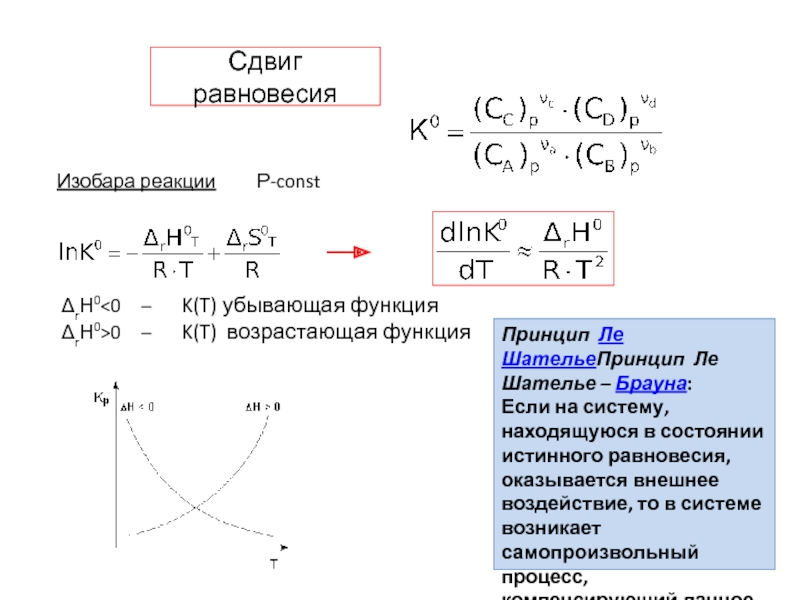
Слайд 3Сдвиг равновесия
Изобара реакции Р-const
ΔrН00 – K(T) возрастающая функция
Принцип Ле
Если на систему, находящуюся в состоянии истинного равновесия, оказывается внешнее воздействие, то в системе возникает самопроизвольный процесс, компенсирующий данное воздействие.
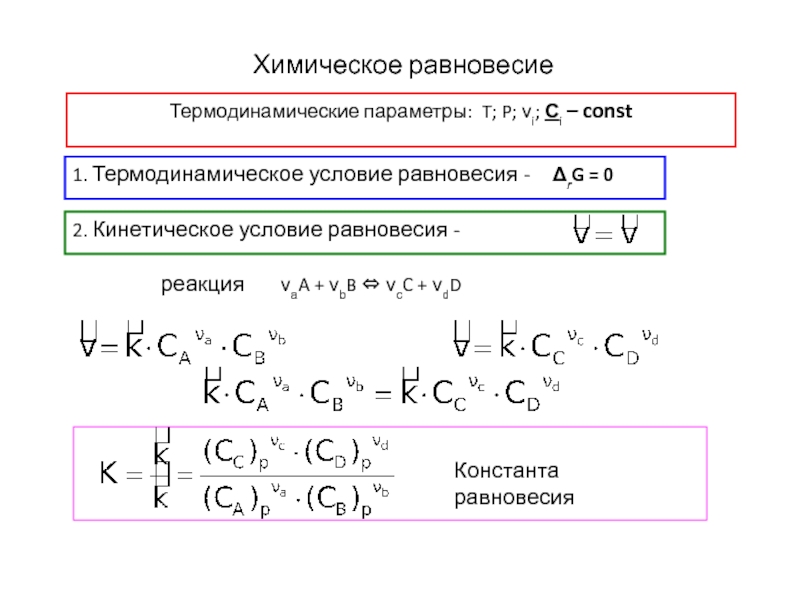
Слайд 4Химическое равновесие
Термодинамические параметры: T; P; νi; Сi – const
1. Термодинамическое условие
реакция νаA + νbB ⇔ νсC + νdD
Слайд 6Константа равновесия
KX - концентрации задаются мольными долями (безразмерная величина)
Kp - концентрации
Δν = (νc+ νd) - (νa+ νb)
KC – концентрации задаются молярной концентрацией - (моль/л)Δν
Слайд 10Диссоциация воды
H2O ⇔ H+ + OH-
Нейтральная среда [H+] = [OH–]
Кислая среда [H+] > 10-7 [OH–] <10-7 [моль/л]
Щелочная среда [H+] < 10-7 [OH–] > 10-7 [моль/л]
Слайд 11Водородный показатель
pH = –lg[H+]
Нейтральная среда pH = 7
Кислая среда
Щелочная среда pH > 7
pОH = –lg[ОH–]
pH + pОH = 14
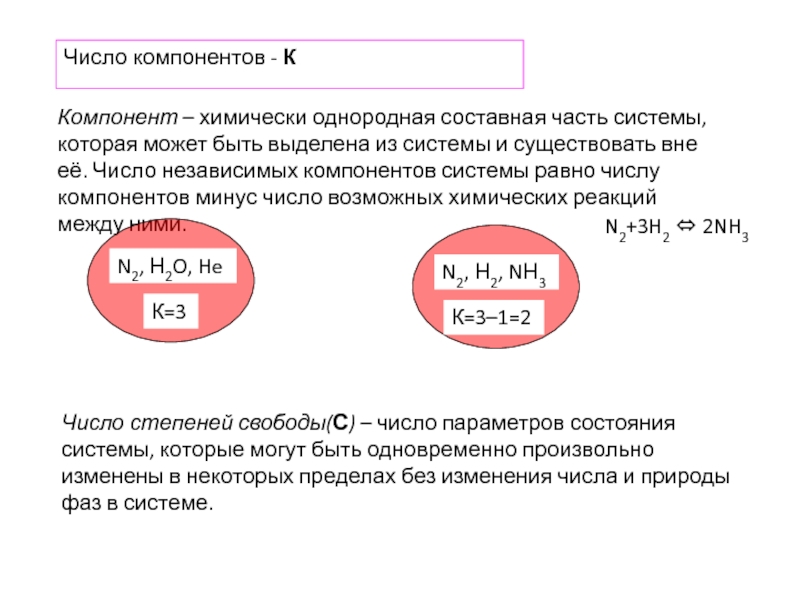
Слайд 13Число компонентов - К
Компонент – химически однородная составная часть системы,
К=3
К=3–1=2
N2+3H2 ⇔ 2NH3
Число степеней свободы(С) – число параметров состояния системы, которые могут быть одновременно произвольно изменены в некоторых пределах без изменения числа и природы фаз в системе.
Слайд 14Число степеней свободы равновесной термодинамической системы С равно числу независимых компонентов
Правило фаз Гиббса - С = К – Ф + 2
Системы: ( по числу компонентов ) одно-, двухкомпонентные и т.д.
(по числу степеней свободы) инвариантные, моно-, дивариантные и т.д.
графическая зависимость состояния системы от внешних условий – диаграммы состояния
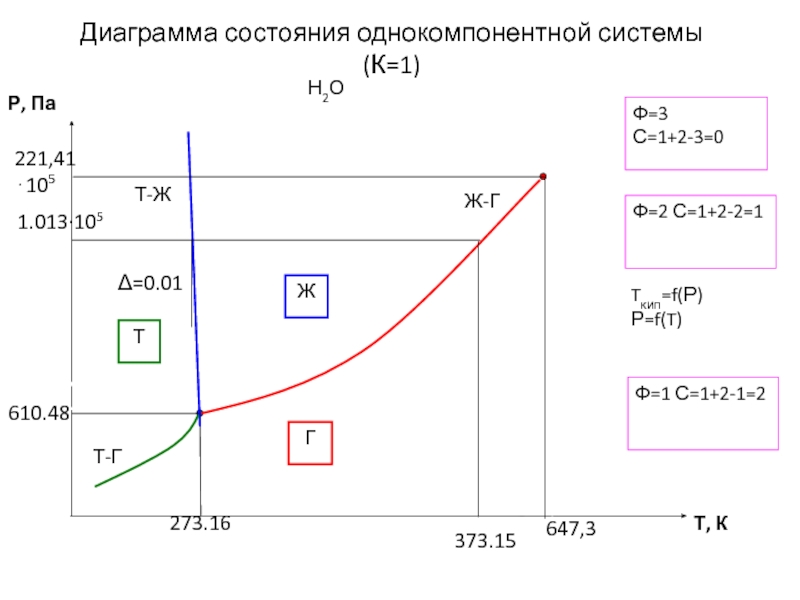
Слайд 15Диаграмма состояния однокомпонентной системы (К=1)
Н2О
Ф=2 С=1+2-2=1
Ф=3
С=1+2-3=0
Ф=1 С=1+2-1=2
Ж
Г
Т
Tкип=f(Р) Р=f(T)
Слайд 17Двухкомпонентная система (К=2)
α→0
Двухфазное равновесие
С = 2 + 2 – 2
1) Т⇔Ж; Ж ⇔ Г
2) Т⇔ Г
Ф=3 С = 2 + 2 – 3 = 1
Слайд 19Кипение и кристаллизация растворов
Повышение температуры кипения раствора по сравнению с
См [моль/кг] – моляльная концентрация
Kэб [К⋅кг/моль]– эбуллиоскопическая постоянная растворителя
Понижение температуры кристаллизации раствора по сравнению с чистым растворителем прямо пропорционально концентрации растворенного вещества
Kкр [К⋅кг/моль]– криоскопическая постоянная растворителя
ΔТкип = Kэб⋅См
ΔТкр = Kкр⋅См
Слайд 21Изотонический коэффициент - i
- показывает увеличение числа частиц в растворе
АxВy ⇔ x А+ + y В-
α - степень диссоциации
N0 - число молекул растворенного вещества
m = x + y




![Диссоциация водыH2O ⇔ H+ + OH-Нейтральная среда [H+] = [OH–] = 10-7 [моль/л]Кислая среда](/img/tmb/5/437811/4a07a18186e21d2c489e8a3bc7405296-800x.jpg)
![Водородный показательpH = –lg[H+]Нейтральная среда pH = 7Кислая среда pH < 7Щелочная среда](/img/tmb/5/437811/9c19c0f0772b590b6470f7852967c93a-800x.jpg)
![Произведение растворимости[Kat+]= x·C [моль/л] [An-]= y·C [моль/л]](/img/tmb/5/437811/cad70bdcb636701bccc343f69c51989d-800x.jpg)