- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Термические превращения углеводородов и других компонентов нефти презентация
Содержание
- 1. Термические превращения углеводородов и других компонентов нефти
- 3. Термические превращения углеводородов Радикально-цепной механизм
- 4. Инициирование цепи Алканы- распад алифатических углеводородов осуществляется
- 5. Инициирование цепи Алкены
- 7. Рост и продолжение цепи (реакции радикалов)
- 8. Обрыв цепи Обрыв цепи осуществляется по следующим
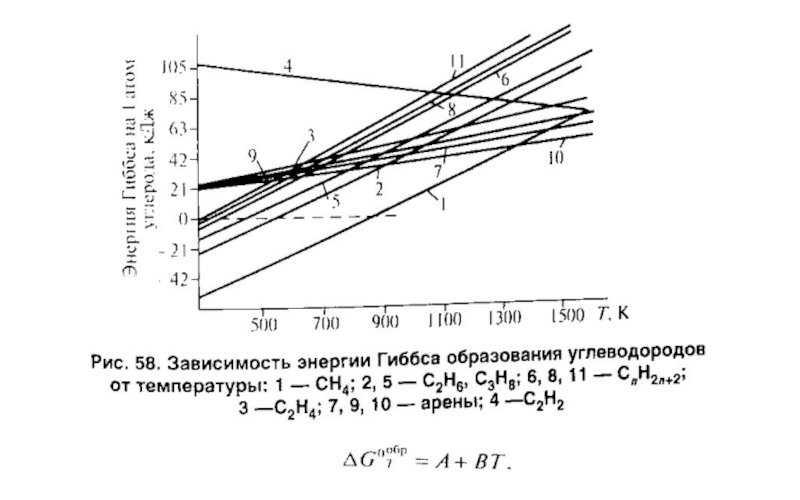
- 9. Термические превращения углеводородов в газовой фазе
- 10. Этан менее устойчив чем метан: деструкция начинается
- 11. Начиная с бутана, распад алканов по связи
- 12. ПРЕВРАЩЕНИЯ ЦИКЛОАЛКАНОВ Реакция протекает по не цепному
- 14. ВЫСШИЕ АЛКЕНЫ И АЛКАДИЕНЫ Для высших алканов
- 16. ПРЕВРАЩЕНИЯ СМЕСИ УГЛЕВОДОРОДОВ Цепные реакции, протекающие в
- 17. ОСОБЕННОСТИ РЕАКЦИЙ В ЖИДКОЙ ФАЗЕ Соотношение скоростей
- 18. «Клеточный эффект» жидкофазных реакций В жидкой фазе
- 19. ЗАКОНОМЕРНОСТИ ТЕРМИЧЕСКОГО РАЗЛОЖЕНИЯ УГЛЕВОДОРОДОВ Термический крекинг –
- 20. ОБРАЗОВАНИЕ НЕФТЯНОГО КОКСА Кокс образуется в жидкофазных
- 22. При коксовании (400-500оС) протекают следующие превращения основных
- 23. ПРОМЫШЛЕННЫЕ ПРОЦЕССЫ ТЕРМИЧЕСКОЙ ПЕРЕРАБОТКИ НЕФТИ И НЕФТЯНЫХ ФРАКЦИЙ Термический крекинг
- 24. ПРОМЫШЛЕННЫЕ ПРОЦЕССЫ ТЕРМИЧЕСКОЙ ПЕРЕРАБОТКИ НЕФТИ И НЕФТЯНЫХ ФРАКЦИЙ Пиролиз
- 25. ПРОМЫШЛЕННЫЕ ПРОЦЕССЫ ТЕРМИЧЕСКОЙ ПЕРЕРАБОТКИ НЕФТИ И НЕФТЯНЫХ ФРАКЦИЙ Коксование
- 26. На суммарный результат жидкофазного термолиза нефтяного сырья существенное влияние
Слайд 3Термические превращения углеводородов
Радикально-цепной механизм процесса термического разложения углеводородов имеет
три стадии:
- инициирование цепи
- рост и продолжение цепи
- обрыв цепи
- инициирование цепи
- рост и продолжение цепи
- обрыв цепи
Слайд 4Инициирование цепи
Алканы- распад алифатических углеводородов осуществляется по наиболее слабой связи С-С
Циклоалканы
Слайд 5Инициирование цепи
Алкены
Энергия раскрытия π-связи в алкене - 249 кДж/моль,
а в сопряженном
диене - 188 кДж/моль.
Слайд 8Обрыв цепи
Обрыв цепи осуществляется по следующим реакциям
Рекомбинация радикалов:
Диспропорционирование радикалов (обратный процесс
реакции образования радикалов)
Энергия этих реакций равна нулю
Энергия этих реакций равна нулю
Слайд 9Термические превращения углеводородов в газовой фазе
Превращения алканов
Метан термически устойчив. Термическая деструкция
возможна при температуре выше 560оС, с заметной скоростью – выше 1000оС. Основная первичная реакция является цепной и развивается последующей схеме
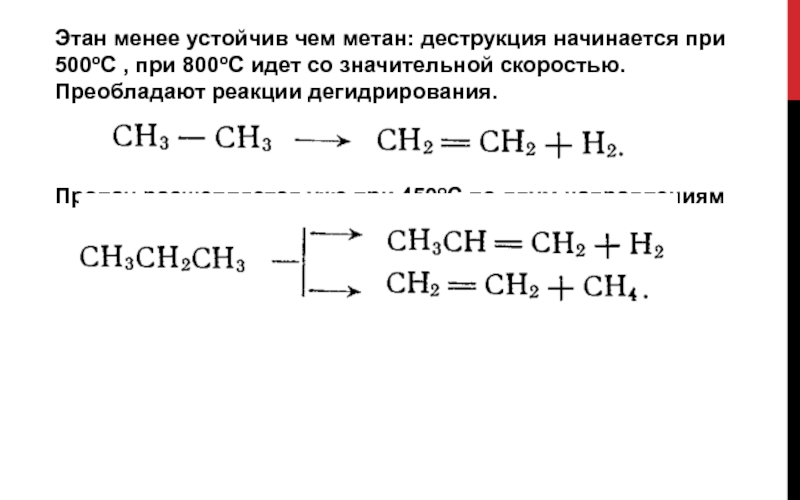
Слайд 10Этан менее устойчив чем метан: деструкция начинается при 500оС , при
800оС идет со значительной скоростью. Преобладают реакции дегидрирования.
Пропан расщепляется уже при 450оС по двум направлениям
Пропан расщепляется уже при 450оС по двум направлениям
Слайд 11Начиная с бутана, распад алканов по связи С-С становится преобладающим.
Относительная скорость
термического крекинга алканов возрастает с увеличением молекулярной массы.
Слайд 12ПРЕВРАЩЕНИЯ ЦИКЛОАЛКАНОВ
Реакция протекает по не цепному механизму.
Накопление алкенов
инициирует
радикально-цепной
процесс.
Бициклические нафтены
также подвергаются крекингу
дециклизации и
дегидрированию.
Бициклические нафтены
также подвергаются крекингу
дециклизации и
дегидрированию.
Слайд 13
ПРЕВРАЩЕНИЯ АЛКЕНОВ
В условиях термических
процессов при деструкции алканов и циклоалканов образуются алкены, которые подвергаются следующим превращениям.
Дегидрирование
Полимеризация
Дегидроконденсация
Реакции протекают по радикально-цепному механизму.
С ростом температуры и снижения давления увеличивается выход ацетилена(1). При относительно низкой температуре но высоком давлении идет полимеризация низших алкенов. В промежуточных условиях реакция (3).
Дегидрирование
Полимеризация
Дегидроконденсация
Реакции протекают по радикально-цепному механизму.
С ростом температуры и снижения давления увеличивается выход ацетилена(1). При относительно низкой температуре но высоком давлении идет полимеризация низших алкенов. В промежуточных условиях реакция (3).
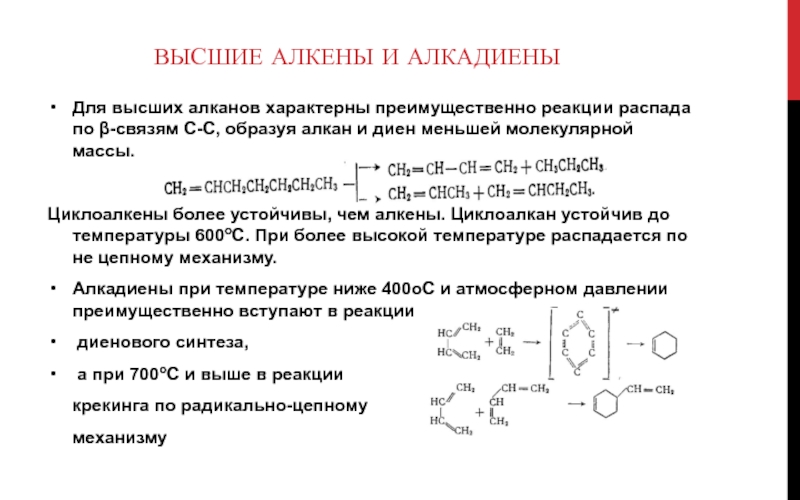
Слайд 14ВЫСШИЕ АЛКЕНЫ И АЛКАДИЕНЫ
Для высших алканов характерны преимущественно реакции распада по
β-связям С-С, образуя алкан и диен меньшей молекулярной массы.
Циклоалкены более устойчивы, чем алкены. Циклоалкан устойчив до температуры 600оС. При более высокой температуре распадается по не цепному механизму.
Алкадиены при температуре ниже 400оС и атмосферном давлении преимущественно вступают в реакции
диенового синтеза,
а при 700оС и выше в реакции
крекинга по радикально-цепному
механизму
Циклоалкены более устойчивы, чем алкены. Циклоалкан устойчив до температуры 600оС. При более высокой температуре распадается по не цепному механизму.
Алкадиены при температуре ниже 400оС и атмосферном давлении преимущественно вступают в реакции
диенового синтеза,
а при 700оС и выше в реакции
крекинга по радикально-цепному
механизму
Слайд 15 ПРЕВРАЩЕНИЯ АРЕНОВ
Термическая устойчивость аренов
сильно изменяется в зависимости от строения.
Незамещенные арены подвергаются только дегидроконденсации по радикально-цепному механизму. Для бензола
Для нафталина
Замещенные арены с длинными
боковыми алкильными цепями подвергаются распаду алкильных цепей
Реакции дегидроконденсации аренов вместе с реакциями диенового синтеза и дегидроконденсацией алкенов лежат в основе процессов коксообразования при термическом крекинге и пиролизе.
Незамещенные арены подвергаются только дегидроконденсации по радикально-цепному механизму. Для бензола
Для нафталина
Замещенные арены с длинными
боковыми алкильными цепями подвергаются распаду алкильных цепей
Реакции дегидроконденсации аренов вместе с реакциями диенового синтеза и дегидроконденсацией алкенов лежат в основе процессов коксообразования при термическом крекинге и пиролизе.
Слайд 16ПРЕВРАЩЕНИЯ СМЕСИ УГЛЕВОДОРОДОВ
Цепные реакции, протекающие в системе всегда взаимосвязаны. Инициирование является
самой энергоемкой стадией цепного процесса. Дальнейшие превращения радикалов происходят с очень небольшими энергиями активации.
Вследствие увеличения скорости инициирования термический распад смеси углеводородов протекает с большей скоростью, чем распад индивидуальных соединений.
Так как скорость взаимодействия фенильного радикала с алканом выше, чем с бензолом, последний практически не расходуется и образование дифенила не происходит.
В результате взаимного влияния углеводородов на стадии развития цепи состав продуктов термического распада смеси углеводородов отличается от продуктов распада индивидуальных веществ
Вследствие увеличения скорости инициирования термический распад смеси углеводородов протекает с большей скоростью, чем распад индивидуальных соединений.
Так как скорость взаимодействия фенильного радикала с алканом выше, чем с бензолом, последний практически не расходуется и образование дифенила не происходит.
В результате взаимного влияния углеводородов на стадии развития цепи состав продуктов термического распада смеси углеводородов отличается от продуктов распада индивидуальных веществ
Слайд 17ОСОБЕННОСТИ РЕАКЦИЙ В ЖИДКОЙ ФАЗЕ
Соотношение скоростей моно и бимолекулярных реакций в
жидкой фазе равносильно проведению их в газовой фазе под давлением 10МПа. (При 1 атм в 1 см3 газа -1019 молекул, а в жидкости - 1021 ).
При равных температурах жидкофазные термические реакции углеводородов и нефтепродуктов приводят к к значительно большему выходу продуктов конденсации и меньшему выходу продуктов распада.
При равных температурах жидкофазные термические реакции углеводородов и нефтепродуктов приводят к к значительно большему выходу продуктов конденсации и меньшему выходу продуктов распада.
Слайд 18«Клеточный эффект» жидкофазных реакций
В жидкой фазе на протекание реакций определенное влияние
оказывает сольватация (для полярных частиц)и локальный «клеточный эффект».
Для удаления радикалов на расстояние, при котором они становятся кинетически независимыми частицами, необходимо преодолеть дополнительный активационный барьер, равный энергии активации диффузии радикала из «клетки» (окружение рядом находящихся молекул).
Для рекомбинации радикалы также должны преодолеть «клеточный эффект».
«Клеточный эффект» изменяет стационарную концентрацию радикалов, что приводит к изменению энергии активации жидкофазной реакции относительно газофазной.
Для удаления радикалов на расстояние, при котором они становятся кинетически независимыми частицами, необходимо преодолеть дополнительный активационный барьер, равный энергии активации диффузии радикала из «клетки» (окружение рядом находящихся молекул).
Для рекомбинации радикалы также должны преодолеть «клеточный эффект».
«Клеточный эффект» изменяет стационарную концентрацию радикалов, что приводит к изменению энергии активации жидкофазной реакции относительно газофазной.
Слайд 19ЗАКОНОМЕРНОСТИ ТЕРМИЧЕСКОГО РАЗЛОЖЕНИЯ УГЛЕВОДОРОДОВ
Термический крекинг – термический процесс при температуре 470-540оС.
Пиролиз - термический процесс при температуре 700-1000оС. Температура влияет на механизм процесса и на состав продуктов.
Суммарные реакции протекающие при пиролизе и крекинге:
первичные реакции крекинга и дегидрирования, приводящие к образованию алкенов;
вторичные реакции превращения алкенов - полимеризации и конденсации;
Реакции прямого молекулярного распада, при котором образуются пироуглерод, водород и частично ацетилен.
Суммарные реакции протекающие при пиролизе и крекинге:
первичные реакции крекинга и дегидрирования, приводящие к образованию алкенов;
вторичные реакции превращения алкенов - полимеризации и конденсации;
Реакции прямого молекулярного распада, при котором образуются пироуглерод, водород и частично ацетилен.
Слайд 20ОБРАЗОВАНИЕ НЕФТЯНОГО КОКСА
Кокс образуется в жидкофазных термических процессах как целевой продукт
и в газофазных, как нежелательный побочный продукт.
Нефтяной кокс –это твердое вещество плотностью 1400-1500кг/м3 с высоким содержанием углерода. Атомное соотношение С: Н в коксе составляет 1.1-1.4.
Кокс образуется при жидкофазной термической переработке нефтяных остатков (сырье) по схеме:
Арены → Смолы → Асфальтены → Кокс → Графит
Нефтяной кокс –это твердое вещество плотностью 1400-1500кг/м3 с высоким содержанием углерода. Атомное соотношение С: Н в коксе составляет 1.1-1.4.
Кокс образуется при жидкофазной термической переработке нефтяных остатков (сырье) по схеме:
Арены → Смолы → Асфальтены → Кокс → Графит
Слайд 22При коксовании (400-500оС) протекают следующие превращения основных компонентов сырья:
парафино-нафтеновая часть
масел крекируется до жидких и газообразных продуктов;
в моно и бицикло-ароматические углеводородах наряду с реакциями крекинга протекают реакции перераспределения водорода, приводящие к образованию алканов и полиароматических, пополняющих твердую фазу асфальтенов;
смолы частично крекируются до газообразных и жидких продуктов, теряют кислородсодержащие функциональные группы и превращаются в асфальтены;
Асфальтены при температуре выше 300оС разлагаются с образованием газа, жидких продуктов и кокса. В условиях коксования асфальтены лишаются своей сольватной оболочки, которая подвергается крекингу. Расстояния между молекулами сокращается, ассоциаты становятся более компактными, увеличивается энергия их дисперсного притяжения и по мере потери водорода переходят в карбены, карбоиды и кокс.
По данным рентгенографического анализа кокс представляет собой агломерат хаотично расположенных трехмерно неупорядочных кристаллитов, сходных по строению и размерам с ассоциатами асфальтенов, но с меньшим межслоевым расстоянием 0.348-0.350.
в моно и бицикло-ароматические углеводородах наряду с реакциями крекинга протекают реакции перераспределения водорода, приводящие к образованию алканов и полиароматических, пополняющих твердую фазу асфальтенов;
смолы частично крекируются до газообразных и жидких продуктов, теряют кислородсодержащие функциональные группы и превращаются в асфальтены;
Асфальтены при температуре выше 300оС разлагаются с образованием газа, жидких продуктов и кокса. В условиях коксования асфальтены лишаются своей сольватной оболочки, которая подвергается крекингу. Расстояния между молекулами сокращается, ассоциаты становятся более компактными, увеличивается энергия их дисперсного притяжения и по мере потери водорода переходят в карбены, карбоиды и кокс.
По данным рентгенографического анализа кокс представляет собой агломерат хаотично расположенных трехмерно неупорядочных кристаллитов, сходных по строению и размерам с ассоциатами асфальтенов, но с меньшим межслоевым расстоянием 0.348-0.350.
Слайд 26На суммарный результат жидкофазного термолиза нефтяного сырья существенное влияние оказывает клеточный эффект.
При
газофазном распаде молекулы углеводорода образующиеся радикалы мгновенно разлетаются.
В жидкой же фазе радикалы окружены клеткой из соседних молекул.
Для удаления радикалов на расстояние, при котором они становятся кинетически независимыми частицами, необходимо преодолеть дополнительный активационный барьер, равный энергии активации диффузии радикала из клетки.
Тем самым клеточный эффект приводит к изменению энергии активации жидкофазной реакции относительно газофазной, а также стационарной концентрации радикалов.
В жидкой же фазе радикалы окружены клеткой из соседних молекул.
Для удаления радикалов на расстояние, при котором они становятся кинетически независимыми частицами, необходимо преодолеть дополнительный активационный барьер, равный энергии активации диффузии радикала из клетки.
Тем самым клеточный эффект приводит к изменению энергии активации жидкофазной реакции относительно газофазной, а также стационарной концентрации радикалов.