- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Сырьё для получения фенолальдегидных полимеров презентация
Содержание
- 1. Сырьё для получения фенолальдегидных полимеров
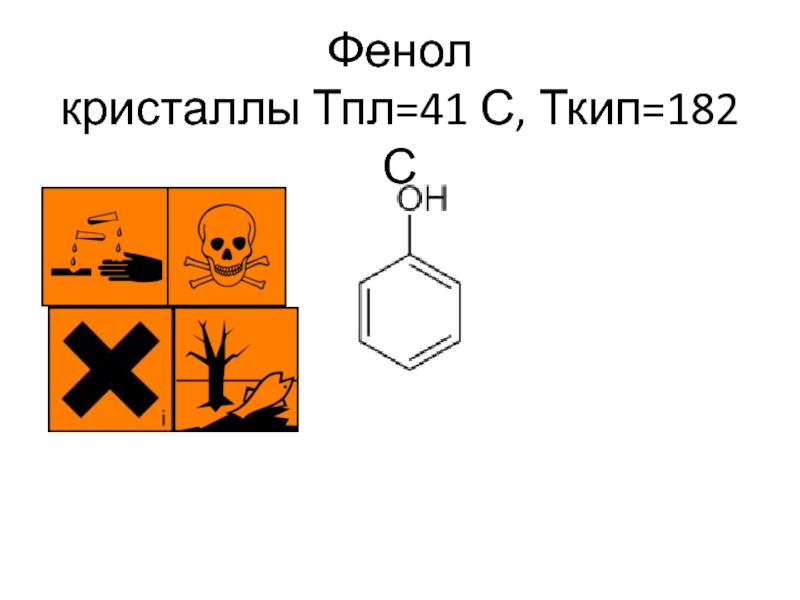
- 2. Фенол кристаллы Тпл=41 С, Ткип=182 С
- 3. Синтетические способы получения фенола: 1. бензолсульфонатный
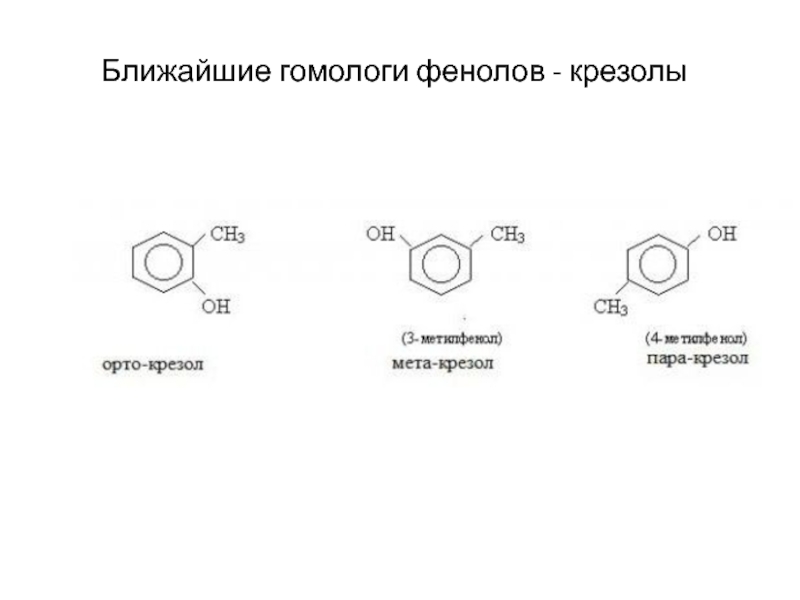
- 4. Ближайшие гомологи фенолов - крезолы
- 5. Ксилинолы
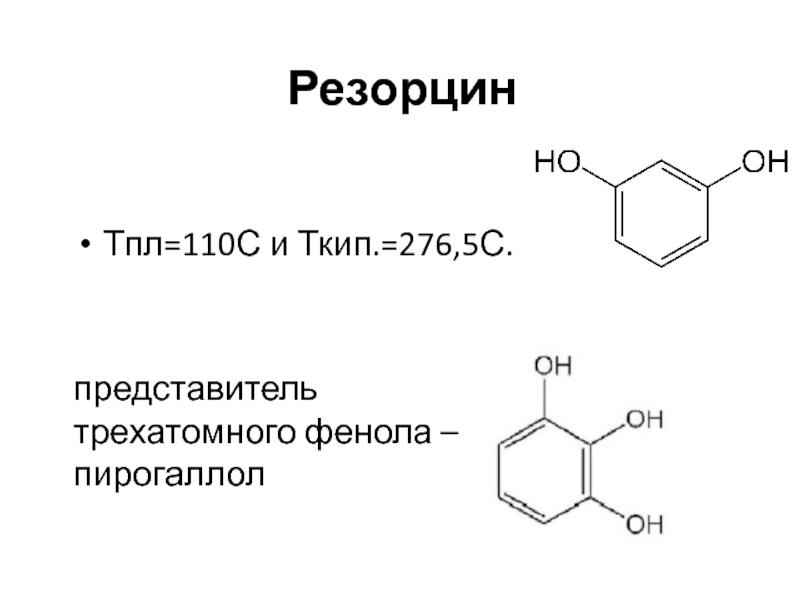
- 6. Резорцин Тпл=110С и Ткип.=276,5С. представитель трехатомного фенола – пирогаллол
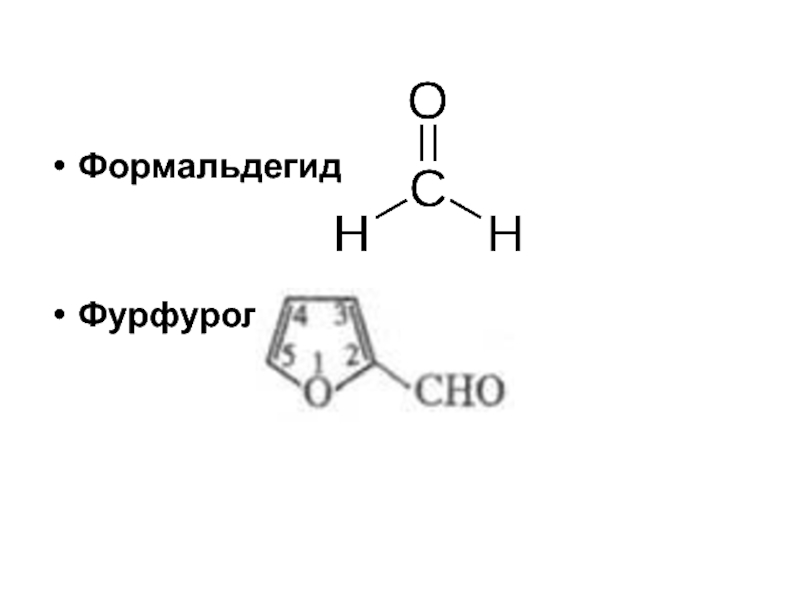
- 7. Формальдегид Фурфурол
- 8. Синтез фенолальдегидных полимеров При
- 9. Основные факторы, определяющие строение и свойства
- 10. Функциональность фенолов – число атомов водорода в
- 11. При поликонденсации формальдегида и фурфурола с
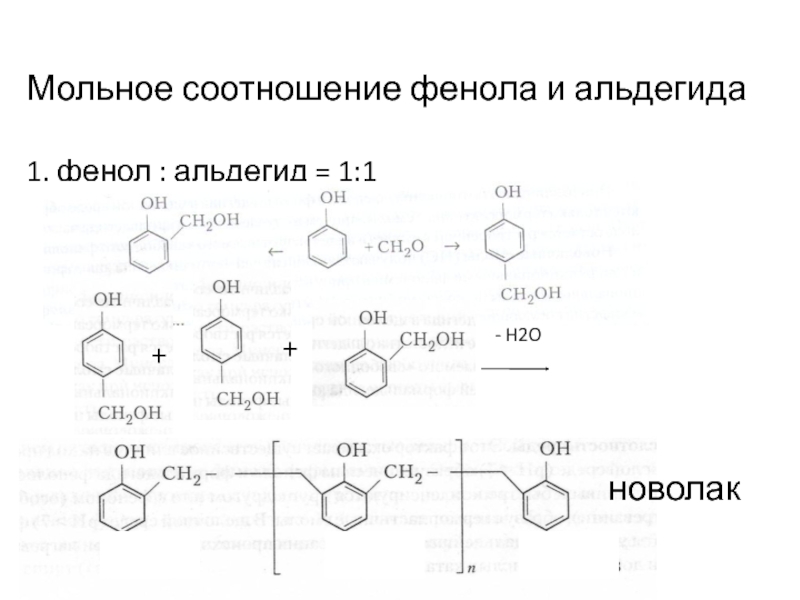
- 12. Мольное соотношение фенола и альдегида
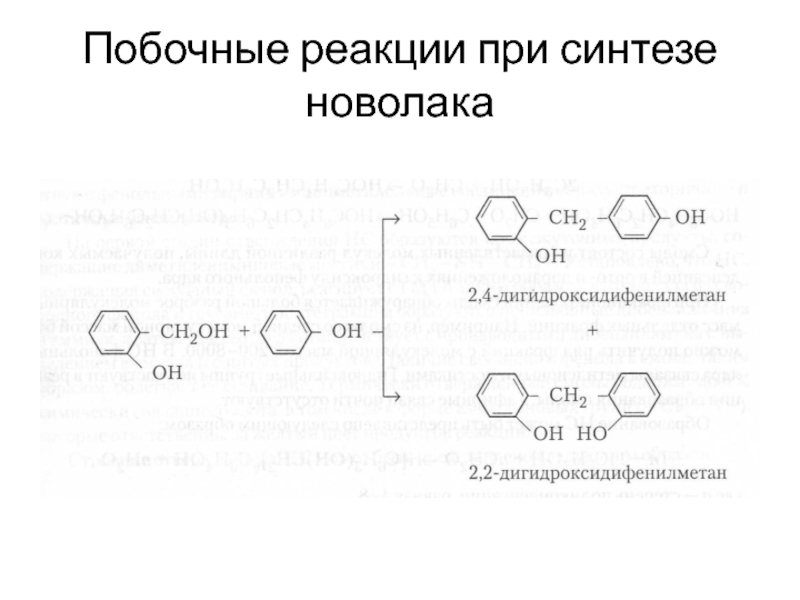
- 13. Побочные реакции при синтезе новолака
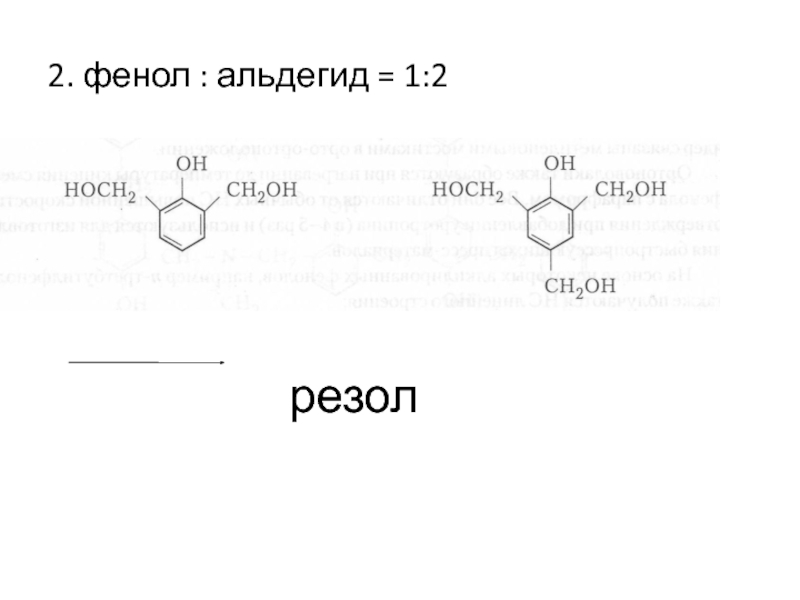
- 14. 2. фенол : альдегид = 1:2 резол
- 15. Кислотность среды Кислая среда (рН < 7):
- 16. Взаимодействие трифункциональных фенолов с формальдегидом Образование новолака
- 17. Реактивные свободные центры в новолачных смолах
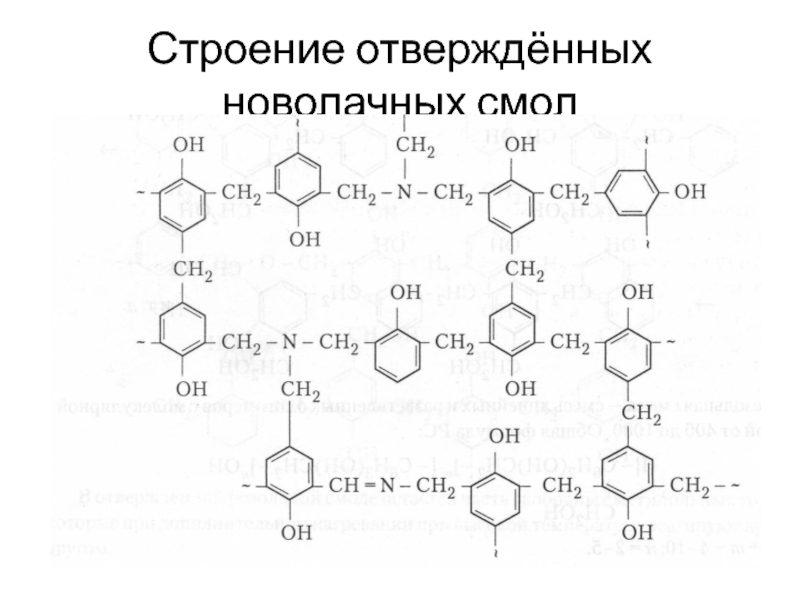
- 18. Строение отверждённых новолачных смол
- 19. Резол – смесь линейных и разветвлённых продуктов общей формулы:
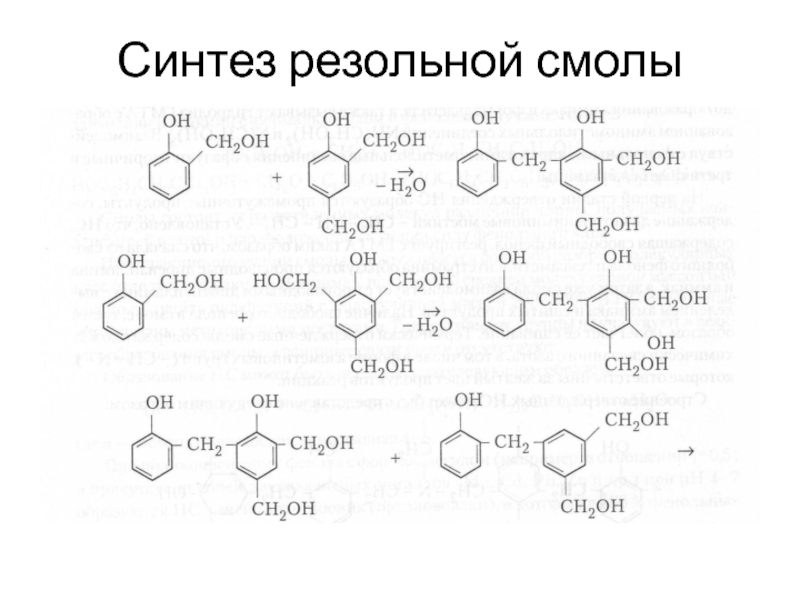
- 20. Синтез резольной смолы
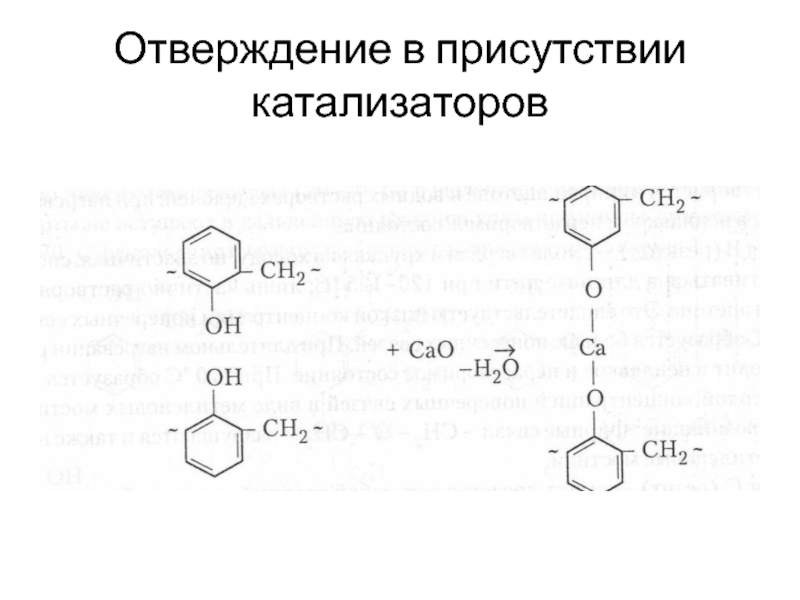
- 21. Отверждение в присутствии катализаторов
- 22. Стадии отверждения Стадия А (резольная) – олигомер
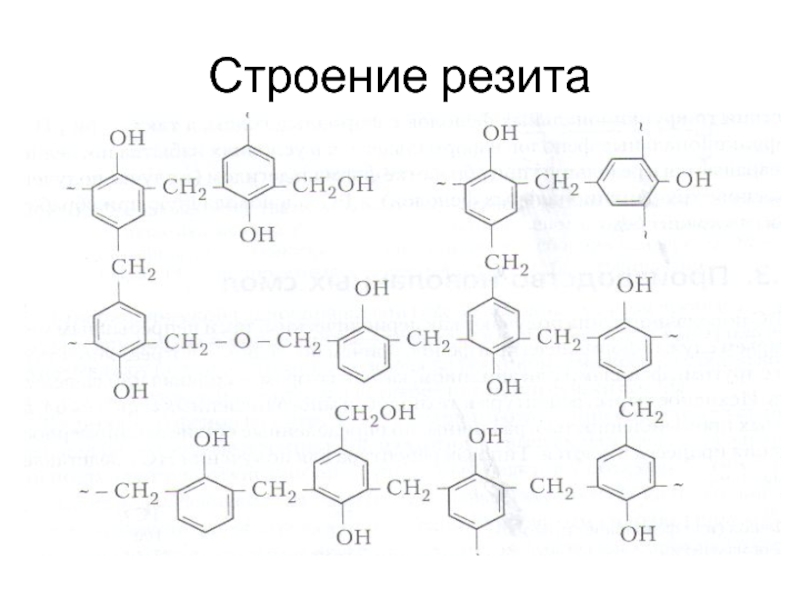
- 23. Строение резита
- 24. Типовая рецептура производства новолачных (НС) и резольных смол (РС)
Слайд 1Сырьё для получения фенолальдегидных полимеров
Основное сырьё – фенол и формальдегид.
Гомологи
Другие альдегиды – фурфурол
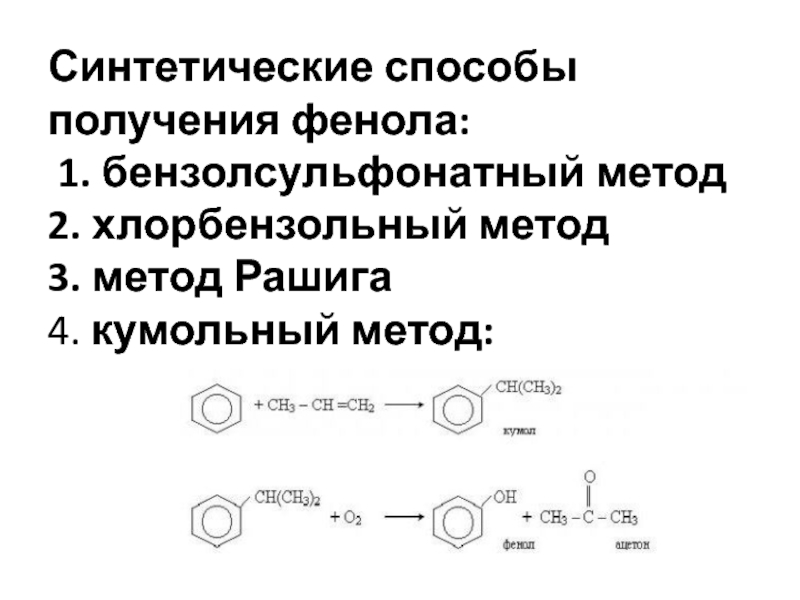
Слайд 3Синтетические способы получения фенола: 1. бензолсульфонатный метод 2. хлорбензольный метод 3. метод Рашига
Слайд 8
Синтез фенолальдегидных полимеров
При поликонденсации фенола и его гомологов с альдегидами могут
Термопластичные фенолальдегидные олигомеры – новолачные (или новолаки), а термореактивные – резольные (или резолы)
Слайд 9
Основные факторы, определяющие строение и свойства фенолальдегидных полимеров:
функциональность фенола
мольное соотношение фенола
рН среды.
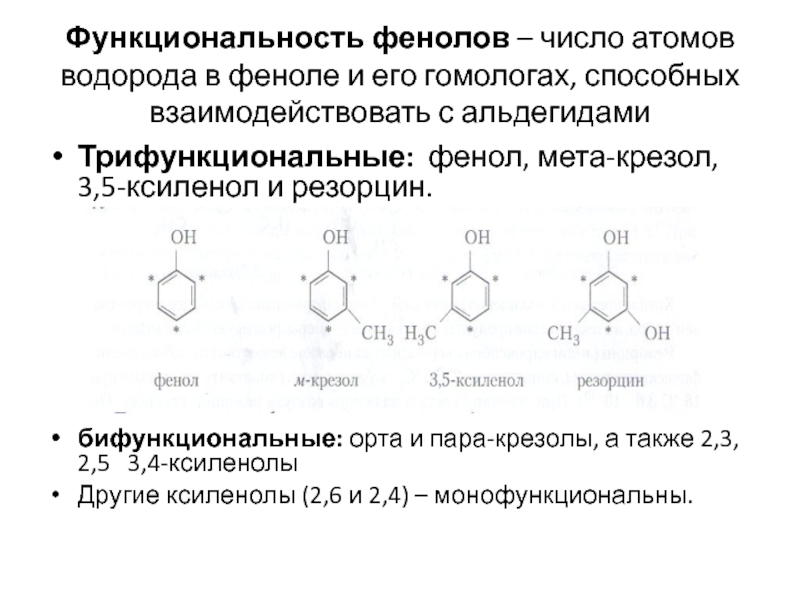
Слайд 10Функциональность фенолов – число атомов водорода в феноле и его гомологах,
Трифункциональные: фенол, мета-крезол, 3,5-ксиленол и резорцин.
бифункциональные: орта и пара-крезолы, а также 2,3, 2,5 3,4-ксиленолы
Другие ксиленолы (2,6 и 2,4) – монофункциональны.
Слайд 11
При поликонденсации формальдегида и фурфурола с трифункциональными фенолами - как термопластичные,
Формальдегид и фурфурол при поликонденсации с трифункциональными фенолами – как термореактивные, так и термопластичные олигомеры.
Другие альдегиды – (уксусный, масляный и т.д.) - только термопластичные олигомеры (у них низкая реакционная способность).
Слайд 15Кислотность среды
Кислая среда (рН < 7): фенолоспирты неустойчивы →быстрая конденсация →
Щелочная среда (рН > 7): фенолоспирты устойчивы → конденсация при нагревании или при добавлении кислых катализаторов.
Слайд 16Взаимодействие трифункциональных фенолов с формальдегидом
Образование новолака
Избыток фенола (фенол/формальдегид=1/ 0,78-0,86). Кислая среда.
Большой избыток формальдегида (фенол/формальдегид=1/ 2-2,5). Сильная кислота –катализатор. При добавлении небольшого кол-ва основания – новолаки переходят в резолы.
Образование резола
Избыток трифункционального фенола и основной катализатор. Избыток фенола может оставаться в продуктах реакции.
При небольшом избытке формальдегида в присутствии как основных так и кислых катализаторов.
Слайд 17
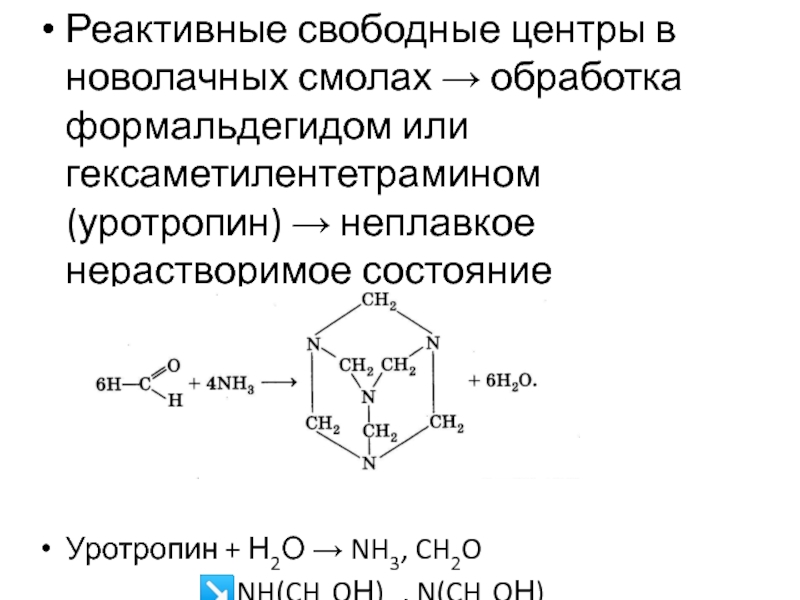
Реактивные свободные центры в новолачных смолах → обработка формальдегидом или гексаметилентетрамином
Уротропин + Н2О → NH3, CH2O
↘NH(CH2OН)2 , N(CH2OН)3
Слайд 22Стадии отверждения
Стадия А (резольная) – олигомер по свойствам близок к новолаку
Стадия В (резитол). Растворимость – частичная. Не плавится, но при нагревании размягчается (переходит в высокоэластичное, каучукоподобное состояние). Ограниченно набухает в растворителях.
Стадия С (резит) – конечная стадия отверждения. Неплавкий и нерастворимый продукт, не набухает в растворителях и не размягчается при нагревании.