- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Свободные радикалы и болезни человека презентация
Содержание
- 1. Свободные радикалы и болезни человека
- 2. Антиоксиданты, и способы их изучения
- 3. Антиоксиданты - соединения, тормозящие процессы оксидативного стресса
- 4. O-O → HO-O• → HO-OH → HO•
- 5. О2 Доноры электронов (восстановители, митохондрии) е-
- 6. Антиоксидантные ферменты Супероксид дисмутаза
- 7. O-O → HO-O• → HO-OH → HO•
- 8. Метаболизм супероксида в биологических системах HO2•
- 9. Супероксиддисмутаза Супероксиддисмутаза (СОД) - единственный известный в
- 10. Дисмутация HО2• супероксиддисмутазой Реакция, катализируемая СОД, состоит
- 11. Дисмутация HО2• супероксиддисмутазой Сu2+ Zn2+ Zn2+ Сu2+
- 12. Измерение активности СОД Генерацию радикалов осуществляют: -физически
- 13. Антиоксидантные ферменты Каталаза и Пероксидазы
- 14. O-O → HO-O• → HO-OH → HO•
- 15. Дезактивация перекиси водорода Перекись водорода (Н2О2)
- 16. Как работают каталаза и пероксидаза?
- 17. Каталаза представляет собой гемовый фермент, состоящий из
- 18. Пероксидазы Пероксидазы также являются ферментами, разрушающими
- 19. Перехватчики радикалов Антиоксиданты, и способы их изучения
- 20. O-O → HO-O• → HO-OH → HO•
- 21. Перехватчики радикалов В качестве системы защиты организма
- 22. Принцип действия перехватчиков радикалов Антиоксидантные свойства обычно
- 23. R-N=N-R → 2R• + N2 → 2ROO•
- 24. Определение общей антиоксидантной активности R-N=N-R → 2R•
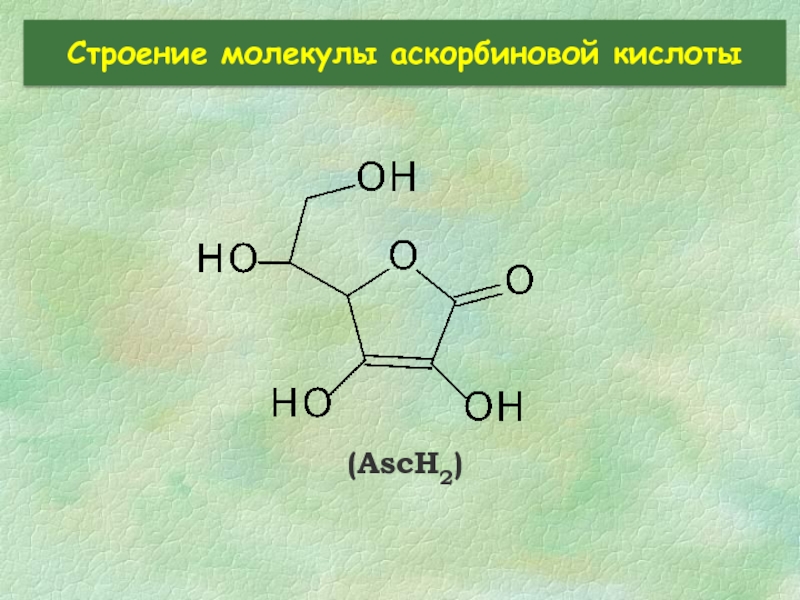
- 25. Строение молекулы аскорбиновой кислоты (AscH2)
- 26. AscH2 – двухосновная кислота При pH 7.4,
- 27. Аскорбиновая кислота Отрыв одного электрона от аскорбиновой
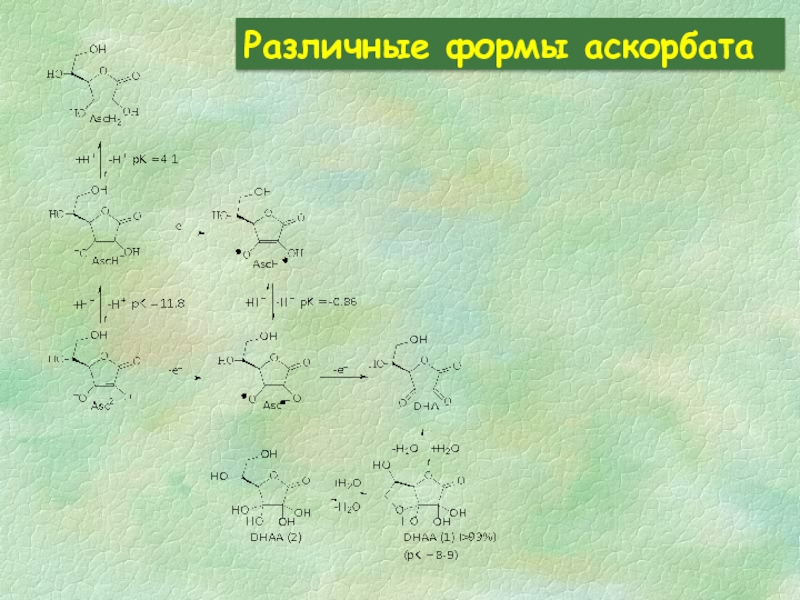
- 28. Различные формы аскорбата
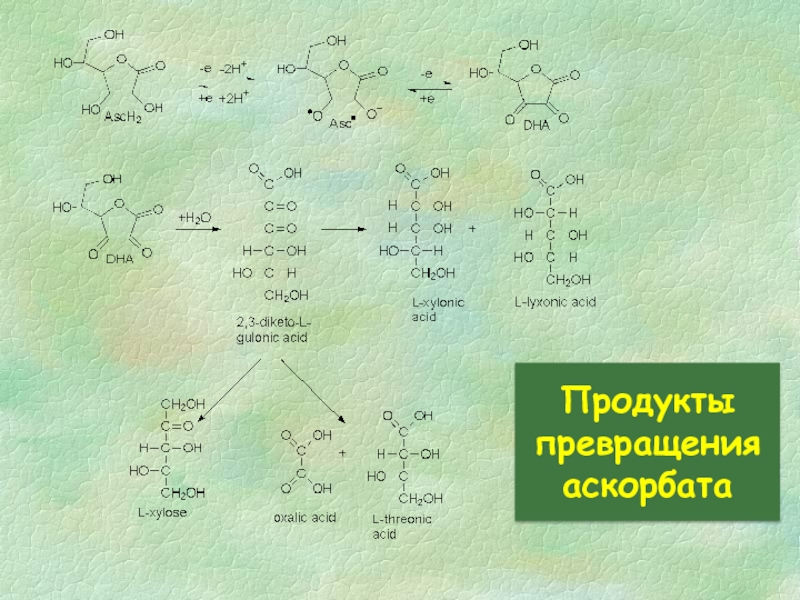
- 29. Продукты превращения аскорбата
- 30. AscH- - это антиоксидант-восстановитель AscH- при взаимодействии
- 31. Сигнал ЭПР Asc∙- Радикал аскорбата представляет
- 32. Сигнал ЭПР Asc∙- высокого разрешения aH4
- 33. Константы скорости взаимодействия аскорбата с некоторыми радикалами
- 34. Asc∙- - маркер окислительного стресса [Asc∙-] – пропорциональна степени окисления аскорбата
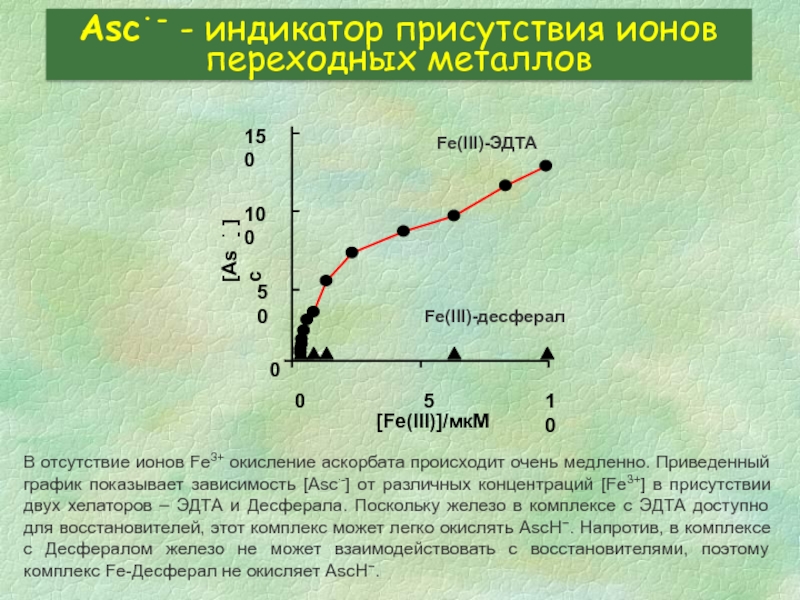
- 35. Asc∙- - индикатор присутствия ионов переходных металлов
- 36. Аскорбиновая кислота Здесь представлено изменение кинетики хемилюминесценции,
Слайд 1Свободные радикалы и болезни человека
Ю.А. Владимиров, А.Н. Осипов
2018
Биофизические основы патологии клетки
Слайд 3Антиоксиданты - соединения, тормозящие процессы оксидативного стресса
Оксидативный стресс - процесс, повреждения
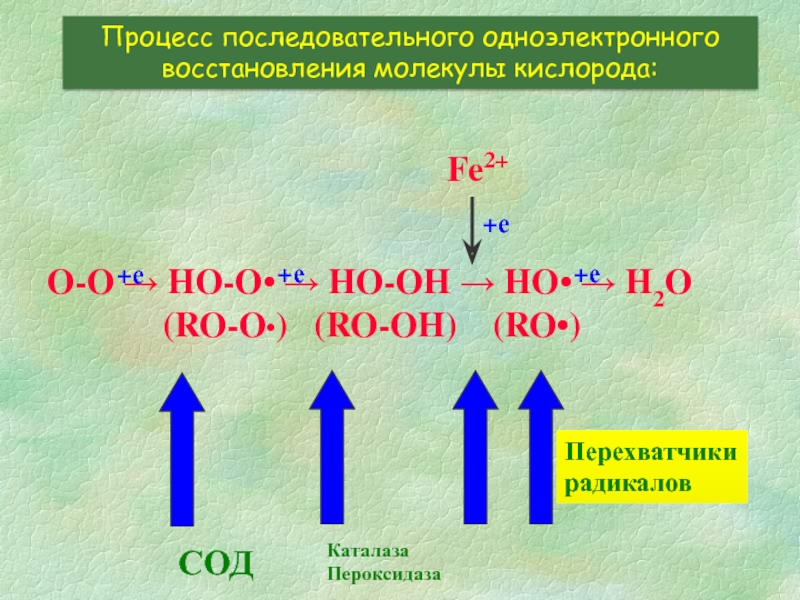
Слайд 4O-O → HO-O• → HO-OH → HO• → H2O
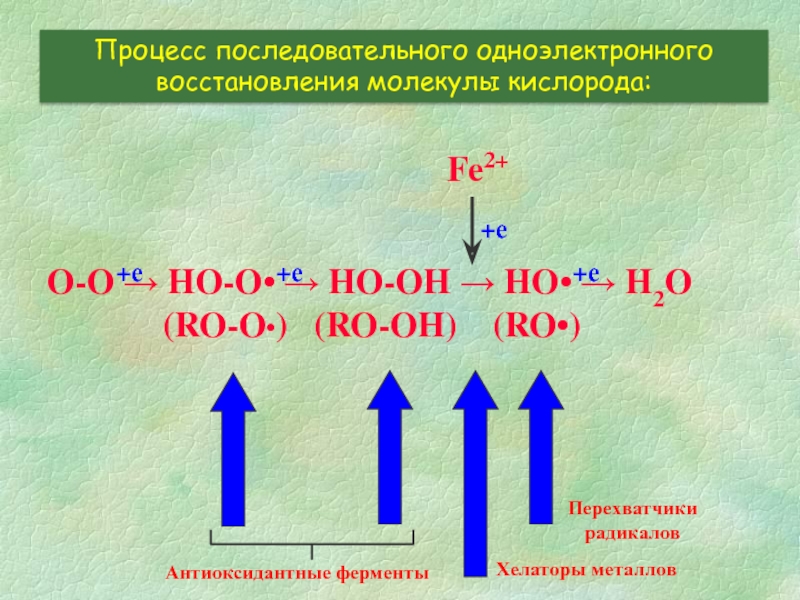
Процесс последовательного одноэлектронного восстановления молекулы кислорода:
Антиоксидантные ферменты
Хелаторы металлов
Перехватчики
радикалов
+е
+е
+е
+е
Слайд 5О2
Доноры электронов (восстановители, митохондрии)
е-
ОО-
ОО-
Супероксиддисмутаза
НООН
Каталаза
Fe3+
Fe2+
Хелаторы металлов
Инициация
ПОЛ
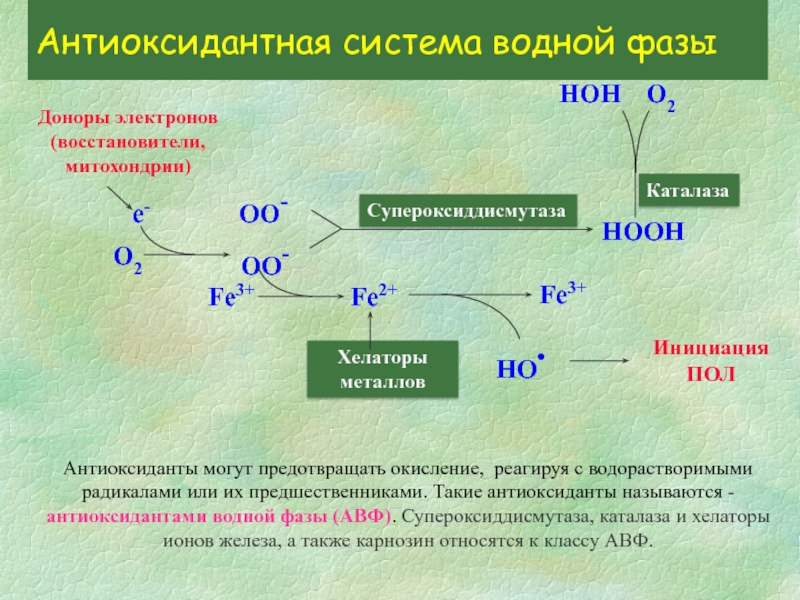
Антиоксиданты могут предотвращать окисление, реагируя с водорастворимыми
Антиоксидантная система водной фазы
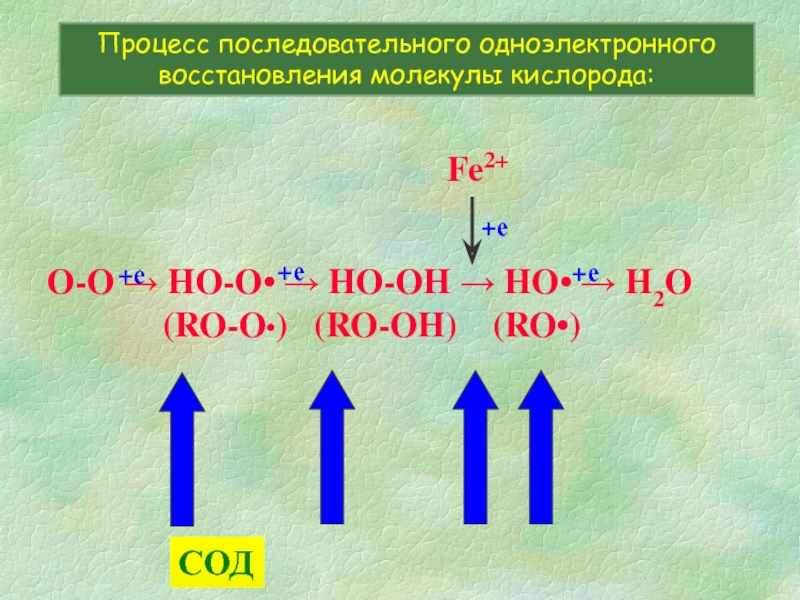
Слайд 7O-O → HO-O• → HO-OH → HO• → H2O
Процесс последовательного одноэлектронного восстановления молекулы кислорода:
СОД
+е
+е
+е
+е
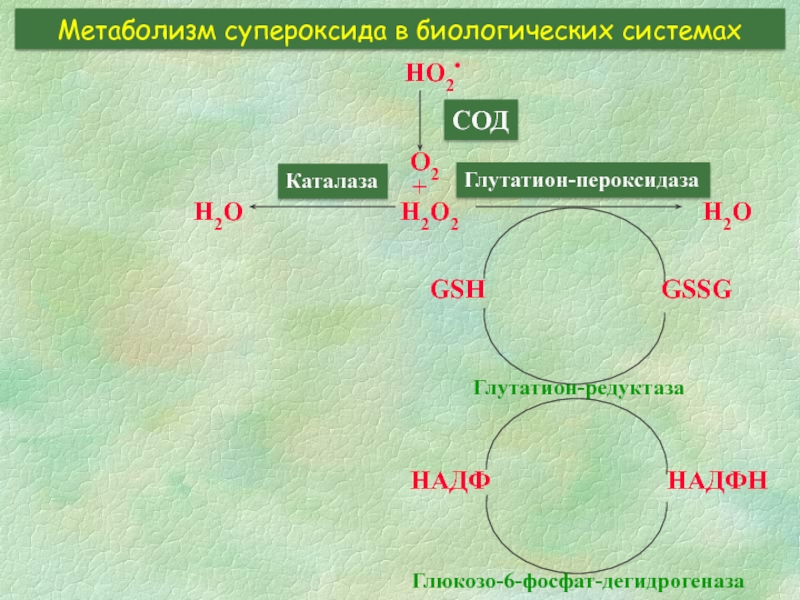
Слайд 8Метаболизм супероксида в биологических системах
HO2•
СОД
O2
+
H2O2
GSH
GSSG
Глутатион-редуктаза
НАДФ
НАДФН
Глюкозо-6-фосфат-дегидрогеназа
Слайд 9Супероксиддисмутаза
Супероксиддисмутаза (СОД) - единственный известный в настоящее время фермент, субстратом которого
Супероксиддисмутаза катализирует следующую реакцию:
2HO2• → O2 + H2O2
Фермент, обнаруженный МакКордом и Фридовичем, имеет молекулярную массу 32 кД и состоит из двух субъединиц, каждая из которых содержит по одному атому Сu и одному атому Zn:
Слайд 10Дисмутация HО2• супероксиддисмутазой
Реакция, катализируемая СОД, состоит из двух стадий и заключается
1.
СОД-Сu2+
+
HO2•
СОД-Сu+
+
O2
2.
СОД-Сu+
+
СОД-Сu2+
+
Н2О2
Zn2+ не участвует в каталитическом цикле, хотя и входит в активный центр. Ионы металлов защищают молекулу СОД от воздействий различных протеаз.
HO2•
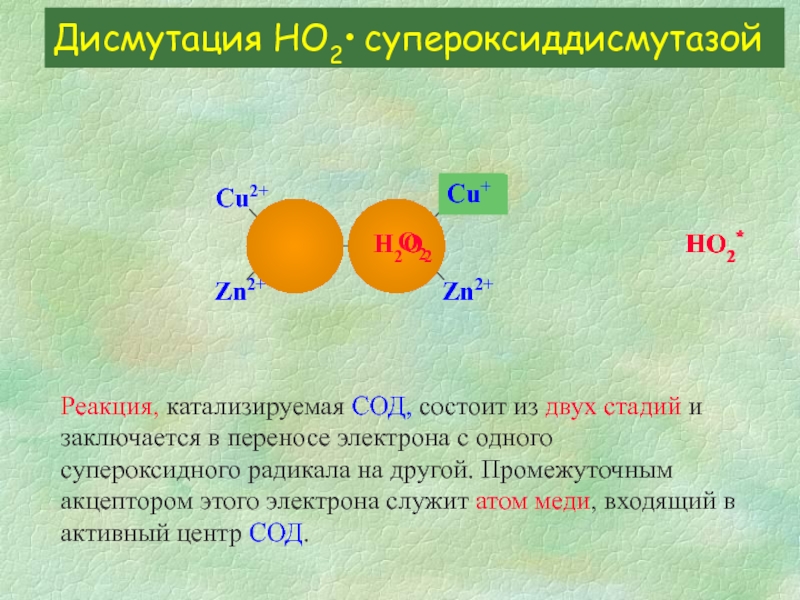
Слайд 11Дисмутация HО2• супероксиддисмутазой
Сu2+
Zn2+
Zn2+
Сu2+
HO2*
H2O2
Реакция, катализируемая СОД, состоит из двух стадий и заключается
Сu+
O2
HO2*
Слайд 12Измерение активности СОД
Генерацию радикалов осуществляют:
-физически (например, радиолиз, электролиз);
-химически (например, распад пероксида
-биохимически (например, энзиматически с помощью КсО).
Индикацию О2*- можно проводить непосредственно, измеряя его поглощение, либо опосредованно, с помощью измерения изменения свойств вспомогательного вещества или образования нового продукта.
Здесь представлен метод фотохемилюминесценции:
интенсивность люминесценции рибофлавина падает при добавлении СОД. Количество фермента приводящее к 50% падению сигнала принимается за единицу его активности
контроль(без СОД)
в присутствии СОД
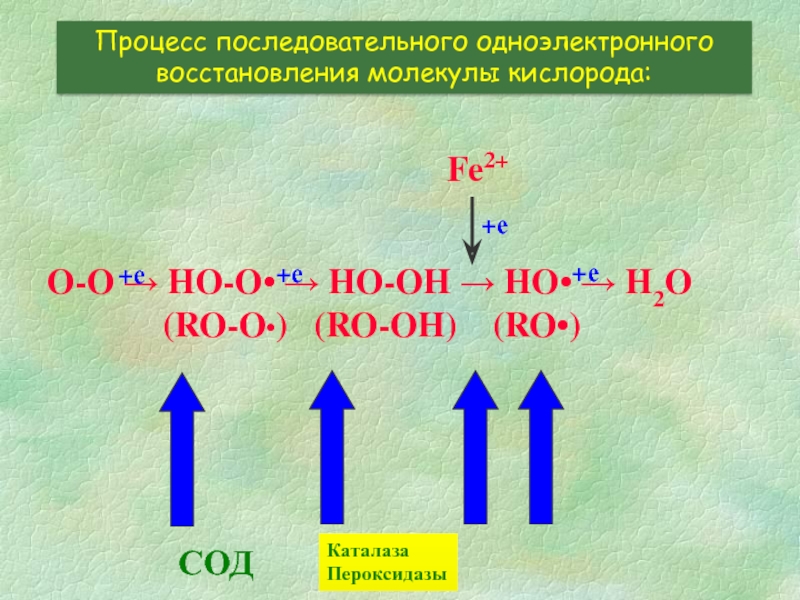
Слайд 14O-O → HO-O• → HO-OH → HO• → H2O
Процесс последовательного одноэлектронного восстановления молекулы кислорода:
СОД
Каталаза
Пероксидазы
+е
+е
+е
+е
Слайд 15Дезактивация перекиси водорода
Перекись водорода (Н2О2) - основной источник самых токсичных
Следовательно, снижение уровня Н2О2 приведет к снижению
концентрации НО∙ радикалов.
Удаление Н2О2 осуществляют два класса ферментов:
Каталаза:
2Н2О2
каталаза
2Н2О
+
О2
Пероксидазы:
Н2О2
+
АН2
пероксидаза
2Н2О
+
А
Слайд 16
Как работают каталаза и пероксидаза?
Стадии ферментативного цикла каталазы:
Стадии ферментативного цикла пероксидазы:
1.
Cat-Fe3+
+
H2O2
Cat-Fe5+(соединение 1)
+
2H2O
2.
+
+
О2
Cat-Fe5+(соединение 1)
H2O2
Cat-Fe3+
1.
Per-Fe3+
+
H2O2
Per-Fe5+(соединение 1)
+
2H2O
2.
+
+
A
Per-Fe5+(соединение 1)
AH2
Per-Fe3+
Слайд 17Каталаза представляет собой гемовый фермент, состоящий из четырех субъединиц с общей
В основе действия каталазы лежит вышеприведенная реакция, протекающая в две стадии:
Каталаза
Слайд 18Пероксидазы
Пероксидазы также являются ферментами, разрушающими
Н2О2 нерадикальным путем и образующими Н2О;
окислению подвергается не вторая молекула Н2О2, как в случае
каталазы, а другие субстраты (АН2).
Рассмотрим реакцию с участием глутатион-пероксидазы:
Глутатион-пероксидаза
Слайд 20O-O → HO-O• → HO-OH → HO• → H2O
Процесс последовательного одноэлектронного восстановления молекулы кислорода:
СОД
Каталаза
Пероксидаза
Перехватчики
радикалов
+е
+е
+е
+е
Слайд 21Перехватчики радикалов
В качестве системы защиты организма от повреждающего действия радикалов кислорода
Аскорбиновая кислота (витамин С)
a –токоферол (витамин Е)
Сульфгидрильные соединения (глутатион, цистеин)
Мочевая кислота
Одно- и многоатомные спирты (этанол, рибоза, глюкоза)
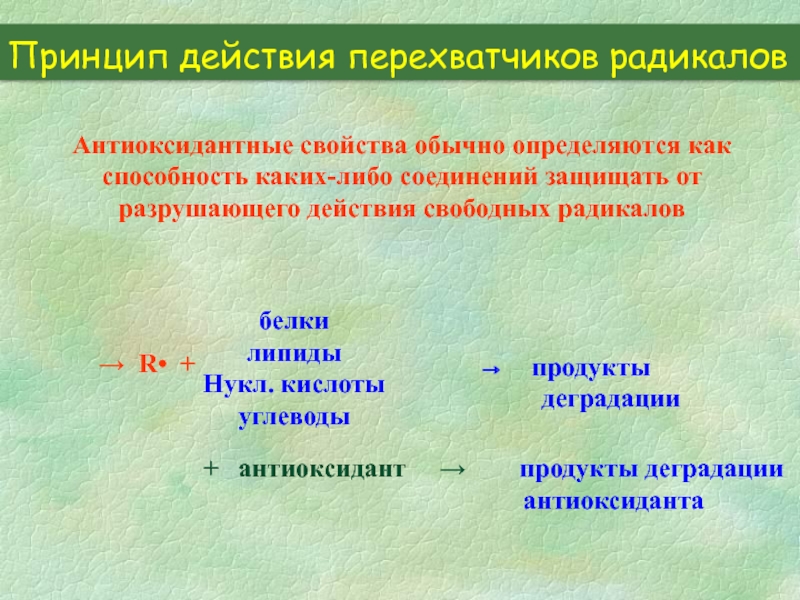
Слайд 22Принцип действия перехватчиков радикалов
Антиоксидантные свойства обычно определяются как способность каких-либо соединений
→ R• +
белки
липиды
Нукл. кислоты
углеводы
продукты
деградации
+ антиоксидант → продукты деградации
антиоксиданта
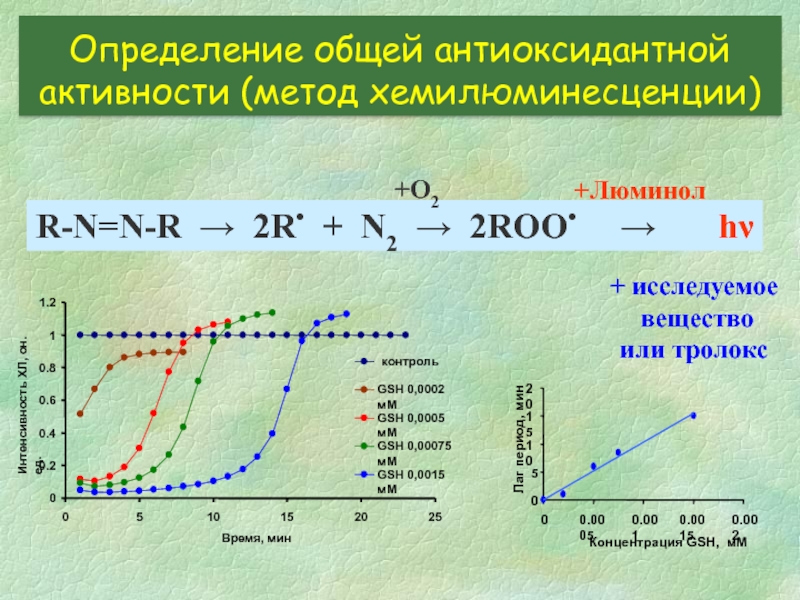
Слайд 23R-N=N-R → 2R• + N2 → 2ROO• →
+O2
+Люминол
0
0.2
0.4
0.6
0.8
1
1.2
0
5
10
15
20
25
Время, мин
Интенсивность ХЛ, он. ед.
контроль
GSH 0,0002 мМ
GSH 0,0005 мМ
GSH 0,00075 мМ
GSH 0,0015 мМ
0
5
10
15
20
0
0.0005
0.001
0.0015
0.002
Концентрация GSH, мМ
Лаг период, мин
Определение общей антиоксидантной активности (метод хемилюминесценции)
+ исследуемое
вещество
или тролокс
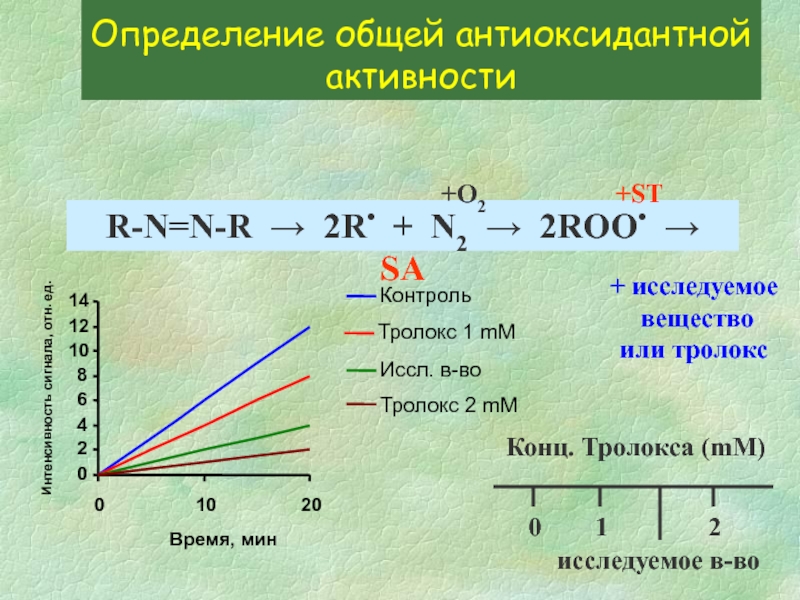
Слайд 24Определение общей антиоксидантной активности
R-N=N-R → 2R• + N2 → 2ROO• →
+O2
+ST
0
2
4
6
8
10
12
14
0
10
20
Время, мин
Интенсивность сигнала, отн. ед.
Контроль
Тролокс 1 mM
Иссл. в-во
Тролокс 2 mM
+ исследуемое
вещество
или тролокс
Конц. Тролокса (mM)
0
1
2
исследуемое в-во
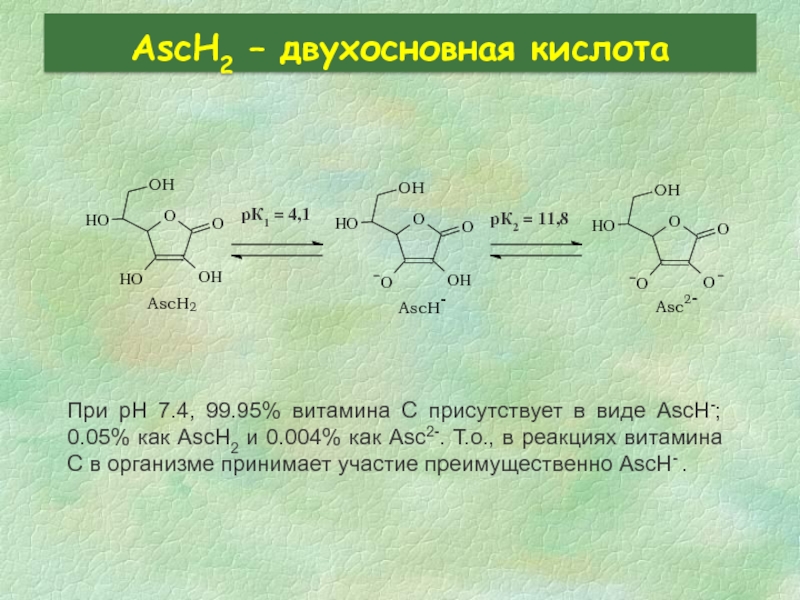
Слайд 26AscH2 – двухосновная кислота
При pH 7.4, 99.95% витамина C присутствует в
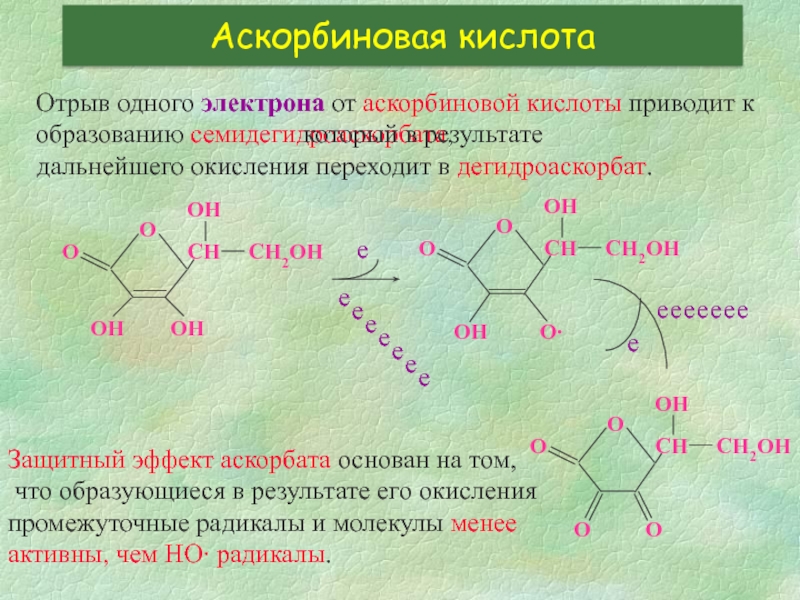
Слайд 27Аскорбиновая кислота
Отрыв одного электрона от аскорбиновой кислоты приводит к
образованию семидегидроаскорбата,
е
е
е
е
е
е
е
дальнейшего окисления переходит в дегидроаскорбат.
е
е
е
е
е
е
е
Защитный эффект аскорбата основан на том,
что образующиеся в результате его окисления
промежуточные радикалы и молекулы менее
активны, чем НО∙ радикалы.
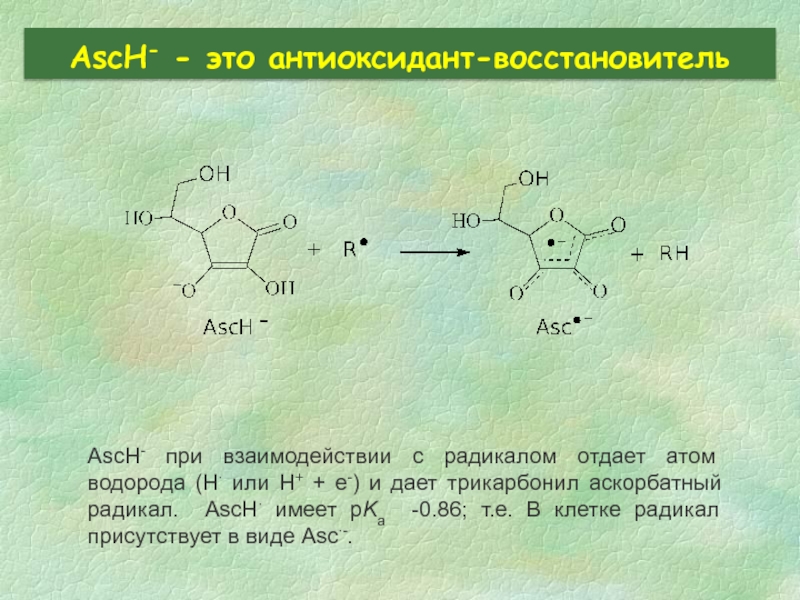
Слайд 30AscH- - это антиоксидант-восстановитель
AscH- при взаимодействии с радикалом отдает атом водорода
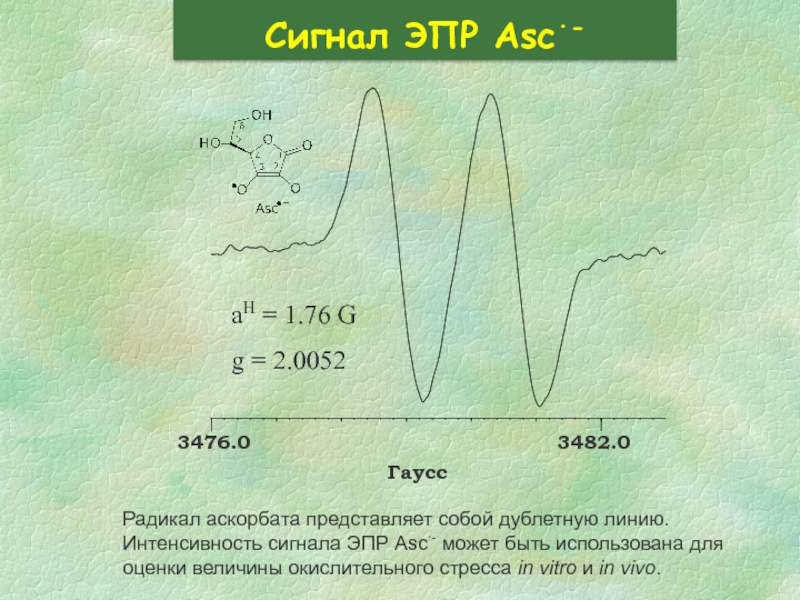
Слайд 31Сигнал ЭПР Asc∙-
Радикал аскорбата представляет собой дублетную линию. Интенсивность сигнала
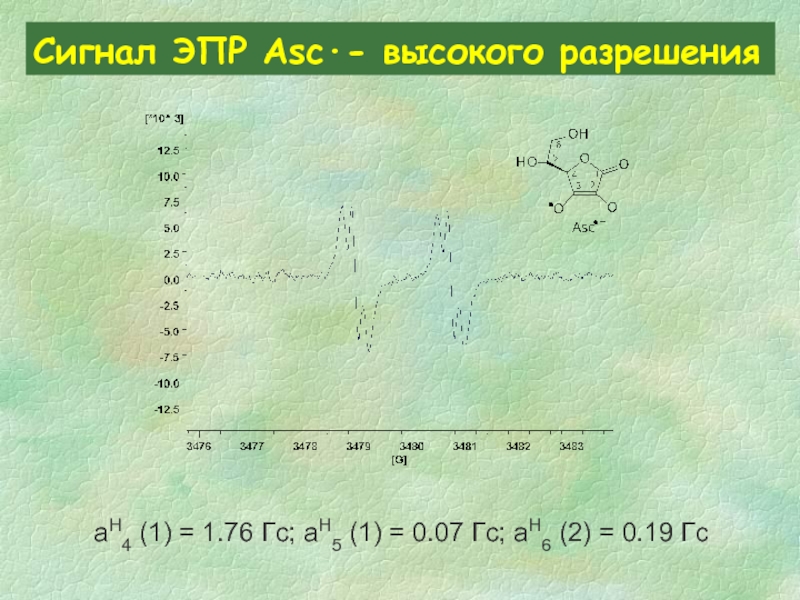
Слайд 32Сигнал ЭПР Asc∙- высокого разрешения
aH4 (1) = 1.76 Гс; aH5
Слайд 33Константы скорости взаимодействия аскорбата с некоторыми радикалами
Приведенные константы скорости соответствуют реакции:
AscH−
Слайд 35Asc∙- - индикатор присутствия ионов переходных металлов
В отсутствие ионов Fe3+ окисление
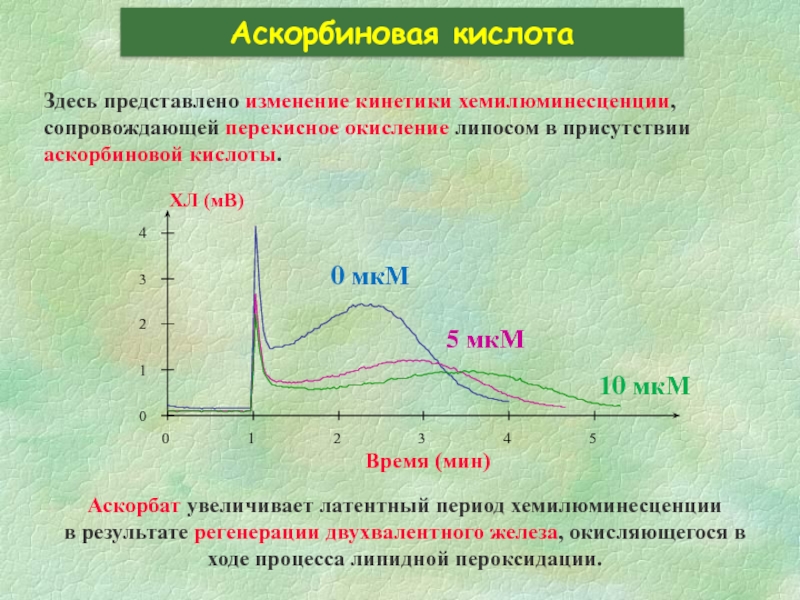
Слайд 36Аскорбиновая кислота
Здесь представлено изменение кинетики хемилюминесценции, сопровождающей перекисное окисление липосом в
Аскорбат увеличивает латентный период хемилюминесценции
в результате регенерации двухвалентного железа, окисляющегося в ходе процесса липидной пероксидации.
0 мкМ
5 мкМ
10 мкМ















![Asc∙- - маркер окислительного стресса[Asc∙-] – пропорциональна степени окисления аскорбата](/img/tmb/5/425495/5906e63dc9cea2b36108b2f9d6b55f98-800x.jpg)