- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Сульфатна кислота. Фізичні та хімічні властивості сульфатної кислоти презентация
Содержание
- 1. Сульфатна кислота. Фізичні та хімічні властивості сульфатної кислоти
- 2. SO2 SO3 Н2S S Н2SO3
- 3. Без цієї речовини не обходиться жодна галузь
- 4. Цю кислоту можна придбати в магазині під назвою «акумуляторна» Н2SO4
- 5. Сульфатна кислота. Фізичні та хімічні властивості сульфатної кислоти. Тема уроку:
- 6. Мета уроку: познайомитися з фізичними і хімічними властивостями сульфатної кислоти.
- 7. молекулярна формула структурна формула Характеристика:
- 8. Фізичні властивості H2SO4 конц : Робота з
- 9. Правила з ТБ під час роботи з
- 10. Хімічні властивості H2SO4 роз. : Дослідіть хімічні
- 11. Хімічні властивості H2SO4 конц. : 1. H2SO4
- 12. 2. H2SO4 конц. – сильний окисник, тому
- 13. не реагують зовсім
- 14. Виробництво сульфатної кислоти контактним способом
- 15. Сировина: FeS2 – залізний колчедан, пірит
- 16. І етап – некаталітичне окиснення.
- 17. Аерозолі сірчаної і сірчистої кислот конденсуються у
- 18. H2SO4 Виробництво
- 19. З якими із запропонованих речовин: Na
- 20. Домашнє завдання: § 30 Впр. 4, 8 с.135
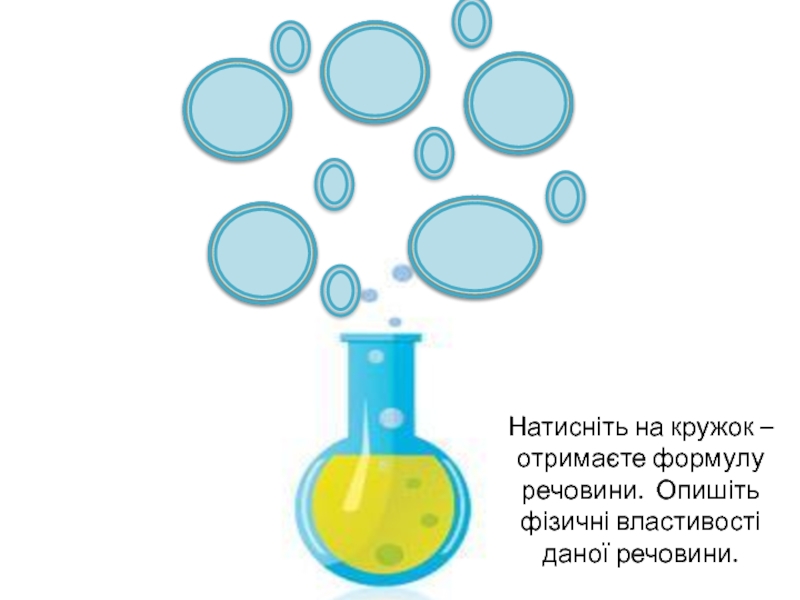
Слайд 2SO2
SO3
Н2S
S
Н2SO3
Натисніть на кружок – отримаєте формулу речовини. Опишіть фізичні властивості даної
Слайд 3Без цієї речовини не обходиться жодна галузь хімічної промисловості. Тому дану
Здогадайтеся, яку речовину ми будемо сьогодні вивчати.
Слайд 7молекулярна формула
структурна формула
Характеристика:
двохосновна;
оксигеновмісна;
сильний електроліт;
H2SO4 роз. - слабкий окисник;
Слайд 8Фізичні властивості H2SO4 конц :
Робота з підручником с. 128
Безбарвна
Важка ρ = 1,84 г/см3
Нелетка, без запаху
Гігроскопічна (поясніть, чому маса стакана з H2SO4 з часом зростає?)
При розчинені у воді виділяє багато теплоти.
Слайд 9Правила з ТБ під час роботи з H2SO4.
При розведенні треба
При попаданні Н2SO4 на шкіру, її потрібно змити великою кількістю води і нейтралізувати розчином питної соди.
Н2SO4
Н2O
Слайд 10Хімічні властивості H2SO4 роз. :
Дослідіть хімічні властивості розведеної сульфатної кислоти,
H2SO4 роз— сильний електроліт, виявляє типові хімічні властивості кислот.
Слайд 11Хімічні властивості H2SO4 конц. :
1. H2SO4 конц. – дуже гігроскопічна. Вона
Натисніть на малюнок для перегляду відео досліду “Гігроскопічність сульфатної кислоти”
Слайд 122. H2SO4 конц. – сильний окисник, тому взаємодіє з металами незалежно
Натисніть на малюнок для перегляду відео досліду “взаємодія сульфатної кислоти з металами”.
Слайд 13
не реагують зовсім
Li Rb K Ba Sr Ca Na Mg
H2S S, H2S, SO2 SO2
При н.у не реагують
Допишіть рівняння реакції. Урівняйте методом електронного балансу.
H2SO4 конц + Na →
H2SO4 конц + Zn →
H2SO4 конц + Cu →
Слайд 15Сировина:
FeS2 – залізний колчедан, пірит
S – сірка
Сu2S, ZnS, PbS –
СаSO4 ∙ 2H2O – гіпс
Н2S – сірководень
Процеси:
FeS2
S SO2 → SO3 → H2SO4
Н2S
Слайд 16І етап – некаталітичне окиснення.
FeS2 + O2 →
ІІ етап –каталітичне
V2O5
SO2 + O2 →
ІІІ етап – гідратація.
SO3 + H2O =
Слайд 17Аерозолі сірчаної і сірчистої кислот конденсуються у водяній парі атмосфери і
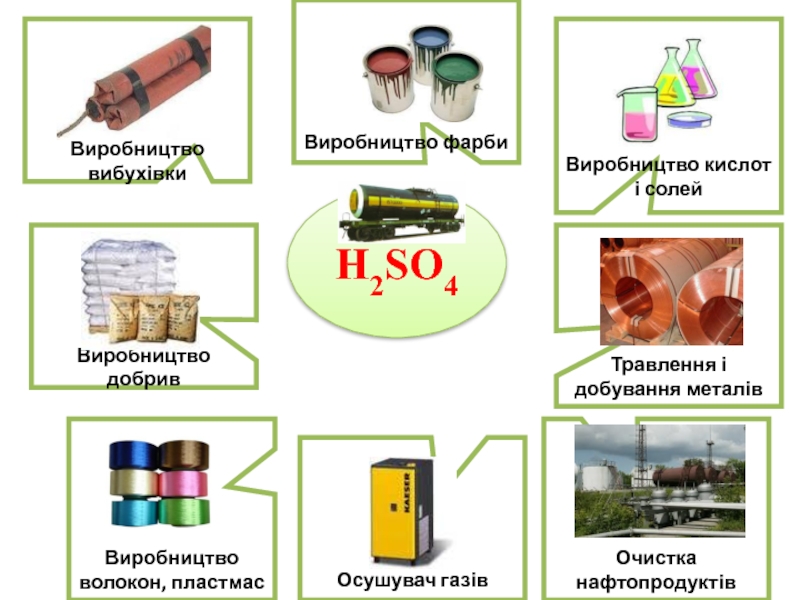
Слайд 18H2SO4
Виробництво вибухівки
Виробництво добрив
Виробництво волокон, пластмас
Виробництво кислот і солей
Виробництво фарби
Очистка нафтопродуктів
Травлення і добування металів
Осушувач газів