- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Строение электронных оболочек атомов презентация
Содержание
- 2. Строение электронных оболочек атомов Задачи урока: Познакомиться
- 3. Соотнесите химические формулы и формы существования химических
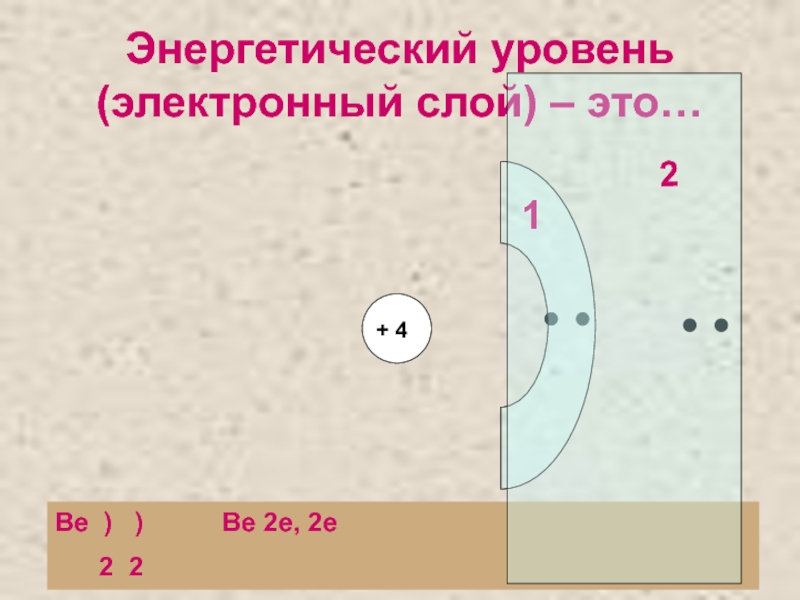
- 4. Энергетический уровень (электронный слой) – это…
- 5. Число энергетических уровней = номеру периода Максимальное
- 6. Запишите схемы строения электронных оболочек атомов: углерода,
- 7. Повторение 1. Электроны в атомах располагаются …
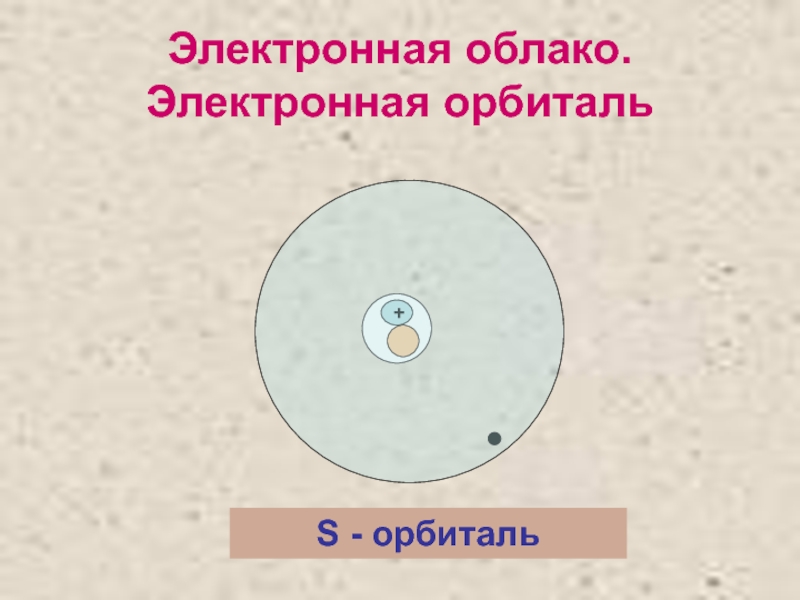
- 8. Электронная облако. Электронная орбиталь + S - орбиталь
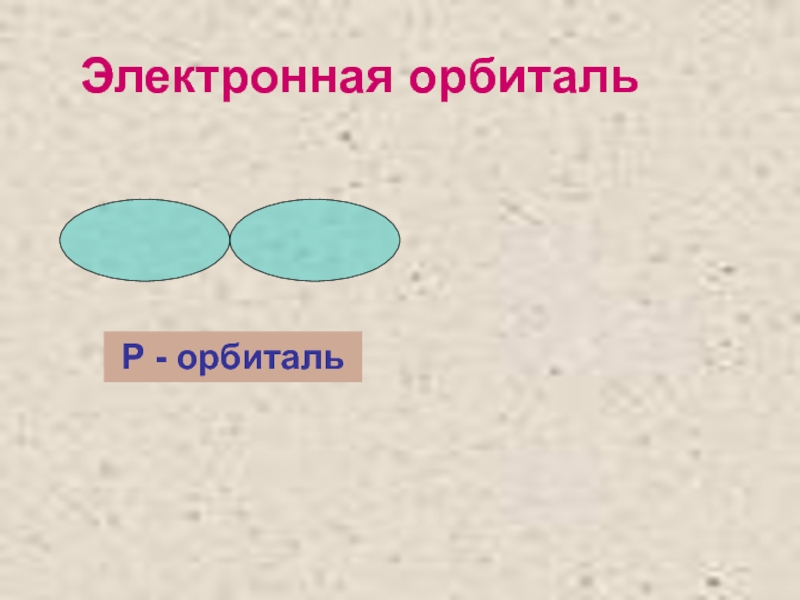
- 9. Электронная орбиталь Р - орбиталь
- 10. Электронная орбиталь Р - орбитали
- 11. На одной орбитали не может находится более
- 12. Электронные формулы H )1 1S1 He )2
- 13. Повторение 1. Пространство вокруг ядра атома
- 14. По положению в Периодической таблице определите:
Слайд 2Строение электронных оболочек атомов
Задачи урока:
Познакомиться со строением электронных оболочек атомов
Научиться составлять
Слайд 3Соотнесите химические формулы и формы существования химических элементов
1) 2S
2) S8
3) 3H2O
4)
5) 2Al
6) CuO
1) свободные атомы
2) простые вещества
3) сложные вещества
1
2
3
3
1
3
Слайд 5Число энергетических уровней = номеру периода
Максимальное число электронов на уровне =
1 уровень – 2 электрона
2 уровень – 8 электронов
3 уровень – 18 электронов
Максимальное число электронов на внешнем уровне - 8
Завершенный уровень -…
Слайд 6Запишите схемы строения электронных оболочек атомов: углерода, азота,кислорода, фтора.
Соотнесите число электронов
Число электронов на внешнем уровне равно номеру группы
Слайд 7Повторение
1. Электроны в атомах располагаются …
2. Электроны одного энергетического уровня имеют
3. Число уровней равно ….
4. Максимальное число электронов на уровне = …
5. Уровень, содержащий максимальное количество электронов называют …
6. Завершенный внешний уровень содержит ….. электронов
7. Число электронов на внешнем уровне = …
Слайд 11На одной орбитали не может находится более 2 электронов
Количество орбиталей на
1 уровень – S - орбиталь
2 уровень – S, P - орбитали
Слайд 13Повторение
1. Пространство вокруг ядра атома ,где наиболее вероятно нахождение электрона
2. S и P – орбитали различаются ….
3. Каждый уровень начинается ... орбиталью
4. На S – орбитали может находиться …. электрона, на Р – орбиталях - …. Электронов
5. Объясните, что обозначают цифры и буквы в записи: 1S2 2S22P2
Слайд 14
По положению в Периодической таблице определите: а) что лучший окислитель -
Возрастают или уменьшаются восстановительные свойства элементов в ряду Li-Na-K-Rb-Cs?