- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Строение атома углерода презентация
Содержание
- 1. Строение атома углерода
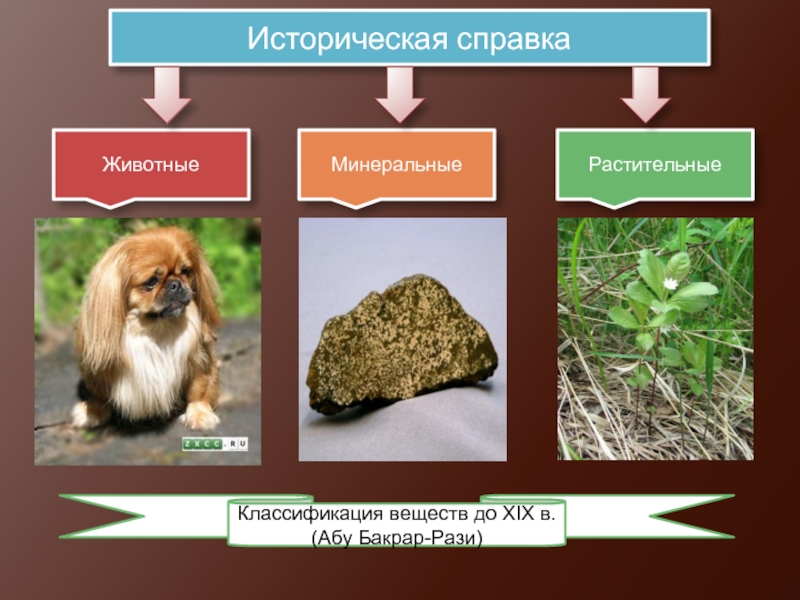
- 2. Классификация веществ до XIX в. (Абу Бакрар-Рази) Животные Минеральные Растительные Историческая справка
- 3. Долгое время считали, что органические вещества содержатся только в организмах (витализм)
- 4. Берцелиус Йёнс Якоб (1779-1848)
- 5. В середине 19 столетия были проведены первые
- 6. Органическая химия - это химия соединений углерода (Кекуле, середина XIX в.)
- 7. Особенности органических веществ.
- 8. 1) В состав органических
- 9. 4) Органические вещества построены более сложно, чем
- 10. Самая большая формула: C5750 H7227 О4131 N2215 S690 В составе ДНК бактериофагов (19913 атомов!)
- 11. Строение атома углерода. Валентные состояния атома углерода.
- 12. Графическая и электронная формула внешнего
- 13. Графическая и электронная формула внешнего энергетического уровня
- 14. Гибридизация – взаимное выравнивание электронных облаков в
- 15. Типы гибридизации: sp3-гибридизация sp2-гибридизация sp-гибридизация
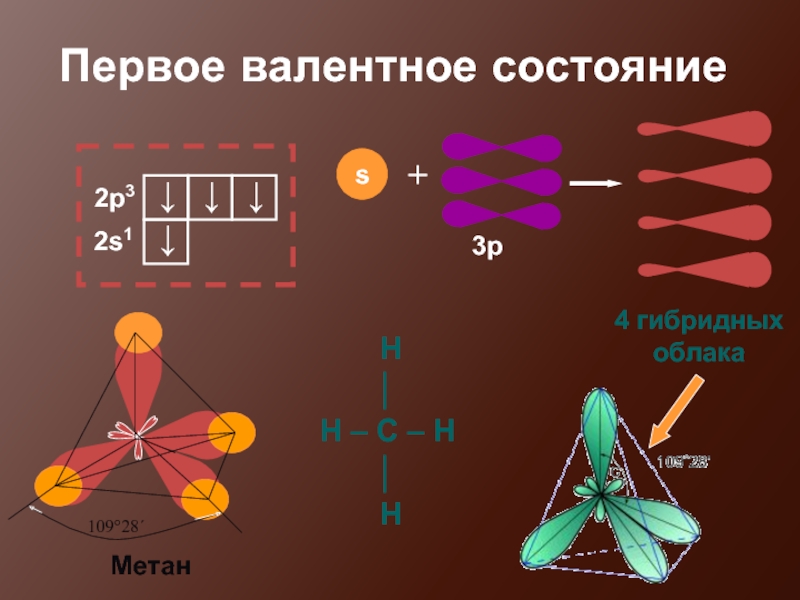
- 16. Первое валентное состояние 4 гибридных облака
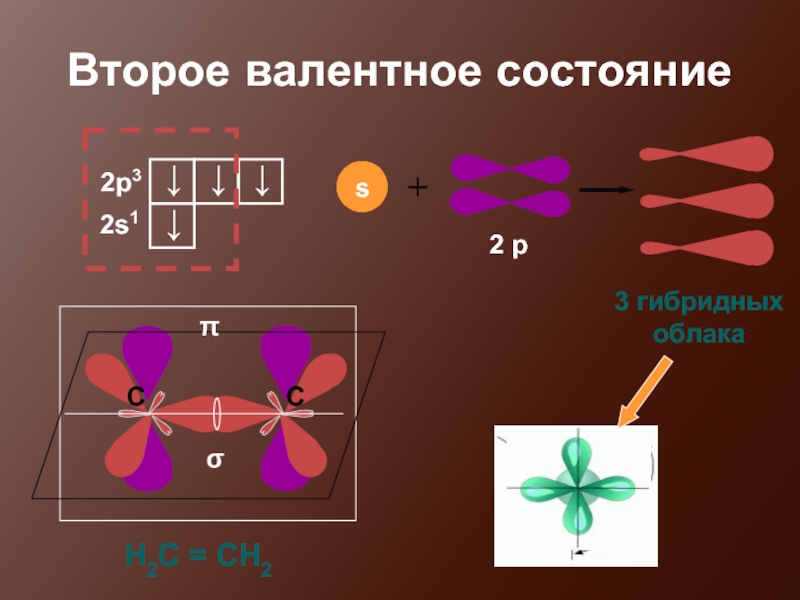
- 17. Второе валентное состояние 3 гибридных облака σ π Н2С = СН2
- 18. σ и π - связи Осевое перекрывание
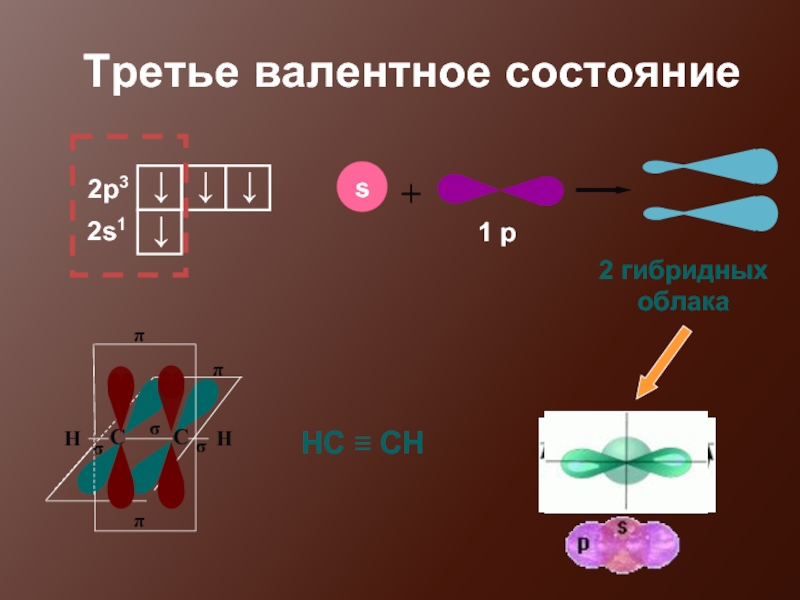
- 19. Третье валентное состояние 2 гибридных облака НС ≡ СН
- 20. ! Чем больше перекрывается электронных областей, тем
- 21. Проблемный вопрос: каким образом можно определить величину
- 22. 1) Что такое гибридизация? Какие бывают
Слайд 2Классификация веществ до XIX в. (Абу Бакрар-Рази)
Животные
Минеральные
Растительные
Историческая справка
Слайд 4Берцелиус Йёнс Якоб (1779-1848)
Впервые ввел термин органическая химия
Органическую химию определил как химию растительных и животных веществ, образующихся под влиянием особой «жизненной силы».
Слайд 5В середине 19 столетия были проведены первые синтезы органических веществ:
1828 г.
1842 г. русский химик Н.Н. Зинин получил анилин (C6H5NH2 )
1845 г. нем. химик А. Кольбе - уксусную кислоту (С2Н4О2)
1861 г. русский химик А.М. Бутлеров –сахаристое вещество
Слайд 8 1) В состав органических веществ входят углерод и
Слайд 94) Органические вещества построены более сложно, чем неорганические, и многие имеют
Слайд 10Самая большая формула:
C5750 H7227 О4131 N2215 S690
В составе ДНК бактериофагов
(19913 атомов!)
Слайд 12
Графическая и электронная формула внешнего энергетического уровня атома углерода
+6С 1s2
……
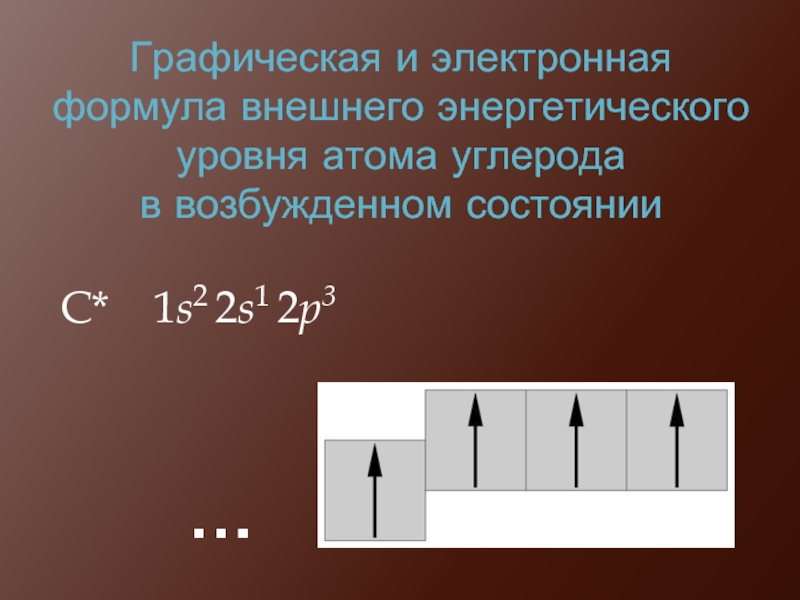
Слайд 13Графическая и электронная формула внешнего энергетического уровня атома углерода в возбужденном состоянии
С*
……
Слайд 14Гибридизация – взаимное выравнивание электронных облаков в атоме углерода по форме
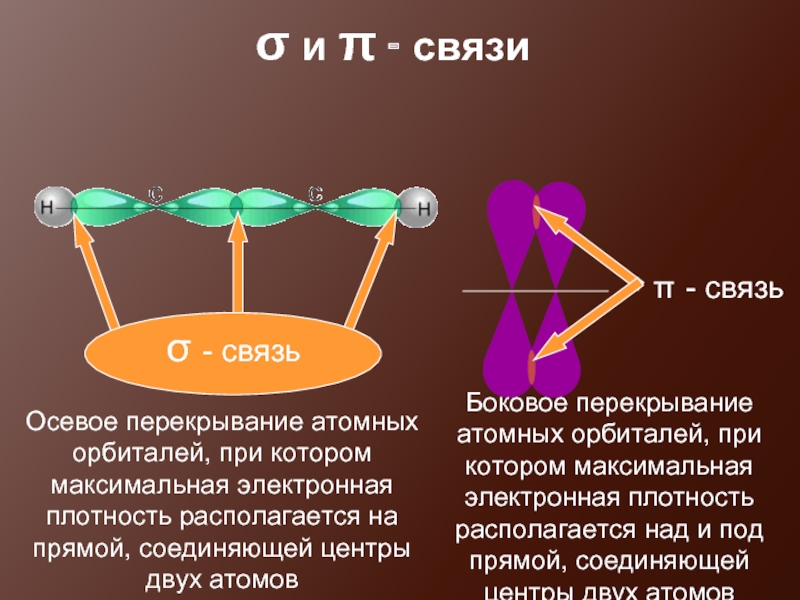
Слайд 18σ и π - связи
Осевое перекрывание атомных орбиталей, при котором максимальная
π - связь
Боковое перекрывание атомных орбиталей, при котором максимальная электронная плотность располагается над и под прямой, соединяющей центры двух атомов
Слайд 20! Чем больше перекрывается электронных областей, тем больше выделяется энергии –
L C – C – 0,154 нм – первое гибридное состояние
L С = С – 0,134 нм – второе гибридное состояние
L С ≡ С – 0,112 нм – третье гибридное состояние
L С – Н – мало изменяется от класса к классу и равна, примерно, 0,111 нм.
Слайд 21Проблемный вопрос:
каким образом можно определить величину энергии связи?
Е С – С
Е С = С - 614 кДж/моль
Е С ≡ С – 840 кДж/моль
Е С- Н – 415 кДж/моль