- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Строение атома кремния презентация
Содержание
- 1. Строение атома кремния
- 3. Строение атома кремния
- 4. Строение атома Положение в ПС: период III;
- 5. Свойства атома Si0 - 4е
- 7. Физические свойства кремния Кремний – неметалл, существует
- 8. Кристаллическая структура кремния Кристаллическая решетка
- 9. Электрофизические свойства Элементарный кремний —
- 10. Кремний в природе Кремний в свободном виде
- 11. Кремень
- 12. Разновидности минералов на основе оксида кремния
- 13. Знаете ли вы, что… В чистом виде
- 14. Знаете ли вы, что.. Кремний в
- 15. Знаете ли вы, что…
- 16. Знаете ли вы, что.. Способ
- 17. Получение кремния В промышленности кремний получают восстанавливая
- 18. Получение кремния Лабораторный способ получения:
- 19. Химические свойства кремния Химически кремний малоактивен.
- 20. Химические свойства кремния При нагревании до
- 21. Химические свойства кремния с хлором, бромом и
- 22. Химические свойства кремния При взаимодействии с металлом,
- 23. Химические свойства кремния С водородом кремний непосредственно
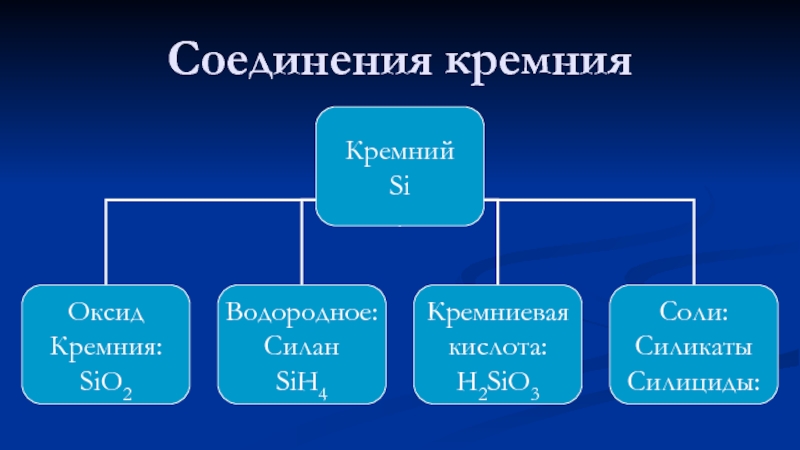
- 24. Соединения кремния
- 25. Свойства оксида
- 26. Свойства кислот
- 27. Соли
- 28. Применение кремния и его соединений Стекло Цемент Кирпич Фарфор Фаянс Клей Силикон Асбест Гранит Керамика
Слайд 4Строение атома
Положение в ПС: период III; группа IV, главная;
Заряд ядра: +14
Относительная атомная масса: Ar (Si)=28
Строение атома: p=14, e=14, n=28 - 14 =14
Электронная формула: +14 Si 2e;8e;4e;
+14 Si 1s2 2s2 2p6 3s2 3p2
Неметалл;
Слайд 5Свойства атома
Si0
- 4е
восстановитель
+ 4е
окислитель
Si+4
Si-4
Кремний, отдавая все внешние электроны более ЭО
Принимая 4 электрона на свой внешний энергетический уровень, восстанавливается до Si -4;
Слайд 7Физические свойства кремния
Кремний – неметалл, существует в кристаллическом и аморфном состоянии.
Кристаллический
р = 2,33 г/см3; t пл. = 14150С; tкип. = 35000С;
Слайд 8Кристаллическая структура кремния
Кристаллическая решетка
кремния кубическая
гранецентрированная типа алмаза.
между Si – Si, твердость кремния значительно меньше, чем алмаза.
Кремний хрупок, только при нагревании выше 8000С.
Слайд 9Электрофизические свойства
Элементарный кремний —
На электрофизические свойства
кристаллического кремния большое
влияние оказывают содержащиеся
в нем микропримеси.
Для получения монокристаллов кремния
с дырочной проводимостью в кремний
вводят добавки элементов III-й группы —
бор, алюминия, галлия и индия, с электронной проводимостью —
добавки элементов V-й группы — фосфора, мышьяка или сурьма.
Слайд 10Кремний в природе
Кремний в свободном виде в природе не встречается.
Кремний –
В природе встречается в
виде кремнезема (SiO2), силикатов и алюмосиликатов.
Слайд 11Кремень
Кремень, именно этот
невзрачный и очень
прочный камень,
положил
начало каменному
веку – веку
кремневых орудий труда.
Причин две:
- распространенность и доступность кремния;
- способность образовывать при сколе острые режущие края;
Слайд 12Разновидности минералов на основе оксида кремния
Агат
Горный
хрусталь
Цитрин
Кошачий
глаз
Аметист
Яшма
Сердолик
Опал
Слайд 13Знаете ли вы, что…
В чистом виде кремний был выделен
в 1811 году
Жозеф Луи Гей-Люссак
Луи Жаком Тенор
Слайд 14Знаете ли вы, что..
Кремний в элементарном состоянии был впервые получен
Слайд 15Знаете ли вы, что…
введено в 1834 г.
российским химиком
Германом Ивановичем
Гессом.
Слайд 16
Знаете ли вы, что..
Способ получения кремния
в чистом виде разработан
Николаем
Бекетовым.
Кремний в России производится
на заводах:
г. Каменск - Уральский (Свердловская область)
г. Шелех (Иркутская область).
Слайд 17Получение кремния
В промышленности кремний получают восстанавливая расплав SiO2 коксом при
t
Слайд 19Химические свойства кремния
Химически кремний малоактивен.
При комнатной температуре реагирует только c
Si + 2F2→ SiF4
Слайд 20Химические свойства кремния
При нагревании до 400 – 5000С кремний реагирует с
Si + O2 → SiO2
Слайд 21Химические свойства кремния
с хлором, бромом и йодом —
с образованием соответствующих
легко
Si + 2Cl2 → SiCl4
Si + 2Br2 → SiBr4
Слайд 22Химические свойства кремния
При взаимодействии с металлом, кремний проявляет себя как окислитель.
При взаимодействии образуются: силициды.
2Са + Si→ Ca2Si
Кремний легко растворяется в щелочах.
Слайд 23Химические свойства кремния
С водородом кремний непосредственно не реагирует.
Водородное соединение силан, получают
Ca2Si + 4HCl → 2CaCl2 + SiH4↑.