М.Л.
Харьков - 2016
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Строение атома. Атомные орбитали. Типы связей. Основные органогенные элементы, их роль презентация
Содержание
- 1. Строение атома. Атомные орбитали. Типы связей. Основные органогенные элементы, их роль
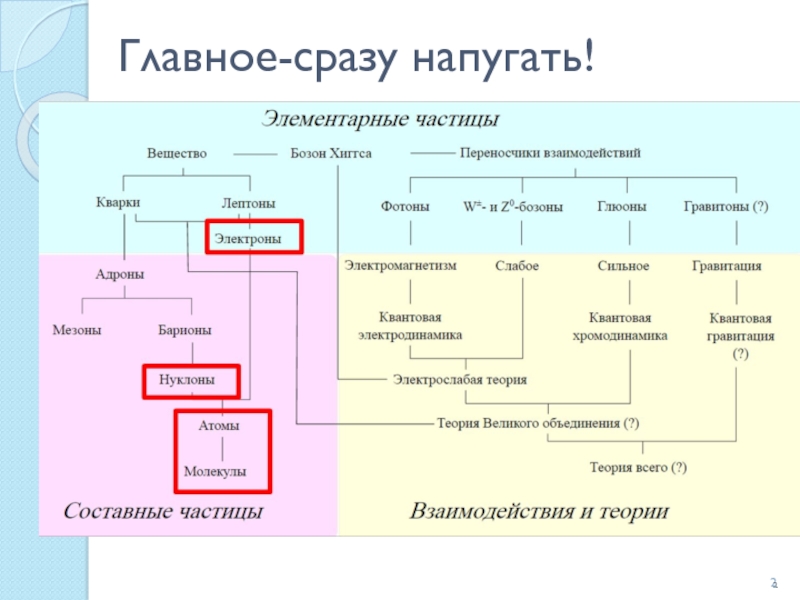
- 2. Главное-сразу напугать!
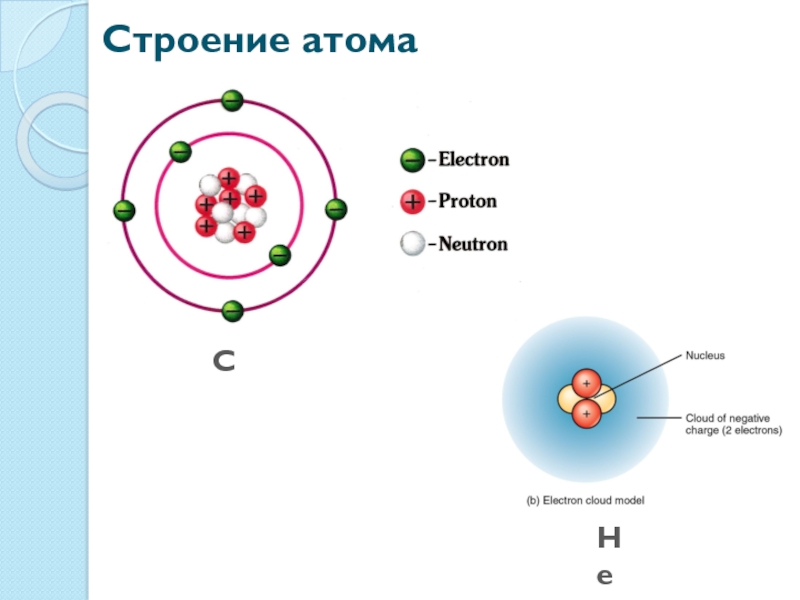
- 3. Строение атома He C
- 4. Типы атомных орбиталей
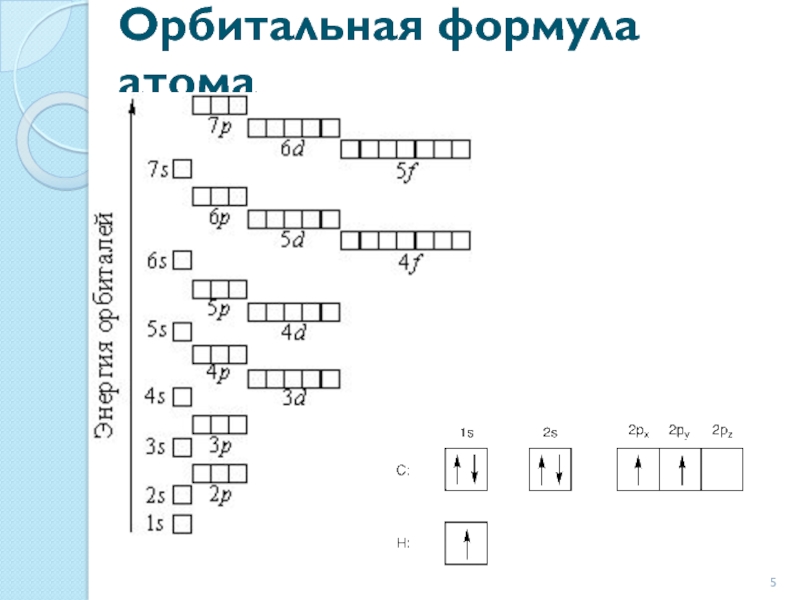
- 5. Орбитальная формула атома
- 6. Каждый уважающий себя атом стремится к электронному
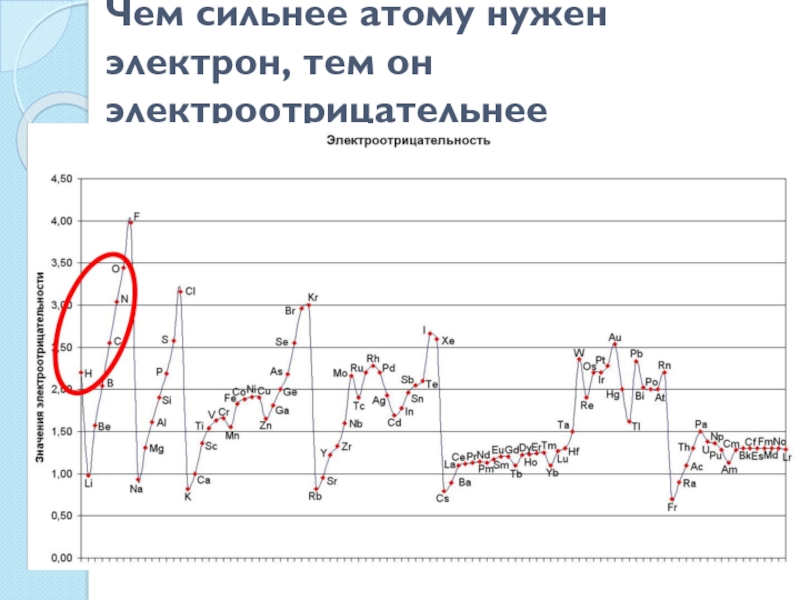
- 7. Чем сильнее атому нужен электрон, тем он электроотрицательнее
- 8. Приобрёл стабильность – стал ионом!
- 9. Понял, что нужно атому – понял, что такое валентность
- 10. Химическая связь Ковалентная Одноэлектронная n е
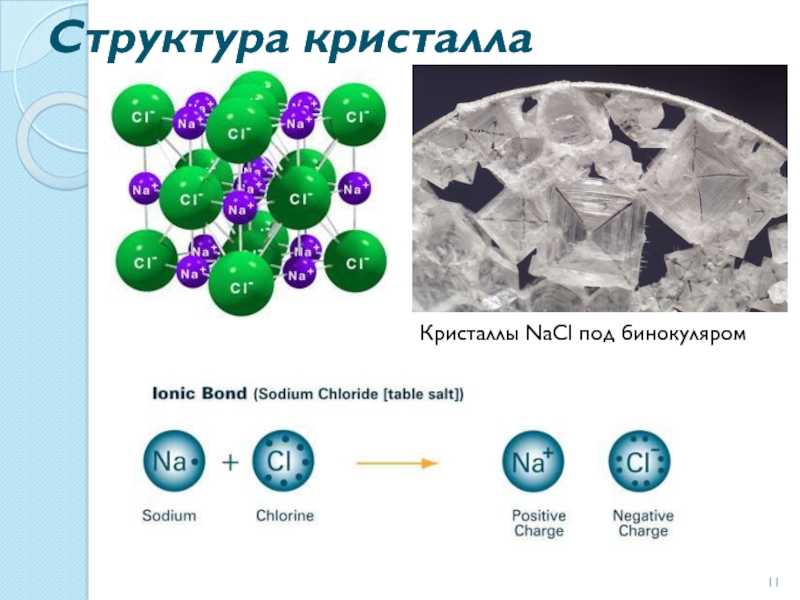
- 11. Структура кристалла Кристаллы NaCl под бинокуляром
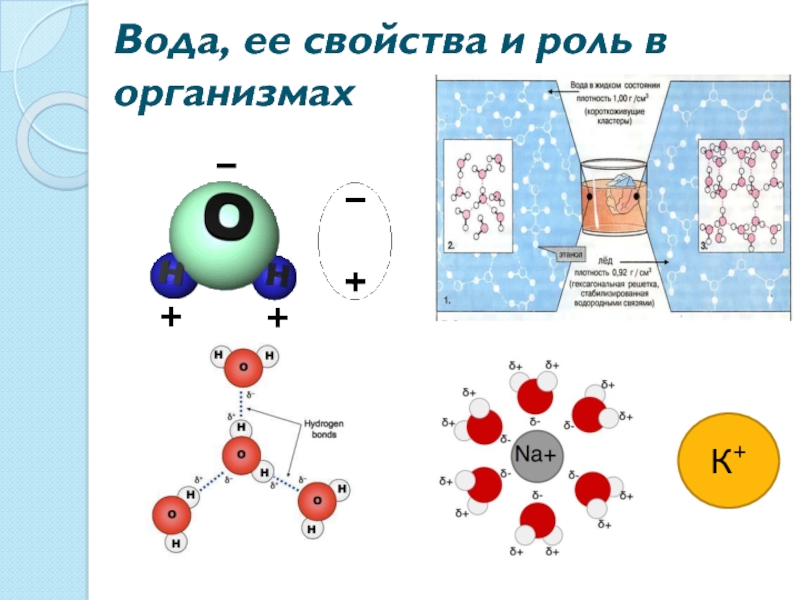
- 12. Вода, ее свойства и роль в организмах К+
- 13. Водородные связи Поверхностное натяжение воды, вязкость Поддержание
- 14. Гидрофобные взаимодействия Правило первое: полярному хорошо с полярным Правило второе: неполярному хорошо с неполярным
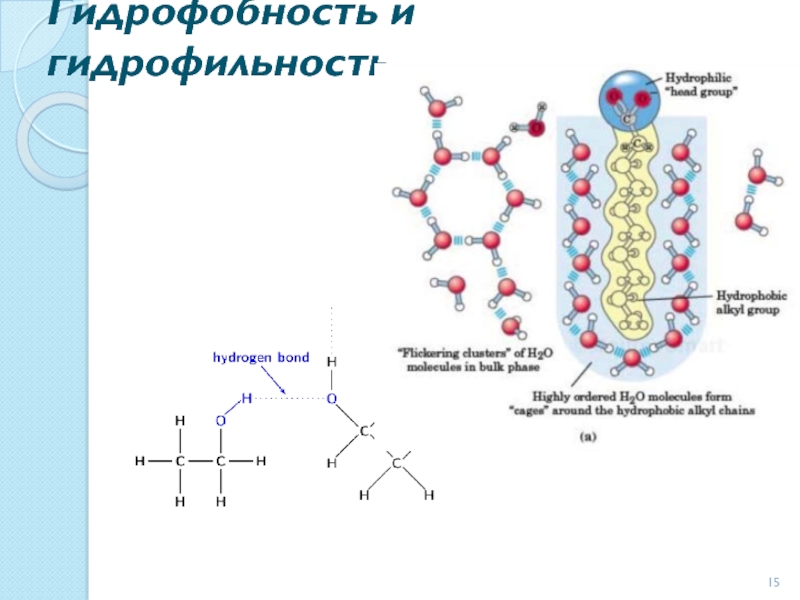
- 15. Гидрофобность и гидрофильность
- 16. Ван-дер-ваальсовы взаимодействия Сцепление частиц малых астероидов кольца́
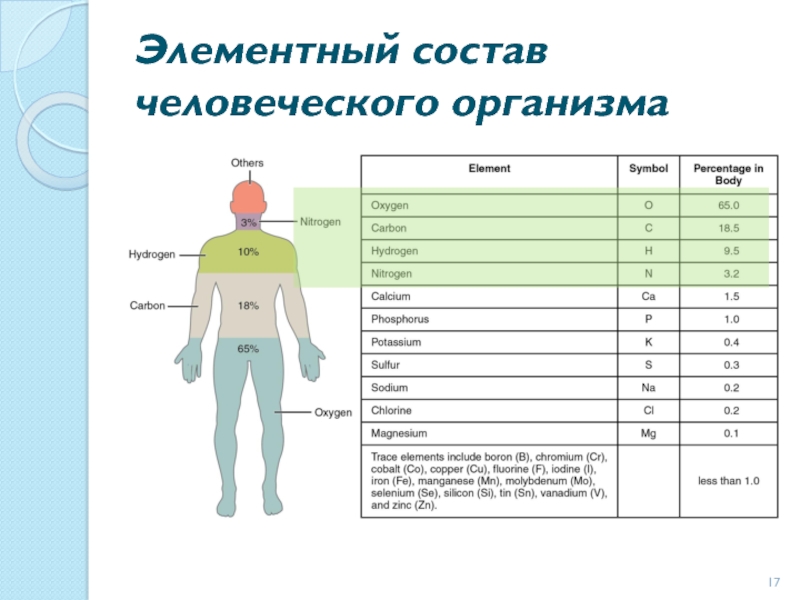
- 17. Элементный состав человеческого организма
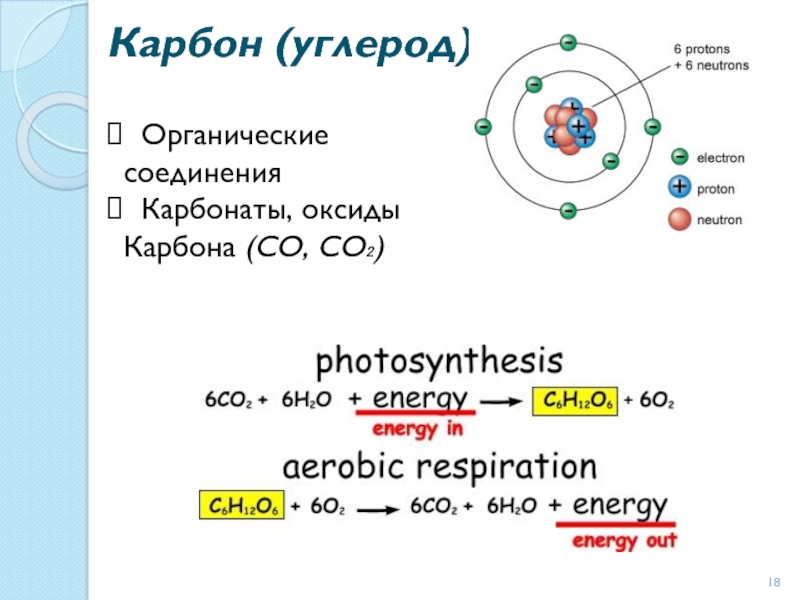
- 18. Карбон (углерод) Органические соединения Карбонаты, оксиды Карбона (СО, СО₂)
- 19. Оксиген (кислород) Вода Простые вещества
- 20. Гидроген Простые вещества (катионы водорода Н⁺)
- 21. Нитроген Тройная связь в молекуле азота (N₂)
- 22. Спасибо за внимание!
Слайд 1Строение атома. Атомные орбитали. Типы связей. Основные органогенные элементы, их роль
Шлахтер
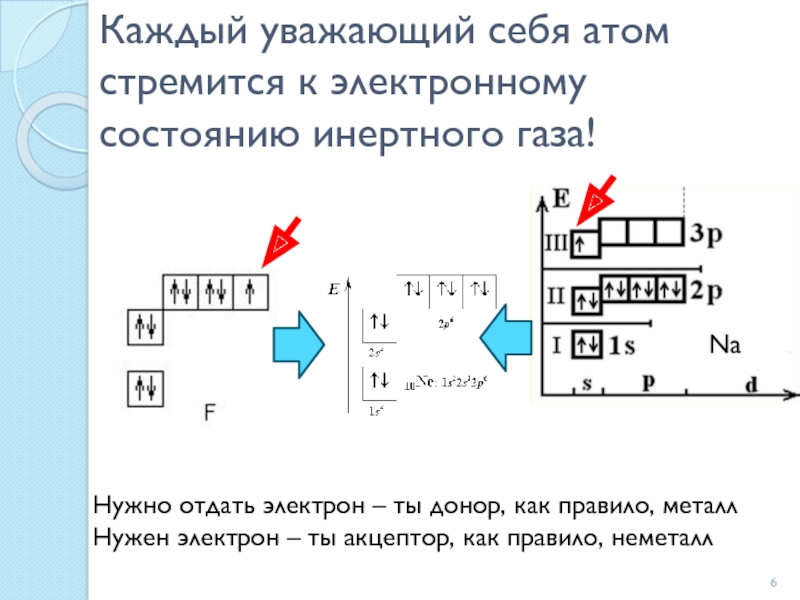
Слайд 6Каждый уважающий себя атом стремится к электронному состоянию инертного газа!
Нужно отдать
электрон – ты донор, как правило, металл
Нужен электрон – ты акцептор, как правило, неметалл
Нужен электрон – ты акцептор, как правило, неметалл
Слайд 10Химическая связь
Ковалентная
Одноэлектронная
n
е
Одинарная/кратная
е
Полярная
Неполярная
Трёхцентровая/многоцентровая
n
n
Сэндвичева
Металлическая
Ионная
Водородная
Ван-дер-ваальсова
Слайд 13Водородные связи
Поверхностное натяжение воды, вязкость
Поддержание структуры белка
Поддержание структуры нуклеиновых кислот
Поддержание структуры
углеводных полимеров
Гидрофобные взаимодействия
Гидрофобные взаимодействия
Слайд 14Гидрофобные взаимодействия
Правило первое: полярному хорошо с полярным
Правило второе: неполярному хорошо с
неполярным
Слайд 16Ван-дер-ваальсовы взаимодействия
Сцепление частиц малых астероидов кольца́ Сатурна
Способность гекконов взбираться по гладким
поверхностям, например, по стеклу
В системе редактирования геномов TALEN второй аминокислотный остаток в Repeat Variable Diresidue (RVD) взаимодействует с нуклеотидом,но при этом природа этого взаимодействия различна: аспарагин и аспарагиновая кислота образуют водородные связи c азотистыми основаниями, а изолейцин и глицин связываются с целевым нуклеотидом за счет сил Ван-дер-Ваальса.
В системе редактирования геномов TALEN второй аминокислотный остаток в Repeat Variable Diresidue (RVD) взаимодействует с нуклеотидом,но при этом природа этого взаимодействия различна: аспарагин и аспарагиновая кислота образуют водородные связи c азотистыми основаниями, а изолейцин и глицин связываются с целевым нуклеотидом за счет сил Ван-дер-Ваальса.
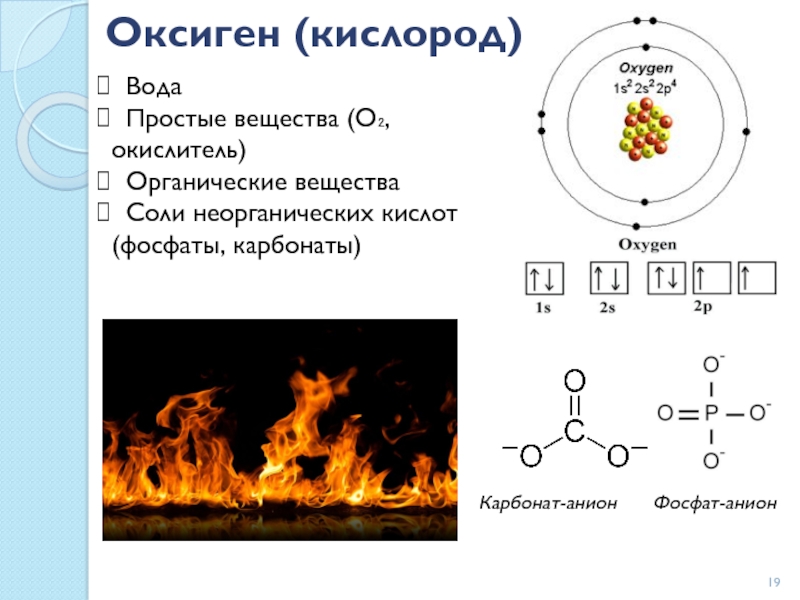
Слайд 19Оксиген (кислород)
Вода
Простые вещества (О₂, окислитель)
Органические вещества
Соли неорганических
кислот (фосфаты, карбонаты)
Карбонат-анион
Фосфат-анион
Слайд 20Гидроген
Простые вещества (катионы водорода Н⁺)
Вода
Все органические соединения
Неорганические кислоты
Хлоридная кислота
Аррениус
Если
молекула диссоциирует с образованием протона, то это кислота, если с образованием гидроксил-аниона, то это основание
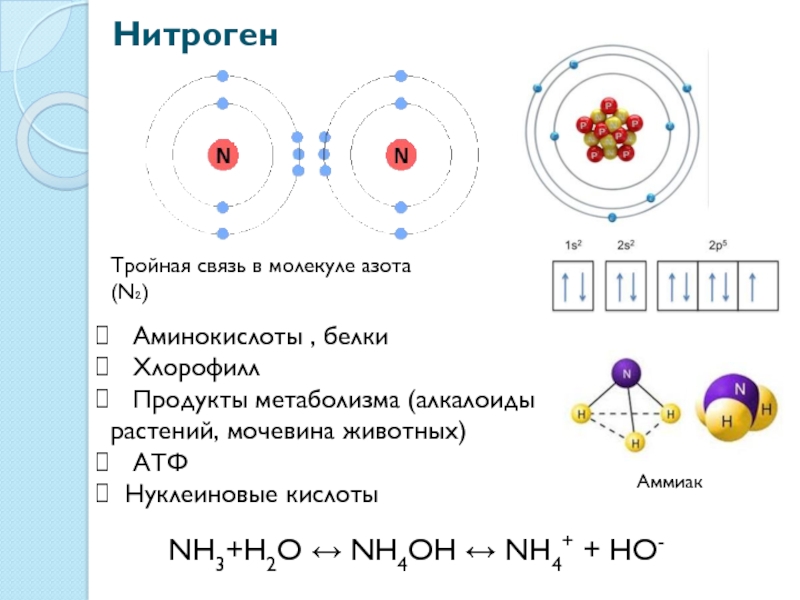
Слайд 21Нитроген
Тройная связь в молекуле азота (N₂)
Аминокислоты , белки
Хлорофилл
Продукты метаболизма (алкалоиды растений, мочевина животных)
АТФ
Нуклеиновые кислоты
Продукты метаболизма (алкалоиды растений, мочевина животных)
АТФ
Нуклеиновые кислоты
Аммиак
NH3+H2O ↔ NH4OH ↔ NH4+ + HO-