- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Степень окисления презентация
Содержание
- 1. Степень окисления
- 2. Цель урока: Разобраться, что такое «степень окисления» Научиться находить степень окисления по формуле
- 3. Поваренная соль NaCl «Хлеб да соль» -
- 4. Влияние Na на организм человека Хранят простое
- 5. Влияние Cl2 на организм человека Хлор – отравляющее вещество, применявшееся во время первой мировой войны
- 6. Образование сложного вещества Na0 +11 2е,8е,1е
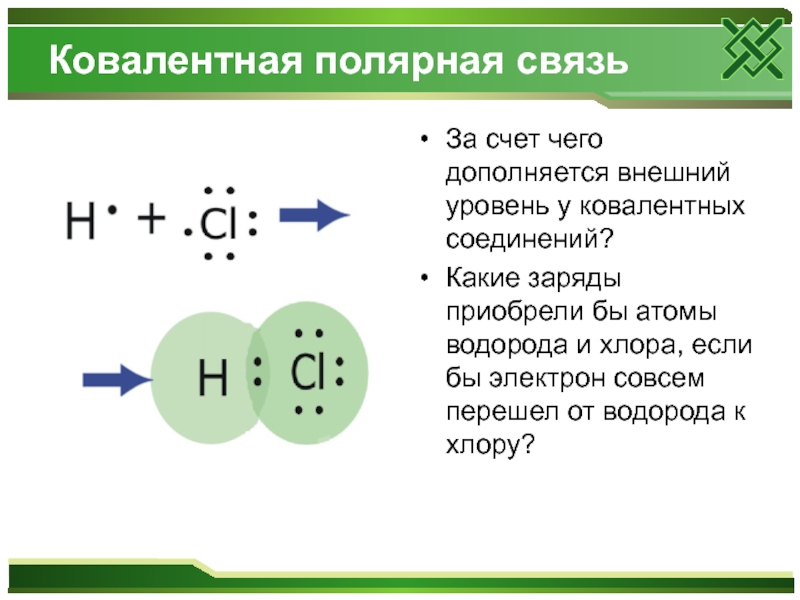
- 7. Ковалентная полярная связь За счет чего дополняется
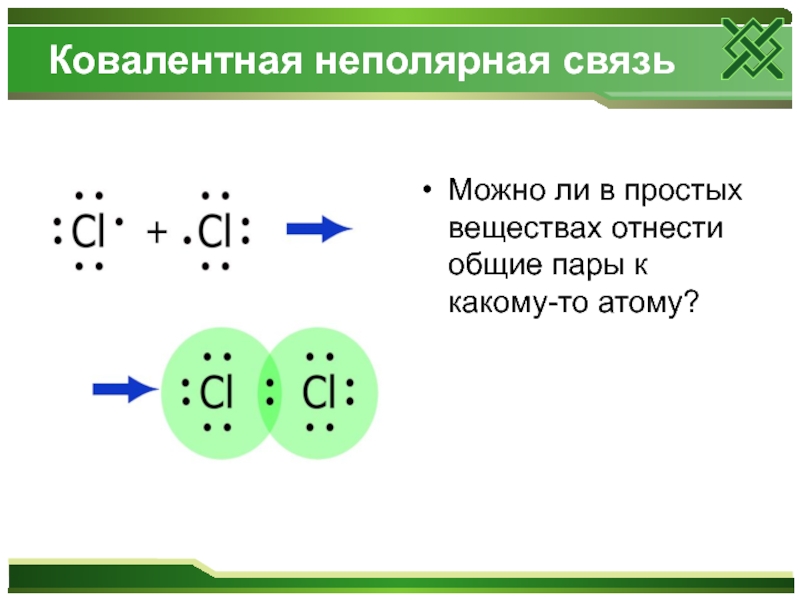
- 8. Ковалентная неполярная связь Можно ли в простых веществах отнести общие пары к какому-то атому?
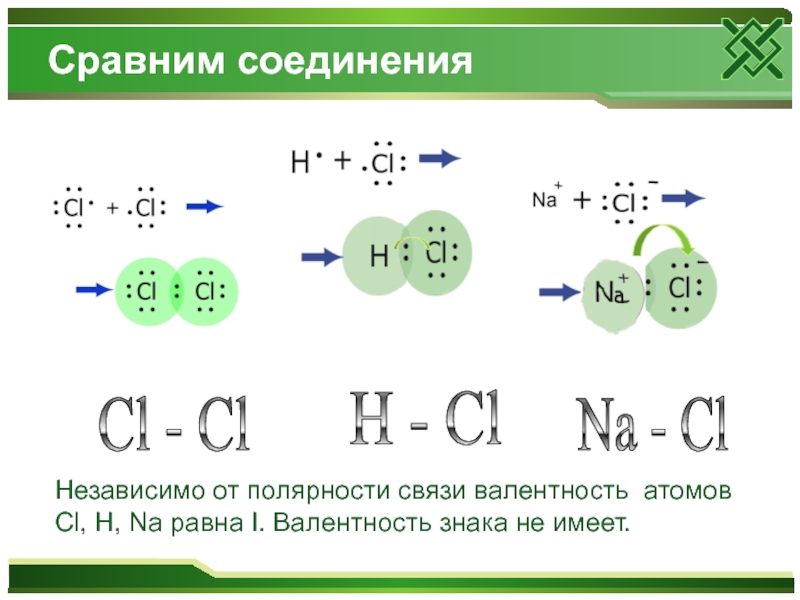
- 9. Сравним соединения H - Cl
- 10. Степень окисления – это условный заряд
- 11. Правила определения с.о. Сумма С.О. атомов равна
- 12. Возможные с.о. Положительная «+» равна числу отданных
- 13. Промежуточные с.о. Рассмотрим возможные с.о. серы –
- 14. Определение с.о. N2O3 На первом месте стоит
- 15. Задание 1 Определите С.О. по формулам Cl2O7, NaH, Na2S, MgO, H3N, N2, Al2S3, Cu2O
- 16. Домашнее задание §43, выучить основные понятия
Слайд 2Цель урока:
Разобраться, что такое «степень окисления»
Научиться находить степень окисления по формуле
Слайд 3Поваренная соль NaCl
«Хлеб да соль» - пожелание добра
«Надо вместе съесть
пуд соли, чтобы узнать человека»
За какое время это можно сделать?
Пуд – 16 кг
3,5 – 5,5 кг в год
Примерно 2 года
За какое время это можно сделать?
Пуд – 16 кг
3,5 – 5,5 кг в год
Примерно 2 года
Слайд 4Влияние Na на организм человека
Хранят простое вещество «натрий» как Кощееву смерть.
Как
может повлиять натрий на организм человека?
Слайд 5Влияние Cl2 на организм человека
Хлор – отравляющее вещество, применявшееся во время
первой мировой войны
Слайд 6Образование сложного вещества
Na0 +11 2е,8е,1е
Cl0 +17 2e,8e,7e
Какой вид связи
может образоваться между этими атомами?
Na0 + Cl0 → Na+ + Cl- → Na+Cl-
Na0 + Cl0 → Na+ + Cl- → Na+Cl-
Слайд 7Ковалентная полярная связь
За счет чего дополняется внешний уровень у ковалентных соединений?
Какие заряды приобрели бы атомы водорода и хлора, если бы электрон совсем перешел от водорода к хлору?
Слайд 8Ковалентная неполярная связь
Можно ли в простых веществах отнести общие пары к
какому-то атому?
Слайд 9Сравним соединения
H - Cl
Cl - Cl
Na - Cl
Независимо
от полярности связи валентность атомов Cl, H, Na равна I. Валентность знака не имеет.
Слайд 10Степень окисления –
это условный заряд атомов химических элементов в соединении,
вычисленный на основе предположения, что все соединения состоят из ионов
Слайд 11Правила определения с.о.
Сумма С.О. атомов равна нулю
С.о. атомов в простых веществах
= 0
С.о. фтора = -1
С.о. кислорода = -2 (кроме Н2О2-1, O+2F2)
С.о. водорода = +1 (кроме МеН-1)
С.о.Ме I, II, III групп = номеру группы
С.о неМе «+» = номеру группы
С.о. неМе «-» = 8 – номер группы
С.о. фтора = -1
С.о. кислорода = -2 (кроме Н2О2-1, O+2F2)
С.о. водорода = +1 (кроме МеН-1)
С.о.Ме I, II, III групп = номеру группы
С.о неМе «+» = номеру группы
С.о. неМе «-» = 8 – номер группы
Слайд 12Возможные с.о.
Положительная «+» равна числу отданных электронов. Максимальная с.о. равна номеру
группы
Отрицательная «-» равна числу принятых электронов. Минимальная с.о. равна 8 – номер группы
Нулевое значение с.о. имеют атомы в молекулах с неполярной связью
Отрицательная «-» равна числу принятых электронов. Минимальная с.о. равна 8 – номер группы
Нулевое значение с.о. имеют атомы в молекулах с неполярной связью
Слайд 13Промежуточные с.о.
Рассмотрим возможные с.о. серы – S
Максимальная +6 SO3
Минимальная -2
H2S
Сера может проявлять с.о. 0,+2,+4 – это промежуточные с.о.
Сера может проявлять с.о. 0,+2,+4 – это промежуточные с.о.
Слайд 14Определение с.о.
N2O3
На первом месте стоит элемент с «+» с.о., на втором
с «-»
У кислорода постоянная с.о.=-2
У азота переменная с.о.
x -2
N2O3
У кислорода постоянная с.о.=-2
У азота переменная с.о.
x -2
N2O3