НГУ - 2009
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Становление органической химии как отдельной науки. (Модуль 1) презентация
Содержание
- 1. Становление органической химии как отдельной науки. (Модуль 1)
- 2. Становление органической химии как отдельной науки 1 1. Длинные углерод-углеродные цепи 2. Изомерия
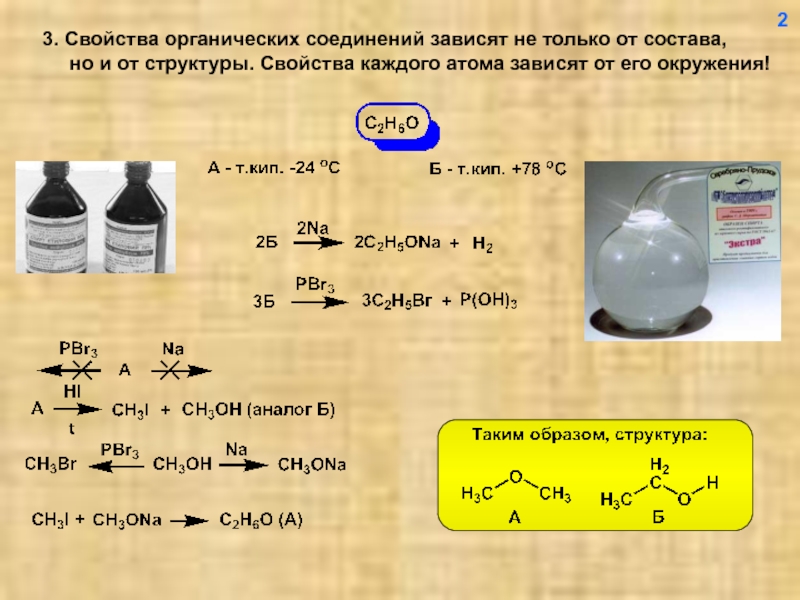
- 3. 3. Свойства органических соединений зависят не только
- 4. Установление состава органического соединения 1. Установление индивидуальности 2. Элементный анализ (сжигание) 3
- 5. 3. Определение молекулярной массы (эбулиоскопия или криоскопия) 4
- 6. От атомов к молекулам Химическая связь Необходимое
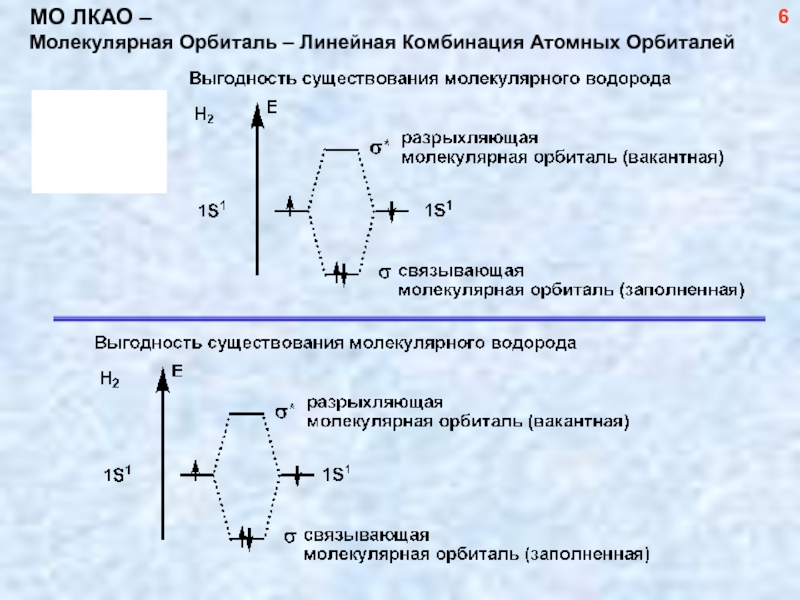
- 7. МО ЛКАО – Молекулярная Орбиталь – Линейная Комбинация Атомных Орбиталей 6
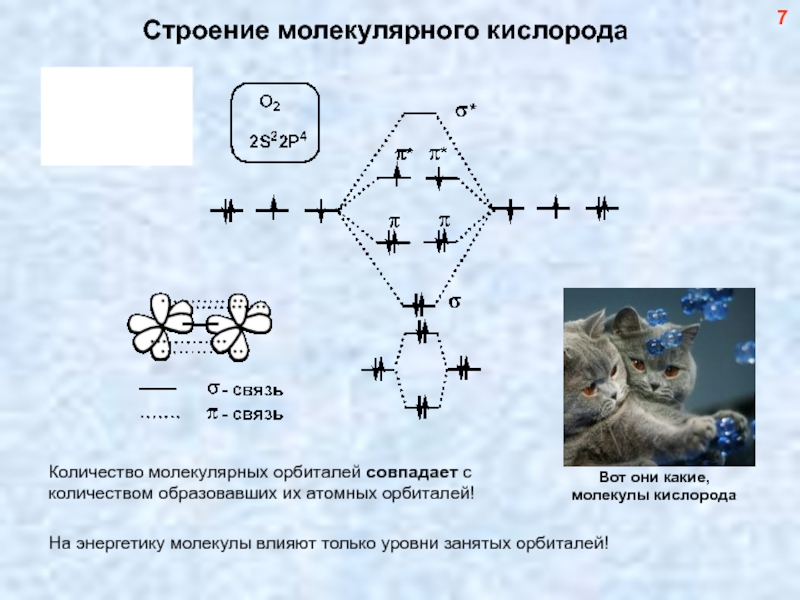
- 8. Строение молекулярного кислорода 7
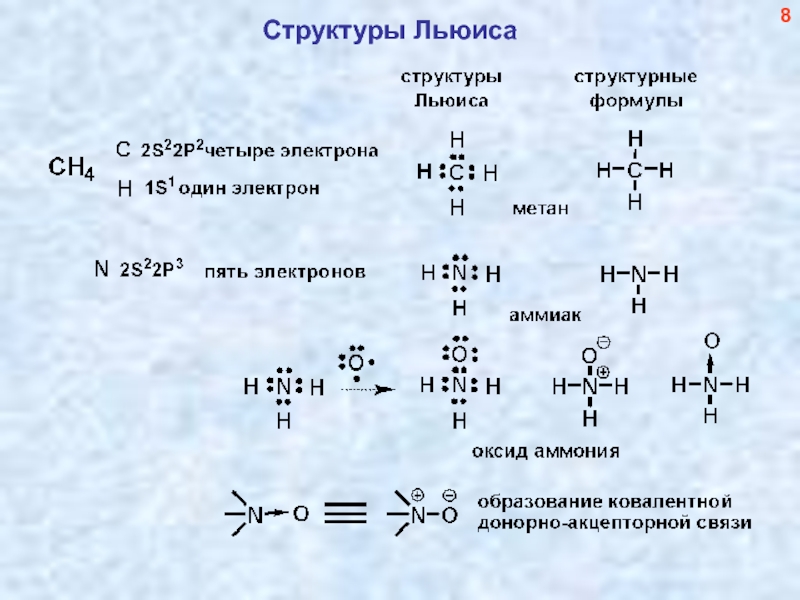
- 9. Структуры Льюиса 8
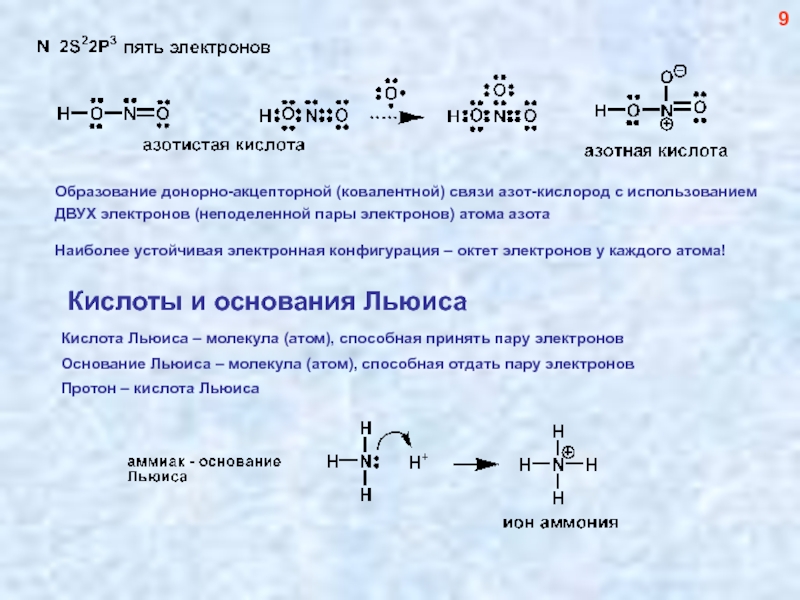
- 10. Образование донорно-акцепторной (ковалентной) связи азот-кислород с использованием
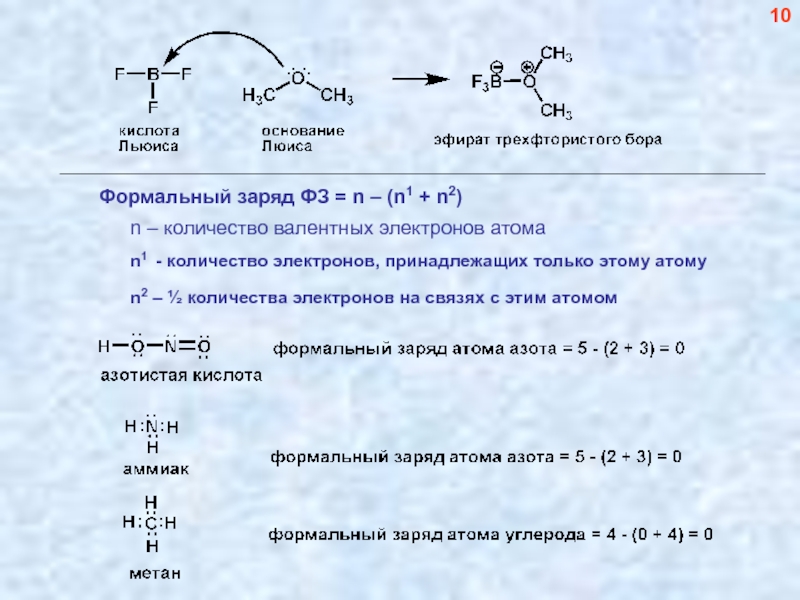
- 11. 10
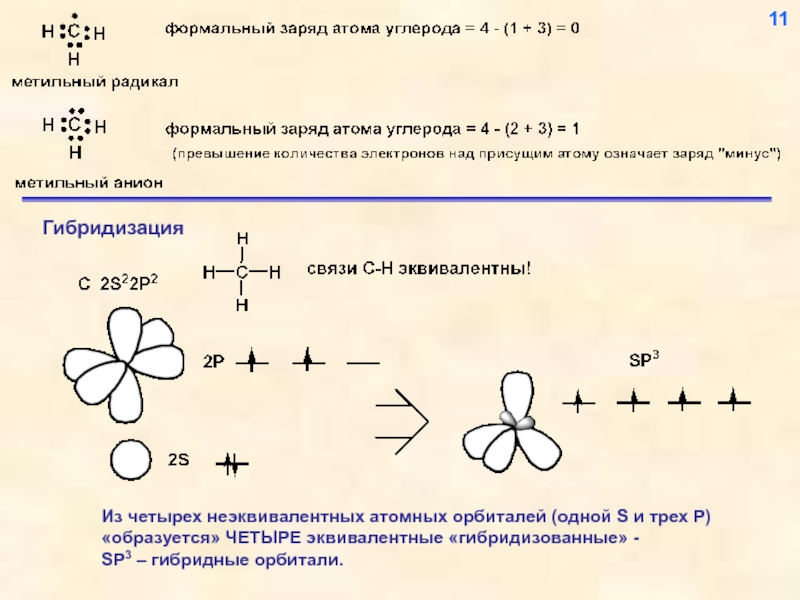
- 12. 11
- 13. 12
- 14. 13
- 15. 14
- 16. Гибридизованные орбитали располагаются в пространстве максимально далеко
- 17. Распределение заряда в молекуле 1. Индуктивный эффект 16
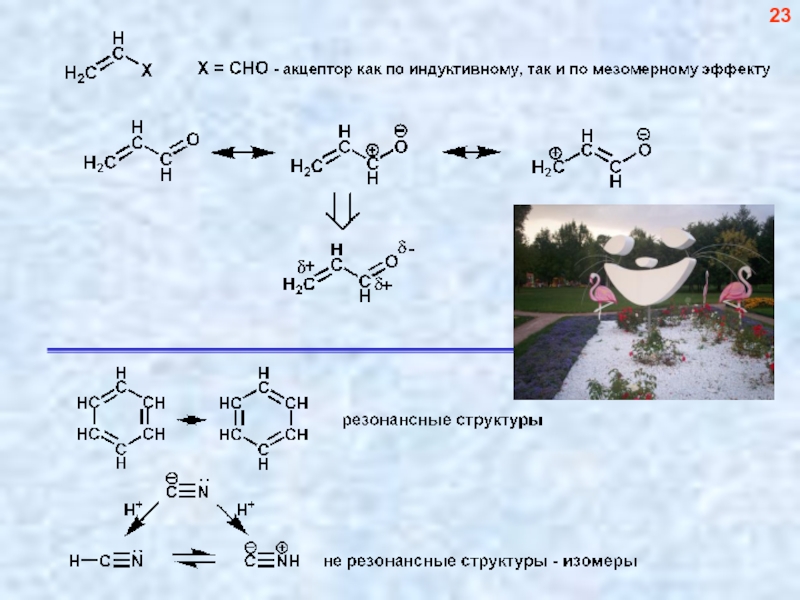
- 18. 2. Мезомерный эффект, теория резонанса 17
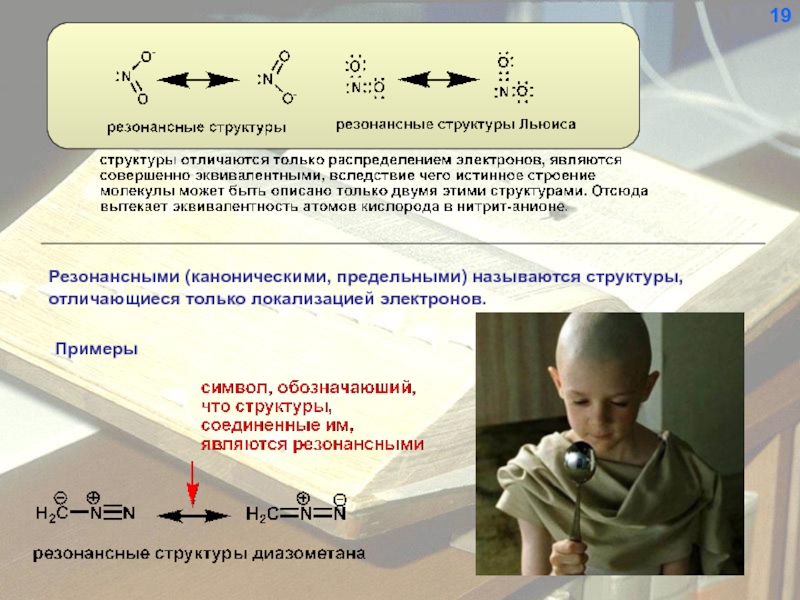
- 19. 18
- 20. Резонансными (каноническими, предельными) называются структуры, отличающиеся только локализацией электронов. 19
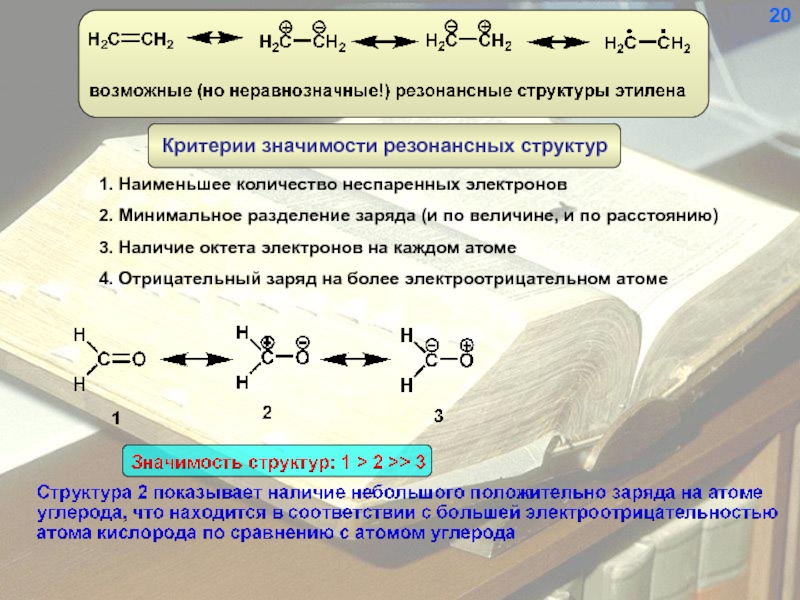
- 21. 1. Наименьшее количество неспаренных электронов 2. Минимальное
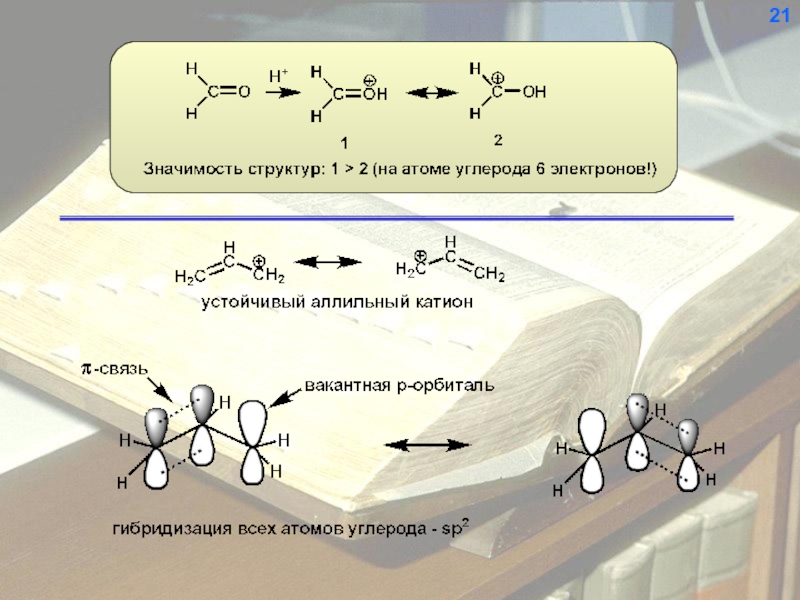
- 22. 21
- 23. 22
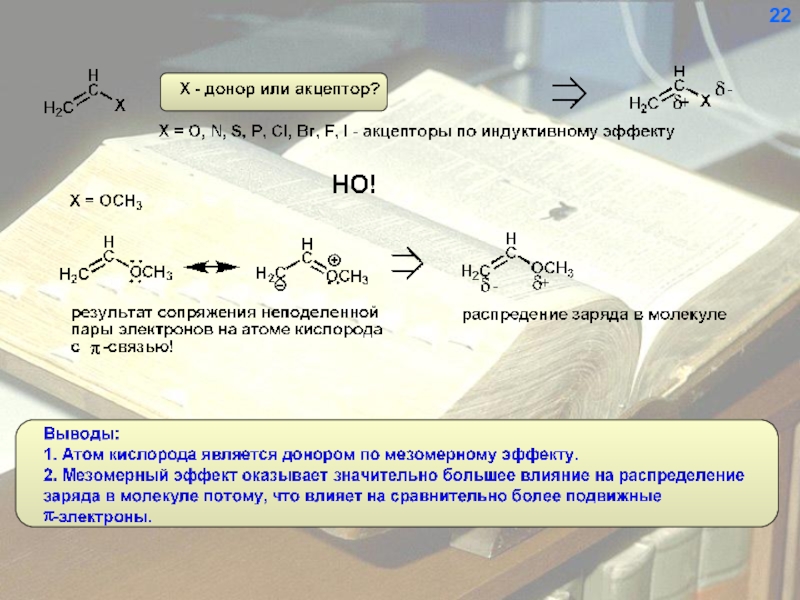
- 24. 23
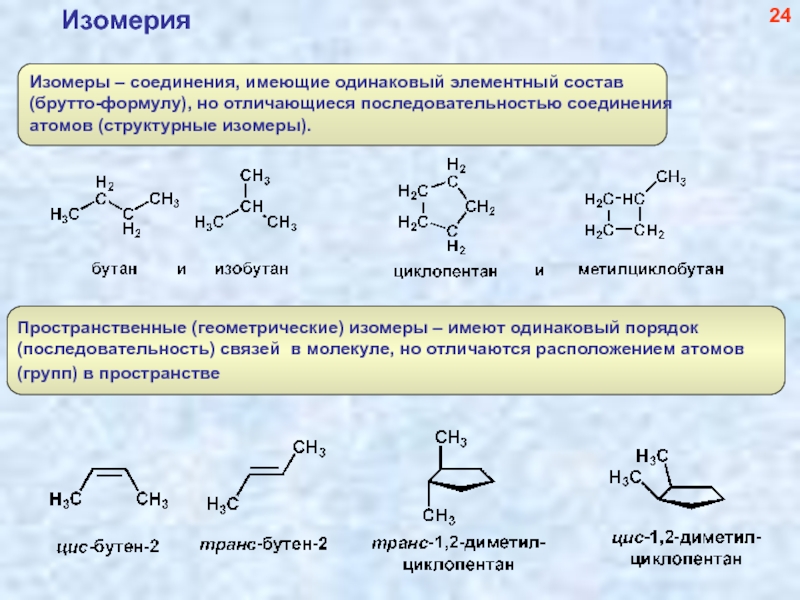
- 25. Изомерия 24
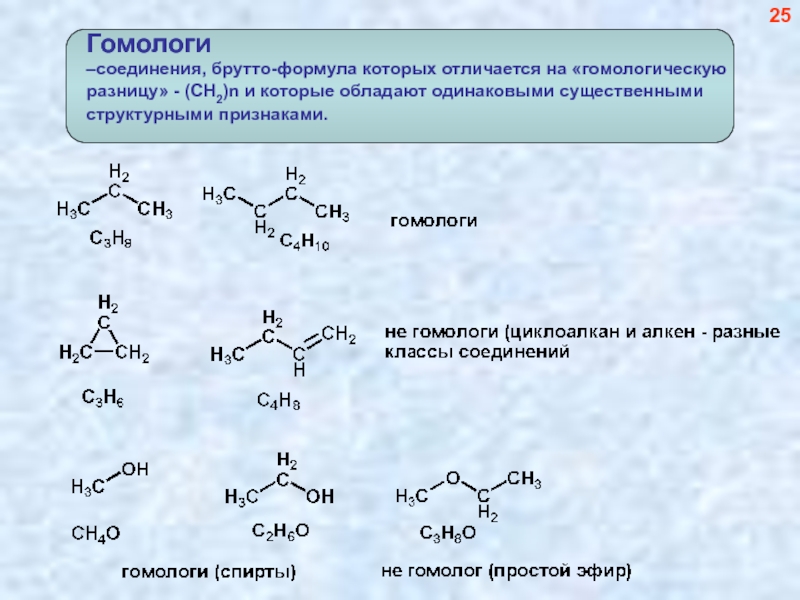
- 26. 25
- 27. Энантиомеры – зеркальные антиподы, несовпадающие друг с другом 26
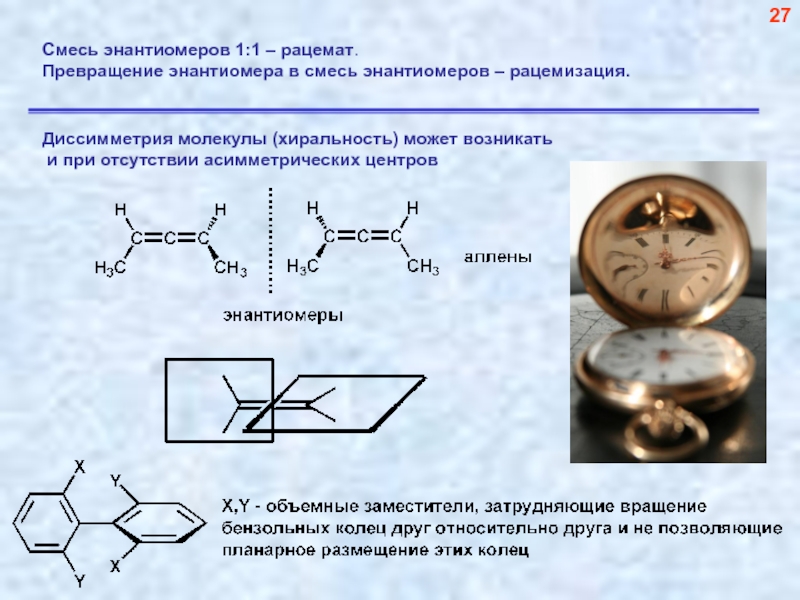
- 28. Смесь энантиомеров 1:1 – рацемат. Превращение энантиомера в смесь энантиомеров – рацемизация. 27
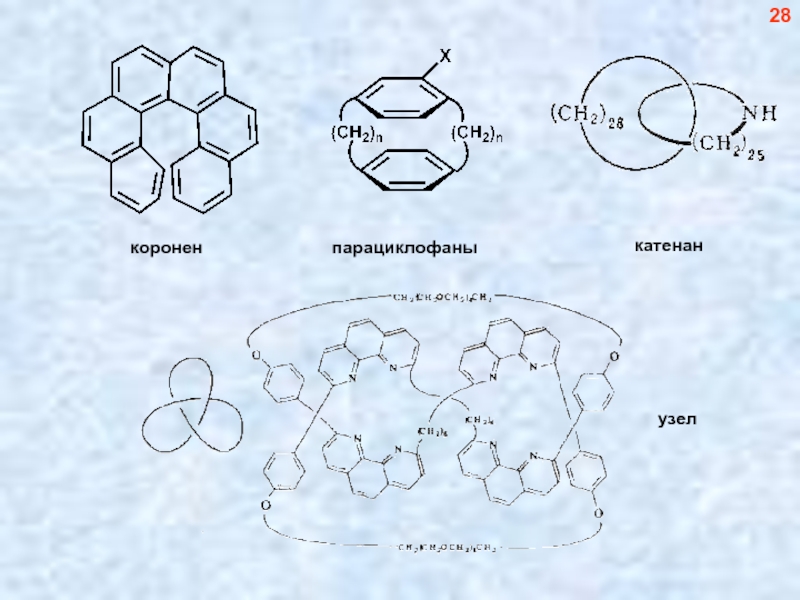
- 29. коронен парациклофаны катенан узел 28
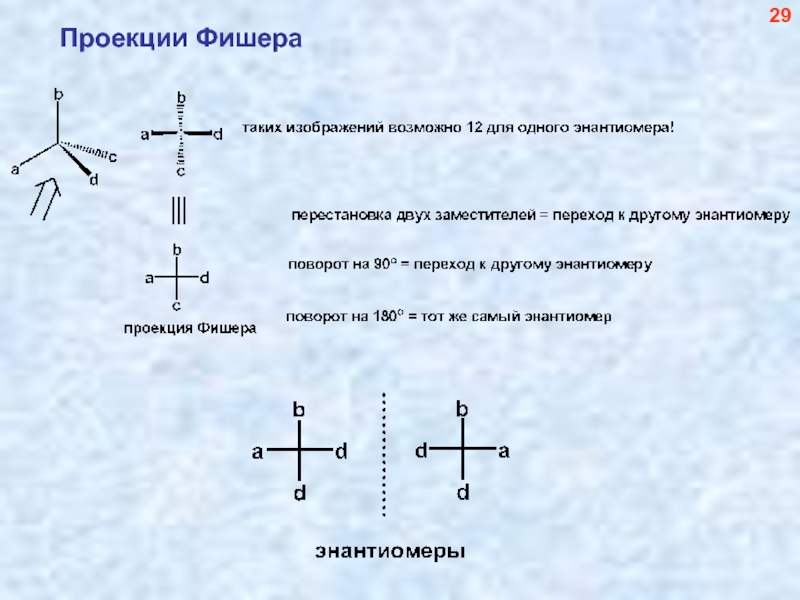
- 30. Проекции Фишера 29
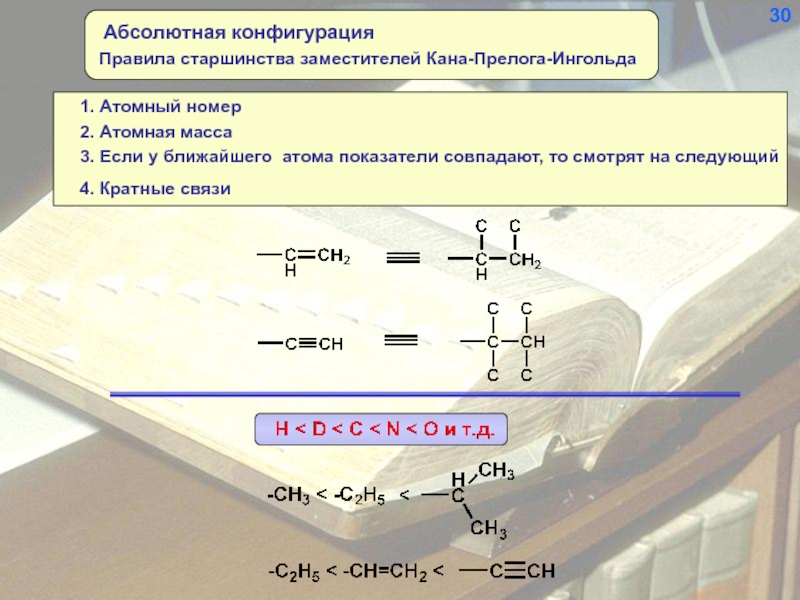
- 31. 2. Атомная масса 3. Если у ближайшего
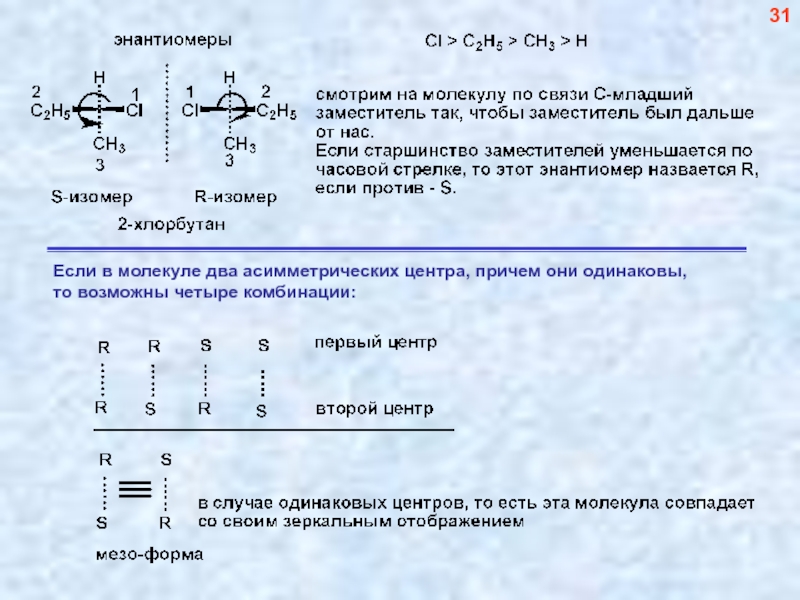
- 32. 31
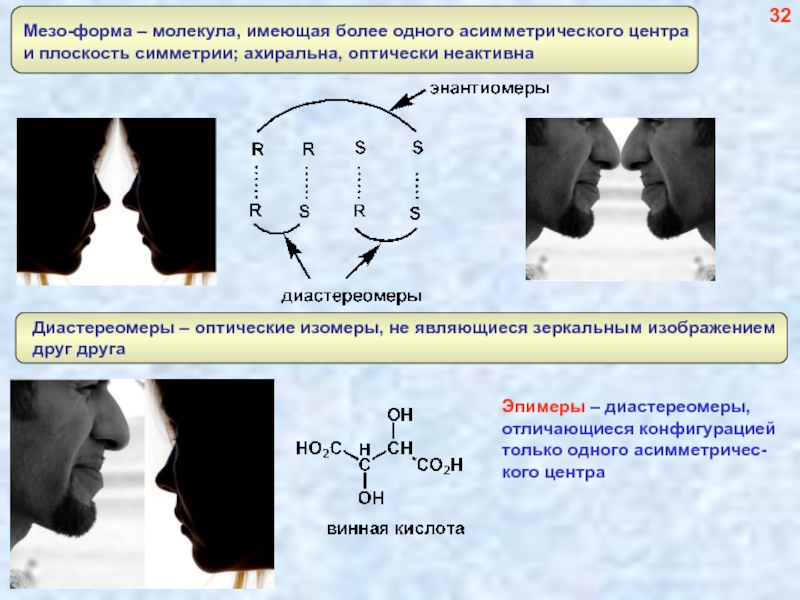
- 33. 32 Эпимеры – диастереомеры, отличающиеся конфигурацией только одного асимметричес- кого центра
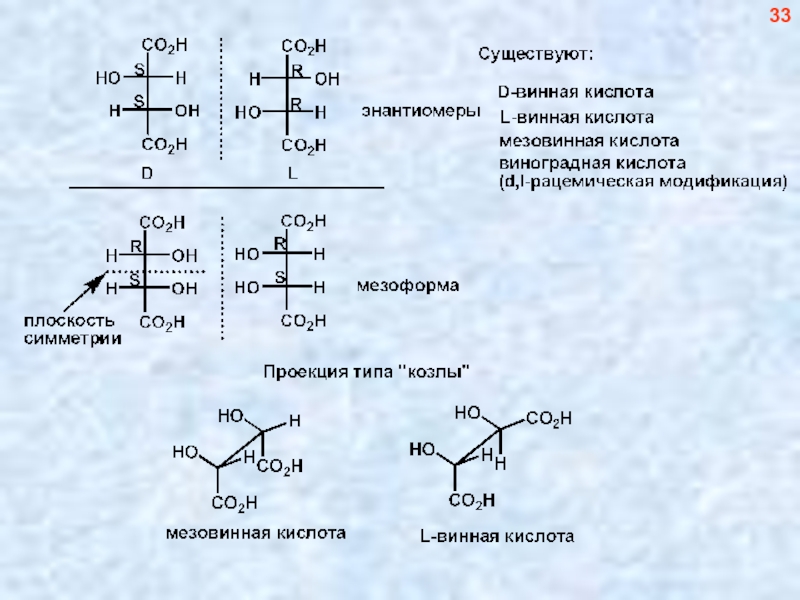
- 34. 33
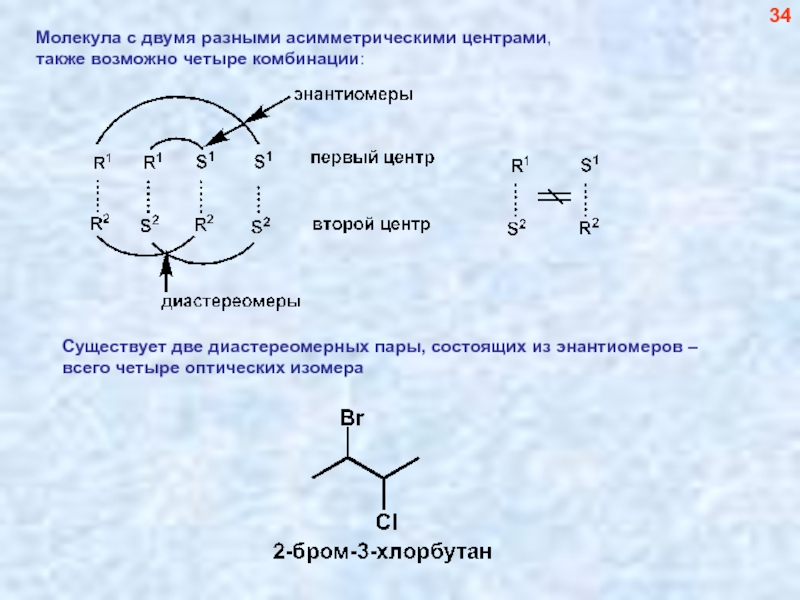
- 35. Существует две диастереомерных пары, состоящих из энантиомеров – всего четыре оптических изомера 34
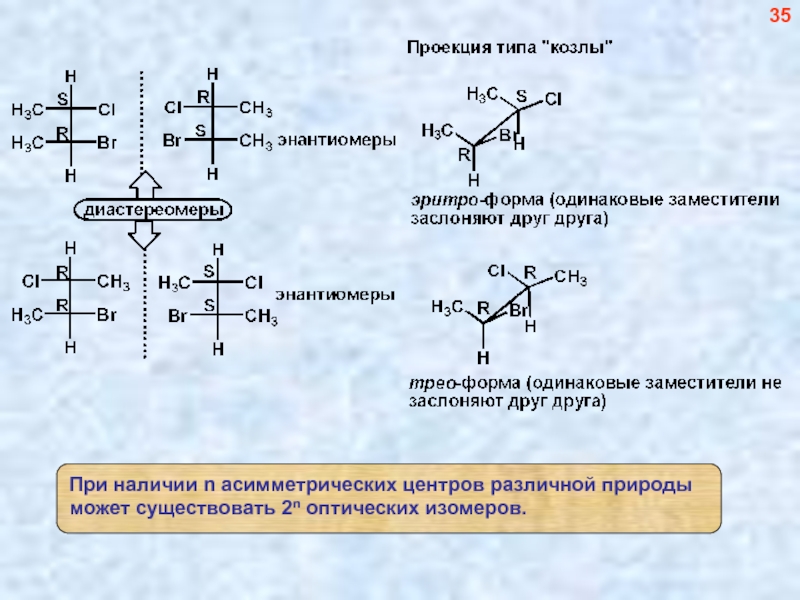
- 36. 35
- 37. Разница в химическом поведении энантиомеров проявляется только
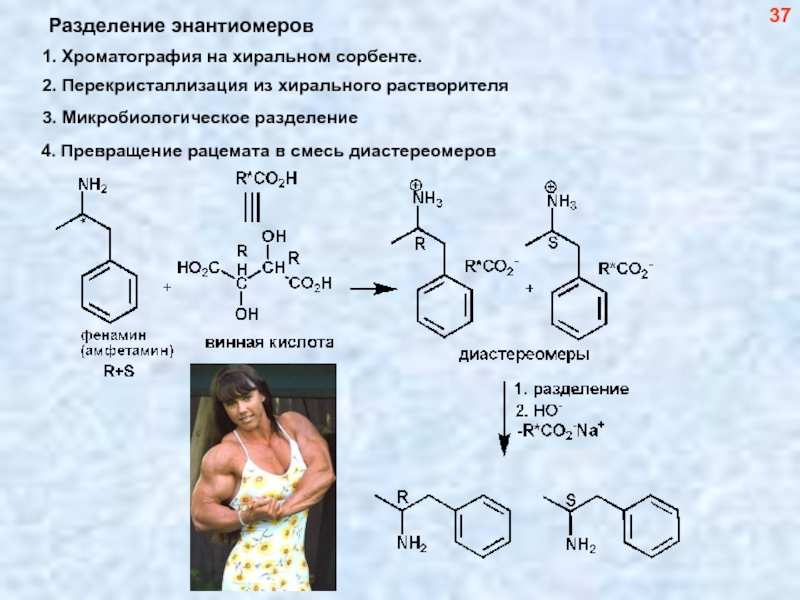
- 38. Разделение энантиомеров 37
- 39. Алканы Источники: Природный газ ~ 75% метан,
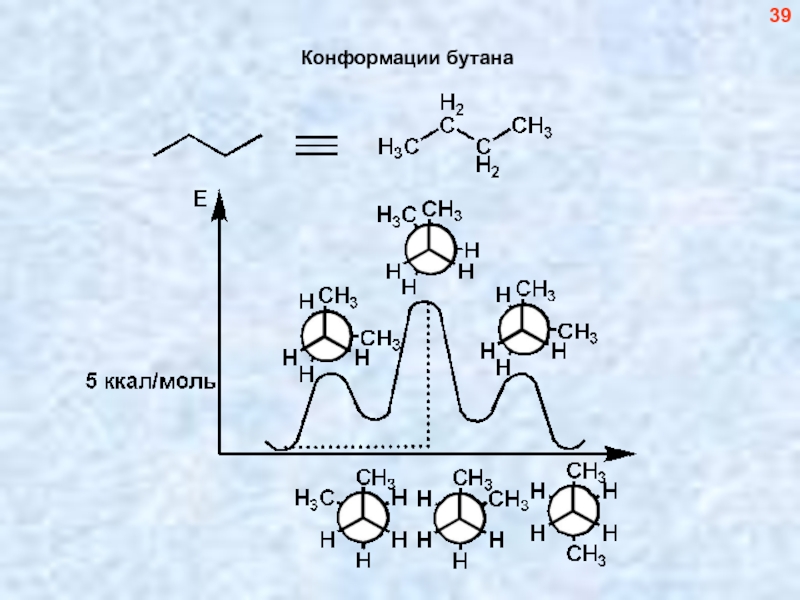
- 40. Конформации бутана 39
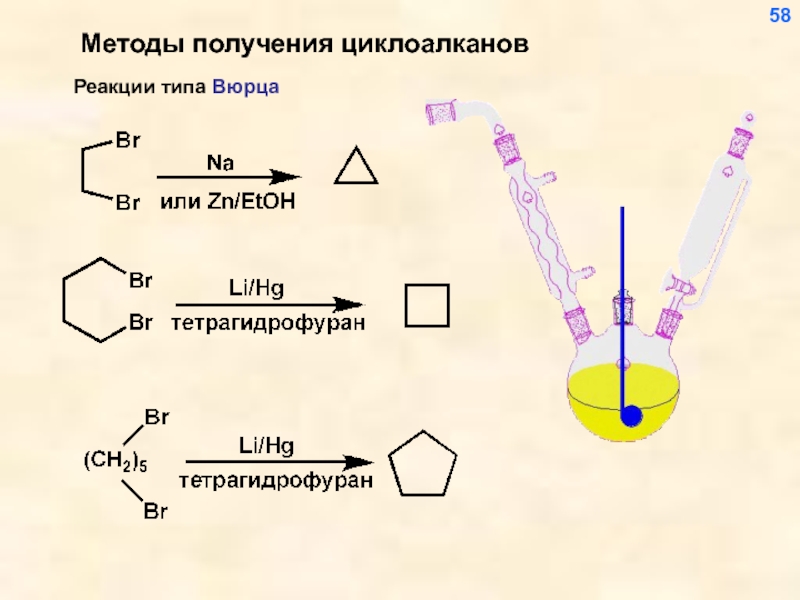
- 41. Методы синтеза алканов 1. Ректификация газа и нефти 40
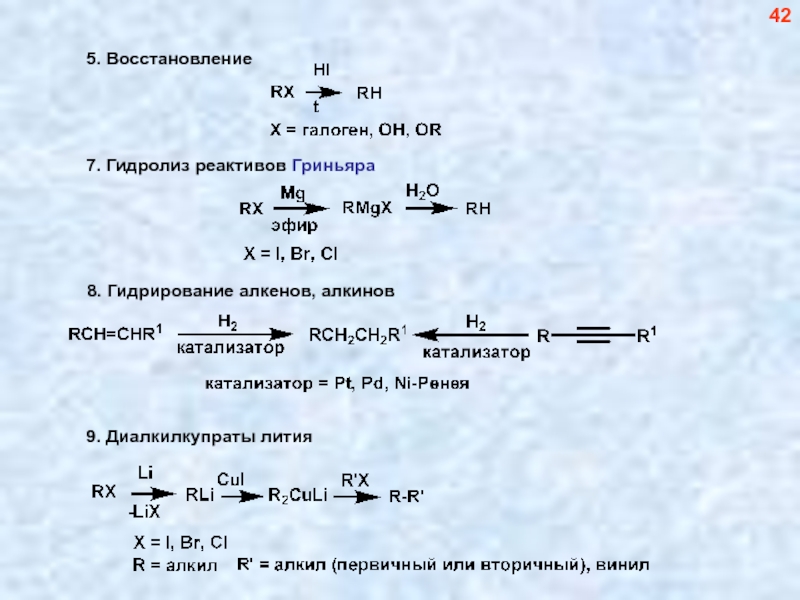
- 42. Лабораторные методы синтеза алканов 41
- 43. 42
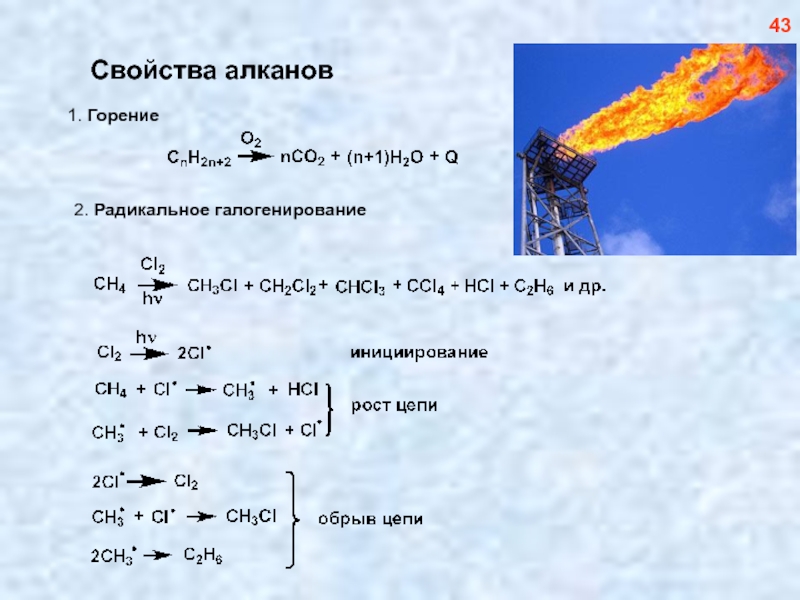
- 44. Свойства алканов 43
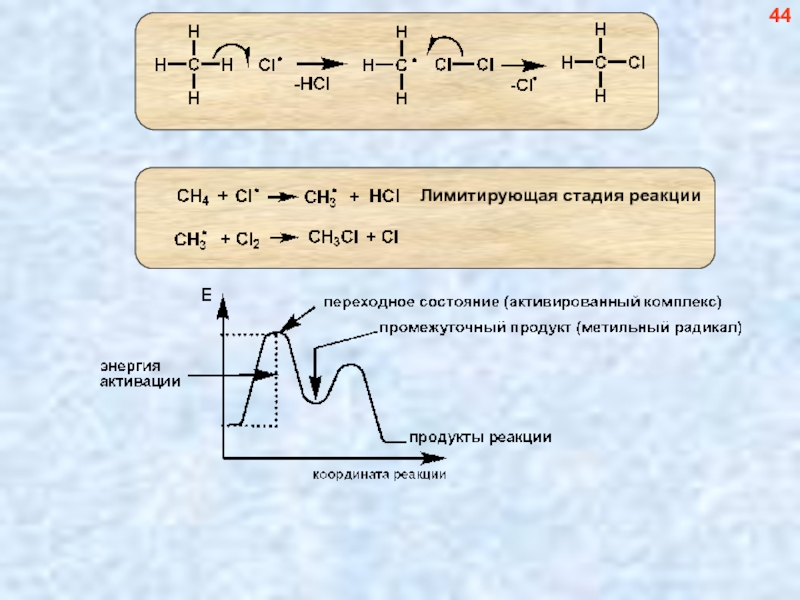
- 45. 44
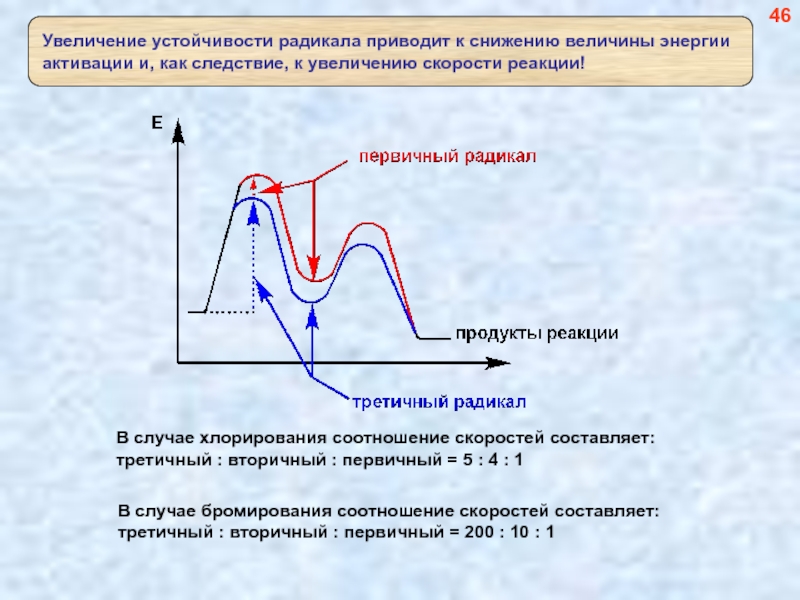
- 46. 45 Во всех случаях, когда в молекуле
- 47. В случае хлорирования соотношение скоростей составляет: третичный
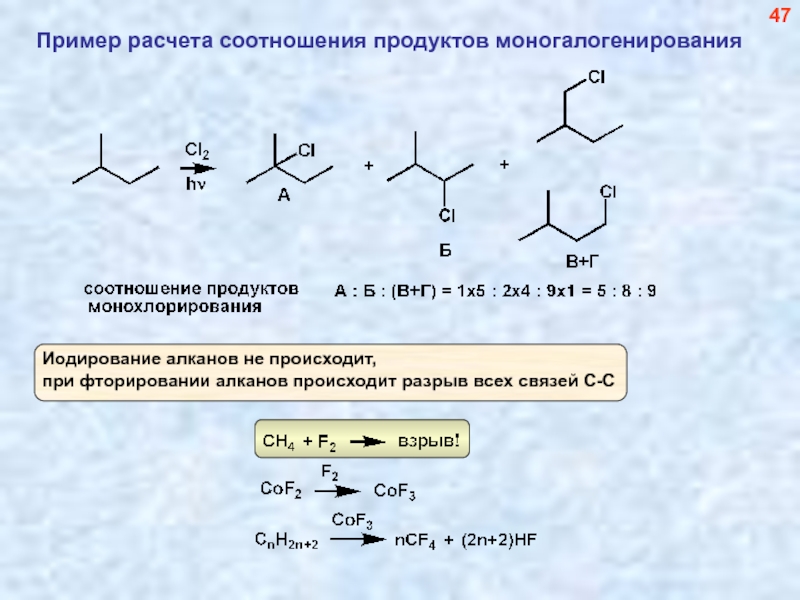
- 48. Пример расчета соотношения продуктов моногалогенирования 47
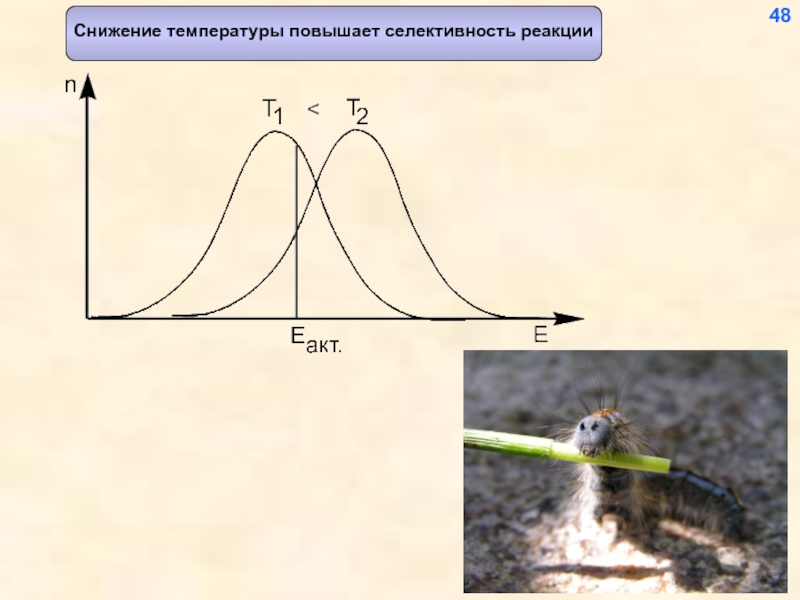
- 49. Снижение температуры повышает селективность реакции 48
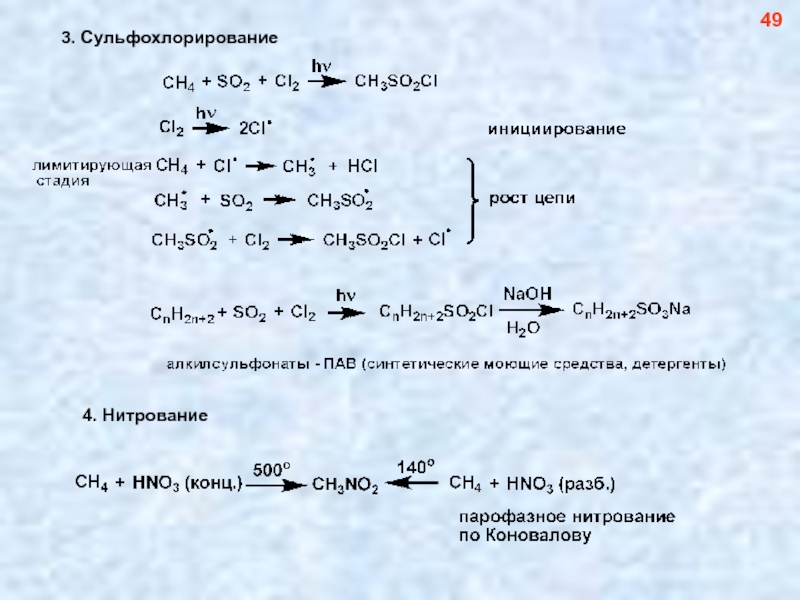
- 50. 3. Сульфохлорирование 49
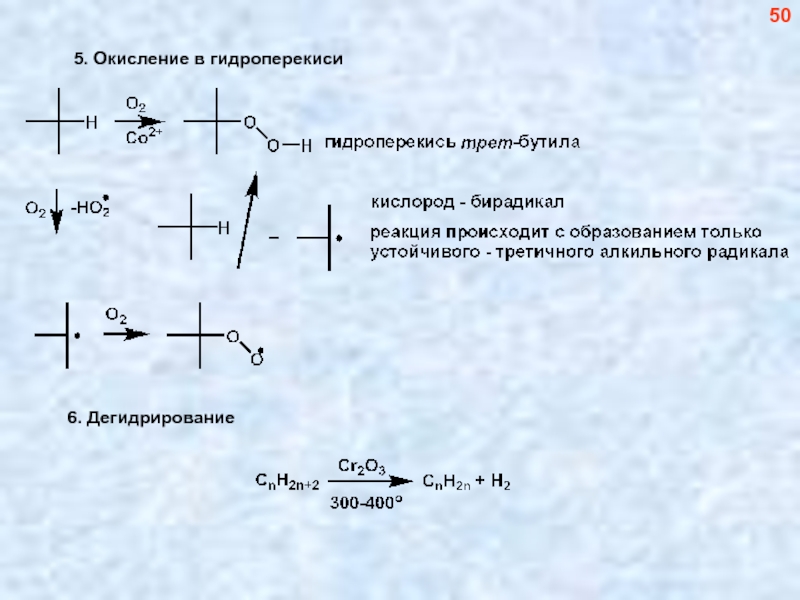
- 51. 5. Окисление в гидроперекиси 50
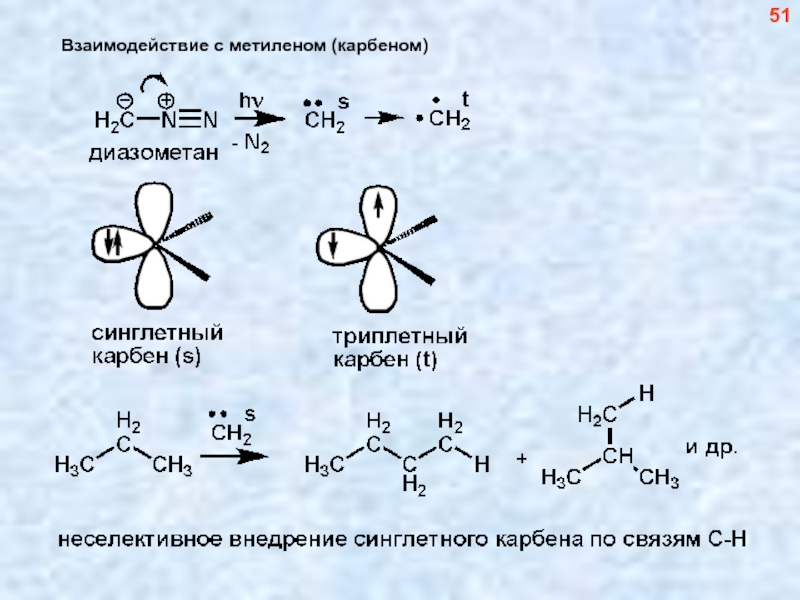
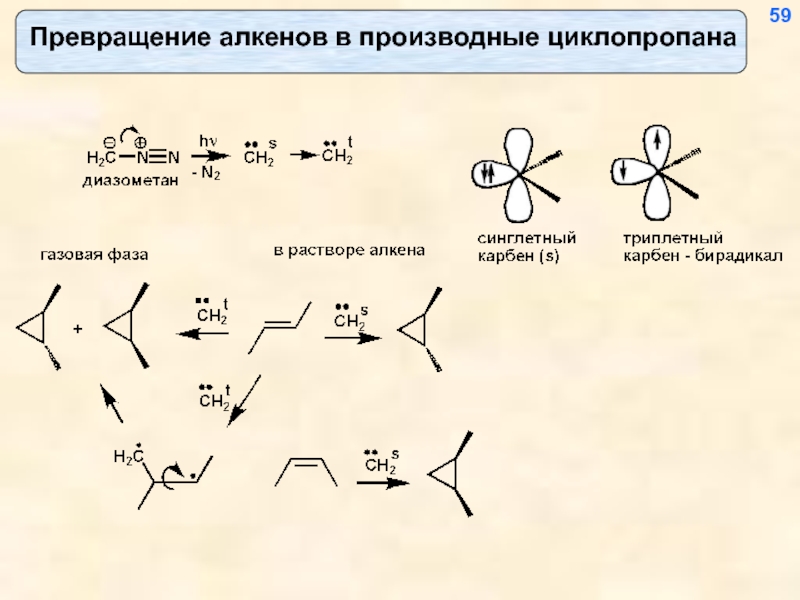
- 52. Взаимодействие с метиленом (карбеном) 51
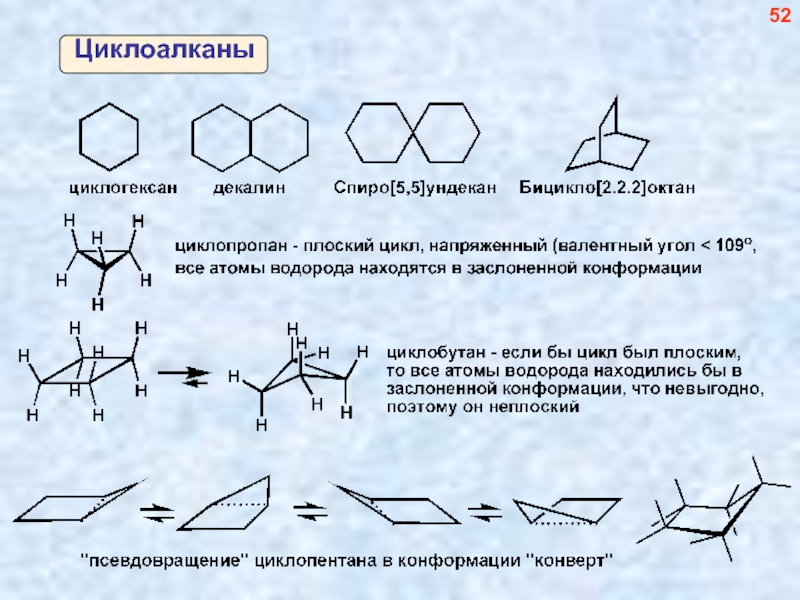
- 53. Циклоалканы 52
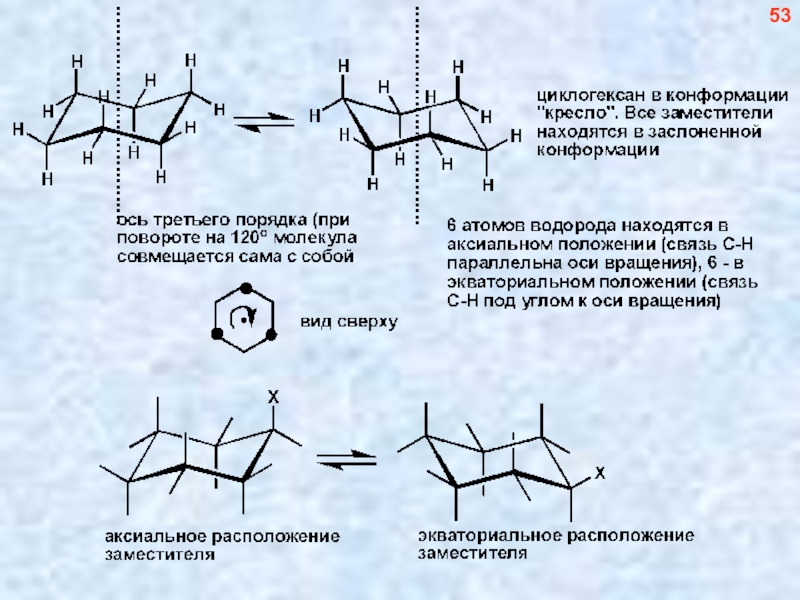
- 54. 53
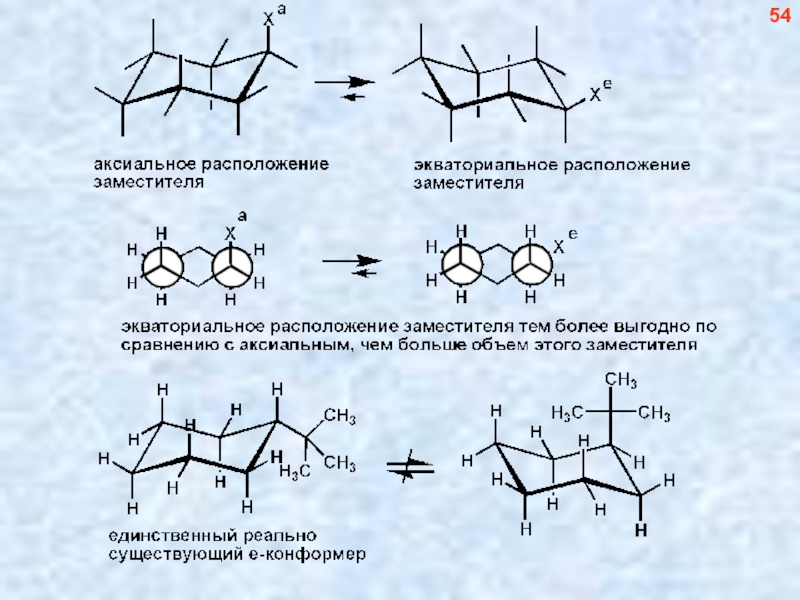
- 55. 54
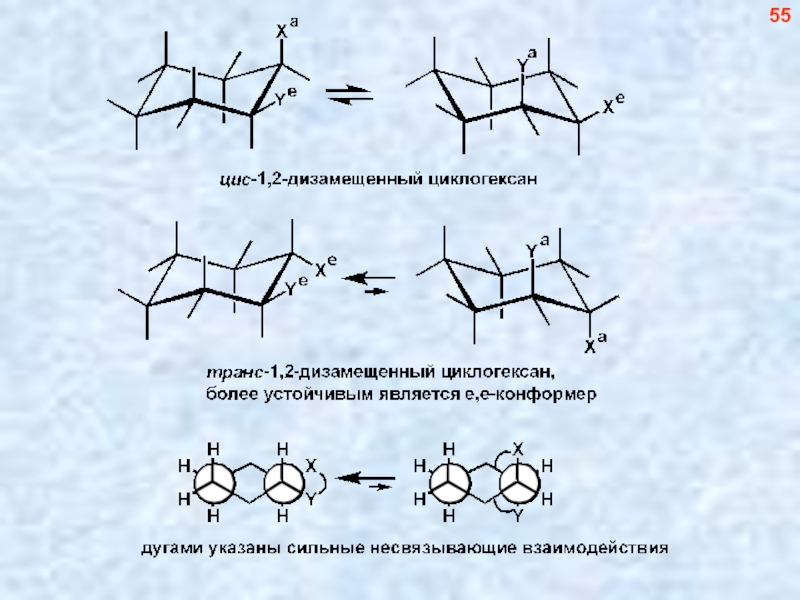
- 56. 55
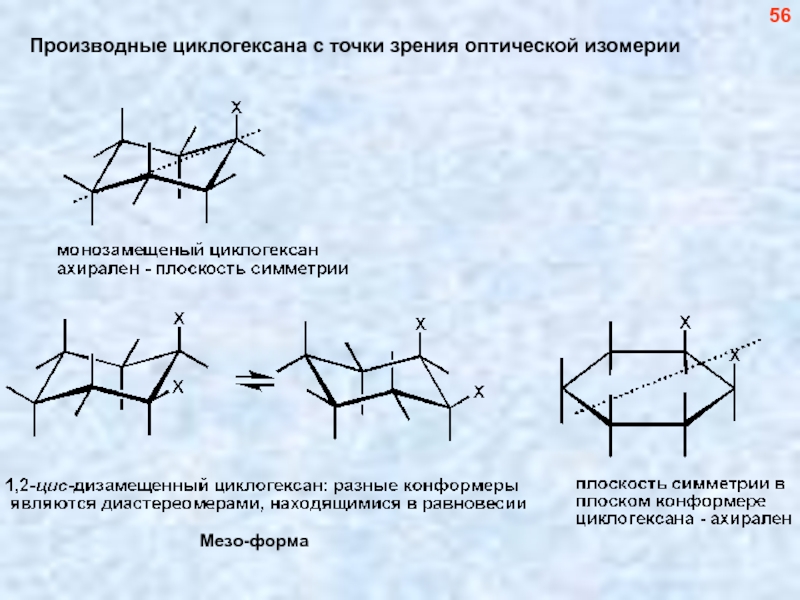
- 57. Производные циклогексана с точки зрения оптической изомерии Мезо-форма 56
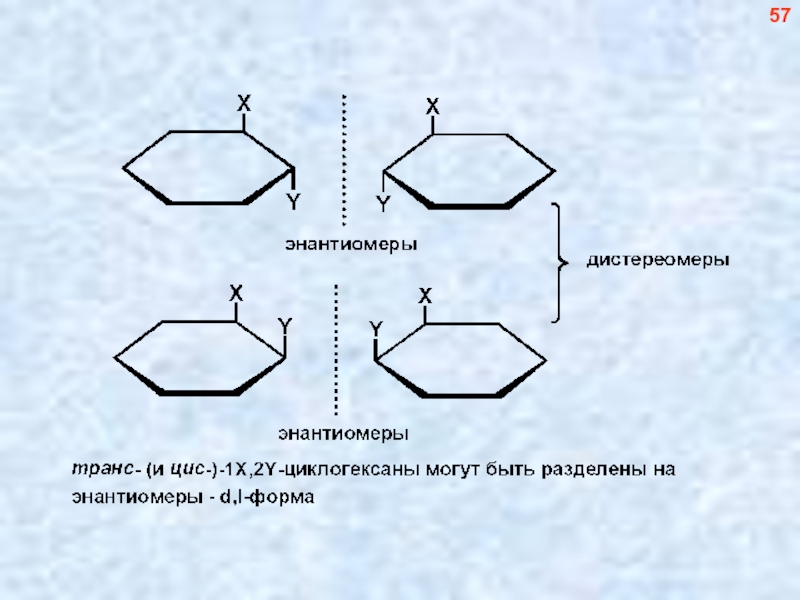
- 58. 57
- 59. Методы получения циклоалканов 58
- 60. 59
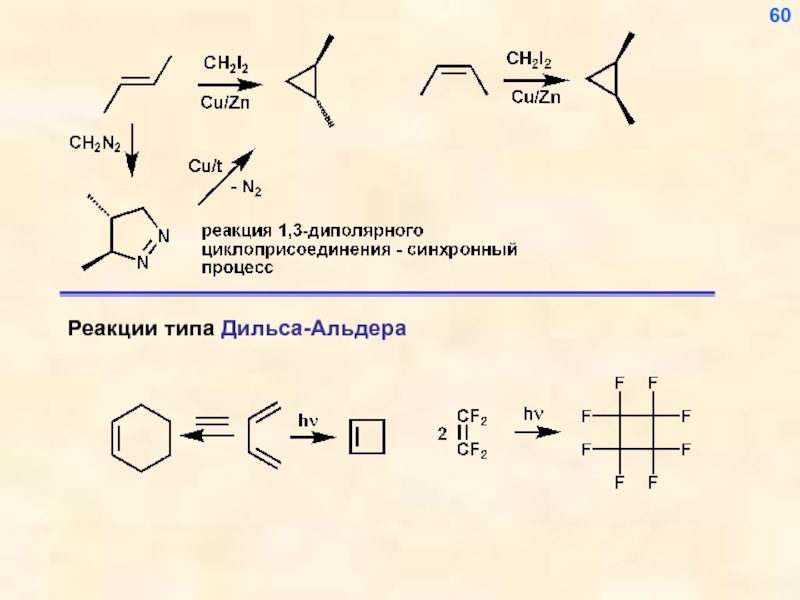
- 61. 60
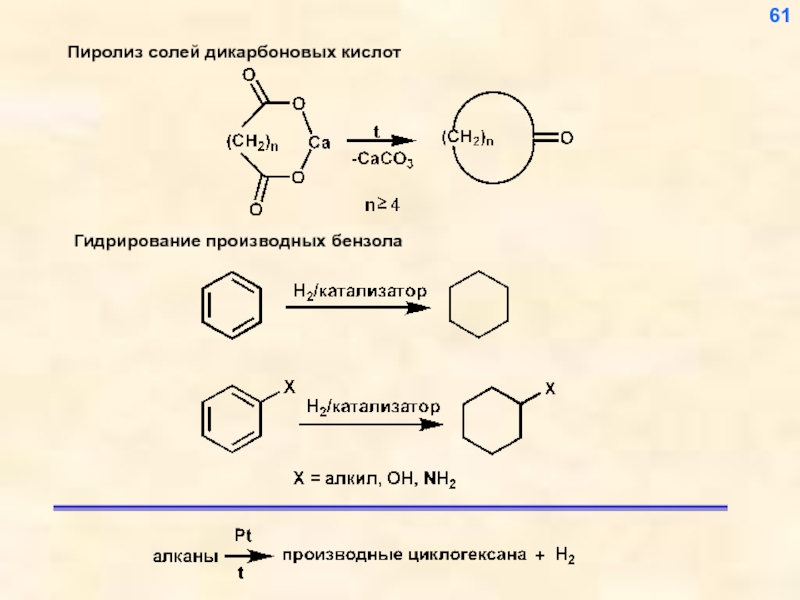
- 62. 61
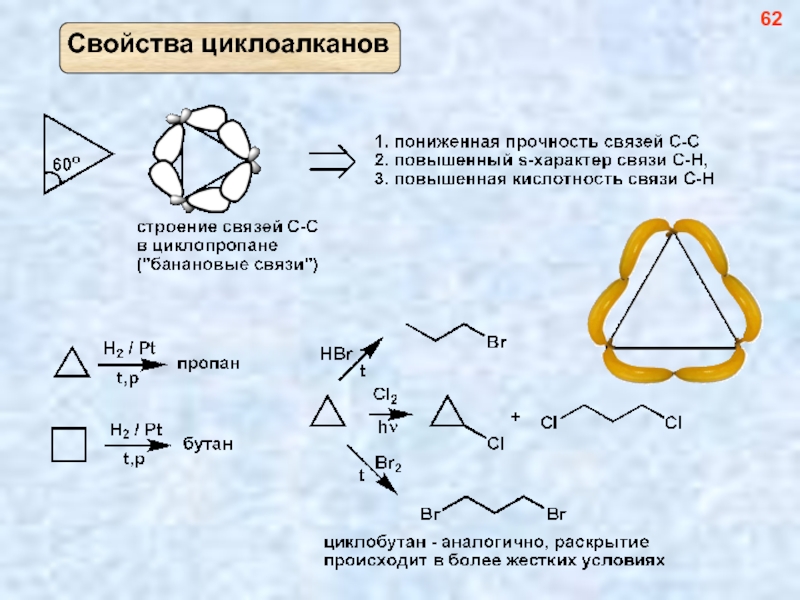
- 63. 62
- 64. Свойства циклоалканов с С > 4 такие
Слайд 1Мультимедийный курс для студентов
биологического отделения ФЕН и МедФ
Резников В.А.
ОРГАНИЧЕСКАЯ ХИМИЯ
Слайд 2Становление органической химии как отдельной науки
1
1. Длинные углерод-углеродные цепи
2. Изомерия
Слайд 33. Свойства органических соединений зависят не только от состава,
2
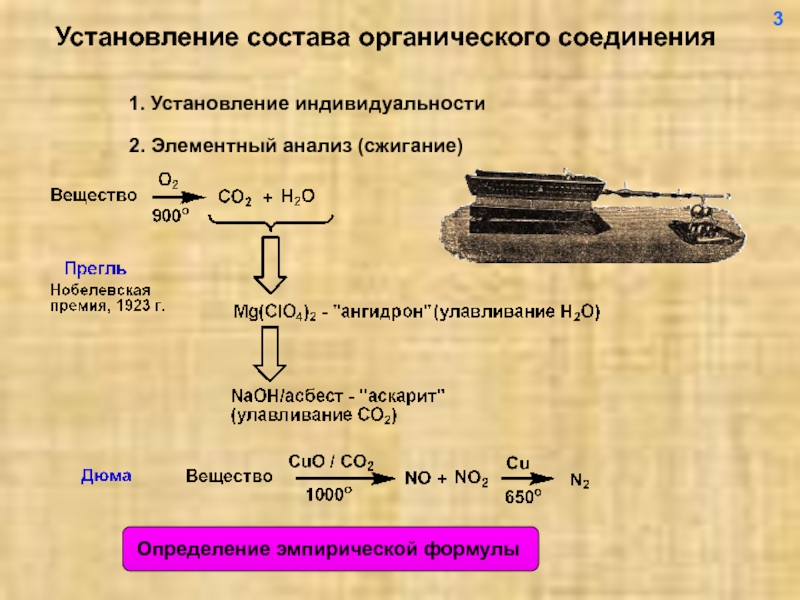
Слайд 4Установление состава органического соединения
1. Установление индивидуальности
2. Элементный анализ (сжигание)
3
Слайд 6От атомов к молекулам
Химическая связь
Необходимое (но недостаточное!) условие образования связи –
наличие двух электронов (по одному от каждого атома или два от
любого из атомов, образующих связь)
5
Слайд 10Образование донорно-акцепторной (ковалентной) связи азот-кислород с использованием
ДВУХ электронов (неподеленной пары
Наиболее устойчивая электронная конфигурация – октет электронов у каждого атома!
9
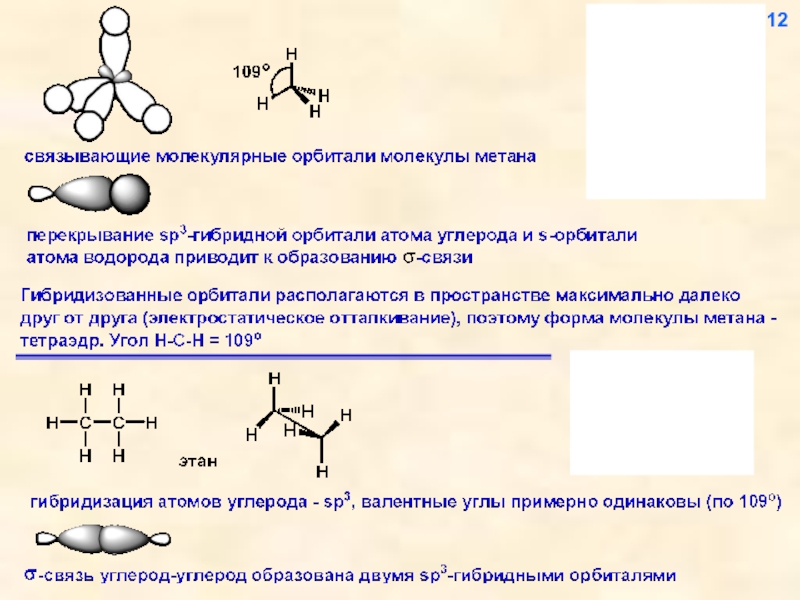
Слайд 16Гибридизованные орбитали располагаются в пространстве максимально далеко друг от друга -
15
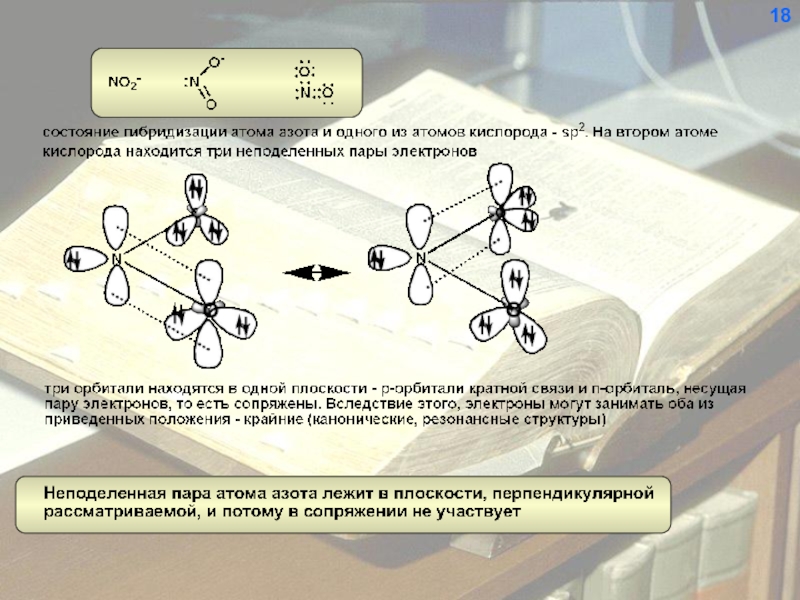
Слайд 20Резонансными (каноническими, предельными) называются структуры,
отличающиеся только локализацией электронов.
19
Слайд 211. Наименьшее количество неспаренных электронов
2. Минимальное разделение заряда (и по величине,
3. Наличие октета электронов на каждом атоме
4. Отрицательный заряд на более электроотрицательном атоме
20
Слайд 28Смесь энантиомеров 1:1 – рацемат.
Превращение энантиомера в смесь энантиомеров –
27
Слайд 312. Атомная масса
3. Если у ближайшего атома показатели совпадают, то смотрят
4. Кратные связи
30
Слайд 3332
Эпимеры – диастереомеры,
отличающиеся конфигурацией
только одного асимметричес-
кого центра
Слайд 35Существует две диастереомерных пары, состоящих из энантиомеров –
всего четыре оптических
34
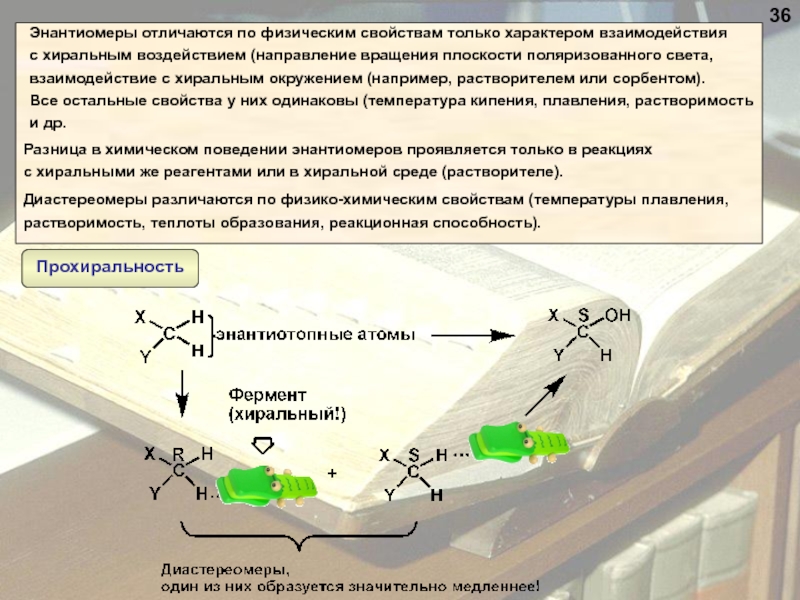
Слайд 37Разница в химическом поведении энантиомеров проявляется только в реакциях
с хиральными
Диастереомеры различаются по физико-химическим свойствам (температуры плавления,
растворимость, теплоты образования, реакционная способность).
36
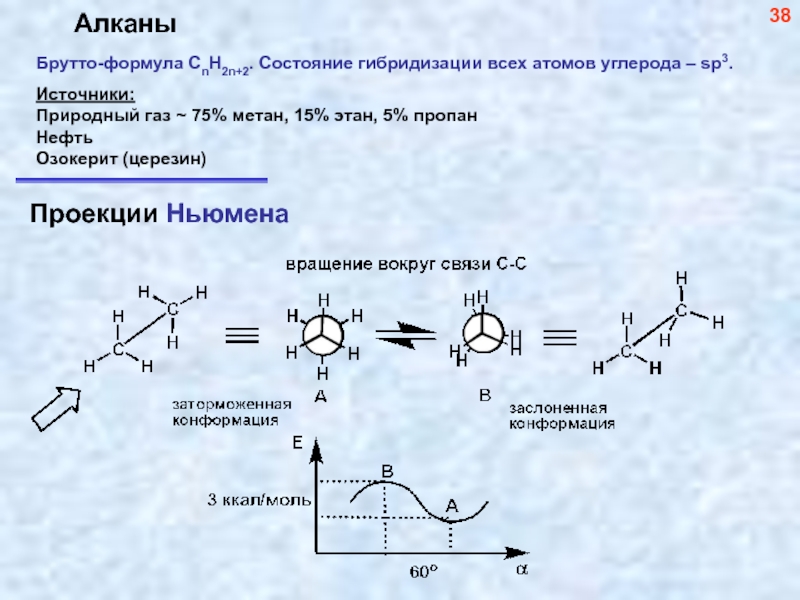
Слайд 39Алканы
Источники:
Природный газ ~ 75% метан, 15% этан, 5% пропан
Нефть
Озокерит (церезин)
Брутто-формула СnH2n+2.
38
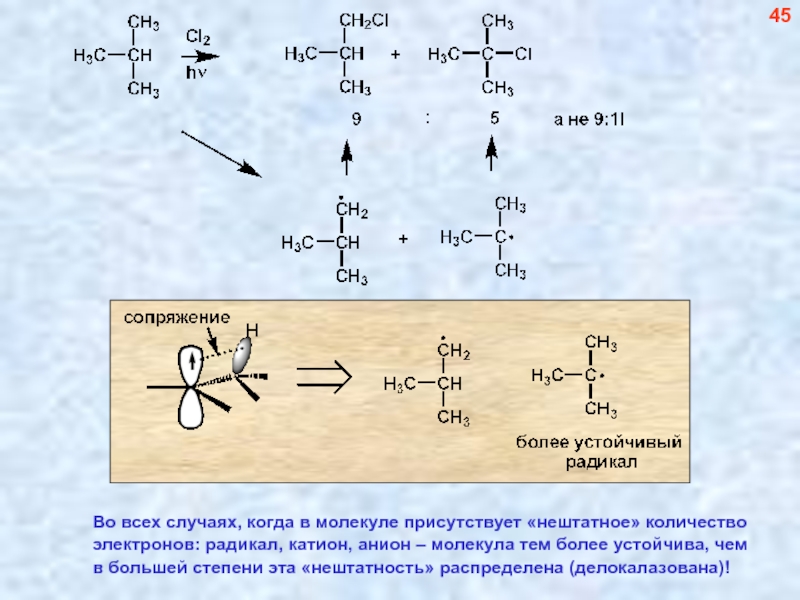
Слайд 4645
Во всех случаях, когда в молекуле присутствует «нештатное» количество
электронов: радикал,
в большей степени эта «нештатность» распределена (делокалазована)!
Слайд 47В случае хлорирования соотношение скоростей составляет:
третичный : вторичный : первичный =
В случае бромирования соотношение скоростей составляет:
третичный : вторичный : первичный = 200 : 10 : 1
46
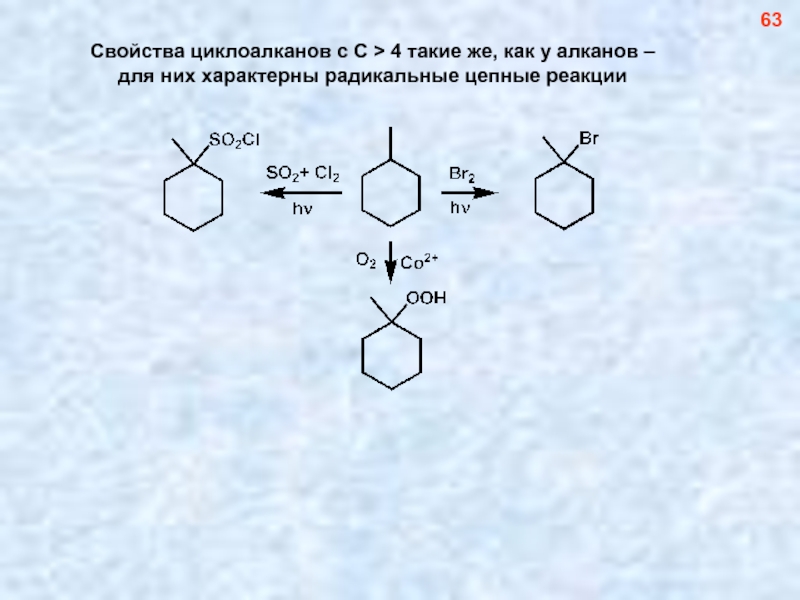
Слайд 64Свойства циклоалканов с С > 4 такие же, как у алканов
для них характерны радикальные цепные реакции
63