- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Соли и их свойства презентация
Содержание
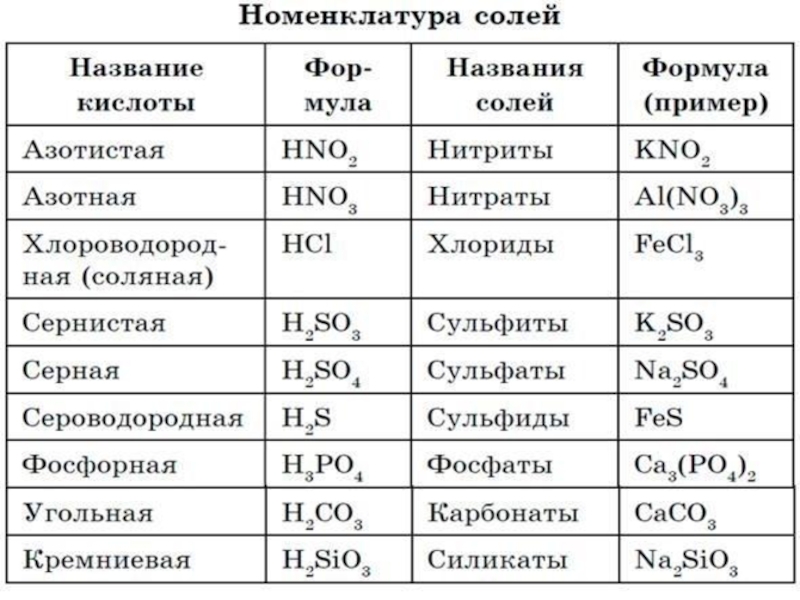
- 1. Соли и их свойства
- 2. Соли - это сложные вещества, состоящие из ионов металлов и кислотного остатка.
- 4. Кислотный остаток образуется, если в формуле кислоты
- 5. Алгоритм (1) называния соли по формуле.
- 6. Пример: Fe2(SO4)3
- 7. Упражнение. Назвать:
- 8. Алгоритм (2) построения формул солей по названию.
- 9. Пример: нитрат меди (II):
- 10. Упражнение. Составьте формулы:
- 11. Классификация солей Соли Растворимые
- 12. Химические свойства. 1. Взаимодействие с кислотами →
- 13. 2. Взаимодействие с щелочами → выпадает осадок.
- 14. 3. Взаимодействие с солями - выпадает осадок.
Слайд 4 Кислотный остаток образуется, если в формуле кислоты убрать атомы водорода.
Заряд
Слайд 5Алгоритм (1) называния соли по формуле.
1. Определить степени окисления металла и
2. Определить по кислотному остатку, какой кислоте соответствует соль, каково название соли.
3. К названию соли добавить русское название металла в родительном падеже, указать в скобках римской цифрой степень окисления металла (если она не постоянна).
Слайд 6Пример: Fe2(SO4)3
+3 -2
1. Fe2(SO4)3
2.
3. Сульфат железа (III).
Слайд 8Алгоритм (2) построения формул солей по названию.
1. Слева записать металл, указанный
2. По названию соли определить, какой кислоте она соответствует, кислотный остаток записать справа от металла, над ним написать степень окисления (из таблицы растворимости).
3. Снести степень окисления крест-накрест.
4. Если надо, индексы сократить.
! Если после кислотного остатка должен быть индекс, кислотный остаток берется в скобки.
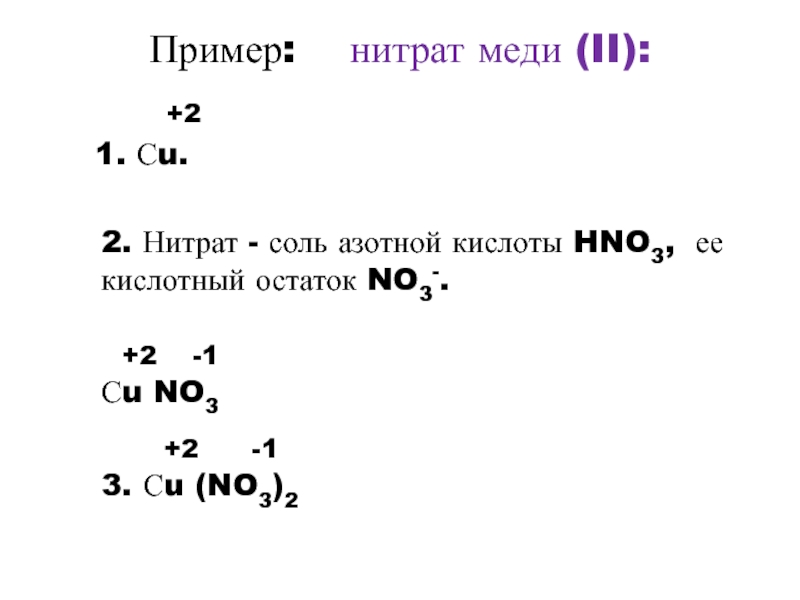
Слайд 9Пример: нитрат меди (II):
+2
1. Сu.
2. Нитрат
+2 -1
Сu NO3
+2 -1
3. Сu (NO3)2
Слайд 10Упражнение.
Составьте формулы:
сульфит магния
бромид
сульфат алюминия.
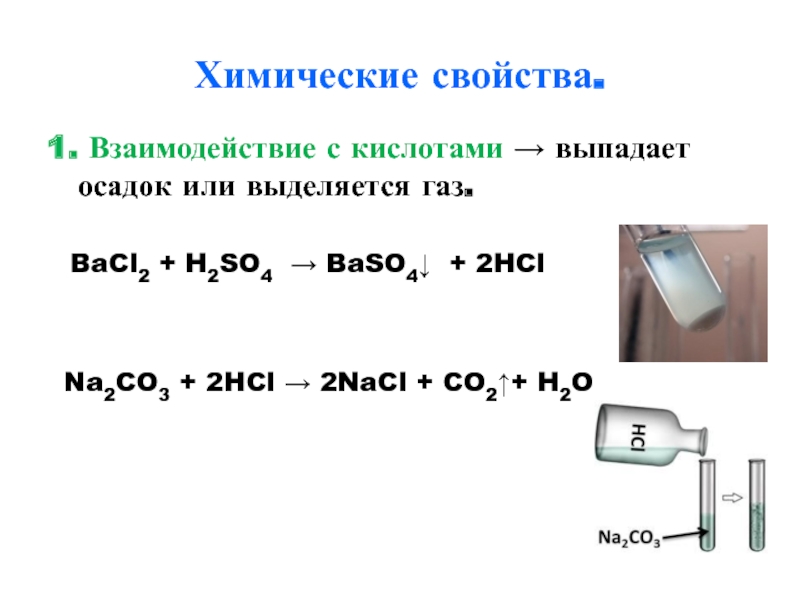
Слайд 12Химические свойства.
1. Взаимодействие с кислотами → выпадает осадок или выделяется газ.
BaCl2
Na2CO3 + 2HCl → 2NaCl + CO2↑+ H2O
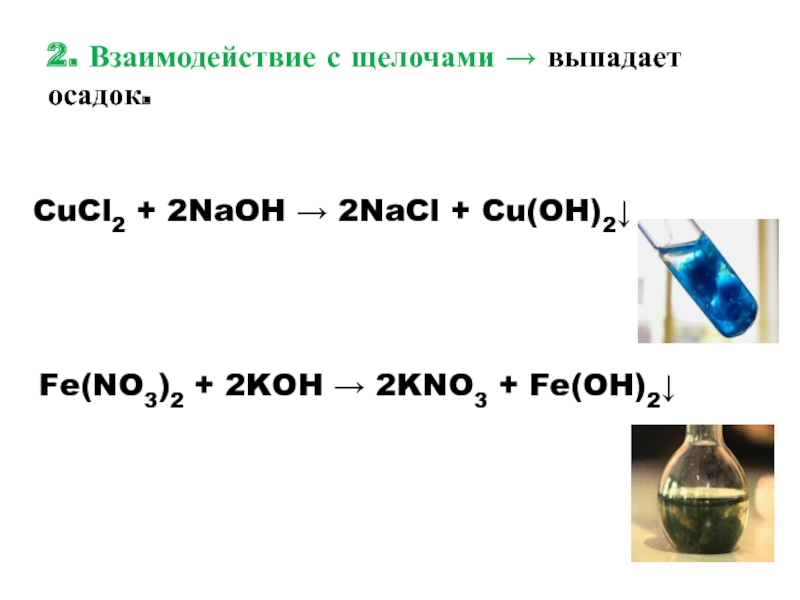
Слайд 132. Взаимодействие с щелочами → выпадает осадок.
CuCl2 + 2NaOH → 2NaCl
Fe(NO3)2 + 2KOH → 2KNO3 + Fe(OH)2↓