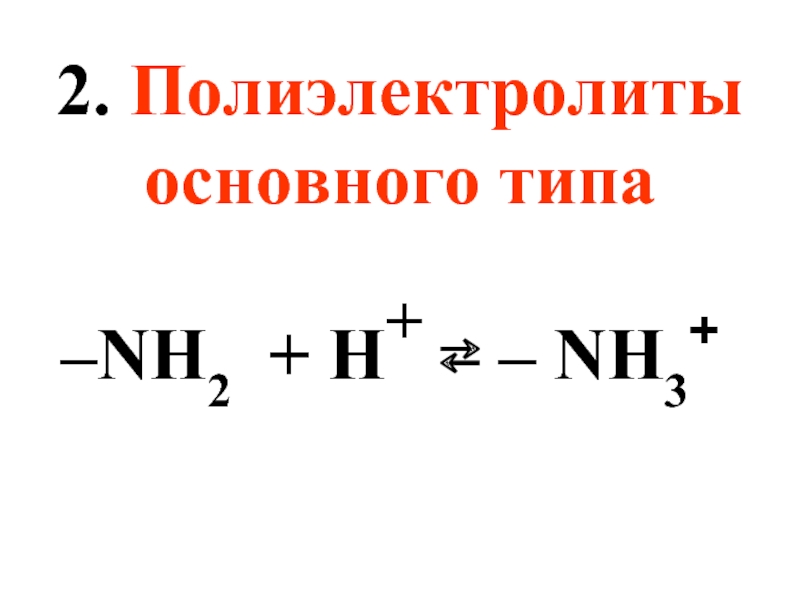- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
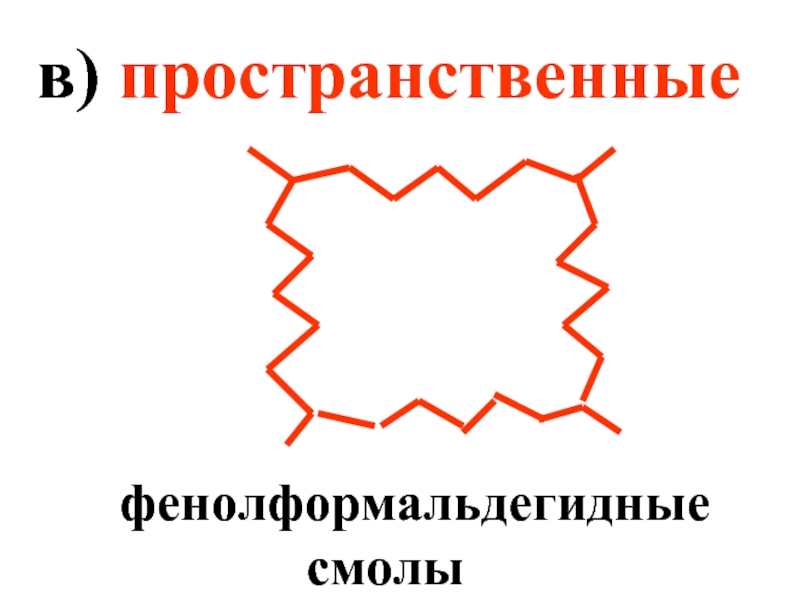
- Недвижимость
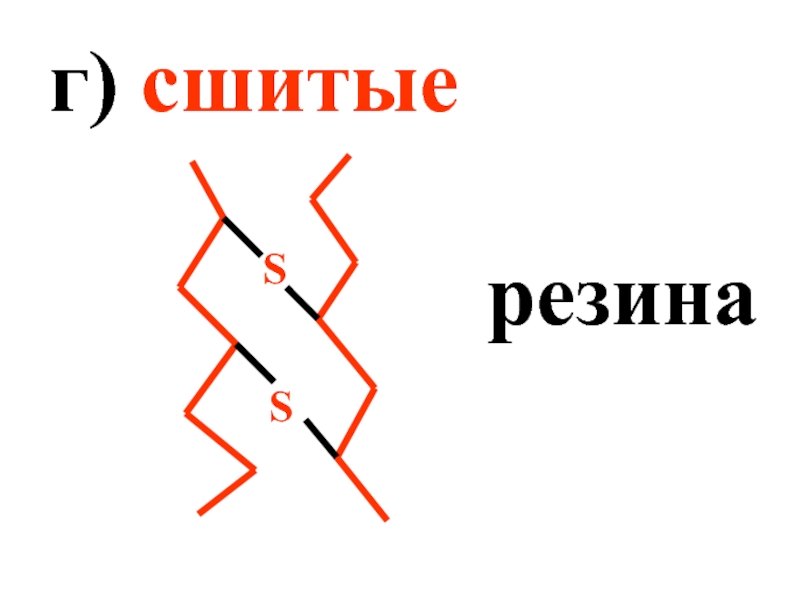
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Растворы ВМС презентация
Содержание
- 1. Растворы ВМС
- 2. ПЛАН 18.1 Общая характеристика ВМС 18.2
- 3. 18.1 Высокомолекулярными соединениями (ВМС) называют вещества, имеющие
- 4. К природным ВМС (биополимерам) относятся крахмал, целлюлоза, декстраны, нуклеиновые кислоты, белки, натуральные каучуки.
- 5. Cинтетические полимеры являются продуктами реакций полимеризации и поликонденсации.
- 6. Реакции полимеризации Полиэтилен n
- 7. 2) Тефлон nCF2=CF2 →
- 8. Реакции поликонденсации Найлон-продукт поликонденсации адипиновой кислоты
- 9. n HOOC-(CH2)4-COOH + n H2N–(CH2)6–NH2
- 10. Классификация ВМС 1.По конфигурации цепи а) линейные желатин, натуральный каучук
- 11. б) разветвленные крахмал, гликоген
- 12. в) пространственные фенолформальдегидные смолы
- 13. г) сшитые резина S S
- 14. 2. По элементному составу: Гомоцепные ВМС
- 15. Гетероцепные ВМС содержат в цепи не
- 16. 3. По значению молярной массы Монодисперсные
- 17. Полидисперсные ВМС состоят из молекул различной
- 18. Специфическими свойствами полимеров являются: Гибкость цепей, Наличие прочных межмолекулярных связей
- 19. 18.2 ВМС могут образовывать как истинные, так и коллоидные растворы.
- 20. Истинные растворы образуются при растворении полярного полимера
- 21. Растворению полимеров предшествует их набухание.
- 22. Набухание ВМС –
- 23. Диффузия молекул ВМС в растворитель не протекает
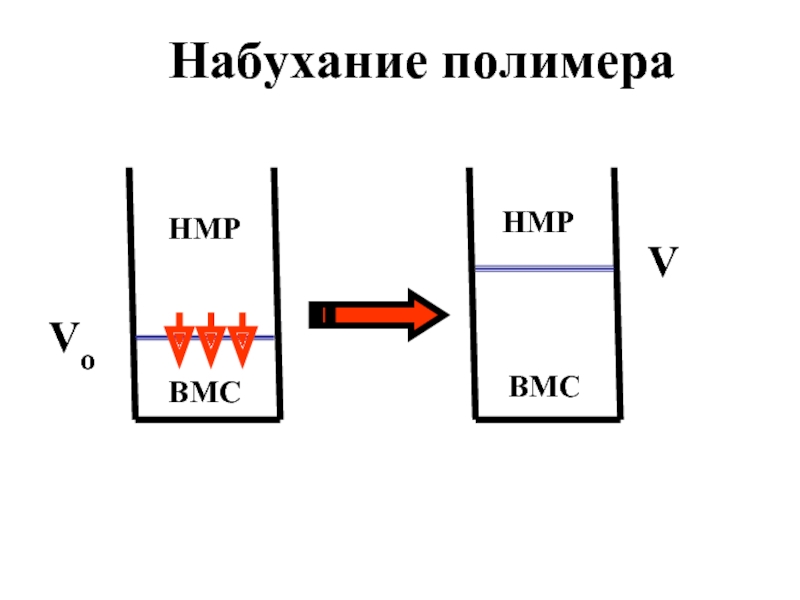
- 24. НМР ВМС ВМС НМР Набухание полимера Vo V
- 25. Мерой набухания служит степень набухания полимера (α):
- 26. α = m - mo mo где
- 27. Набухание Неогра- ниченное Ограни-ченное
- 28. Ограниченное набухание (желатин в холодной воде) приводит
- 29. Неограниченное набухание (желатин в горячей воде) завершается образованием истинного раствора.
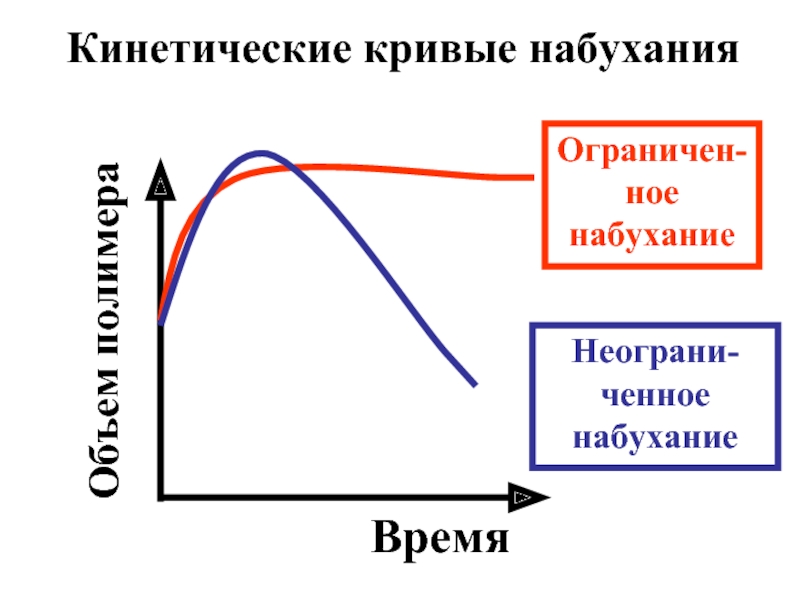
- 30. Время Объем полимера Кинетические кривые набухания Ограничен-ное набухание Неограни-ченное набухание
- 31. На процесс набухания влияет: Природа ВМС и растворителя: «Подобное растворяется в подобном»
- 32. 2) Конфигурация цепи полимера; линейные и разветвленные
- 33. 4) Температура:
- 34. В механизме физиологических процессов набухание играет большую роль: рост организма, сокращение мышц, тканевый обмен.
- 35. К набуханию способны кожа, ткани мозга, стекловидное тело глаза.
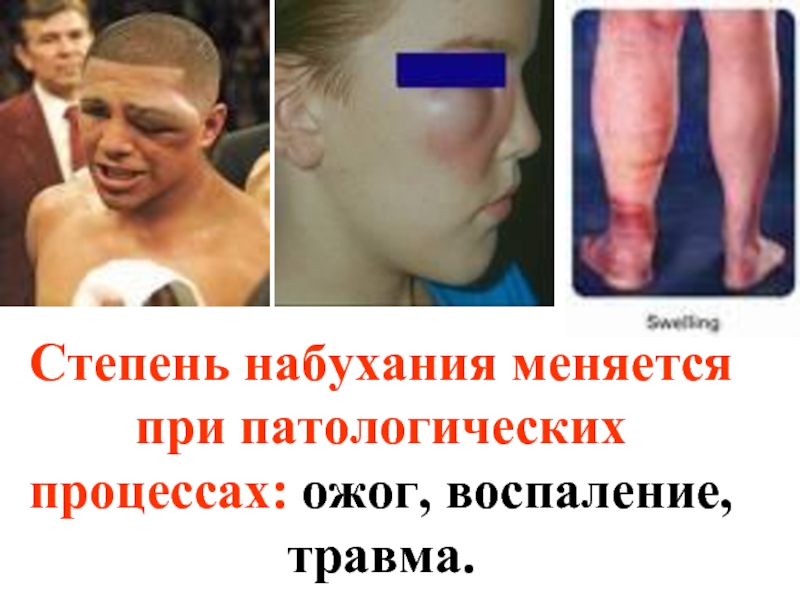
- 36. Степень набухания меняется при патологических процессах: ожог, воспаление, травма.
- 37. Старение человека сопровождается уменьшением способности тканей организма к набуханию.
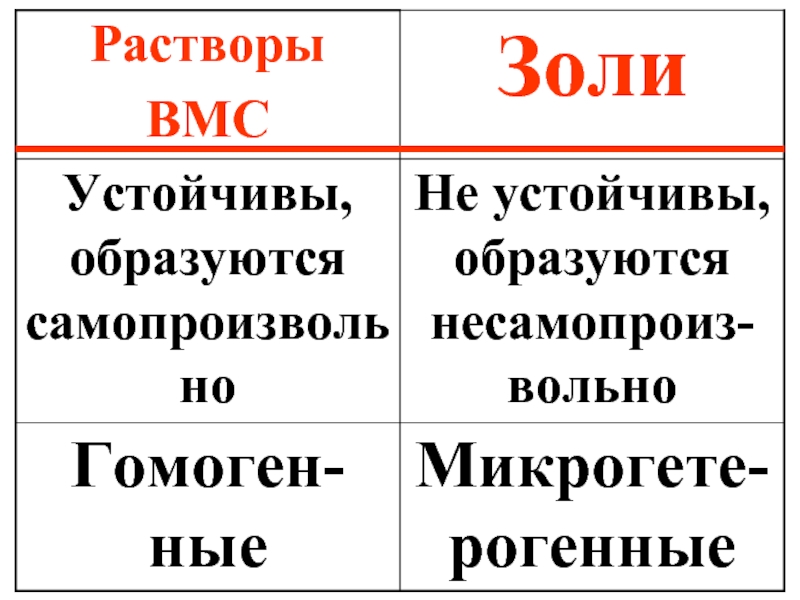
- 38. Растворы ВМС и коллоидные растворы существенно отличаются
- 42. 18.3 Полиэлектролиты – это ВМС, содержащие ионогенные
- 43. 1.Полиэлектролиты кислотного типа – СООН
- 44. 2. Полиэлектролиты основного типа –NH2 + H+ ⇄ – NH3+
- 45. 3. Амфотерные полиэлектролиты (полиамфолиты) – это ВМС,
- 46. Кислотно-основное равновесие в растворах белков
- 47. Особым состоянием белка является его изоэлектрическое состояние,
- 48. Изоэлектрическая точка (ИЭТ или pI)– это значение
- 49. В ИЭТ белки имеют специфические свойства, что объясняется особой конфигурацией их молекул.
- 50. ИЭТ Молекула свернута в спираль Конфигурации
- 51. Методы экспериментального определения ИЭТ белков 1)
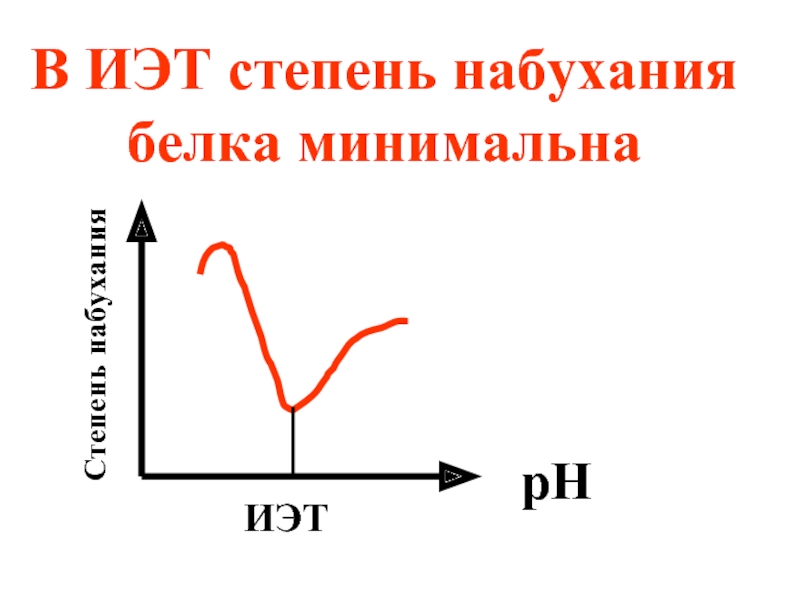
- 52. В ИЭТ степень набухания белка минимальна ИЭТ рН Степень набухания
- 53. 2) Путем измерения степени коагуляции белка в
- 54. Важнейшими факторами, вызывающими коагуляцию белка и других
- 55. Коагулирующее действие как электролитов, так и нерастворителей
- 56. 3) Путем измерения электрофоретической подвижности белков (u)
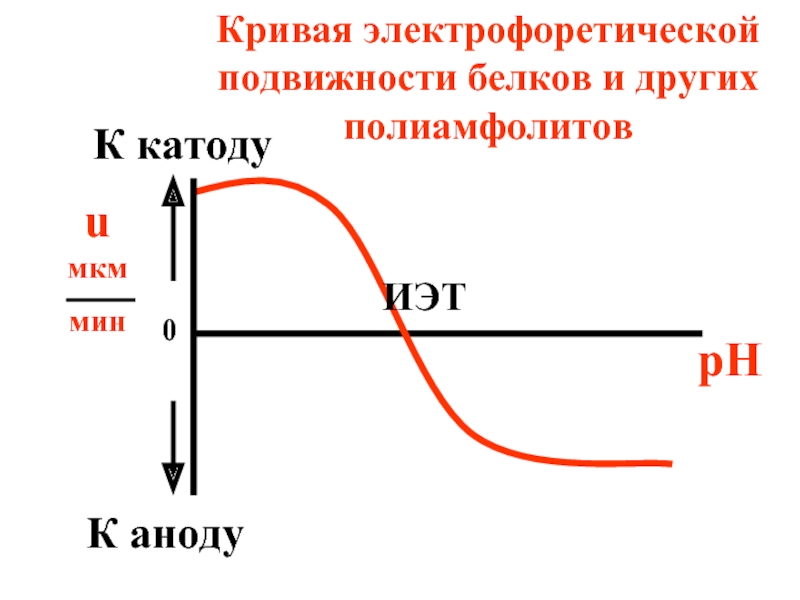
- 57. Кривая электрофоретической подвижности белков и других полиамфолитов
- 58. Электрофорез используют не только для определения ИЭТ, но и для разделения смесей белков на фракции.
- 59. 18.4 Коллоидная защита
- 60. Механизм защитного действия
- 61. Мерой защитного действия ВМС является «золотое»
- 62. желатин 0,008 гемоглобин
- 63. Измерение «золотого» числа спинномозговой жидкости используется как
- 64. Кроме «золотых», для количественной оценки защитного действия
- 65. Коллоидная защита играет важную роль в жизнедеятельности
- 66. При пониженной защитной функции белков возникает целый
- 67. Способность крови удерживать в растворенном состоянии большое
- 68. В фармацевтической промышленности защитные свойства ВМС
- 69. Например, лекарственный препарат колларгол – это коллоидный
- 70. Благодарим за внимание!!!
Слайд 2ПЛАН
18.1 Общая характеристика ВМС
18.2 Набухание и растворение ВМС
18.3 Полиэлектролиты
18.4 Коллоидная защита
Слайд 318.1 Высокомолекулярными соединениями (ВМС) называют вещества, имеющие молекулярную массу от
Слайд 4К природным ВМС (биополимерам) относятся крахмал, целлюлоза, декстраны, нуклеиновые кислоты, белки,
Слайд 6Реакции полимеризации
Полиэтилен
n CH2=CH2 → [–CH2–CH2–]n
Применение:
пленки, трубы, флаконы,
Слайд 72) Тефлон
nCF2=CF2 → [–CF2–CF2–]n
Применение:
протезы сердечного клапана и кровеносных сосудов.
Слайд 8 Реакции поликонденсации
Найлон-продукт поликонденсации адипиновой кислоты с гексаметилендиамином; используется для получения
Слайд 142. По элементному составу:
Гомоцепные ВМС полимерные цепи состоят только из атомов
Слайд 15 Гетероцепные ВМС содержат в цепи не только углерод, но и
Слайд 163. По значению молярной массы
Монодисперсные ВМС состоят из молекул, имеющих
Слайд 17 Полидисперсные ВМС состоят из молекул различной массы
(ДНК, фибриллярные белки, каучуки).
M
Слайд 18 Специфическими свойствами полимеров являются:
Гибкость цепей,
Наличие прочных межмолекулярных связей
Слайд 20Истинные растворы образуются при растворении полярного полимера в полярном растворителе (белок
Слайд 22Набухание ВМС – это увеличение объема и
Слайд 23Диффузия молекул ВМС в растворитель не протекает
Слайд 25Мерой набухания служит степень набухания полимера (α):
α =
V - Vo
Vo
где Vo
Слайд 28Ограниченное набухание (желатин в холодной воде) приводит к образованию геля. Гель
Слайд 29Неограниченное набухание (желатин в горячей воде) завершается образованием истинного раствора.
Слайд 30Время
Объем полимера
Кинетические кривые набухания
Ограничен-ное набухание
Неограни-ченное набухание
Слайд 322) Конфигурация цепи полимера; линейные и разветвленные ВМС лучше набухают, чем
3) Кислотность среды (у амфотерных полиэлектролитов)
Слайд 334) Температура:
Слайд 34В механизме физиологических процессов набухание играет большую роль: рост организма, сокращение
Слайд 38Растворы ВМС и коллоидные растворы существенно отличаются друг от друга, однако
Слайд 4218.3 Полиэлектролиты – это ВМС, содержащие ионогенные группы.
По характеру ионогенных
Слайд 431.Полиэлектролиты кислотного типа
– СООН ⇄ – COO- + H+
– SO3Н ⇄ – SO3- + H+
растворимый крахмал, гуммиарабик.
Слайд 453. Амфотерные полиэлектролиты (полиамфолиты) – это ВМС, содержащие и кислотные, и
Важнейшие из них – белки.
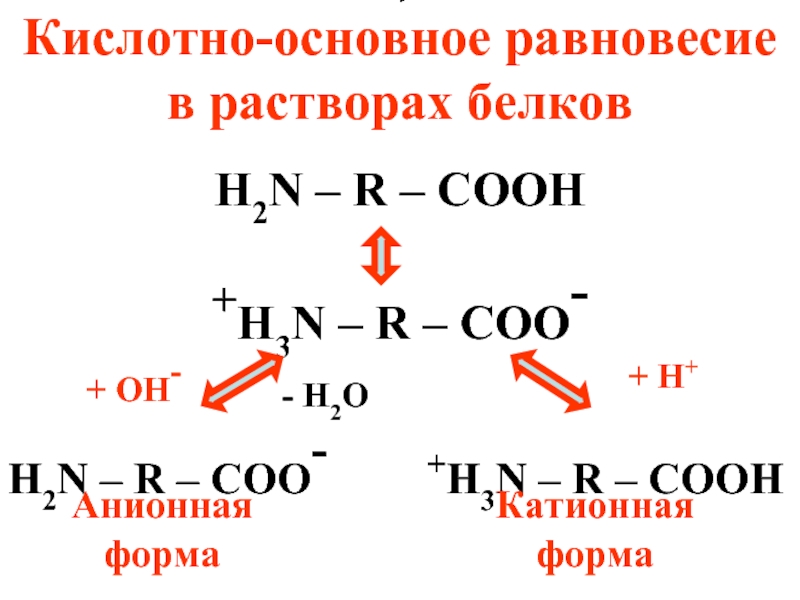
Слайд 46Кислотно-основное равновесие в растворах белков
H2N – R – COOH
+H3N – R – COO-
H2N – R – COO- +H3N – R – COOH
+ OH-
+ H+
Анионная форма
Катионная форма
- H2O
Слайд 47Особым состоянием белка является его изоэлектрическое состояние, в котором суммарный заряд
+H3N – R – COO-
Слайд 48Изоэлектрическая точка (ИЭТ или pI)– это значение рН раствора, при котором
Для большинства белков рI изменяется в диапазоне 4,5-6,0.
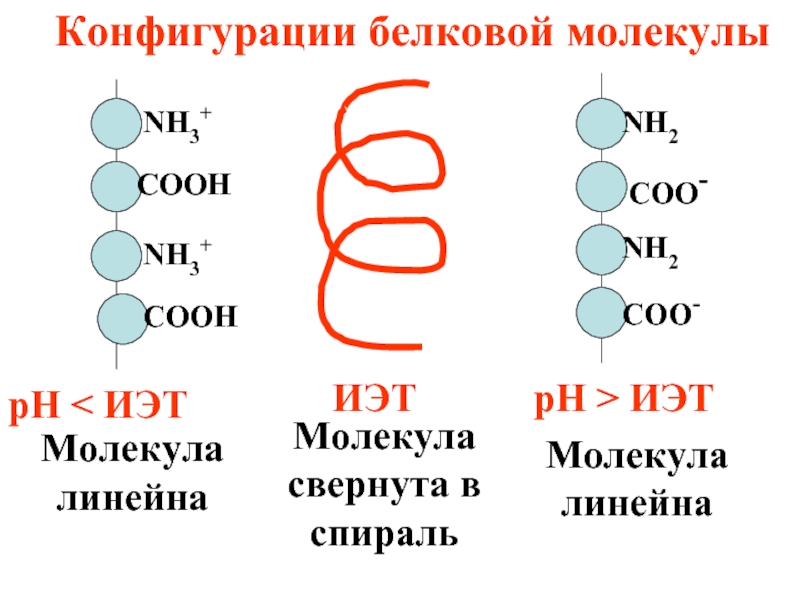
Слайд 50
ИЭТ
Молекула свернута в спираль
Конфигурации белковой молекулы
рН < ИЭТ
рН > ИЭТ
Молекула линейна
Молекула
линейна
NH3+
NH3+
NH2
NH2
COO-
COO-
COOH
COOH
Слайд 51Методы экспериментального определения ИЭТ белков
1) Путем измерения степени набухания белков в
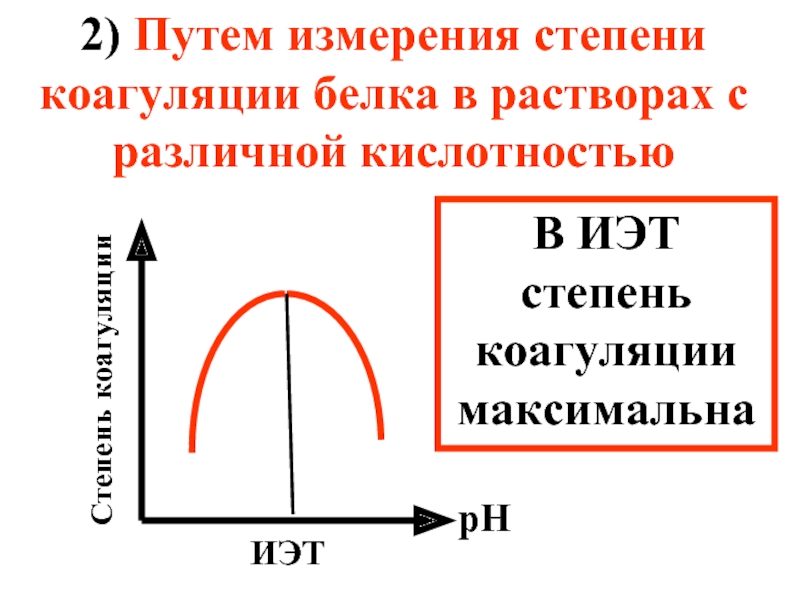
Слайд 532) Путем измерения степени коагуляции белка в растворах с различной кислотностью
рН
Степень
ИЭТ
В ИЭТ степень коагуляции максимальна
Слайд 54Важнейшими факторами, вызывающими коагуляцию белка и других ВМС являются:
добавление электролитов
добавление нерастворителей – жидкостей, в которых полимер практически не растворим.
Слайд 55Коагулирующее действие как электролитов, так и нерастворителей обусловлено их десольватирующем действием;
Слайд 563) Путем измерения электрофоретической подвижности белков (u) в растворах с различной
В ИЭТ электрофоретическая подвижность белков равна нулю, так как их молекулы электронейтральны.
Слайд 57Кривая электрофоретической подвижности белков и других полиамфолитов
u мкм
мин
pH
ИЭТ
0
К аноду
К катоду
Слайд 58Электрофорез используют не только для определения ИЭТ, но и для разделения
Слайд 5918.4 Коллоидная защита
Слайд 60Механизм защитного действия
Слайд 61
Мерой защитного действия ВМС является «золотое» число - минимальная масса (мг)
Слайд 63Измерение «золотого» числа спинномозговой жидкости используется как важный диагностический тест; оно
Слайд 64Кроме «золотых», для количественной оценки защитного действия ВМС используют «рубиновые», «серебряные»,
Слайд 65Коллоидная защита играет важную роль в жизнедеятельности организма.
Белки крови стабилизируют
Слайд 66При пониженной защитной функции белков возникает целый ряд заболеваний: подагра, атеросклероз,
Слайд 67Способность крови удерживать в растворенном состоянии большое количество газов (О2 и
также обусловлена защитным действием белков.





![Реакции полимеризацииПолиэтилен n CH2=CH2 → [–CH2–CH2–]n Применение: пленки, трубы, флаконы, бутылочки.](/img/tmb/2/185041/fcf110689b33b22a3e8779474d3d085e-800x.jpg)
![2) ТефлонnCF2=CF2 → [–CF2–CF2–]n Применение:протезы сердечного клапана и кровеносных сосудов.](/img/tmb/2/185041/7214cbb83734307fd5c89bceb751e9e6-800x.jpg)

![n HOOC-(CH2)4-COOH + n H2N–(CH2)6–NH2[-CO-(CH2)4-CO-NH-(CH2)6-NH-]n + H2O Получение найлона](/img/tmb/2/185041/d2b8182e32d6ccb9449a12c7b775fef4-800x.jpg)