- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
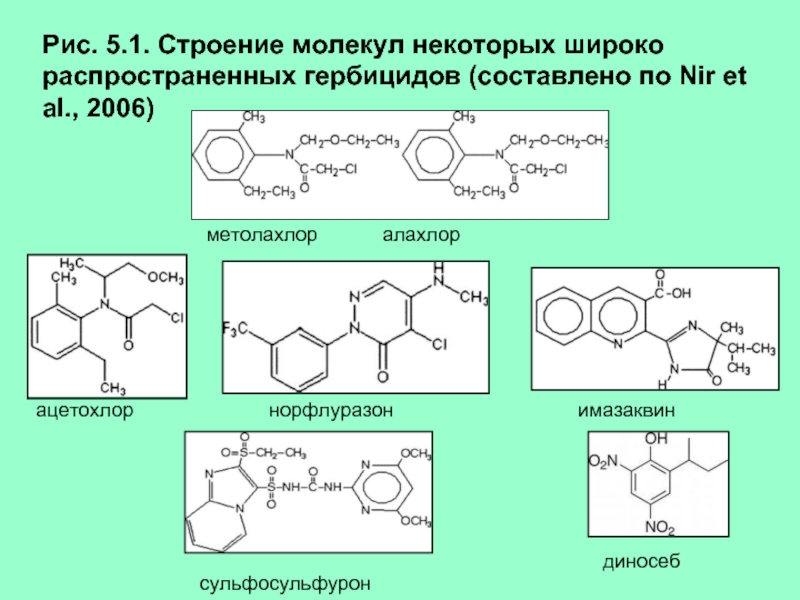
Растворы. Основные понятия и определения презентация
Содержание
- 1. Растворы. Основные понятия и определения
- 2. Основные понятия и определения Грубодисперсные системы Суспензии Эмульсии Аэрозоли
- 3. Основные понятия и определения Коллоидные растворы
- 4. Теории растворов Физическая теория (Вант-Гофф, Аррениус) – Химическая теория (Менделеев, Каблуков)
- 5. Современная теория объединяет обе теории. Растворы обладают
- 6. Сольватная теория Процесс растворения состоит из
- 7. Сольватная теория Сольватация ионов Диффузия сольватов
- 8. Растворимость Растворимость – способность в-ва раст-ся в
- 9. Растворимость На растворимость влияют: 1. Природа компонентов
- 10. Растворимость 2. Температура
- 11. 3. Влияние давления Ув-ние Р приводит к
- 12. Свойства растворов неэлектролитов Идеальный раствор – Образ-ие
- 13. Коллигативные свойства растворов Коллиг-ные св-ва –
- 14. Давление насыщенного пара растворителя над раствором
- 15. Первый закон Рауля Обозначим: Pо – давление
- 16. Первый закон Рауля P1о = Pо ⋅ Х1
- 17. Первый закон Рауля давление насыщенного пара р-ля
- 18. Первый закон Рауля относительное понижение Р
- 19. Температура кипения и замерзания раствора. Второй закон
- 20. Температура кипения и замерзания раствора. Второй закон
- 21. Осмос Осмотическое давление – это такое Р,
- 22. Растворы электролитов Электролиты – это в-ва, способные
- 23. Теория электролитической диссоциации Аррениуса (ТЭД) Основные положения
- 24. Колличественные характеристики процесса диссоциации Константа диссоциации.
- 25. Колличественные характеристики процесса диссоциации Степень диссоциации
- 26. Колличественные характеристики процесса диссоциации α <
- 27. Связь степени дис-ции с изотоническим коэф-том
- 28. Закон разбавления Оствальда
- 29. Факторы, влияющие на степень диссоциации
- 30. Ионное произведение воды
Слайд 3Основные понятия и определения
Коллоидные растворы
Растворы– однофазные системы переменного состава, состоящие
Слайд 4Теории растворов
Физическая теория
(Вант-Гофф, Аррениус) –
Химическая теория
(Менделеев, Каблуков)
Слайд 5Современная теория
объединяет обе теории.
Растворы обладают переменностью состава
К р-рам не применимы стехиом.
Р-ры обладают однородностью состава по всей фазе
Процесс растворения сопровождается объемными и тепловыми эффектами
Слайд 6Сольватная теория
Процесс растворения состоит из 3 стадий
Фазовый переход – разрушение
Слайд 8Растворимость
Растворимость – способность в-ва раст-ся в опред. кол-ве раств-ля.
Мерой раств-ти крист.
Коэф. растворимости – масса раств. в-ва, содержащаяся в 100 г насыщ. р-ра.
Мерой раств-сти газ. в-ва явл-ся:
коэф. абсорбции – объем газа (при н.у.), раств-ся в 1 V растворителя.
Слайд 9Растворимость
На растворимость влияют:
1. Природа компонентов
1) «Подобное раствор-ся в подобном»
2) Н-связи (неограниченно
3) Силы В-дер-В
Слайд 113. Влияние давления
Ув-ние Р приводит к росту раст-сти газов.
Закон Генри: раст-сть
c = k·P
Слайд 12Свойства растворов неэлектролитов
Идеальный раствор –
Образ-ие идеального р-ра не сопровождается объемными и
Слайд 13Коллигативные свойства растворов
Коллиг-ные св-ва –
1. Давление насыщенного пара
р-ля над
2. Температура кипения и замерзания р-ра
3. Осмотическое давление
Слайд 14Давление насыщенного пара растворителя над раствором
(Первый закон Рауля)
жидкость ⮀ пар
Растворение
Слайд 15Первый закон Рауля
Обозначим:
Pо – давление насыщенного пара р-ля над чистым р-лем;
P1о
Х1 – мольная доля р-ля;
Х2 – мольная доля раст-ного в-ва.
Слайд 17Первый закон Рауля
давление насыщенного пара р-ля над р-ром равно его давлению
Слайд 18Первый закон Рауля
относительное понижение Р насыщенного пара р-ля над р-ром =
Слайд 20Температура кипения и замерзания раствора.
Второй закон Рауля
Повышение tкип р-ра и понижение
Δtкип = Кэ⋅Сm
Δtзам = Кк⋅Сm
Кэ – эбулиоскопическая постоянная;
Кк – криоскопическая.
Слайд 21Осмос
Осмотическое давление – это такое Р, которое нужно приложить, чтобы подавить
Вант-Гофф:
Pосм. = См⋅R⋅T
Слайд 22Растворы электролитов
Электролиты – это в-ва, способные диссоциировать в р-рах или расплавах
Доказательство
1. Электропроводность р-ров электролитов.
2. Отклонение от законов Рауля и Вант-Гоффа.
Слайд 23Теория электролитической диссоциации Аррениуса (ТЭД)
Основные положения ТЭД
1. Электролиты в растворах диссоциируют
2. Диссоциация является неполной и к процессу дис-ции применим ЗДМ.
3. Растворы электролитов электропроводны.
Слайд 25Колличественные характеристики
процесса диссоциации
Степень диссоциации – это отношение числа диссоциированных молекул
Слайд 26Колличественные характеристики
процесса диссоциации
α < 3% - слабый электролит
α > 30%
3% ≤ α ≤ 30% - средней силы
Слайд 28Закон разбавления Оствальда
Для слабых электролитов α → 0, а (1
α =
Закон разбавления Оствальда:
степень диссоциации слабого электролита увеличивается при разбавлении раствора
Слайд 29Факторы, влияющие на степень диссоциации
α зависит от конц-ции р-ра.
α
3. α зависит от наличия в р-ре одноименных ионов.
Слайд 30Ионное произведение воды
[H+]⋅[OH-] = 10-14
В чистой воде: [H+] = [OH-]
рН = - lg[H+]
рН - водородный показатель
рОН = - lg[ОH-]




























![Ионное произведение воды [H+]⋅[OH-] = 10-14В чистой воде: [H+] = [OH-] = 10-7рН = -](/img/tmb/4/345415/99d488350b33adcabaebd0e8b95f053e-800x.jpg)