- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Правила образования названий разветвленных алканов по международной номенклатуре (ИЮПАК) презентация
Содержание
- 1. Правила образования названий разветвленных алканов по международной номенклатуре (ИЮПАК)
- 2. Правило. Найти самую длинную (главную)
- 3. Пронумеровать атомы углерода главной цепи. Номер
- 4. Назвать алкильный радикал
- 5. В молекуле с несколькими одинаковыми
- 6. Свойства алканов
- 7. Физические свойства алканов СН4... С4Н10
- 8. Химические свойства алканов Для алканов наиболее характерны
- 9. Реакция замещения (разрыв связей С-Н) или
- 10. Галогенирование (замещение атома водорода атомом галогена с
- 11. 1.2 Нитрование Нитрование (замещение атома водорода нитрогруппой
- 12. 140°C
- 13. 1.3 Сульфирование. Замещение атома водорода сульфогруппой —
- 14. 2. Реакция окисления При обычных условиях алканы устойчивы к действию окислителей (КMnО4, К2Сг207).
- 15. 2.1 Окисление кислородом воздуха при высоких температурах
- 16. 2.2 Окисление кислородом воздуха при невысоких температурах
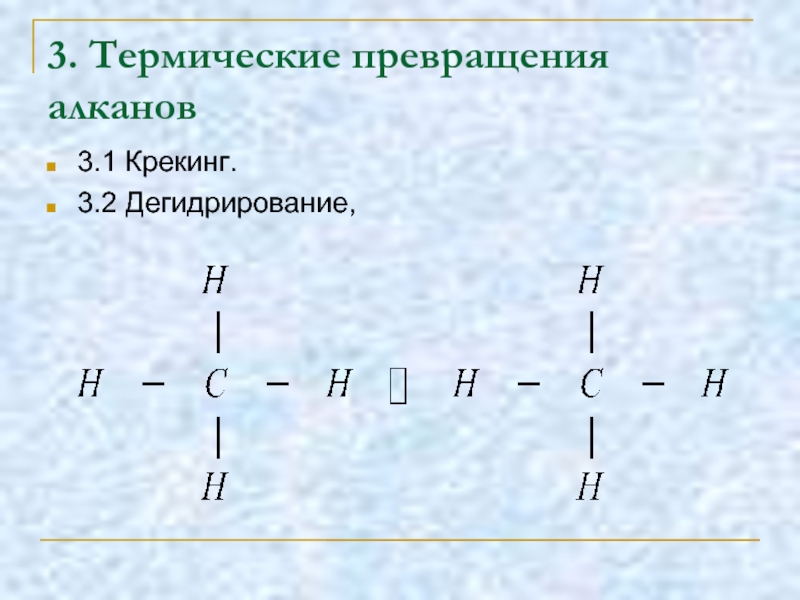
- 17. 3. Термические превращения алканов 3.1 Крекинг. 3.2 Дегидрирование,
- 18. 3.1 Крекинг Крекинг (англ. cracking —
- 19. 3.1 Дегидрирование Дегидрирование: отщепление водорода происходит в
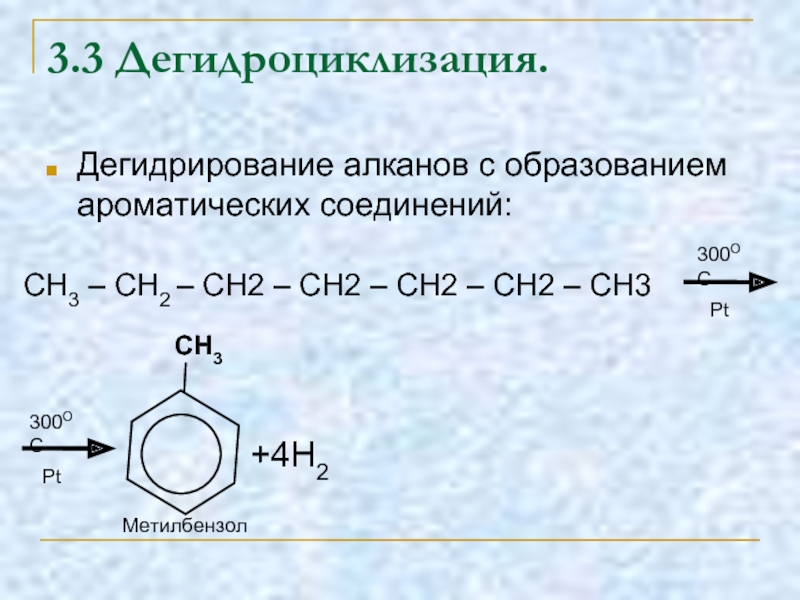
- 20. 3.3 Дегидроциклизация. Дегидрирование алканов с образованием ароматических
- 21. 3.4 Изомеризация Изомеризация – превращение химического
- 22. Способы получения алканов Каждый класс органических соединений
Слайд 1Правила образования названий разветвленных алканов по международной номенклатуре (ИЮПАК)
Лекция №1
Слайд 2Правило.
Найти самую длинную (главную) неразветвленную цепь углеродных атомов.
Таким образом, в данном
1.
2.
3.
4 «С»
5 «С»
6 «С»
Слайд 3
Пронумеровать атомы углерода главной цепи. Номер атома углерода, у которого находится
Указать положение заместителя (номер атома углерода, у которого находится алкильный радикал).
6
5
4
3
2
1
3
3-….
Слайд 4
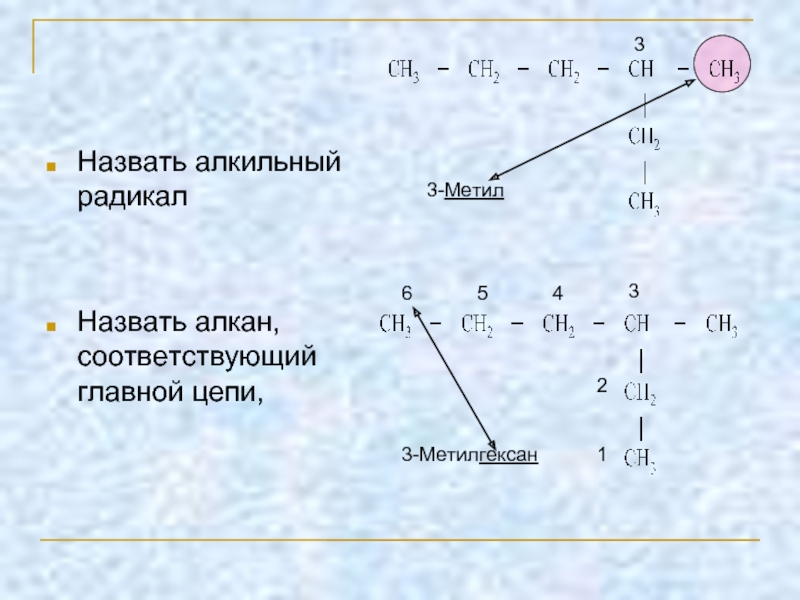
Назвать алкильный радикал
Назвать алкан, соответствующий главной цепи,
3
3-Метил
3
6
5
4
2
1
3-Метилгексан
Слайд 5
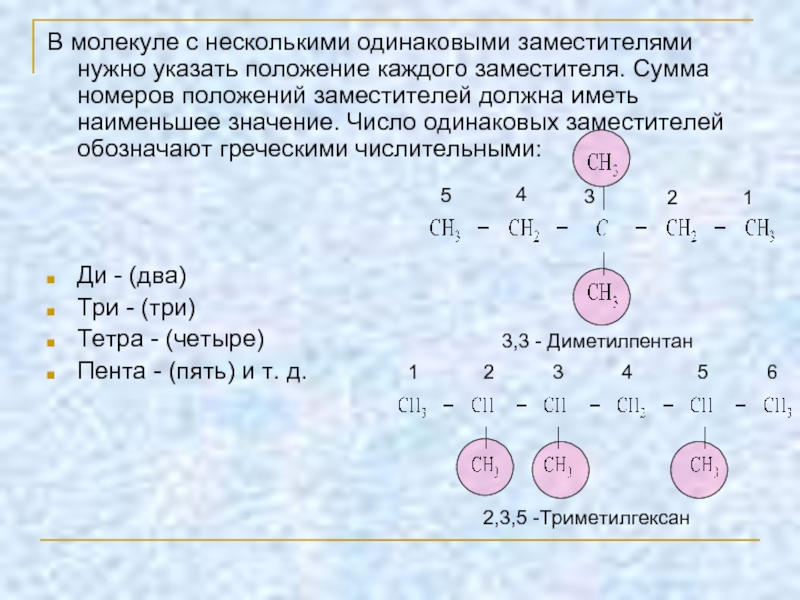
В молекуле с несколькими одинаковыми заместителями нужно указать положение каждого заместителя.
Ди - (два)
Три - (три)
Тетра - (четыре)
Пента - (пять) и т. д.
3,3 - Диметилпентан
3
5
4
2
1
2,3,5 -Триметилгексан
Слайд 7Физические свойства алканов
СН4... С4Н10 — Газы (без запаха)
С5Н12... С15Н32
C16H34 — Твердые вещества (без запаха)
t° кипения и t° плавления увеличиваются
Алканы — бесцветные вещества, легче воды, плохо растворяются в воде.
Слайд 8Химические свойства алканов
Для алканов наиболее характерны реакции замещения.
В этих реакциях
Слайд 10Галогенирование (замещение атома водорода атомом галогена с образованием галогеналкана RHal).
Низшие алканы
1.1 Галогенирование
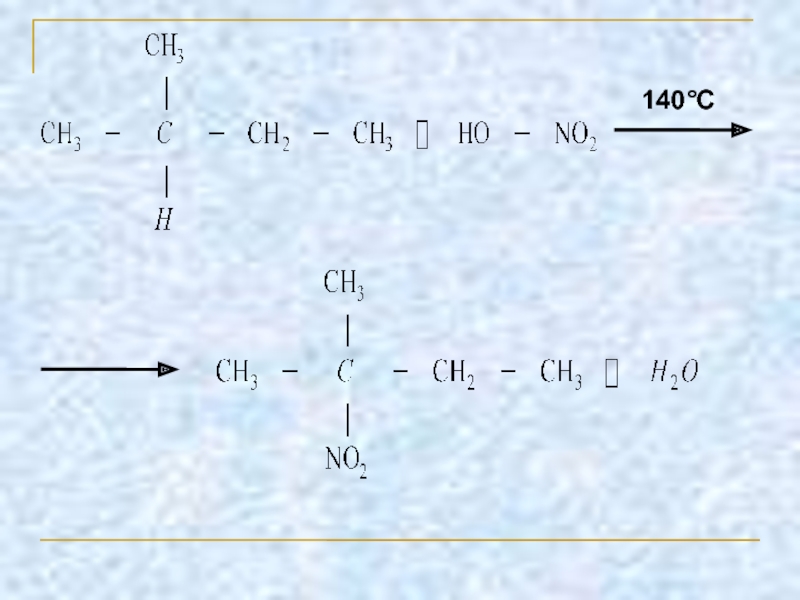
Слайд 111.2 Нитрование
Нитрование (замещение атома водорода нитрогруппой — NO2 с образованием нитроалканов
В результате реакции образуется смесь изомерных нитросоединений. Наиболее легко замещаются атомы водорода у третичного атома углерода, труднее – у вторичного, наиболее трудно – у первичного:
Слайд 131.3 Сульфирование.
Замещение атома водорода сульфогруппой — SO3H с образованием алкансульфокислот.
Сульфирующий
Слайд 142. Реакция окисления
При обычных условиях алканы устойчивы к действию окислителей (КMnО4,
Слайд 152.1 Окисление кислородом воздуха при высоких температурах (горение).
полное окисление (избыток О2)
Не полное окисление (недостаток О2)
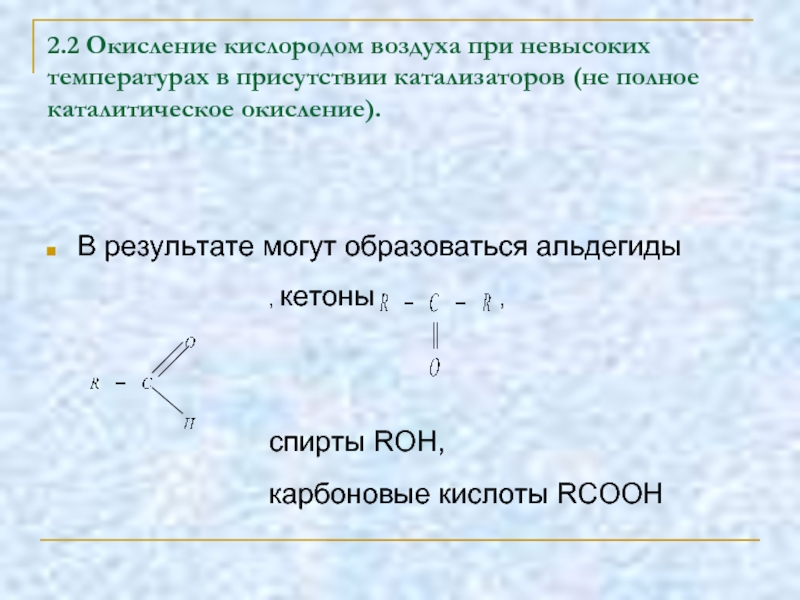
Слайд 162.2 Окисление кислородом воздуха при невысоких температурах в присутствии катализаторов (не
В результате могут образоваться альдегиды
Слайд 183.1 Крекинг
Крекинг (англ. cracking — расщепление) — это разрыв связей
Термический крекинг (пиролиз) осуществляется при температуре 450—700о С.
Слайд 193.1 Дегидрирование
Дегидрирование:
отщепление водорода происходит в результате разрыва связей С — Н;
Осуществляется
При дегидрировании метана образуется этим (ацетилен):
t°, кат.
C2H6
C2H4+H2
этан
этен
Слайд 203.3 Дегидроциклизация.
Дегидрирование алканов с образованием ароматических соединений:
CH3 – CH2 –
300O C
Pt
300O C
Pt
+4H2
CH3
Метилбензол
Слайд 213.4 Изомеризация
Изомеризация – превращение химического соединения в его изомер:
Слайд 22Способы получения алканов
Каждый класс органических соединений характеризуется рядом общих методов синтеза.
Синтез из непредельных углеводородов
Каталитическое гидрирование (+H2) непредельных углеводородов.