- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Практическое занятие по основам биохимии с методами клинико-биохимических исследований. Химия углеводов презентация
Содержание
- 1. Практическое занятие по основам биохимии с методами клинико-биохимических исследований. Химия углеводов
- 2. ОБНАРУЖЕНИЕ УГЛЕВОДОВ Качественные реакции на углеводы позволяют
- 3. Реакция №1 «Проба Биаля (обнаружение
- 4. Реактивы : 1) орцин (5-метилорцин);
- 5. Берут пробирку, подписывают и наливают 5 мл
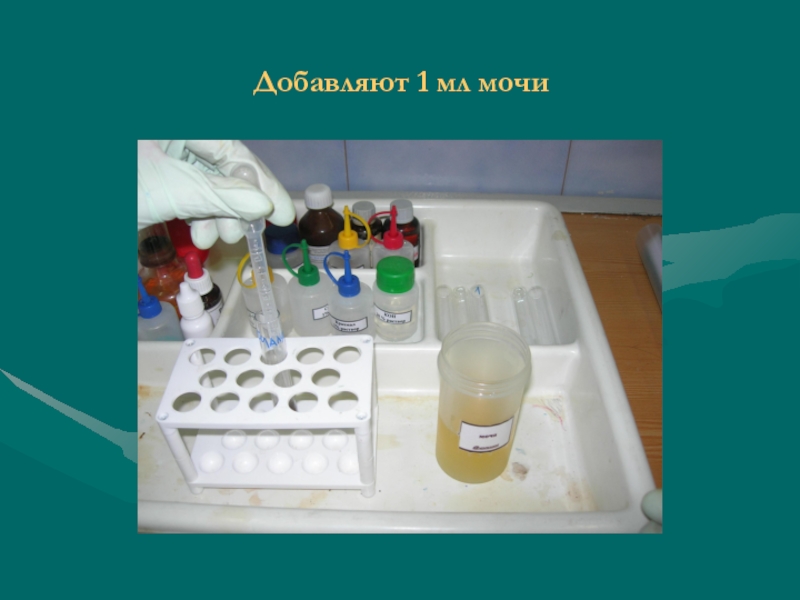
- 6. Добавляют 1 мл мочи
- 7. Пробирку нагревают до кипения
- 8. При положительной реакции появляется желто-зеленое окрашивание. В
- 9. Реакция №2 «Проба Велька (обнаружение лактозы
- 10. Реактивы : 1) аммиак водный, концентрированный;
- 11. Берут три пробирки и номеруют
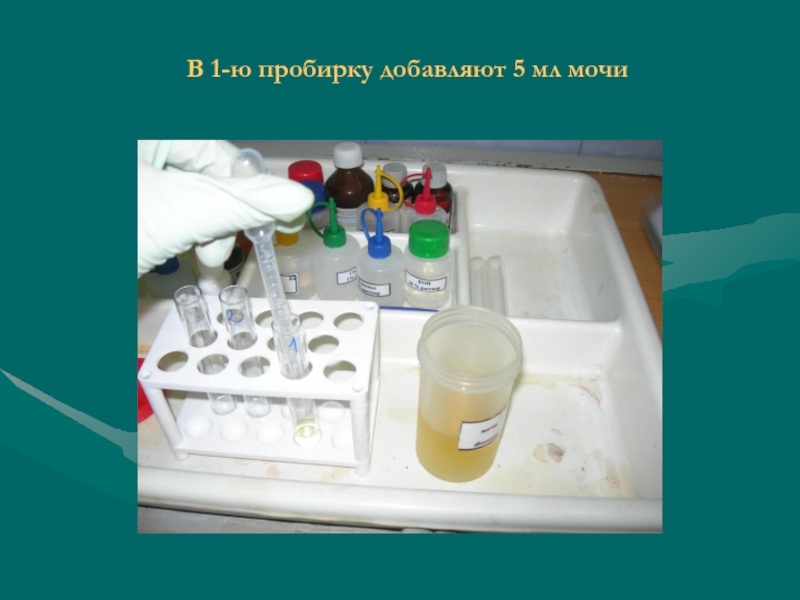
- 12. В 1-ю пробирку добавляют 5 мл мочи
- 13. Во 2-ю пробирку добавляют 5 мл раствора
- 14. В 3-ю пробирку добавляют 5 мл раствора
- 15. Во все три пробирки прибавляют 2,5 мл раствора аммиака
- 16. Затем во все 3 пробирки добавляем 200 мкл (0,2 мл) раствора КОН (20% раствор)
- 17. Пробирки нагревают на водяной бани 30 минут при 600С
- 18. При наличие лактозы появляется коричневая окраска (пробирка №2)
- 19. При наличие мальтозы появляется красная окраска (пробирка №3)
- 20. В моче здорового человека мальтоза и лактоза не обнаруживается (пробирка №1)
- 21. Реакция №3 «Проба Селиванова
- 22. Реактивы : 1) HCl, 1 моль/л;
- 23. Берут 2 пробирки, номеруют
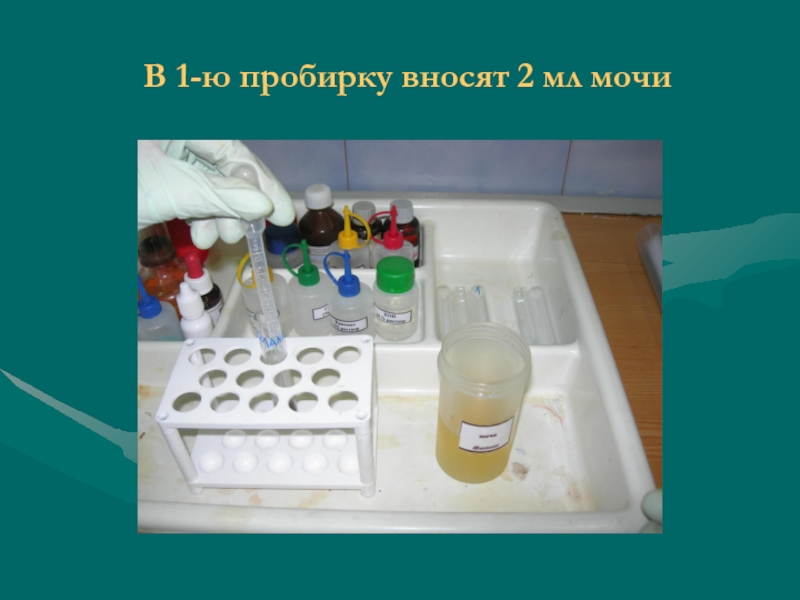
- 24. В 1-ю пробирку вносят 2 мл мочи
- 25. Во 2-ю пробирку вносят 2 мл раствора фруктозы (1% раствор)
- 26. После чего в каждую пробирку приливают по 1 мл раствора резорцина
- 27. Пробирки нагревают до закипания
- 28. При положительной пробе развивается интенсивное красное окрашивание
- 29. В норме окраска не появляется (пробирка №1)
- 30. Оценку пробы проводят в момент закипания,
- 31. Реакция №4 «Обнаружение крахмала»
- 32. Реактивы : 1) 1% раствор крахмала;
- 33. Берут пробирку и подписывают её
- 34. Добавляют 10 капель раствора крахмала (1% раствор)
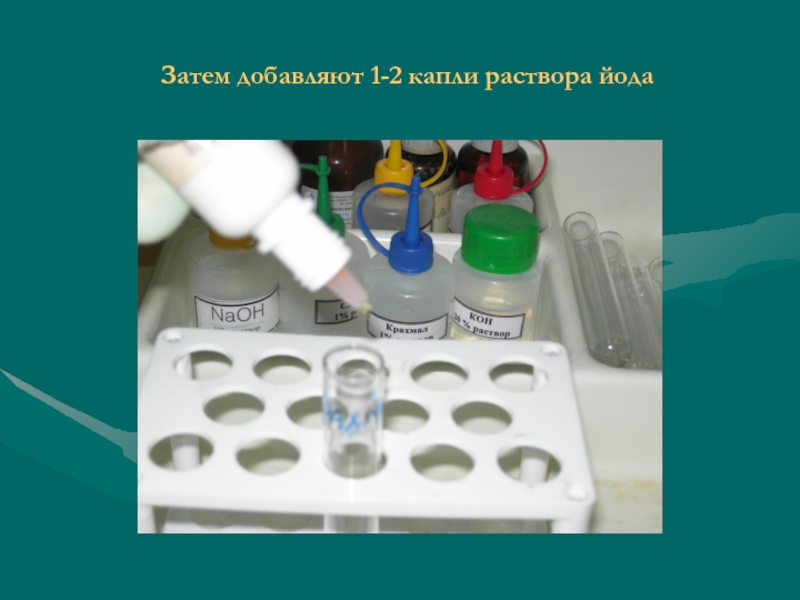
- 35. Затем добавляют 1-2 капли раствора йода
- 36. При положительной реакции на йод появляется ярко-синее окрашивание
- 37. СВОЙСТВА УГЛЕВОДОВ Моносахариды и некоторые дисахариды,
- 38. Реакция №5 «Реакция Троммера»
- 39. Реактивы : 1) глюкоза, 1% раствор;
- 40. Берут 4 пробирки и номеруют
- 41. В 1-ю пробирку добавляют 10 капель
- 42. Во 2-ю пробирку добавляют 10 капель
- 43. В 3ю пробирку добавляют 10 капель
- 44. В 4-ю пробирку добавляют 10 капель
- 45. После чего в каждую пробирку добавляют по 10 капель гидроокиси натрия (NaOH 10% раствор)
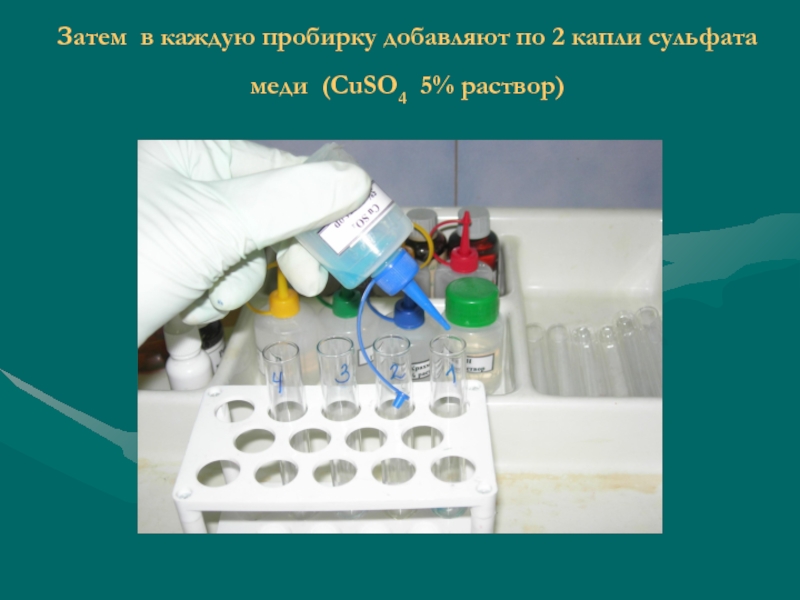
- 46. Затем в каждую пробирку добавляют по 2 капли сульфата меди (CuSO4 5% раствор)
- 47. Каждую пробирку осторожно нагревают до кипения
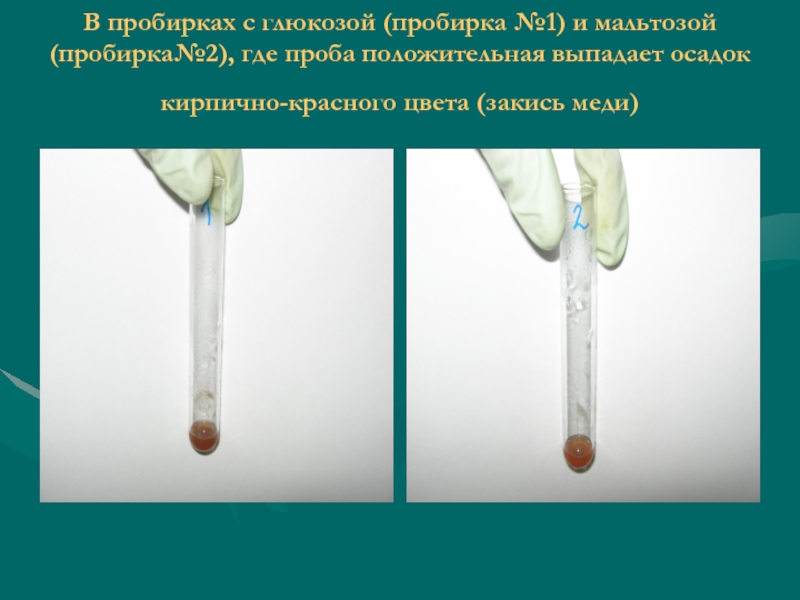
- 48. В пробирках с глюкозой (пробирка №1) и
- 49. В пробирках с сахарозой (пробирка №3) и крахмалом (пробирка№4) реакция отрицательная (изменения цвета не происходит)
- 50. Реакция №6 «Реакция Ниландера»
- 51. Реактивы : 1) глюкоза, 1% раствор;
- 52. Берут 4 пробирки и номеруют
- 53. В 1-ю пробирку добавляют 10 капель
- 54. Во 2-ю пробирку добавляют 10 капель
- 55. В 3ю пробирку добавляют 10 капель
- 56. В 4-ю пробирку добавляют 10 капель
- 57. После чего в каждую пробирку добавляют по 10 капель реактива Ниландера
- 58. Каждую пробирку осторожно кипятят 2 минуты
- 59. В пробирках с глюкозой (пробирка №1) и
- 60. В пробирках с сахарозой (пробирка №3) и крахмалом (пробирка№4) реакция отрицательная (изменения цвета не происходит)
- 61. Надеемся, что наша инструкция поможет вам не сделать ошибок в практической работе. Желаем удачи!
- 62. Составитель: Кузнецова Т.Н. – преподаватель дисциплины «Основы
Слайд 1Практическое занятие
по основам биохимии с методами клинико-биохимических исследований
«ХИМИЯ УГЛЕВОДОВ»
Слайд 2ОБНАРУЖЕНИЕ УГЛЕВОДОВ
Качественные реакции на углеводы позволяют определить их присутствие в различных
биологических жидкостях и провести дифференциацию моно-, ди- и полисахаридов. В клинической лабораторной практике этими реакциями пользуются для обнаружения в моче лактозы, мальтозы и пентоз, что имеет диагностическое значение.
Слайд 3Реакция №1
«Проба Биаля
(обнаружение пентоз)»
Принцип: пентозы с орцином
и треххлористым железом в кислой среде образуют при нагревании соединение желто-зеленого цвета.
Слайд 4Реактивы :
1) орцин (5-метилорцин);
2) концентрированная хлористоводородная кислота; 3) треххлористое
железо FeCI3 x 6H2O, 10% раствор;
4) реактив Биаля (1 г орцина растворяют в 500 мл хлористоводородной кислоты и добавляют 1 мл 10% раствора треххлористого железа);
5) моча;
4) реактив Биаля (1 г орцина растворяют в 500 мл хлористоводородной кислоты и добавляют 1 мл 10% раствора треххлористого железа);
5) моча;
Слайд 8При положительной реакции появляется желто-зеленое окрашивание. В моче здорового человека пентозы
не обнаруживаются (отрицательный результат)
Слайд 9Реакция №2
«Проба Велька (обнаружение лактозы и мальтозы)»
Принцип: лактоза
и мальтоза с аммиаком в щелочной среде образуют при нагревании окрашенные соединения.
Слайд 10Реактивы :
1) аммиак водный, концентрированный;
2) гидроокись калия, 20% раствор;
3) 1% раствор лактозы;
4) 1% раствор мальтозы;
5) моча.
Слайд 21Реакция №3 «Проба Селиванова
(обнаружение фруктозы»
Принцип: при нагревании фруктозы с резорцином в кислой среде образуются соединения, окрашенные в красный цвет.
Слайд 22Реактивы :
1) HCl, 1 моль/л;
2) резорцин (5 г в
1 моль/л раствора HCl);
3) моча;
4) 1% раствор фруктозы.
3) моча;
4) 1% раствор фруктозы.
Слайд 30
Оценку пробы проводят в момент закипания, так как при длительном кипячении
окраска может появиться при наличии глюкозы (при небольшой концентрации глюкозы образуется красно-бурый осадок). Пищевая нагрузка медом и фруктами может дать положительную пробу.
Слайд 31Реакция №4
«Обнаружение крахмала»
Принцип: крахмал с йодом образует окрашенное
соединение синего цвета.
Слайд 37СВОЙСТВА УГЛЕВОДОВ
Моносахариды и некоторые дисахариды, имеющие свободную карбонильную группу, обладают способностью
восстанавливать в щелочной среде металлы из окислов в закисные формы или свободное состояние. Этим свойством пользуются в практике для обнаружения глюкозы в крови и моче.
Слайд 38Реакция №5
«Реакция Троммера»
Принцип: глюкоза в щелочной среде восстанавливает
окись меди в закись, при этом сама окисляется до глюконовой кислоты.
Слайд 39Реактивы :
1) глюкоза, 1% раствор;
2) мальтоза, 1% раствор;
3)
сахароза, 1% раствор;
4) крахмал, 1% раствор;
5) гидроокись натрия, 10% раствор;
6) сульфат меди, 5% раствор.
4) крахмал, 1% раствор;
5) гидроокись натрия, 10% раствор;
6) сульфат меди, 5% раствор.
Слайд 48В пробирках с глюкозой (пробирка №1) и мальтозой (пробирка№2), где проба
положительная выпадает осадок кирпично-красного цвета (закись меди)
Слайд 49В пробирках с сахарозой (пробирка №3) и крахмалом (пробирка№4) реакция отрицательная
(изменения цвета не происходит)
Слайд 50Реакция №6
«Реакция Ниландера»
Принцип: Глюкоза, окисляясь, восстанавливает висмут до
гидрата закиси или свободного состояния.
Слайд 51Реактивы :
1) глюкоза, 1% раствор;
2) мальтоза, 1% раствор;
3)
сахароза, 1% раствор;
4) крахмал, 1% раствор;
5) реактив Ниландера (в фарфоровой ступке смешивают 2 г нитрата висмута и 4 г сигнетовой соли. При тщательном растирании добавляют небольшими пропорциями 10 мл 10% раствора гидроокиси натрия. Фильтруют, хранят в склянке тёмного стекла на холоде).
4) крахмал, 1% раствор;
5) реактив Ниландера (в фарфоровой ступке смешивают 2 г нитрата висмута и 4 г сигнетовой соли. При тщательном растирании добавляют небольшими пропорциями 10 мл 10% раствора гидроокиси натрия. Фильтруют, хранят в склянке тёмного стекла на холоде).
Слайд 59В пробирках с глюкозой (пробирка №1) и мальтозой (пробирка№2), где проба
положительная появляется темно-коричневое окрашивание
Слайд 60В пробирках с сахарозой (пробирка №3) и крахмалом (пробирка№4) реакция отрицательная
(изменения цвета не происходит)
Слайд 61Надеемся, что наша инструкция поможет вам не сделать ошибок в практической
работе.
Желаем удачи!
Слайд 62Составитель: Кузнецова Т.Н. – преподаватель дисциплины «Основы биохимии с методами клинико-биохимических
исследований»
Москва
2008 год