атомное ядро;
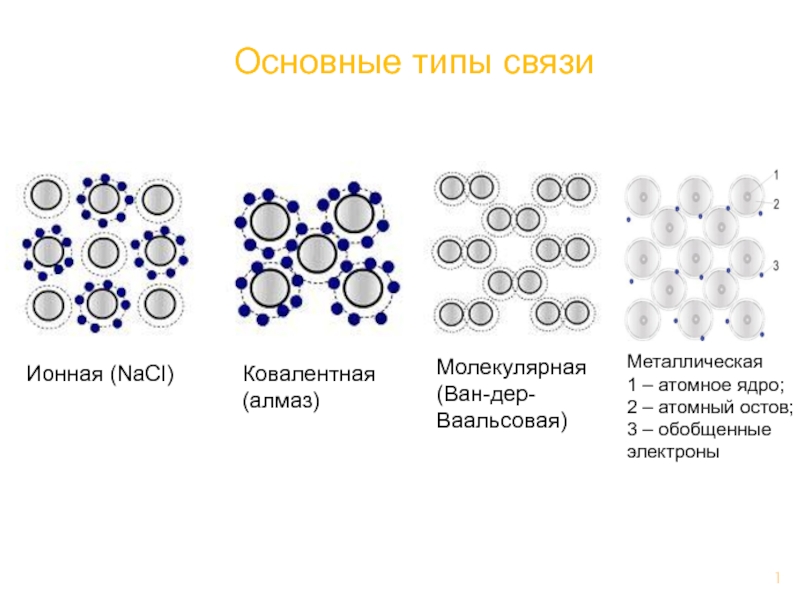
2 – атомный остов;
3 – обобщенные электроны
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Основные типы связи презентация
Содержание
- 1. Основные типы связи
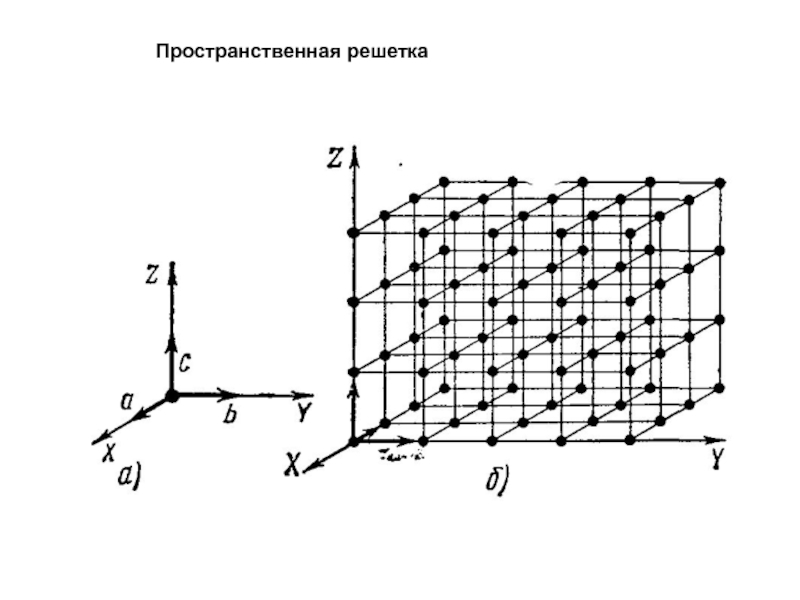
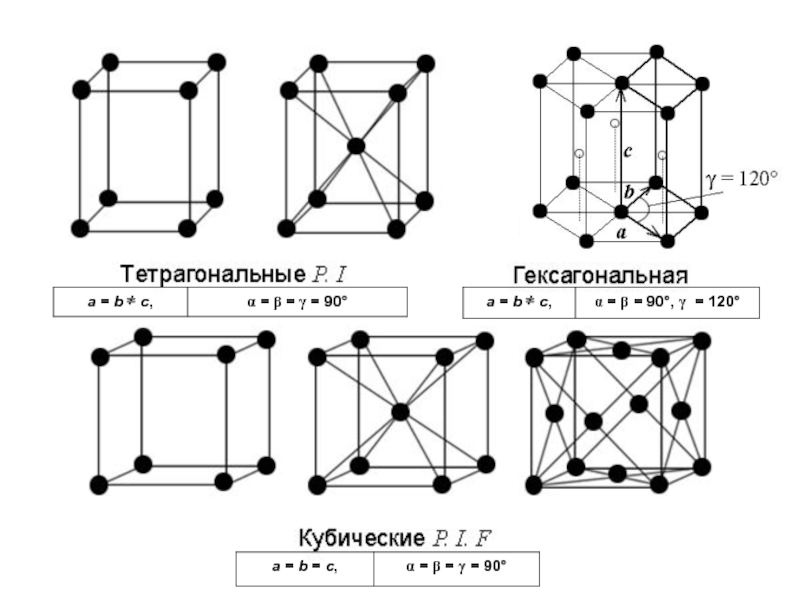
- 2. Пространственная решетка
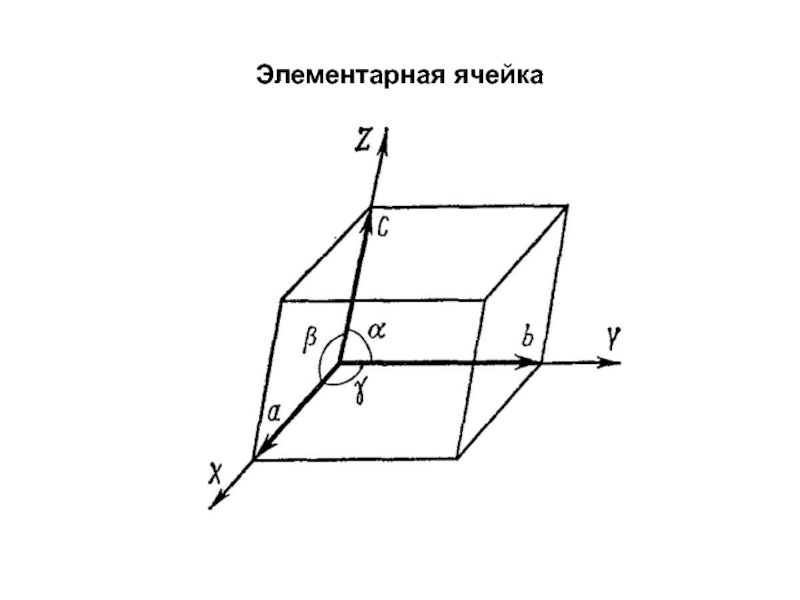
- 3. Элементарная ячейка
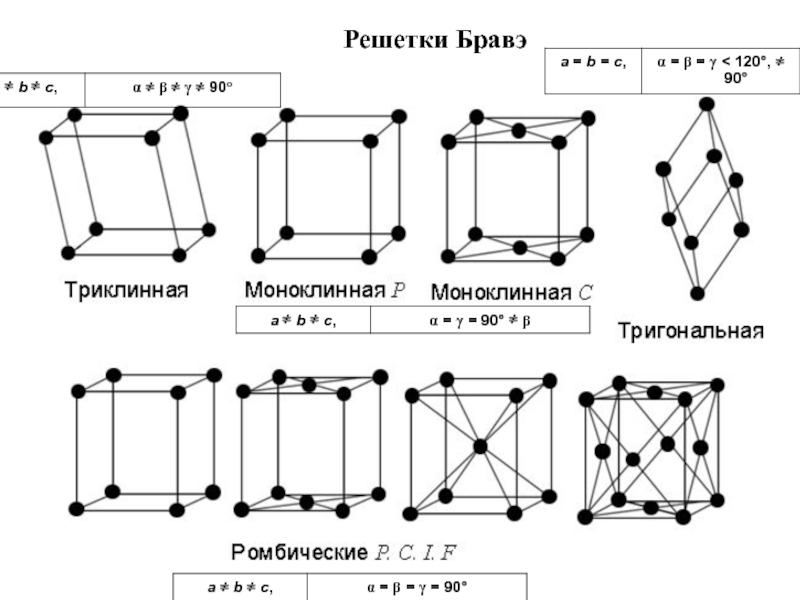
- 4. Решетки Бравэ
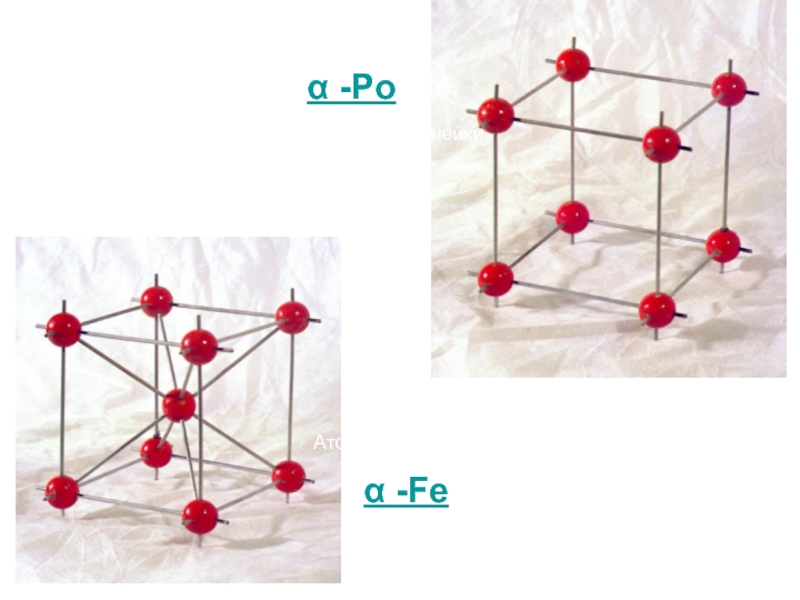
- 6. Атомы в вершинах кубической ячейки α -Po
- 7. Атомы C образуют слои, состоящие из сопряженных
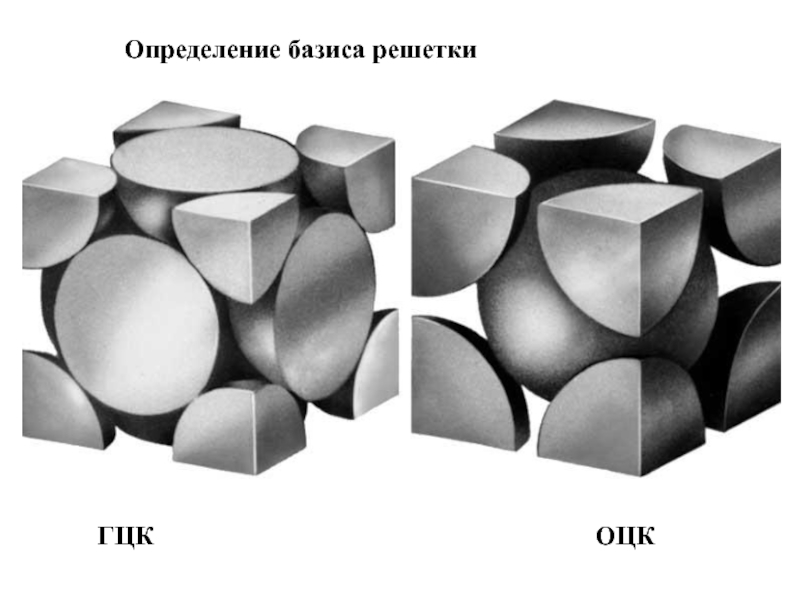
- 8. Определение базиса решетки ГЦК ОЦК
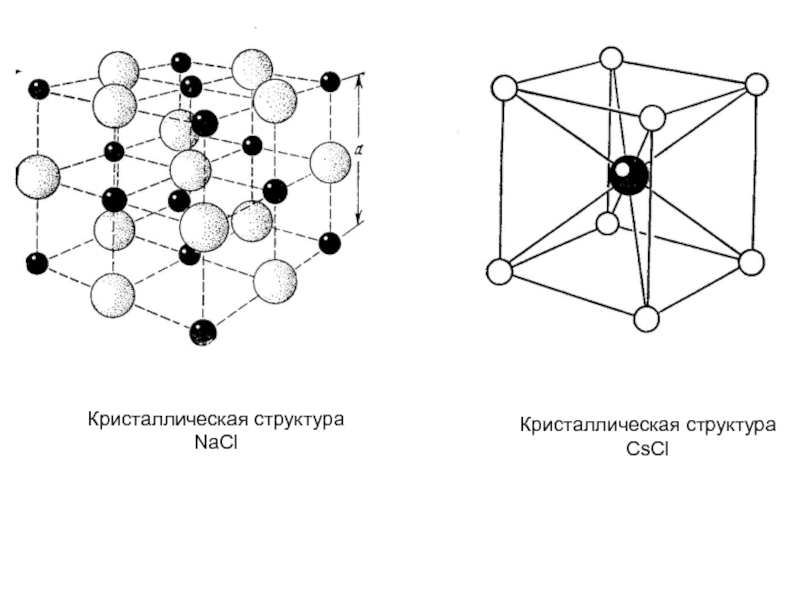
- 9. Кристаллическая структура NaCl Кристаллическая структура CsCl
- 10. Схема координационного числа а – в гранецентрированной
- 11. 1 – вакансия; 2 – межузельный
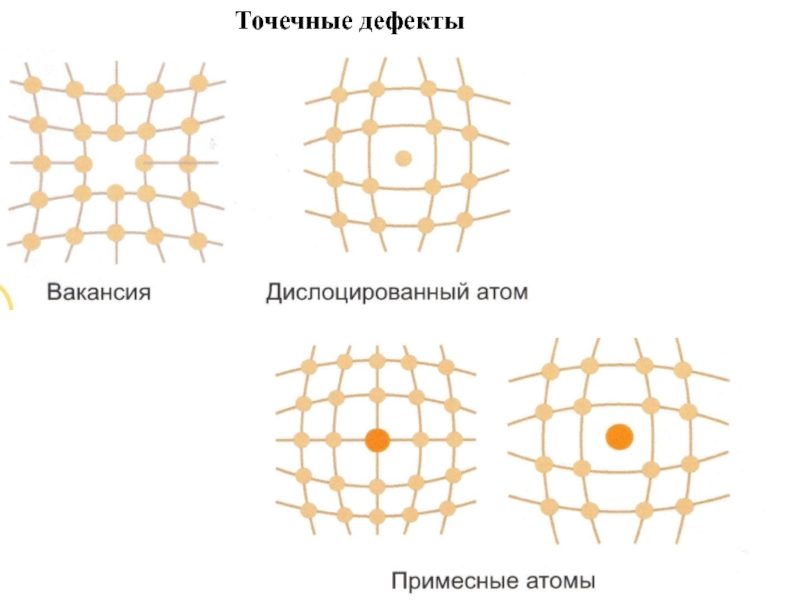
- 12. Точечные дефекты
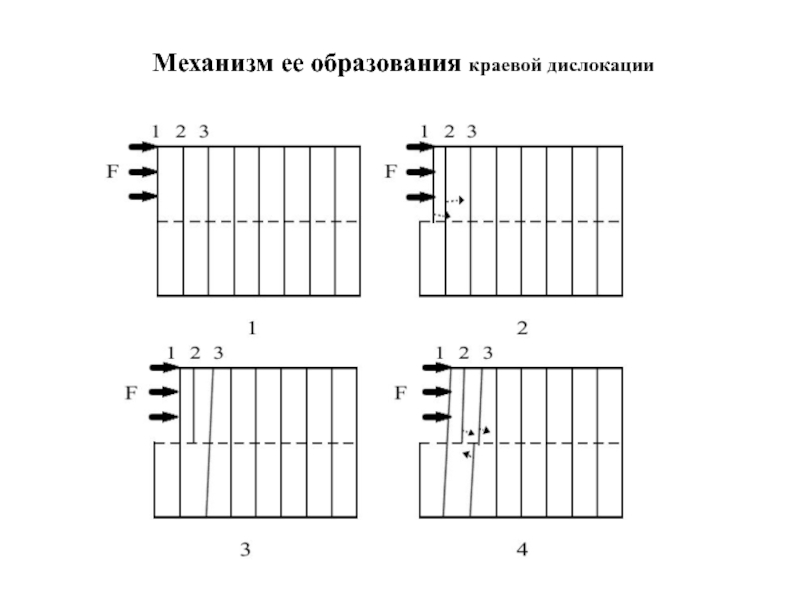
- 13. Механизм ее образования краевой дислокации a б
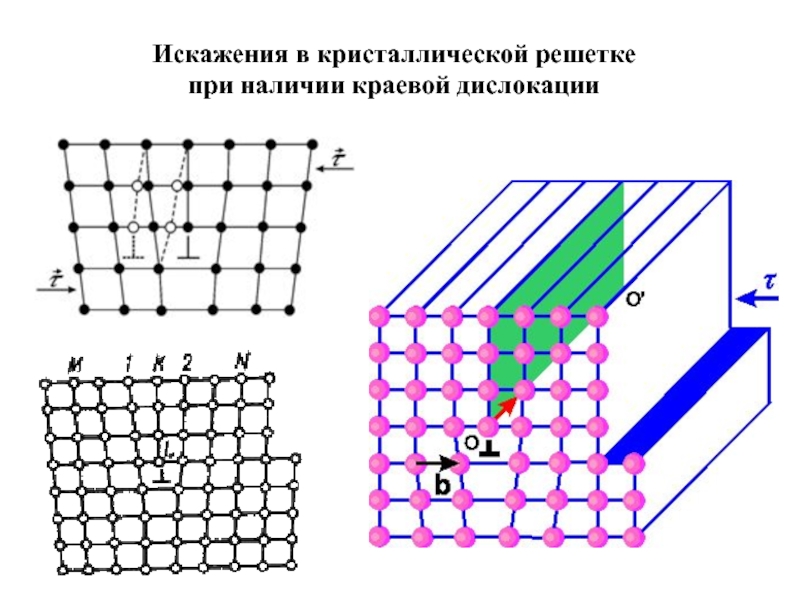
- 14. Искажения в кристаллической решетке при наличии краевой дислокации
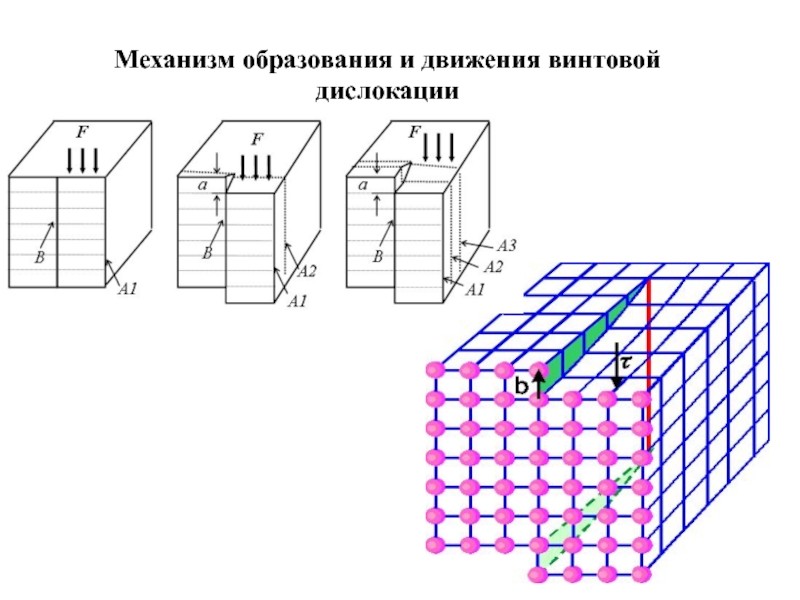
- 15. Механизм образования и движения винтовой дислокации
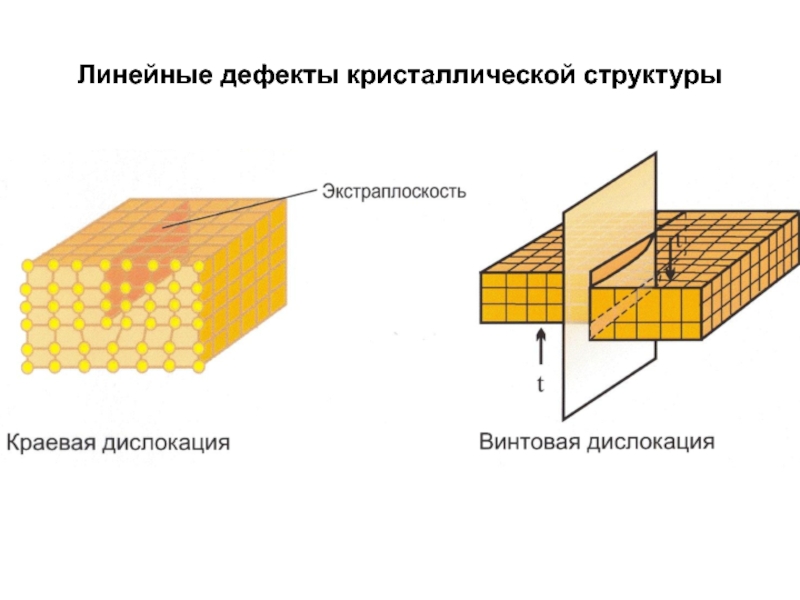
- 16. Линейные дефекты кристаллической структуры
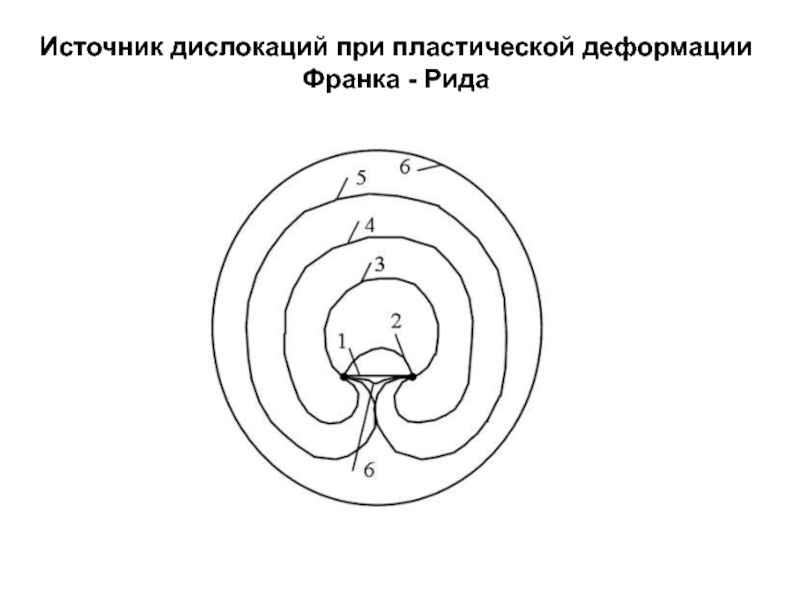
- 18. Источник дислокаций при пластической деформации Франка - Рида
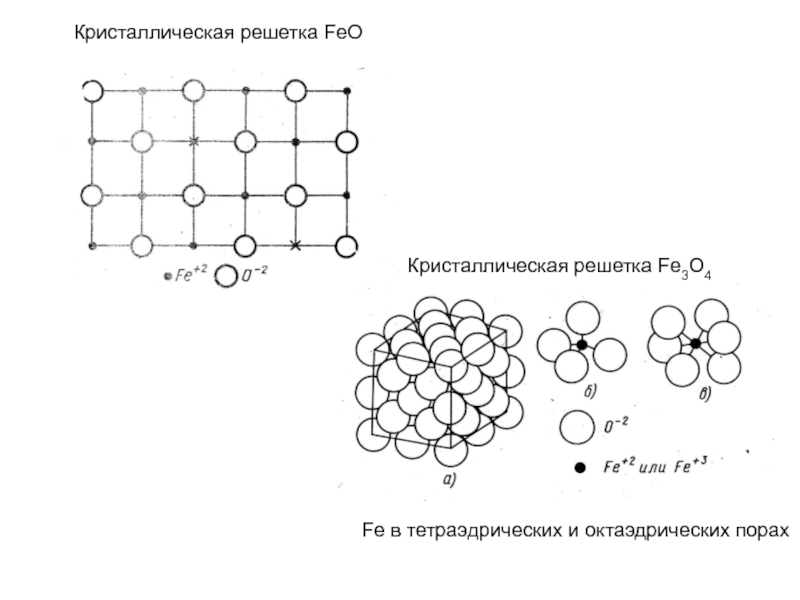
- 19. Кристаллическая решетка FeO Кристаллическая решетка Fe3O4 Fe в тетраэдрических и октаэдрических порах
- 20. (см-2; м-2) Плотность дислокаций Влияние плотности дислокаций на прочность
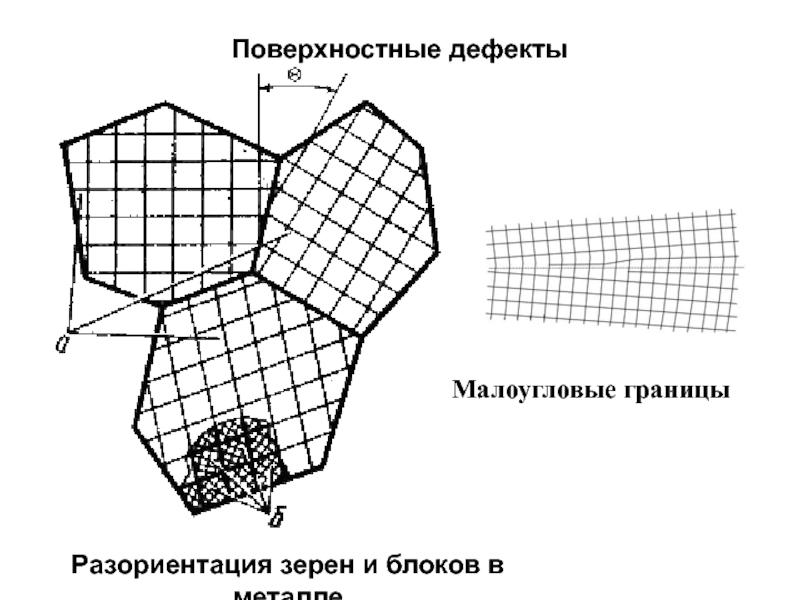
- 21. Разориентация зерен и блоков в металле Поверхностные дефекты Малоугловые границы
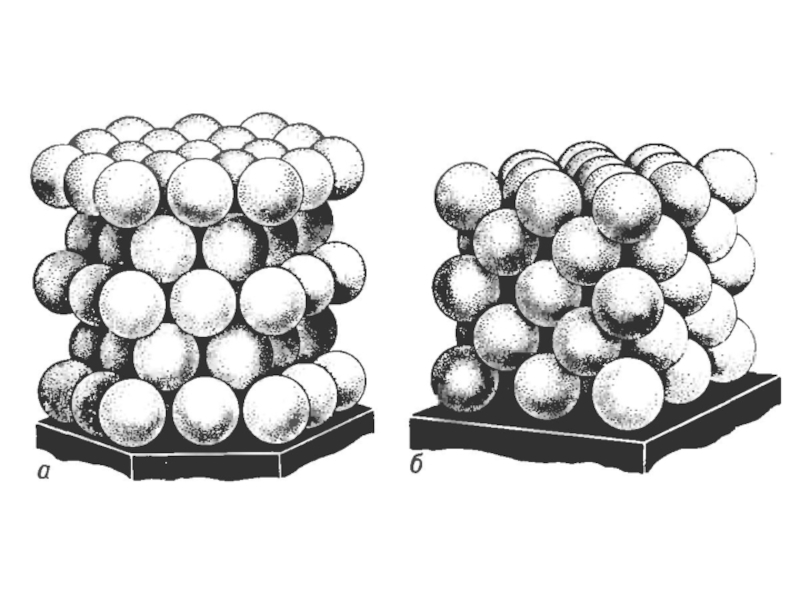
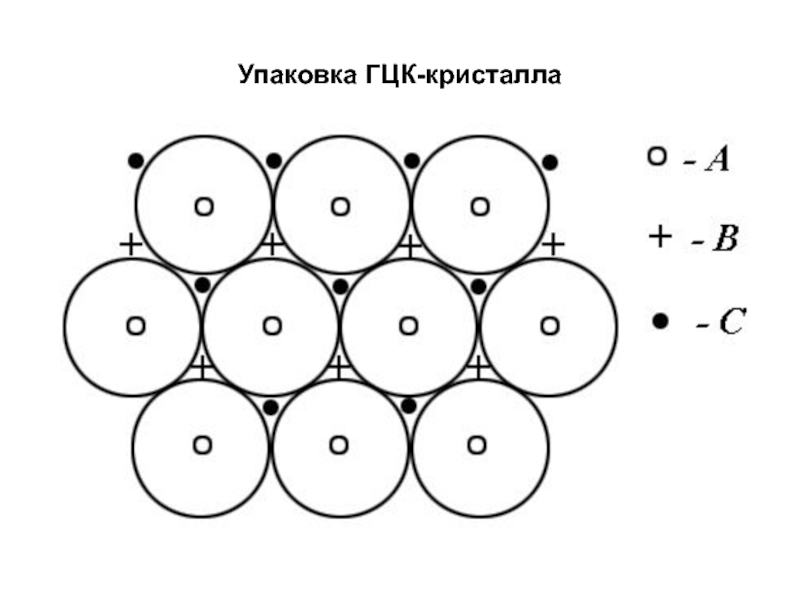
- 23. Упаковка ГЦК-кристалла
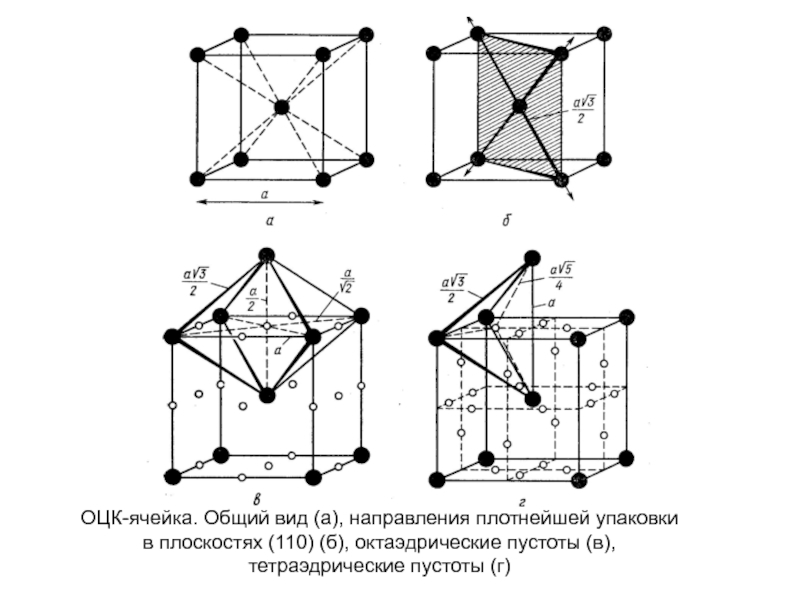
- 24. ОЦК-ячейка. Общий вид (а), направления плотнейшей упаковки
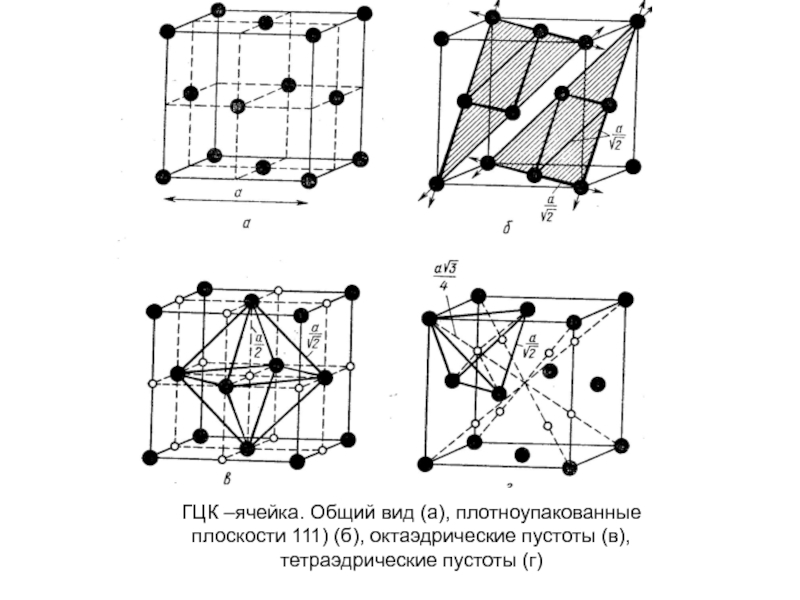
- 25. ГЦК –ячейка. Общий вид (а), плотноупакованные плоскости
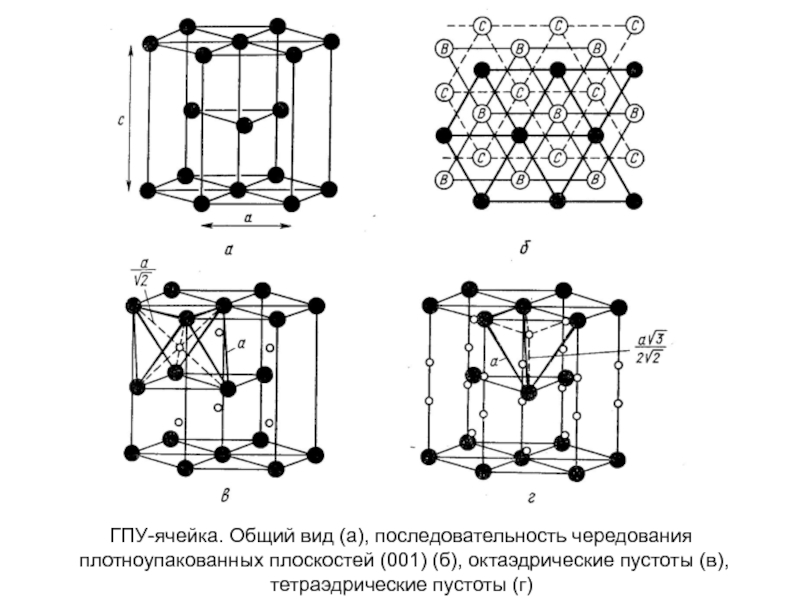
- 26. ГПУ-ячейка. Общий вид (а), последовательность чередования
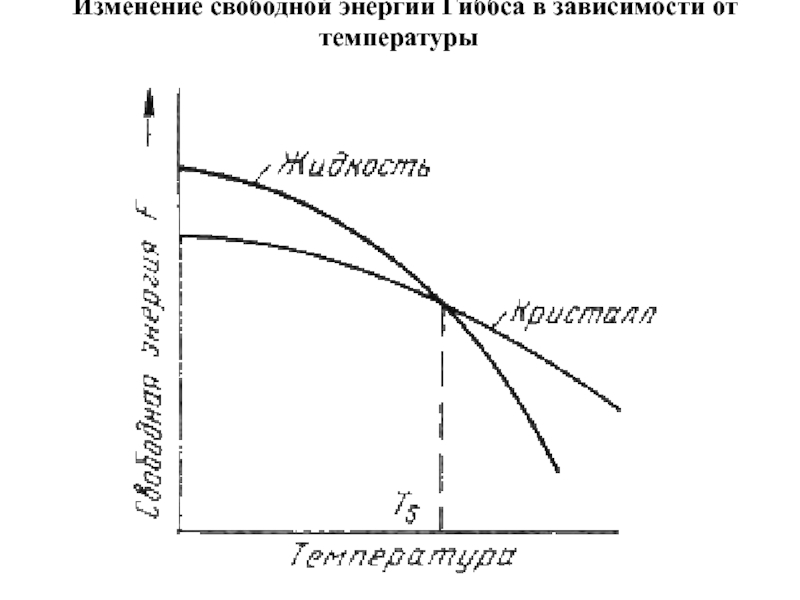
- 27. Изменение свободной энергии Гиббса в зависимости от температуры
- 28. Кривая охлаждения чистого металла
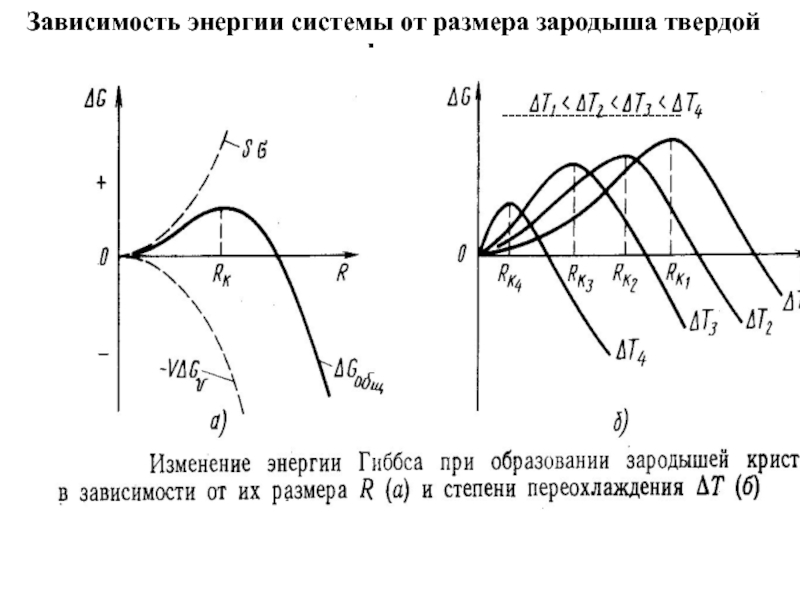
- 29. Зависимость энергии системы от размера зародыша твердой фазы ---------------------------
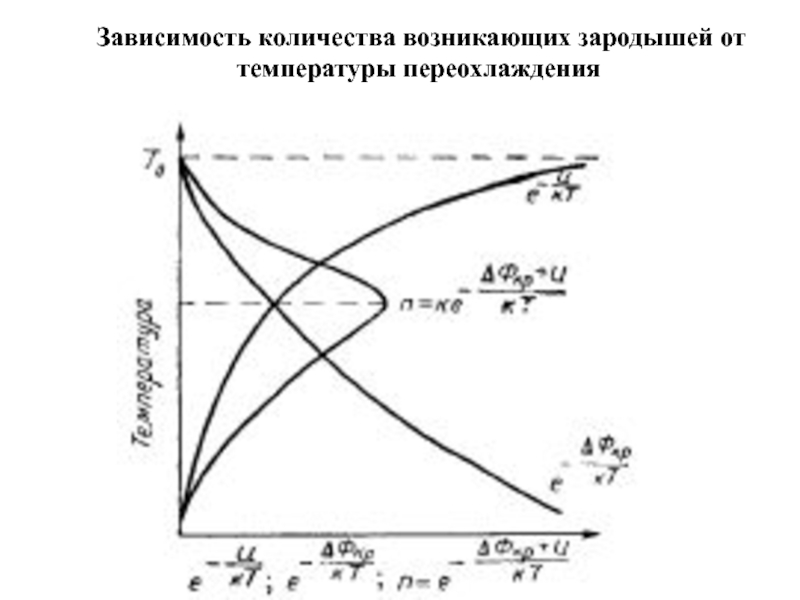
- 30. Зависимость количества возникающих зародышей от температуры переохлаждения
- 31. Зависимость числа центров кристаллизации (а)
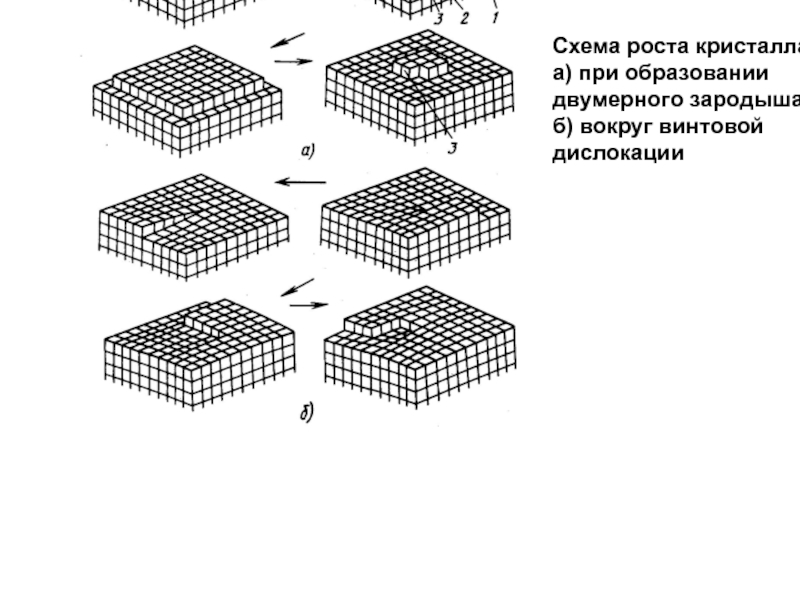
- 32. Схема роста кристалла а) при образовании двумерного зародыша б) вокруг винтовой дислокации
- 33. Зависимость количества закристаллизовавшегося вещества и объемной
- 34. Кинетические кривые кристаллизации металлов в зависимости
- 35. Сводная диаграмма кинетики кристаллизации металлов
- 37. Строение металлического слитка Схема стального слитка, данная
Слайд 1
Основные типы связи
Ионная (NaCl)
Ковалентная (алмаз)
Молекулярная (Ван-дер-Ваальсовая)
Металлическая
1 –
Слайд 7Атомы C образуют слои, состоящие из сопряженных правильных шестиугольников. Слои налагаются
по закону ...ABABAB...; слой B сдвинут относительно слоя A на величину вектора, равного связи C–C.
Отношение параметров c/a = 2,72.
Отношение параметров c/a = 2,72.
αα-графит
Алмаз
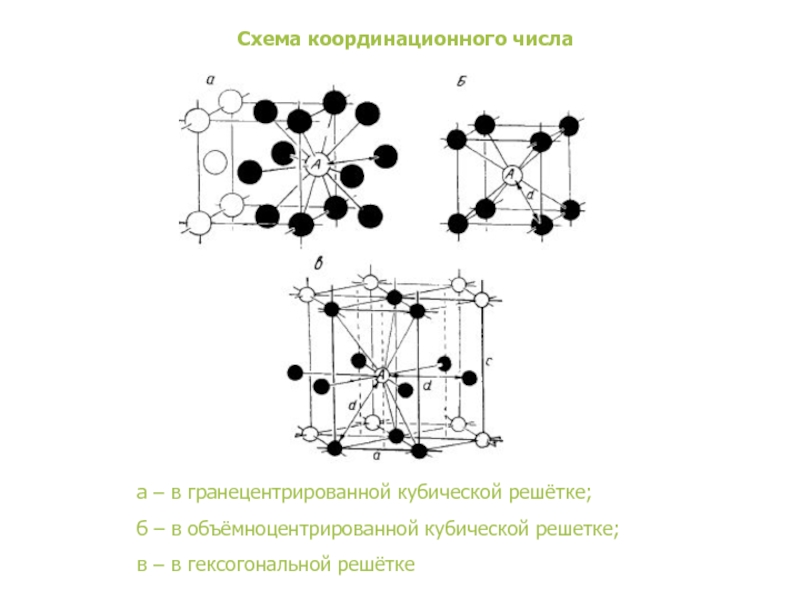
Слайд 10Схема координационного числа
а – в гранецентрированной кубической решётке;
б – в
объёмноцентрированной кубической решетке;
в – в гексогональной решётке
в – в гексогональной решётке
Слайд 11
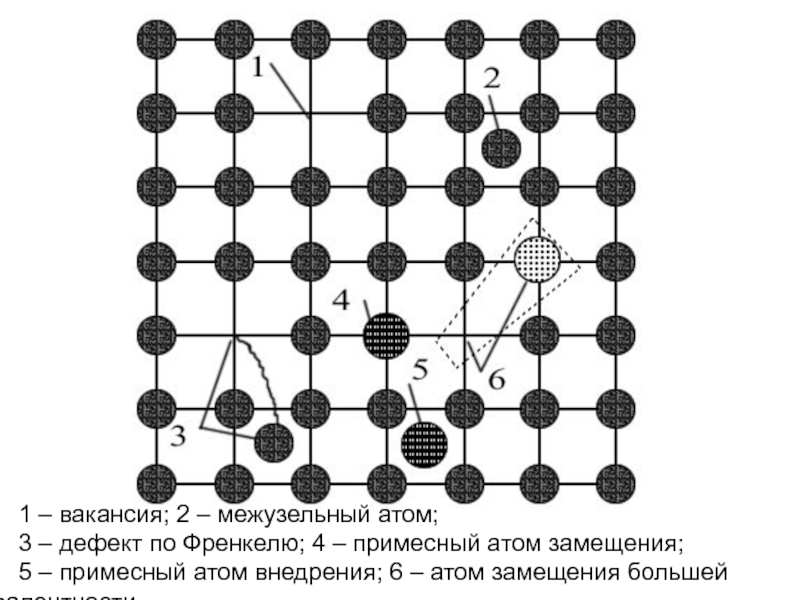
1 – вакансия; 2 – межузельный атом;
3 – дефект по Френкелю;
4 – примесный атом замещения;
5 – примесный атом внедрения; 6 – атом замещения большей валентности
5 – примесный атом внедрения; 6 – атом замещения большей валентности
Слайд 19Кристаллическая решетка FeO
Кристаллическая решетка Fe3O4
Fe в тетраэдрических и октаэдрических порах
Слайд 24ОЦК-ячейка. Общий вид (а), направления плотнейшей упаковки
в плоскостях (110) (б), октаэдрические
пустоты (в),
тетраэдрические пустоты (г)
тетраэдрические пустоты (г)
Слайд 25ГЦК –ячейка. Общий вид (а), плотноупакованные
плоскости 111) (б), октаэдрические пустоты (в),
тетраэдрические
пустоты (г)
Слайд 26ГПУ-ячейка. Общий вид (а), последовательность чередования
плотноупакованных плоскостей (001) (б), октаэдрические
пустоты (в),
тетраэдрические пустоты (г)
тетраэдрические пустоты (г)
Слайд 28
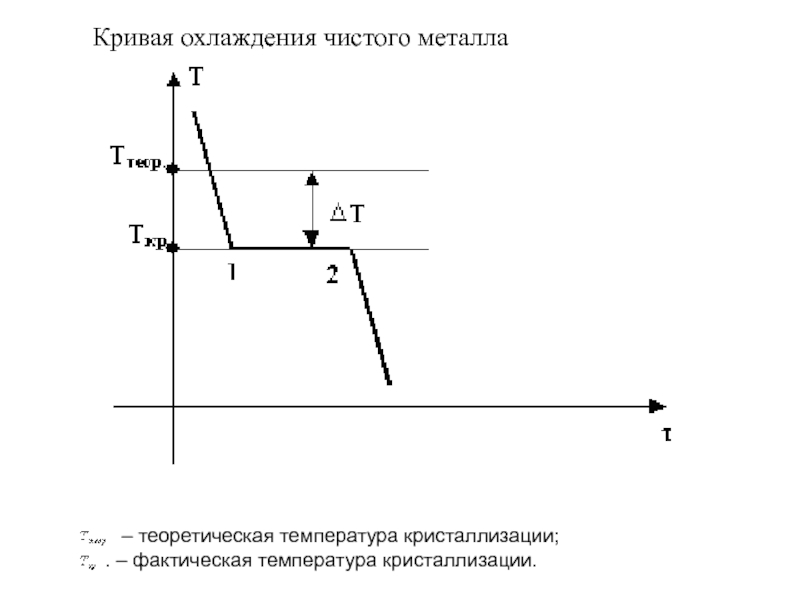
Кривая охлаждения чистого металла
– теоретическая температура кристаллизации;
. –
фактическая температура кристаллизации.
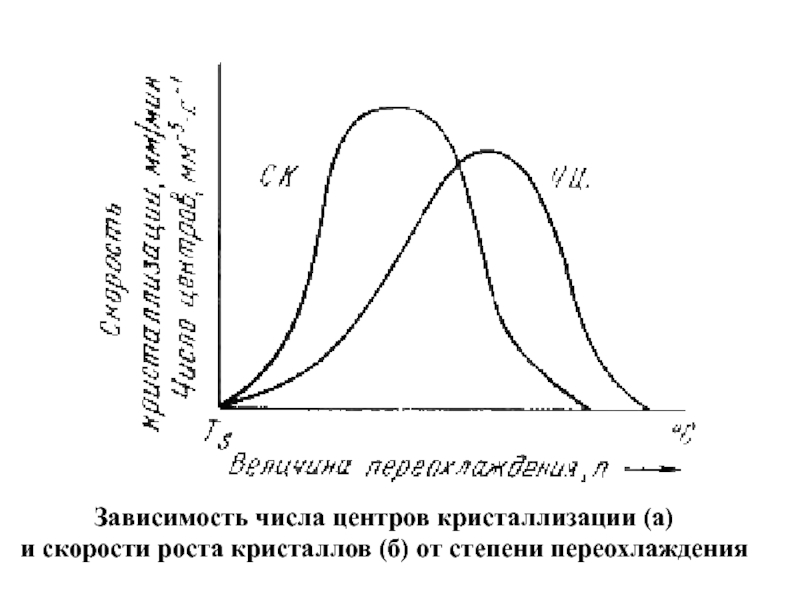
Слайд 31
Зависимость числа центров кристаллизации (а)
и скорости роста кристаллов (б)
от степени переохлаждения
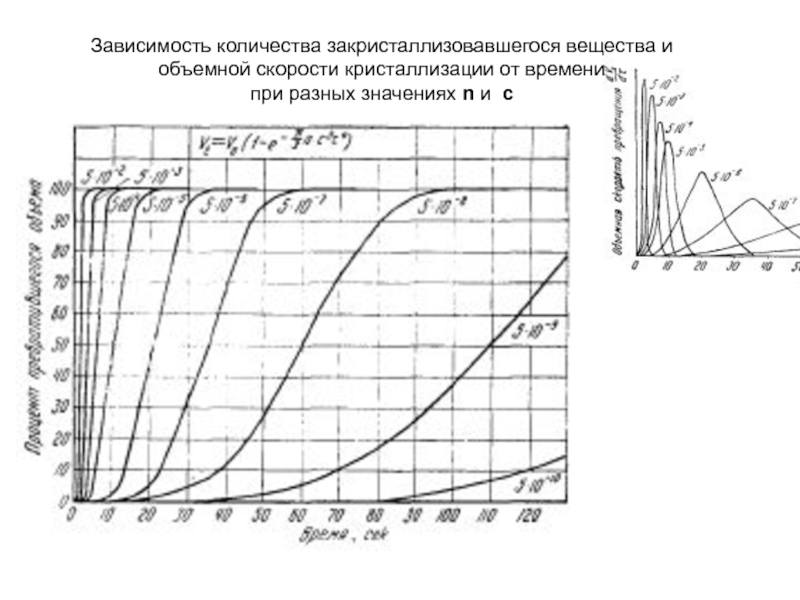
Слайд 33Зависимость количества закристаллизовавшегося вещества и
объемной скорости кристаллизации от времени
при
разных значениях n и c
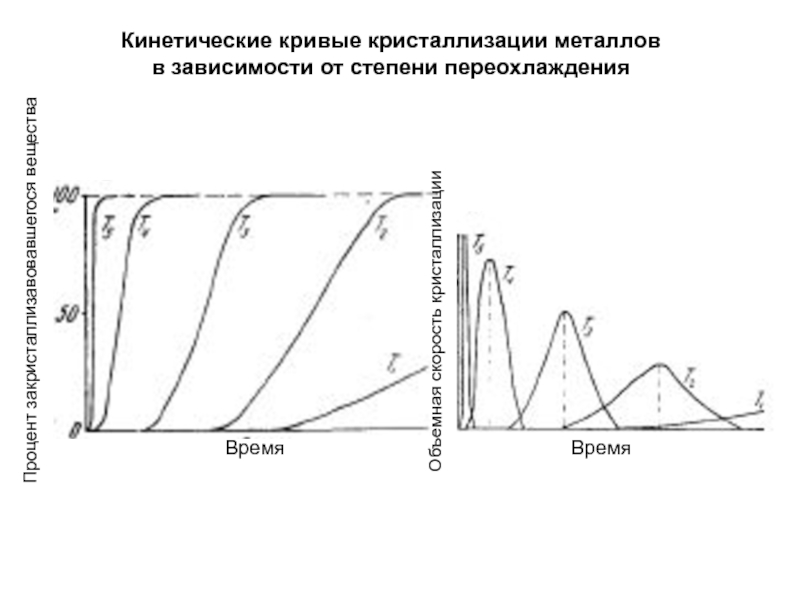
Слайд 34Кинетические кривые кристаллизации металлов
в зависимости от степени переохлаждения
Процент закристаллизавовавшегося вещества
Время
Время
Объемная
скорость кристаллизации
Слайд 37Строение металлического слитка
Схема стального слитка, данная Черновым Д.К., представлена на рис.3.7.
Слиток
состоит из трех зон:
1. мелкокристаллическая корковая зона;
2. зона столбчатых кристаллов;
3. внутренняя зона крупных равноосных кристаллов.
Кристаллизация корковой зоны идет в условиях максимального переохлаждения. Скорость кристаллизации определяется большим числом центров кристаллизации. Образуется мелкозернистая структура.
Жидкий металл под корковой зоной находится в условиях меньшего переохлаждения. Число центров ограничено и процесс кристаллизации реализуется за счет их интенсивного роста до большого размера.
1. мелкокристаллическая корковая зона;
2. зона столбчатых кристаллов;
3. внутренняя зона крупных равноосных кристаллов.
Кристаллизация корковой зоны идет в условиях максимального переохлаждения. Скорость кристаллизации определяется большим числом центров кристаллизации. Образуется мелкозернистая структура.
Жидкий металл под корковой зоной находится в условиях меньшего переохлаждения. Число центров ограничено и процесс кристаллизации реализуется за счет их интенсивного роста до большого размера.