- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Основные классы неорганических соединений презентация
Содержание
- 1. Основные классы неорганических соединений
- 2. Выберите класс неорганических соединений нажатием левой
- 3. ОКСИДЫ Для выбора следующего класса неорганических
- 4. ОСНОВАНИЯ Для выбора следующего класса неорганических
- 5. КИСЛОТЫ Для выбора следующего класса неорганических
- 6. СОЛИ Для выбора следующего класса неорганических
- 7. Э+n O-2 Оксиды это сложные вещества,
- 8. Ме+n (OH)n Oснования - это сложные
- 9. Кислоты это сложные вещества, которые состоят
- 10. Соли это сложные вещества, молекулы которых
- 11. Классификация оксидов Оксиды Ковалентные
- 12. Классификация оснований ОСНОВАНИЯ Одноосновные NaОН,
- 13. Классификация кислот КИСЛОТЫ Одноосновные
- 14. Классификация солей по составу СОЛИ Кислые NaHCO3
- 15. ПОЛУЧЕНИЕ ОКСИДОВ Взаимодействие простых веществ с кислородом
- 16. ПОЛУЧЕНИЕ ОСНОВАНИЙ Взаимодействие активных металлов с
- 17. ПОЛУЧЕНИЕ КИСЛОТ Взаимодействие кислотных оксидов
- 18. ПОЛУЧЕНИЕ СОЛЕЙ Взаимодействием: Металла с
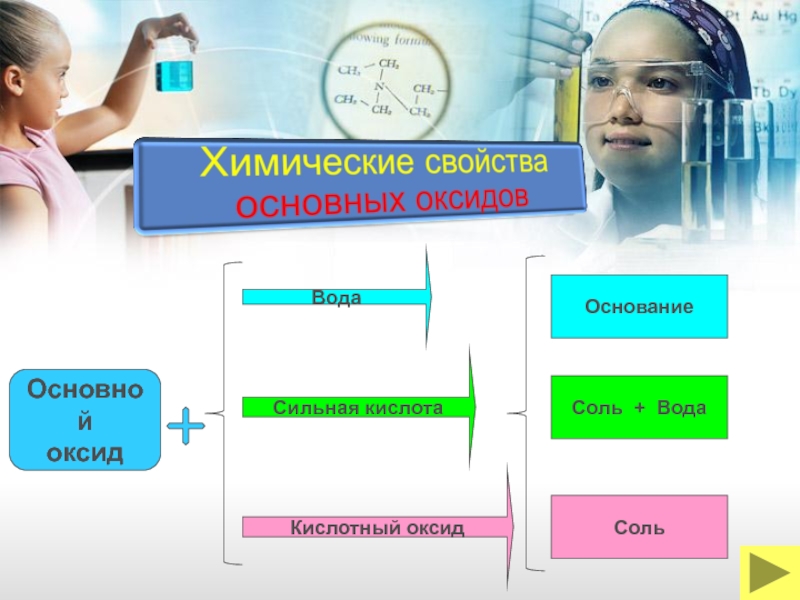
- 19. Вода Основной оксид Сильная кислота
- 20. Вода Кислотный оксид Щелочь
- 22. Кислота Основания Растворимая соль Кислотный
- 23. Основание Кислота (кроме HNO3)
- 24. ТБ при работе с кислотами Запомни правило:
- 25. Щелочь Соль Кислота Металл
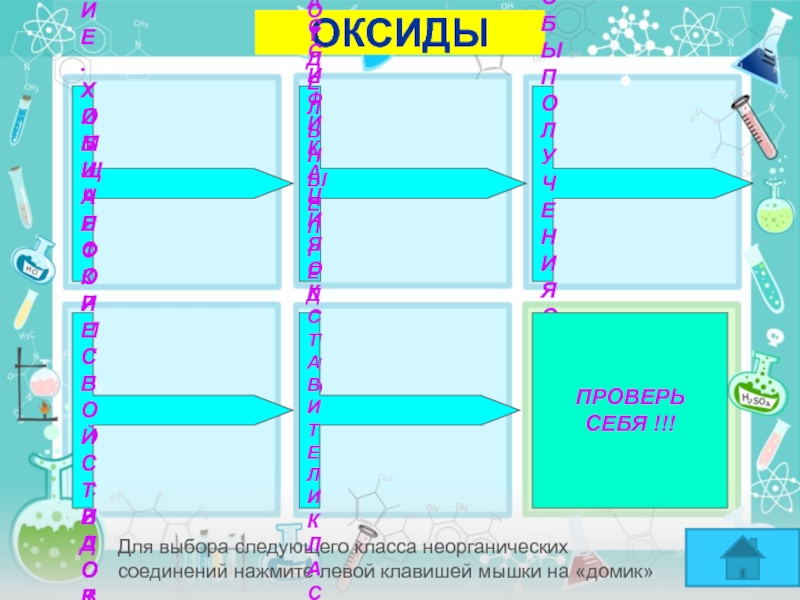
- 26. Названия отдельных представителей класса оксидов
Слайд 1Учебное пособие
для 8-9 классов
«ОСНОВНЫЕ КЛАССЫ
НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ»
Автор: Винюков А.В.
Преподаватель Химии
МОУДД ЦДОДД «Импульс»
г. Черноголовка
Слайд 2Выберите класс неорганических соединений
нажатием левой клавиши мыши. Дополнительные сведения по
Основные классы неорганических соединений
ОКСИДЫ
ОСНОВАНИЯ
КИСЛОТЫ
СОЛИ
Приложения
Слайд 3ОКСИДЫ
Для выбора следующего класса неорганических соединений нажмите левой клавишей мышки на
ОПРЕДЕЛЕНИЕ.
ОБЩАЯ
ФОРМУЛА
ОКСИДОВ
КЛАССИФИКАЦИЯ
ОКСИДОВ
СПОСОБЫ
ПОЛУЧЕНИЯ
ОКСИДОВ
ХИМИЧЕСКИЕ
СВОЙСТВА
ОКСИДОВ
ОТДЕЛЬНЫЕ
ПРЕДСТАВИТЕЛИ
КЛАССА
ОКСИДОВ
ПРОВЕРЬ
СЕБЯ !!!
Слайд 4ОСНОВАНИЯ
Для выбора следующего класса неорганических соединений нажмите левой клавишей мышки на
ОПРЕДЕЛЕНИЕ.
ОБЩАЯ
ФОРМУЛА
ОСНОВАНИЙ
КЛАССИФИКАЦИЯ
ОСНОВАНИЙ
СПОСОБЫ
ПОЛУЧЕНИЯ
ОСНОВАНИЙ
ХИМИЧЕСКИЕ
СВОЙСТВА
ОСНОВАНИЙ
ОТДЕЛЬНЫЕ
ПРЕДСТАВИТЕЛИ
КЛАССА
ОСНОВАНИЙ
ПРОВЕРЬ
СЕБЯ !!!
Слайд 5КИСЛОТЫ
Для выбора следующего класса неорганических соединений нажмите левой клавишей мышки на
ОПРЕДЕЛЕНИЕ.
ОБЩАЯ
ФОРМУЛА
КИСЛОТ
КЛАССИФИКАЦИЯ
КИСЛОТ
СПОСОБЫ
ПОЛУЧЕНИЯ
КИСЛОТ
ХИМИЧЕСКИЕ
СВОЙСТВА
КИСЛОТ
ОТДЕЛЬНЫЕ
ПРЕДСТАВИТЕЛИ
КЛАССА
КИСЛОТ
ПРОВЕРЬ
СЕБЯ !!!
Слайд 6СОЛИ
Для выбора следующего класса неорганических соединений нажмите левой клавишей мышки на
ОПРЕДЕЛЕНИЕ.
ОБЩАЯ
ФОРМУЛА
СОЛЕЙ
КЛАССИФИКАЦИЯ
СОЛЕЙ
СПОСОБЫ
ПОЛУЧЕНИЯ
СОЛЕЙ
ХИМИЧЕСКИЕ
СВОЙСТВА
СОЛЕЙ
ОТДЕЛЬНЫЕ
ПРЕДСТАВИТЕЛИ
КЛАССА
СОЛЕЙ
ПРОВЕРЬ
СЕБЯ !!!
Слайд 7Э+n
O-2
Оксиды
это сложные вещества,
состоящие из двух элементов,
один из которых
n = валентность элемента
Слайд 8Ме+n
(OH)n
Oснования
- это сложные вещества, состоящие из атомов металлов и гидроксильных
n = валентность металла
Слайд 9Кислоты
это сложные вещества, которые состоят из атомов водорода и кислотного
Н+ Кост-n
Значение n смотри в таблице растворимости
Слайд 10Соли
это сложные вещества, молекулы которых состоят из атомов металла и
Ме+m Кост-n
m – валентность металла
Значение n смотри в таблице растворимости
NaCl
CaCO3
NaHCO3
Слайд 11
Классификация оксидов
Оксиды
Ковалентные
SO2
Ионные
Na2O
Смешанные
Fe3O4=FeO·Fe2O3
Пероксиды
Na2O2
Нормальные
MgO, SO3
2. Несолеобразующие СО, NO, N2O
c) Основные
CaO
a)
Аl2O3 ZnO
b) Кислотные
SO3
по типу химической связи
по кислотно-основным свойствам
по составу
Соле-
образующие
Слайд 12
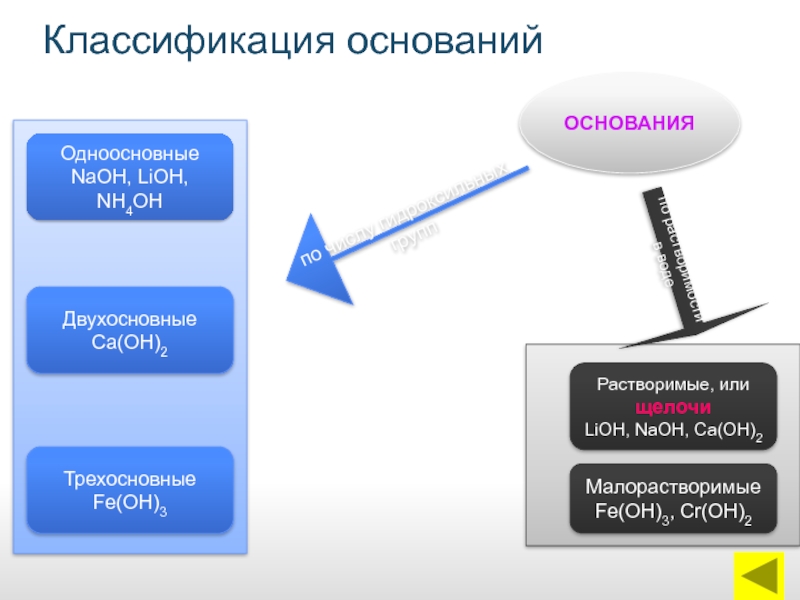
Классификация оснований
ОСНОВАНИЯ
Одноосновные
NaОН, LiОН, NН4ОН
Двухосновные
Са(ОН)2
Трехосновные
Fe(ОН)3
Растворимые, или щелочи
LiОН, NаОН, Са(ОН)2
Малорастворимые
Fe(ОН)3, Сr(ОН)2
по числу гидроксильных
по растворимости в воде
Слайд 13
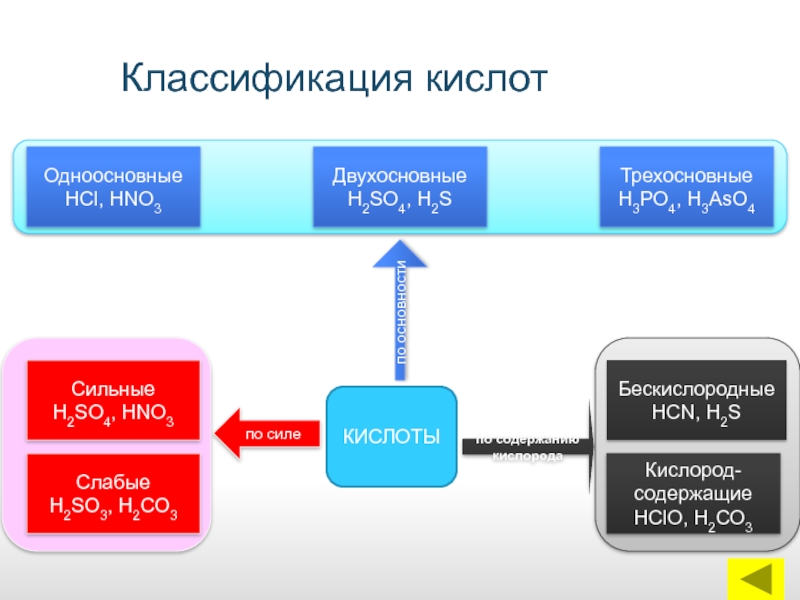
Классификация кислот
КИСЛОТЫ
Одноосновные
НСl, НNО3
Сильные
Н2SO4, НNО3
Слабые
Н2SО3, Н2СО3
Кислород-содержащие
НСlО, Н2СО3
Бескислородные
НСN, Н2S
Трехосновные
Н3РО4, Н3АsО4
Двухосновные
Н2SO4, Н2S
по основности
по
по содержанию кислорода
Слайд 14Классификация солей по составу
СОЛИ
Кислые
NaHCO3
Смешанные
CaClBr
Двойные
KNaSO4
Средние
BaSO4
Основные
Al(OH)2Cl
Комплексные
[Ag(NH3)2]Cl
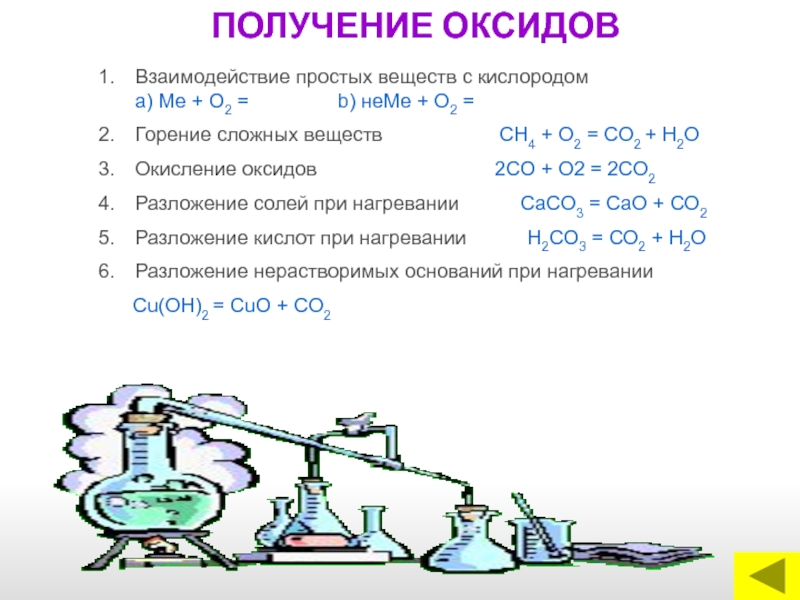
Слайд 15ПОЛУЧЕНИЕ ОКСИДОВ
Взаимодействие простых веществ с кислородом
Горение сложных веществ СН4 + О2 = СО2 + Н2О
Окисление оксидов 2СО + О2 = 2СО2
Разложение солей при нагревании СаСО3 = СаО + СО2
Разложение кислот при нагревании Н2СО3 = СО2 + Н2О
Разложение нерастворимых оснований при нагревании
Сu(ОН)2 = СuО + СО2
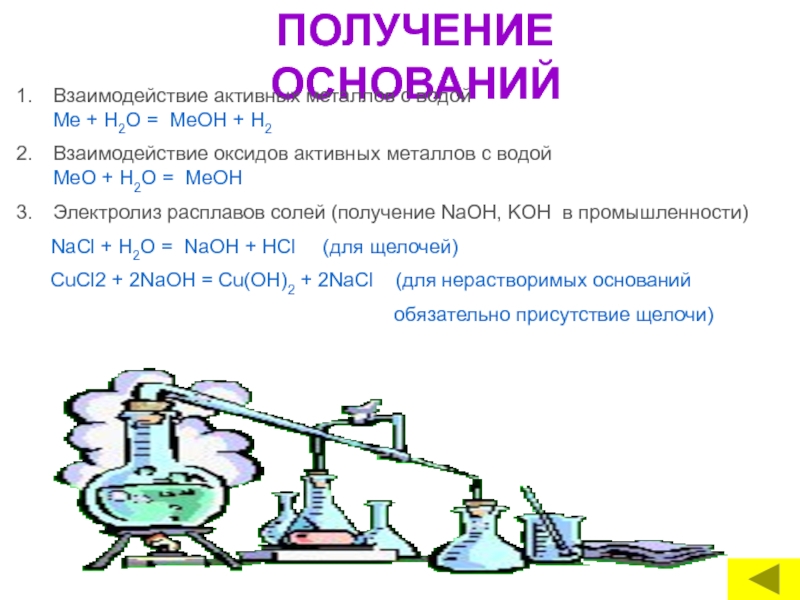
Слайд 16ПОЛУЧЕНИЕ ОСНОВАНИЙ
Взаимодействие активных металлов с водой
Взаимодействие оксидов активных металлов с водой MeО + Н2O = МеОН
Электролиз расплавов солей (получение NaOH, KOH в промышленности)
NaCl + H2O = NaОН + HСl (для щелочей)
CuCl2 + 2NaOH = Cu(OH)2 + 2NaCl (для нерастворимых оснований
обязательно присутствие щелочи)
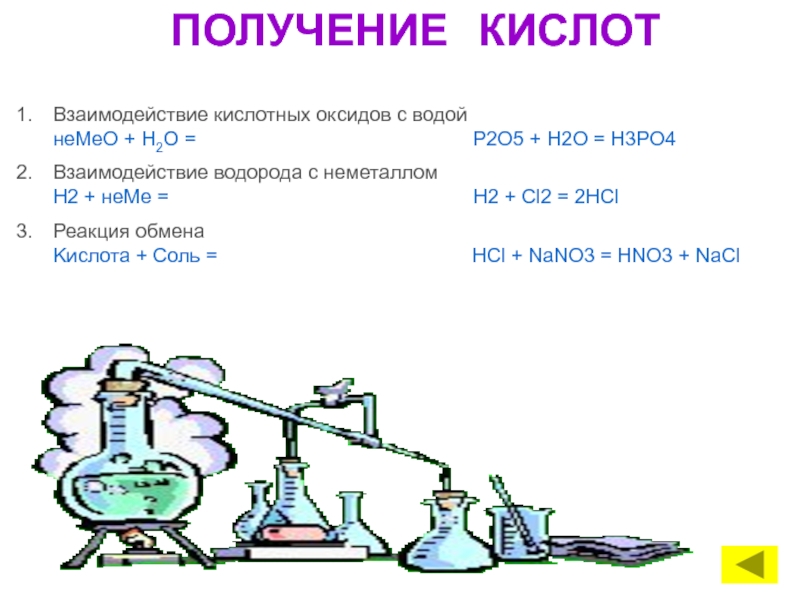
Слайд 17ПОЛУЧЕНИЕ КИСЛОТ
Взаимодействие кислотных оксидов с водой
Взаимодействие водорода с неметаллом Н2 + неМе = Н2 + Сl2 = 2HCl
Реакция обмена Kислота + Cоль = HCl + NaNO3 = HNO3 + NaCl
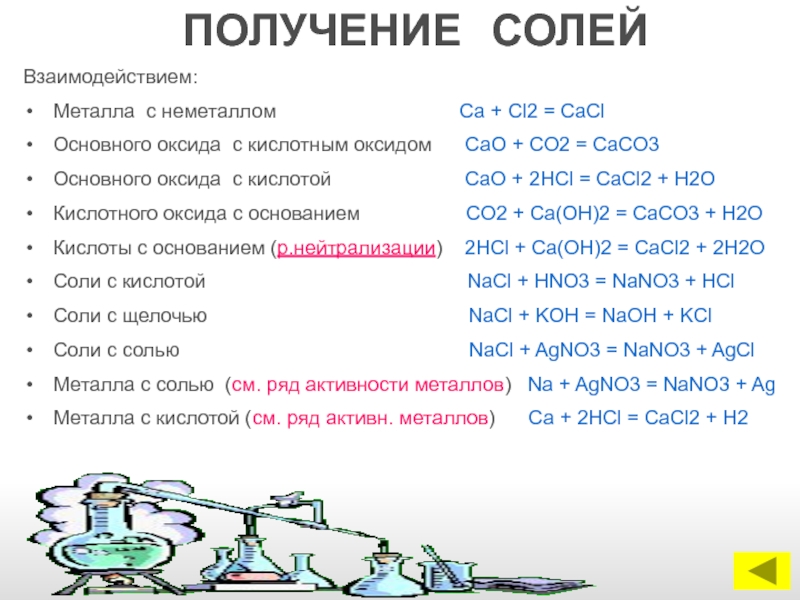
Слайд 18ПОЛУЧЕНИЕ СОЛЕЙ
Взаимодействием:
Металла с неметаллом
Основного оксида с кислотным оксидом СаО + СО2 = СаСО3
Основного оксида с кислотой СаО + 2НСl = CaCl2 + H2О
Кислотного оксида с основанием CO2 + Ca(OH)2 = CaCO3 + H2O
Кислоты с основанием (р.нейтрализации) 2HCl + Ca(OH)2 = CaCl2 + 2H2O
Соли с кислотой NaCl + HNO3 = NaNO3 + HCl
Соли с щелочью NaCl + KOH = NaOH + KCl
Соли с солью NaCl + AgNO3 = NaNO3 + AgCl
Металла с солью (см. ряд активности металлов) Na + AgNO3 = NaNO3 + Ag
Металла с кислотой (см. ряд активн. металлов) Са + 2НСl = CaCl2 + H2
Слайд 22
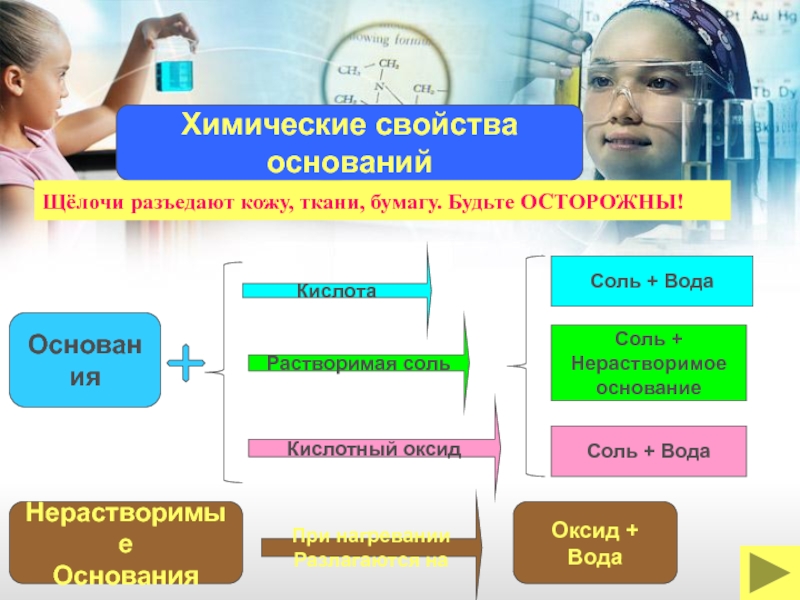
Кислота
Основания
Растворимая соль
Кислотный оксид
Соль + Вода
Соль +
Нерастворимое
основание
Соль + Вода
Химические
оснований
Нерастворимые
Основания
При нагревании
Разлагаются на
Оксид + Вода
Щёлочи разъедают кожу, ткани, бумагу. Будьте ОСТОРОЖНЫ!
Слайд 23
Основание
Кислота
(кроме HNO3)
Металлы от Mg до Pb
Основной оксид
Соль + Вода
Соль
Соль + Вода
Химические свойства
кислот
Соли (карбонаты,
сульфиты )
Новая соль +
Вода + Газ
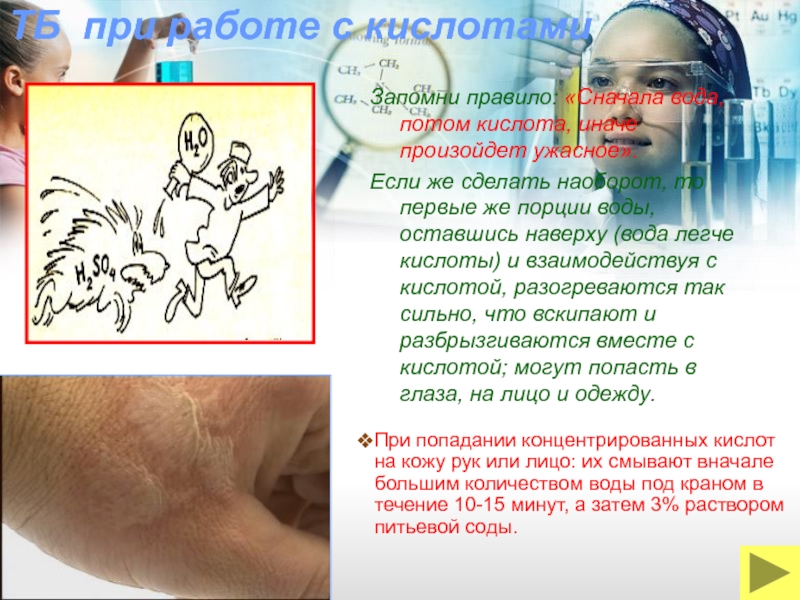
Слайд 24ТБ при работе с кислотами
Запомни правило: «Сначала вода, потом кислота, иначе
Если же сделать наоборот, то первые же порции воды, оставшись наверху (вода легче кислоты) и взаимодействуя с кислотой, разогреваются так сильно, что вскипают и разбрызгиваются вместе с кислотой; могут попасть в глаза, на лицо и одежду.
При попадании концентрированных кислот на кожу рук или лицо: их смывают вначале большим количеством воды под краном в течение 10-15 минут, а затем 3% раствором питьевой соды.
Слайд 25
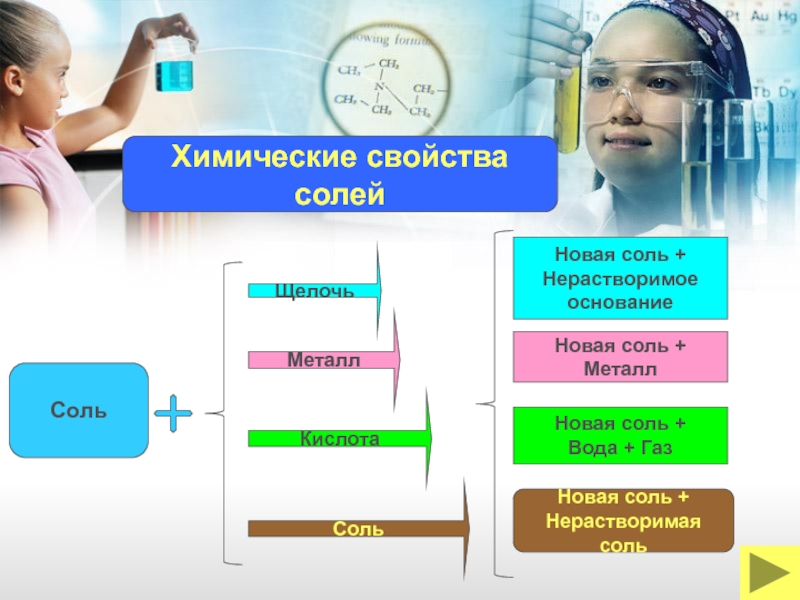
Щелочь
Соль
Кислота
Металл
Новая соль +
Нерастворимое
основание
Новая соль +
Вода +
Новая соль +
Металл
Химические свойства
солей
Соль
Новая соль +
Нерастворимая соль







![Классификация солей по составуСОЛИКислыеNaHCO3СмешанныеCaClBrДвойныеKNaSO4СредниеBaSO4ОсновныеAl(OH)2ClКомплексные[Ag(NH3)2]Cl](/img/tmb/6/512456/c9b58f2a67d37575f5b8f04f05179015-800x.jpg)