оснований.
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Основания. Состав оснований презентация
Содержание
- 1. Основания. Состав оснований
- 2. Основания – это сложные вещества, состоящие из атома металла и одной или нескольких гидроксогрупп.
- 3. Состав оснований: Назовите составные части оснований. Ме(ОН)х
- 4. Выберите формулы оснований. Назовите их.
- 5. Основания NaOH – гидроксид натрия Ca(OH)2 –
- 6. Классификация оснований NaOH KOH Ba(OH)2
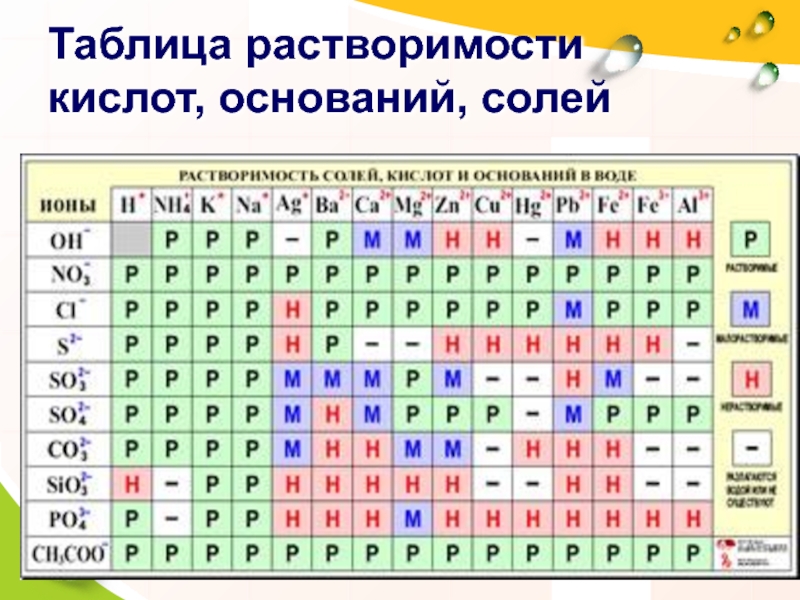
- 7. Таблица растворимости кислот, оснований, солей
- 9. По какому признаку основания разделены на группы?
- 10. Однокислотные NaOH, KOH
- 11. Физические свойства оснований Агрегатное состояние: Все твердые
- 12. Химические свойства нерастворимых оснований. 1). Разлагаются
- 13. Химические свойства щелочей. 1). Изменяют окраску
- 14. ПРАВИЛА БЕЗОПАСНОСТИ Едкое вещество—щелочь! Разрушает и раздражает
- 15. 1). Щелочи изменяют окраску
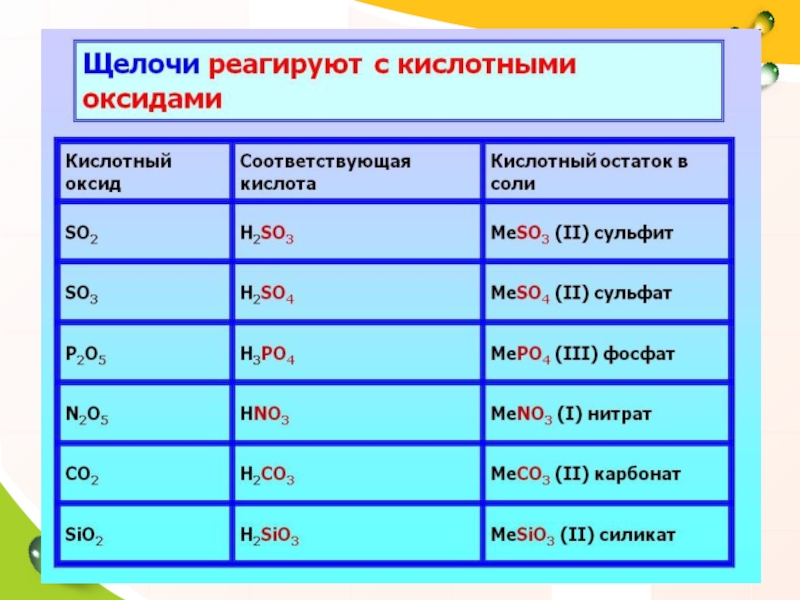
- 16. Щелочь + кислота :
Слайд 1План изучения темы:
Состав, названия и определение оснований.
Классификация оснований.
Физические свойства оснований.
Химические свойства
Слайд 2Основания
– это сложные вещества, состоящие из атома металла и одной или
нескольких гидроксогрупп.
Слайд 3Состав оснований:
Назовите составные части оснований.
Ме(ОН)х
Валентность гидроксогруппы (ОН) – I
Количество гидроксогрупп определяется
валентностью металла, образующего основание.
Слайд 4Выберите формулы оснований. Назовите их.
НСl, NaOH, Na2O, Ca(OH)2, H2SO4, P2O5,
Fe(OH)3, MgO, Cи(OH)2
Слайд 5Основания
NaOH – гидроксид натрия
Ca(OH)2 – гидроксид кальция
Fe(OH)3 – гидроксид железа (III)
Cи(OH)2
– гидроксид меди (III)
Найдите ошибку!
Найдите ошибку!
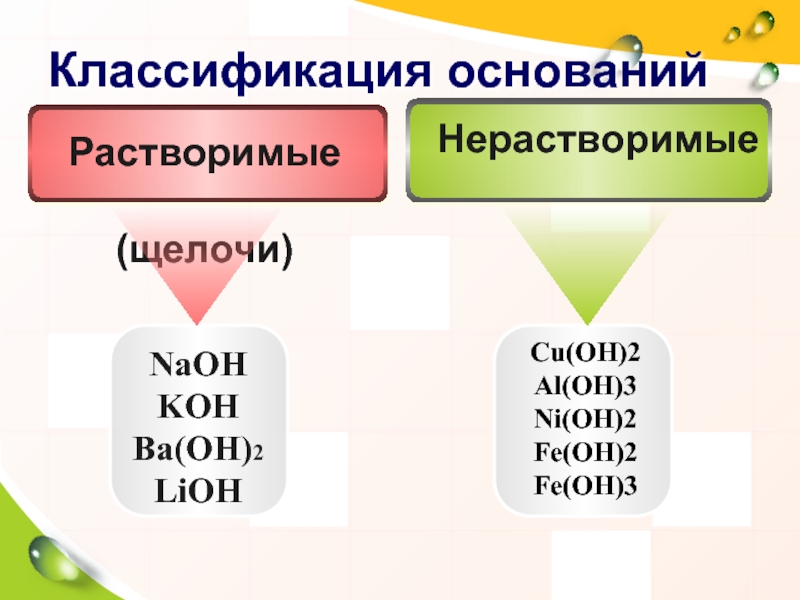
Слайд 6Классификация оснований
NaOH
KOH
Ba(OH)2
LiOH
Cu(OH)2
Al(OH)3
Ni(OH)2
Fe(OH)2
Fe(OH)3
Нерастворимые
Растворимые
(щелочи)
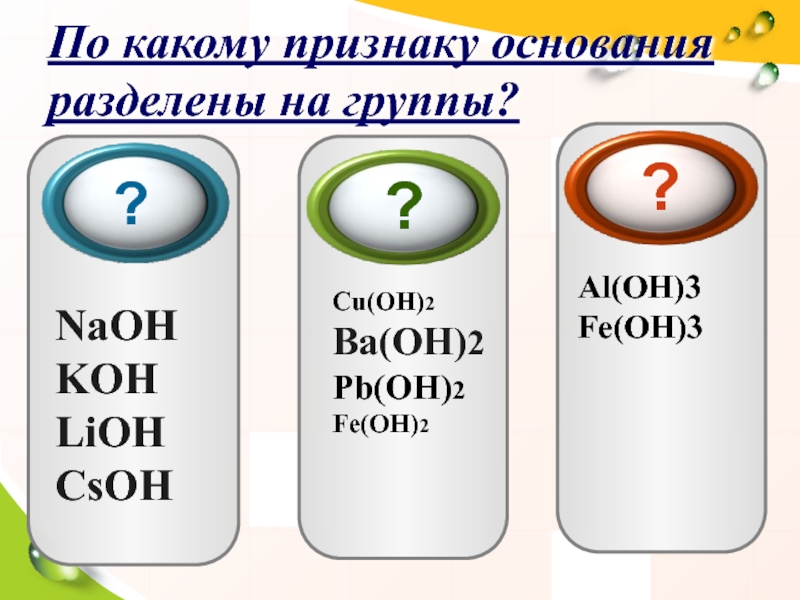
Слайд 9По какому признаку основания разделены на группы?
NaOH
KOH
LiOH
СsOH
Cu(OH)2
Ba(OH)2
Pb(OH)2
Fe(OH)2
Al(OH)3
Fe(OH)3
?
?
?
Слайд 10
Однокислотные
NaOH, KOH
Двухкислотные
Pb(OH)2, Fe(OH)2
Трехкислотные
Al(OH)3
Классификация оснований по числу гидроксогрупп.
Основания
Слайд 11Физические свойства оснований
Агрегатное состояние:
Все твердые вещества
Цвет кислот:
Белого – КОН,
Голубого -
Cu(OH)2
Красно-бурого - Fe(OH)3
Запах – ?
Вкус – ? (горький, солоноватый)
Растворимость в воде - ?
Красно-бурого - Fe(OH)3
Запах – ?
Вкус – ? (горький, солоноватый)
Растворимость в воде - ?
КОН
Cu(OH)2
Слайд 12Химические свойства нерастворимых оснований.
1). Разлагаются при нагревании.
2). Взаимодействуют с кислотами
(реакция нейтрализации).
Слайд 13Химические свойства щелочей.
1). Изменяют окраску индикаторов.
Взаимодействуют с:
2). кислотами (реакция нейтрализации),
3).
кислотными оксидами,
4). солями.
4). солями.
Слайд 14ПРАВИЛА БЕЗОПАСНОСТИ
Едкое вещество—щелочь! Разрушает и раздражает кожу, слизистые оболочки.
Попавшие на кожу
капли раствора щелочи немедленно смойте сильной струей холодной воды, а затем обработайте поврежденную поверхность 1% раствором уксусной кислоты.
Слайд 15
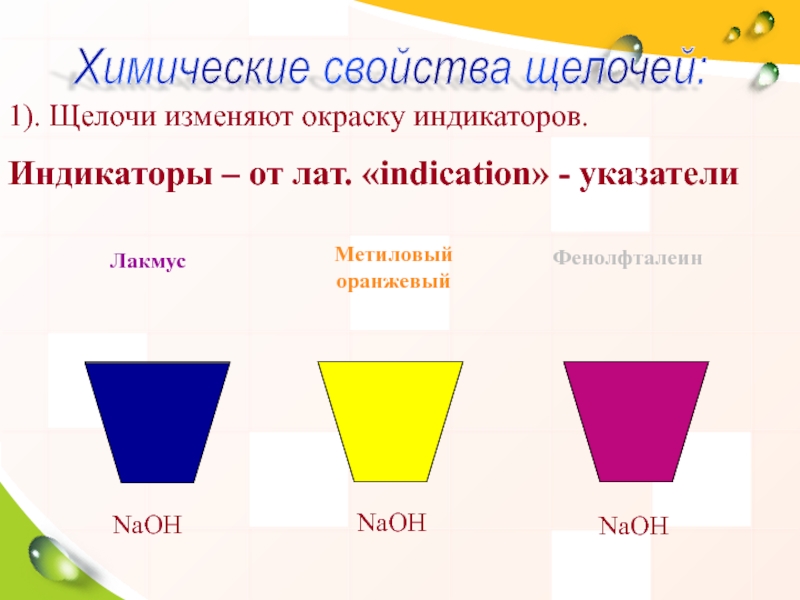
1). Щелочи изменяют окраску индикаторов.
Индикаторы – от лат. «indication» - указатели
NaOH
NaOH
NaOH
Лакмус
Метиловый оранжевый
Фенолфталеин
Химические свойства щелочей: