- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Оксиды. Классы неорганических соединений презентация
Содержание
- 1. Оксиды. Классы неорганических соединений
- 2. Классы неорганических соединений Оксиды
- 3. Классы неорганических соединений
- 4. ОКСИДЫ Это сложные вещества, состоящие из двух
- 5. Если элемент проявляет несколько валентностей? У хлора
- 6. ХИМИЧЕСКИЕ СВОЙСТВА ОКСИДОВ КИСЛОТНЫЕ ОСНОВНЫЕ 1.Реагируют с
- 7. Вывод: Свойства оксидов
- 8. Оксиды реагируют с водой Основные С водой
- 9. Основные Реагируют с кислотами Кислотные Реагируют
- 10. Задание на дом §30 Упр. №
- 11. Составьте формулы оксидов и определите их
- 12. Составьте формулы оксида хлора (5) и оксида
- 13. CaO
- 14. Оксиды хлора Cl2O Оксид хлора (1) Cl2O3
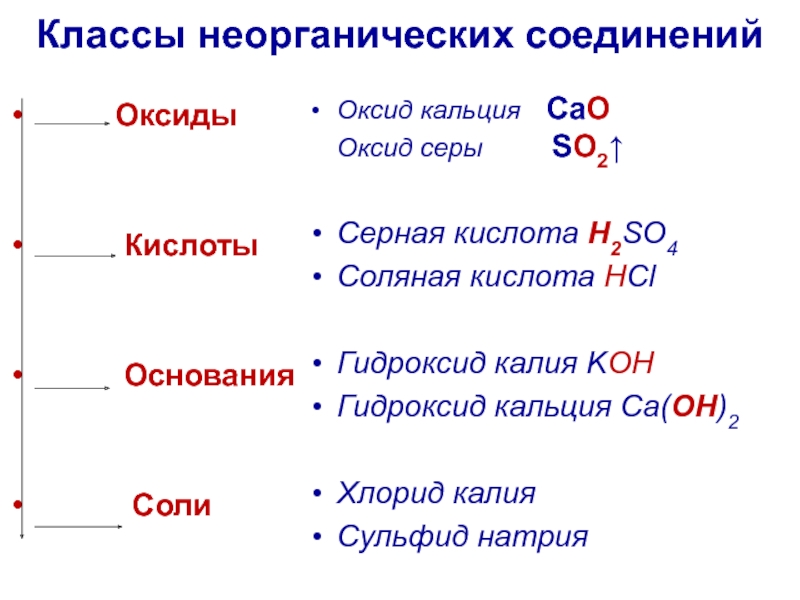
Слайд 3Классы неорганических соединений
Оксиды
Основания
Соли
Оксид кальция CaO Оксид серы SO2↑
Серная кислота H2SO4
Соляная кислота HCl
Гидроксид калия KOH
Гидроксид кальция Ca(OH)2
Хлорид калия
Сульфид натрия
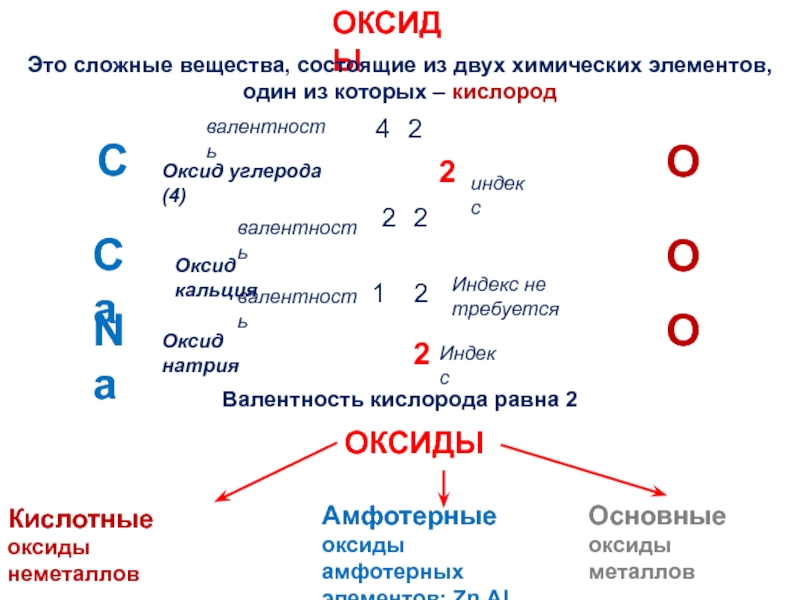
Слайд 4ОКСИДЫ
Это сложные вещества, состоящие из двух химических элементов, один из которых
С
О
4
2
2
валентность
индекс
Са
О
валентность
2
2
Индекс не требуется
Nа
О
1
2
валентность
Индекс
2
Валентность кислорода равна 2
ОКСИДЫ
Оксид углерода (4)
Оксид кальция
Оксид натрия
Слайд 5Если элемент проявляет несколько валентностей?
У хлора есть валентности 1, 3, 5,
Следовательно, хлор будет иметь несколько оксидов
1 2
Cl O
Оксид хлора (1)
3 2
Cl O
Оксид хлора (3)
2
2
3
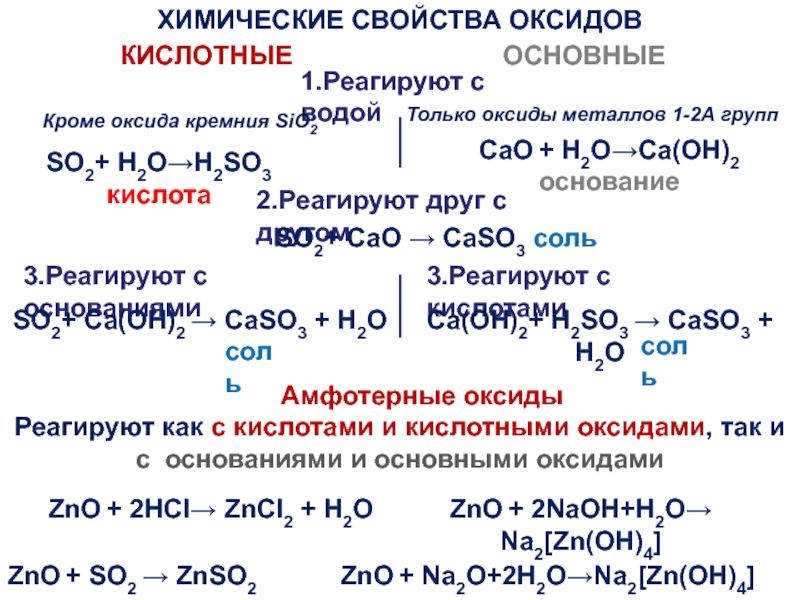
Слайд 6ХИМИЧЕСКИЕ СВОЙСТВА ОКСИДОВ
КИСЛОТНЫЕ
ОСНОВНЫЕ
1.Реагируют с водой
SO2+ H2O→H2SO3 кислота
CaO + H2O→Ca(OH)2 основание
Кроме
Только оксиды металлов 1-2А групп
2.Реагируют друг с другом
SO2+ CaO → CaSO3 соль
3.Реагируют с основаниями
3.Реагируют с кислотами
SO2+ Ca(OH)2 → CaSO3 + H2O
соль
Ca(OH)2+ H2SO3 → CaSO3 + H2O
соль
Амфотерные оксиды
Реагируют как с кислотами и кислотными оксидами, так и с основаниями и основными оксидами
ZnO + 2HCl→ ZnCl2 + H2O
ZnO + 2NaOH+H2O→ Na2[Zn(OH)4]
ZnO + SO2 → ZnSO2
ZnO + Na2O+2H2O→Na2[Zn(OH)4]
Слайд 7
Вывод: Свойства оксидов
Основные оксиды реагируют с кислотными, а кислотные оксиды
Слайд 8Оксиды реагируют с водой
Основные
С водой реагируют только оксиды металлов в ряду
Образуются основания
Кислотные
С водой реагируют все кроме оксида кремния SiO2
Образуются кислоты
Слайд 9Основные
Реагируют с кислотами
Кислотные
Реагируют с основаниями
Реагируют с кислотными оксидами
Реагируют с основными
Слайд 10Задание на дом
§30
Упр. № 6, на стр. 93 учебника
Задача
Дополнительное задание для желающих
Написать все возможные уравнения реакции для оксида углерода (4), оксида калия, оксида алюминия
Слайд 11Составьте формулы оксидов и
определите их характер
Оксида магния
Оксида лития
Оксида фосфора
Оксида меди (2)
Оксида железа (2)
MgO основной
Li2O основной
P2O5 кислотный
CuO основной
FeO основной
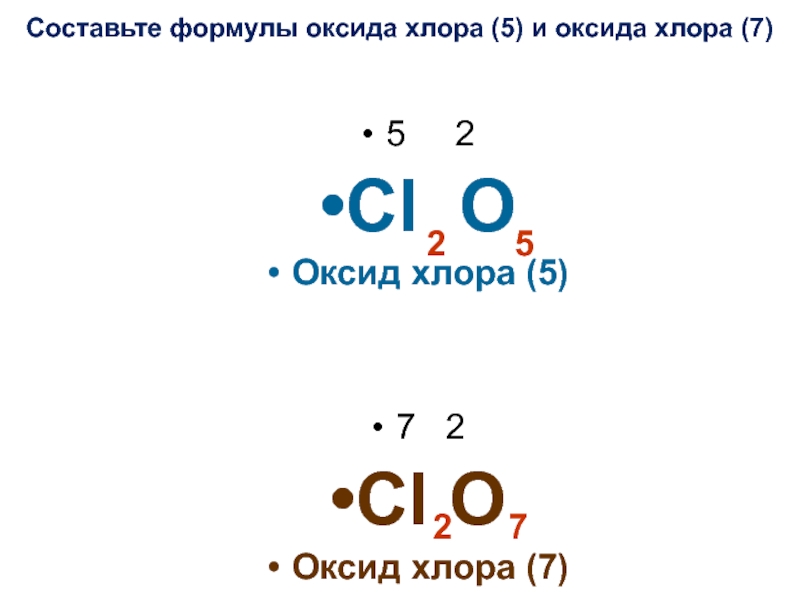
Слайд 12Составьте формулы оксида хлора (5) и оксида хлора (7)
5
Cl O
Оксид хлора (5)
7 2
Cl O
Оксид хлора (7)
5
2
2
7