- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Общая характеристика ферментов как биологических катализаторов презентация
Содержание
- 1. Общая характеристика ферментов как биологических катализаторов
- 2. ФЕРМЕНТЫ (ЭНЗИМЫ) – СОЕДИНЕНИЯ БЕЛКОВОЙ ПРИРОДЫ,
- 3. Сходство ферментов с небиологическими катализаторами заключается в
- 4. Сходство ферментов с небиологическими катализаторами заключается в
- 5. Сходство ферментов с небиологическими катализаторами заключается в
- 6. Отличия ферментов от небиологических катализаторов (основные свойства)
- 7. Структура ферментов Фермент (энзим) Простой белок (РНК-аза,
- 8. Небелковая часть Производные витаминов Гемы, входящие
- 9. Функции небелковой части фермента Перенос атомов водорода,
- 10. Активные центры ферментов Субстратный Каталитический
- 11. Активные центры ферментов Субстратный Каталитический
- 12. Схема строения активного центра фермента
- 13. Формирование активных центров химотрипсина А-цепь(13) В-цепь(140) С-цепь(96) 16-илей 57-гис 102-асп 195-сер
- 14. Активный центр фермента Участок связывания Обеспечивает субстратную
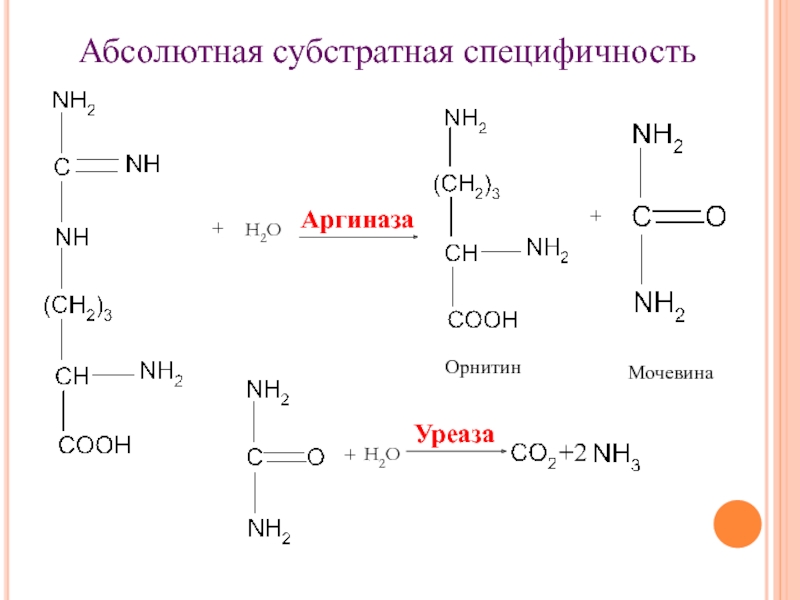
- 15. + Абсолютная субстратная специфичность Аргиназа Орнитин + Мочевина + Уреаза +2 Н2О Н2О
- 16. Активный центр фермента Участок связывания Обеспечивает субстратную
- 17. Групповая субстратная специфичность +2 Триацилглицерол 2-Моноацилглицерол Панкреатическая липаза Н2О
- 18. ГРУППОВАЯ СУБСТРАТНАЯ СПЕЦИФИЧНОСТЬ Пепсин - NH2 (фен,
- 19. ГРУППОВАЯ СУБСТРАТНАЯ СПЕЦИФИЧНОСТЬ Тир Пепсин Химотрипсин
- 20. Активный центр фермента Участок связывания Обеспечивает субстратную
- 21. Стереоспецифичность Стереоспецифичность к D-сахарам + АТФ
- 22. Активный центр фермента Участок связывания Каталитический участок
- 23. КАТАЛИТИЧЕСКАЯ СПЕЦИФИЧНОСТЬ Каталитические пути превращения глюкозо-6-фосфата
- 24. Механизм действия ферментов Е + S ЕS ЕP Е + P Этапы ферментативного катализа
- 25. Механизм действия ферментов Изменение свободной энергии в ходе химической реакции, некатализируемой и катализируемой ферментами
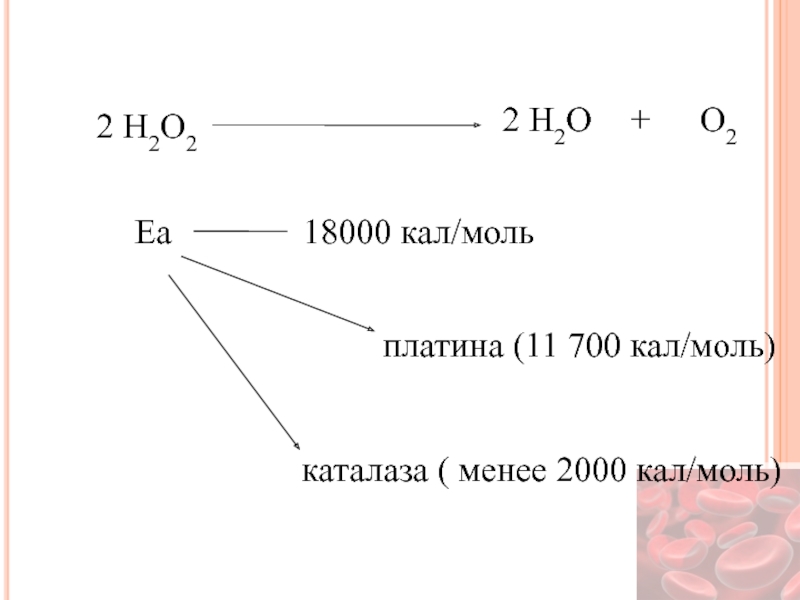
- 26. 2 H2O2 2 H2O O2 +
- 27. Множественные формы ферментов Ферменты – катализирующие одну
- 28. Реакция, катализируемая лактатдегидрогеназой (ЛДГ)
- 29. Изоформы лактатдегидрогеназы
Слайд 2 ФЕРМЕНТЫ (ЭНЗИМЫ) – СОЕДИНЕНИЯ БЕЛКОВОЙ ПРИРОДЫ, СПОСОБНЫЕ КАТАЛИТИЧЕСКИ УСКОРЯТЬ ПРОТЕКАНИЕ ХИМИЧЕСКИХ
Значение для изучения:
Ферменты - биологические регуляторы химических процессов в клетке (основа жизнедеятельности);
Нарушения в их структуре и функции – возникновение энзимопатий.
Энзимодиагностика.
Энзимотерапия.
Использование к качестве реактивов для определения метаболитов.
Слайд 3Сходство ферментов с небиологическими катализаторами заключается в том, что:
Небиологические катализаторы и
Ведут реакции в обход энергетического барьера;
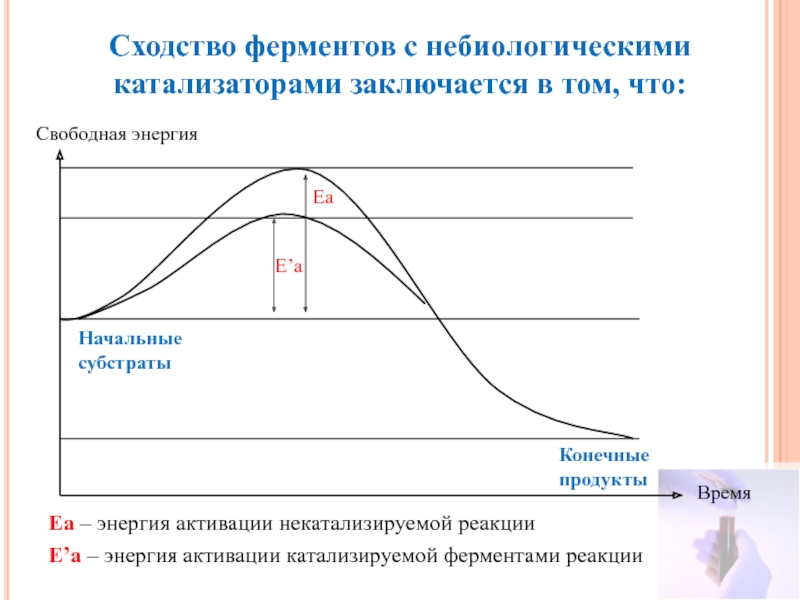
Слайд 4Сходство ферментов с небиологическими катализаторами заключается в том, что:
Свободная энергия
Время
Конечные продукты
Начальные
Е’а
Еа
Е’а – энергия активации катализируемой ферментами реакции
Еа – энергия активации некатализируемой реакции
Слайд 5Сходство ферментов с небиологическими катализаторами заключается в том, что:
В ходе катализа
Не расходуются во время реакции;
Требуется небольшое их количество.
Слайд 6Отличия ферментов от небиологических катализаторов (основные свойства)
Скорость ферментативных реакций значительно
Ферменты обладают высокой специфичностью (субстратной и каталитической);
3. Ферменты обладают конформационной лабильностью.
4. Энзимы действуют при определенных оптимальных условиях (температура, рН, микроэлементы, кооперативность);
5. Скорость ферментативной реакции может регулироваться.
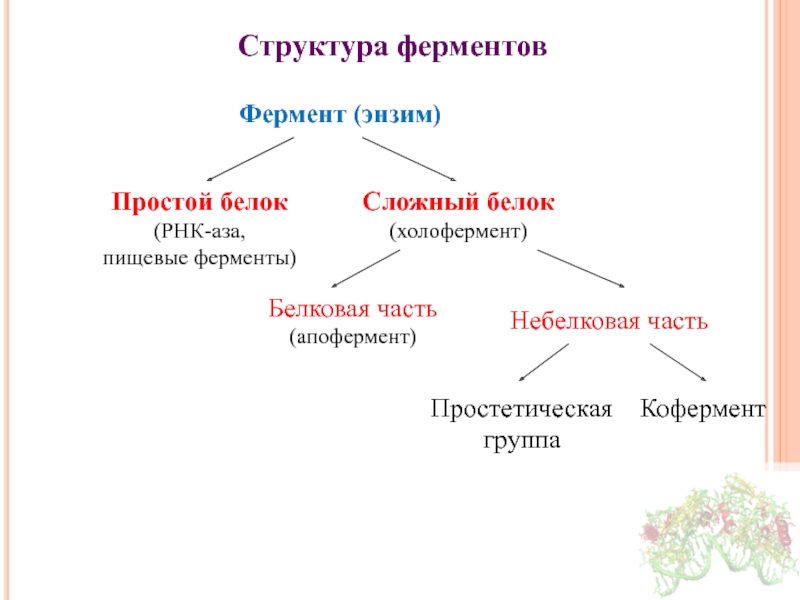
Слайд 7Структура ферментов
Фермент (энзим)
Простой белок
(РНК-аза,
пищевые ферменты)
Сложный белок
(холофермент)
Белковая часть (апофермент)
Небелковая часть
Простетическая группа
Кофермент
Слайд 8Небелковая часть
Производные витаминов
Гемы, входящие в состав цитохромов, каталазы,
Нуклеотиды – доноры и акцепторы остатка фосфорной кислоты
Убихинон, или кофермент Q, участвующий в переносе электронов и протонов
Фосфоаденозилметионин, участвующий в переносе сульфата
S-аденозилметионин – донор метильной группы
Глутатион, участвующий в окислительно-восстановительных реакциях
Слайд 9Функции небелковой части фермента
Перенос атомов водорода, электронов (окислительно-восстановительные реакции – НАД,
Перенос химических групп (фосфопиридоксаль, биотин и др.)
Реакции синтеза, изомеризации, расщепление связей (ТДФ и др.)
Слайд 10Активные центры ферментов
Субстратный
Каталитический
Аллостерический
Закономерности в построении активных центров
1. В
2. Чаще всего в состав центра входят радикалы гис, сер, лиз, асп, цис.
3. В построении центров сложных ферментов участвуют химические группировки небелковой части.
Слайд 11Активные центры ферментов
Субстратный
Каталитический
Аллостерический
Закономерности в построении активных центров
4. Если фермент
5. Энергия взаимодействия субстрата с активным центром слабая с образование нековалентных связей
6. Активные центры формируются при образовании третичной и четвертичной структуры белковой части в процессе взаимодействия с субстратом (индуцированное соответствие).
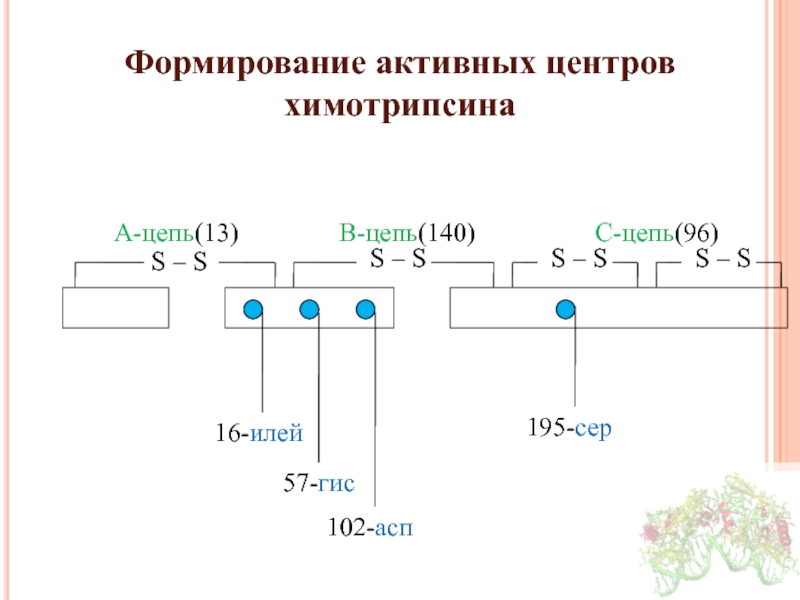
Слайд 13Формирование активных центров химотрипсина
А-цепь(13)
В-цепь(140)
С-цепь(96)
16-илей
57-гис
102-асп
195-сер
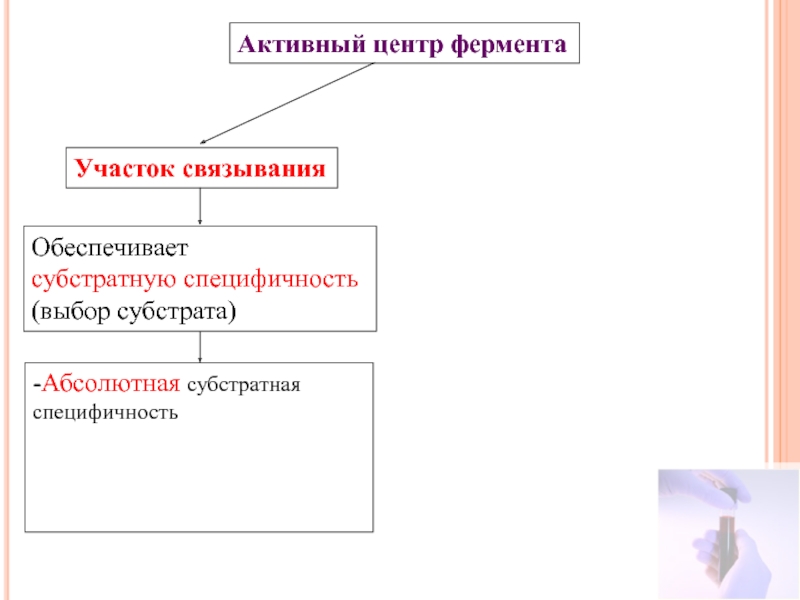
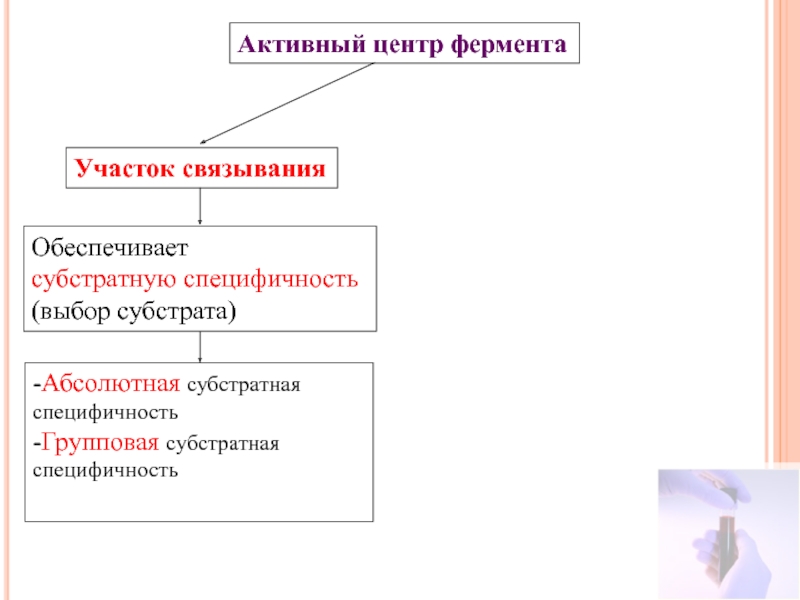
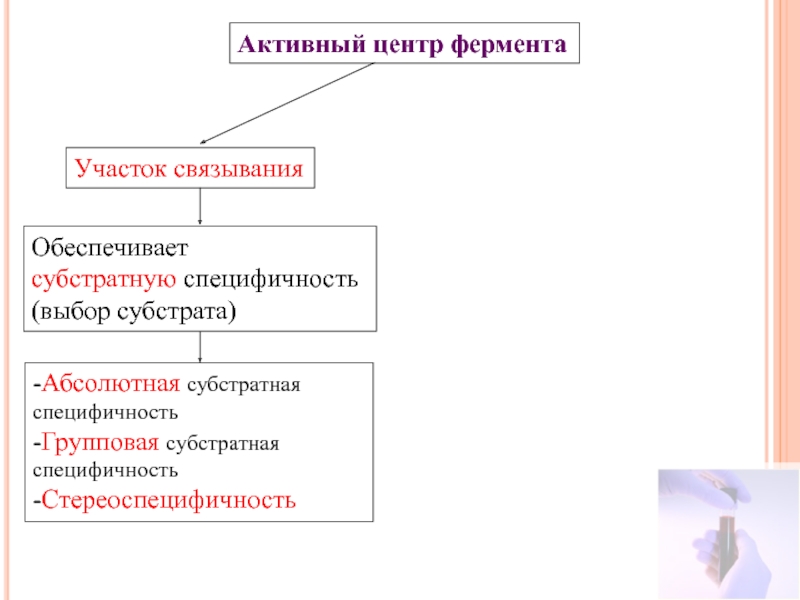
Слайд 14Активный центр фермента
Участок связывания
Обеспечивает
субстратную специфичность
(выбор субстрата)
-Абсолютная субстратная специфичность
-Групповая субстратная специфичность
-Стереоспецифичность
Слайд 16Активный центр фермента
Участок связывания
Обеспечивает
субстратную специфичность
(выбор субстрата)
-Абсолютная субстратная специфичность
-Групповая субстратная специфичность
-Стереоспецифичность
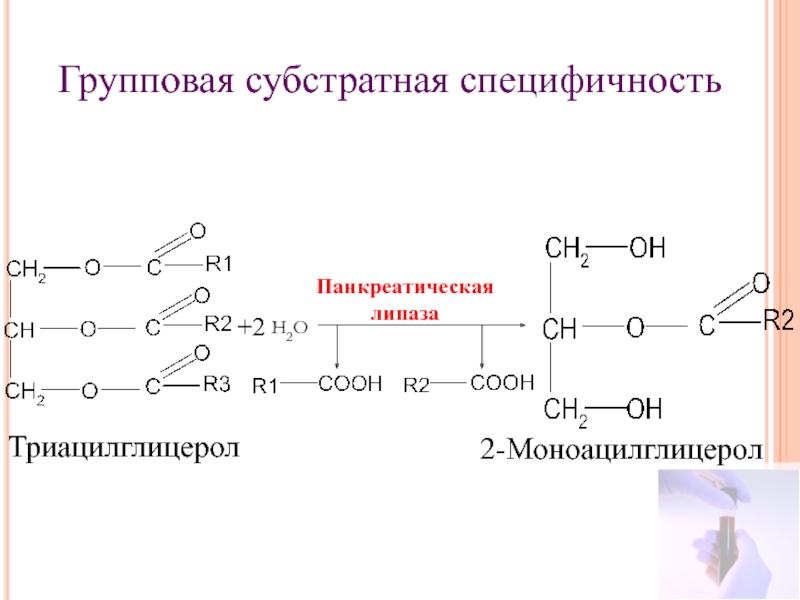
Слайд 17Групповая субстратная специфичность
+2
Триацилглицерол
2-Моноацилглицерол
Панкреатическая
липаза
Н2О
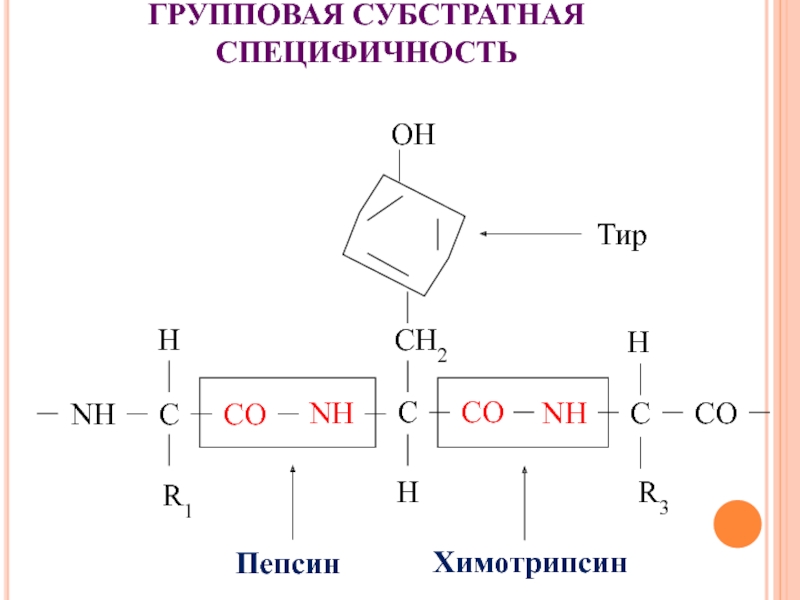
Слайд 18ГРУППОВАЯ СУБСТРАТНАЯ СПЕЦИФИЧНОСТЬ
Пепсин
- NH2
(фен, тир, три, глу, асп)
Трипсин
- СООH
(лиз, арг)
Химотрипсин
- СООH
(тир,
Слайд 20Активный центр фермента
Участок связывания
Обеспечивает
субстратную специфичность
(выбор субстрата)
-Абсолютная субстратная специфичность
-Групповая субстратная специфичность
-Стереоспецифичность
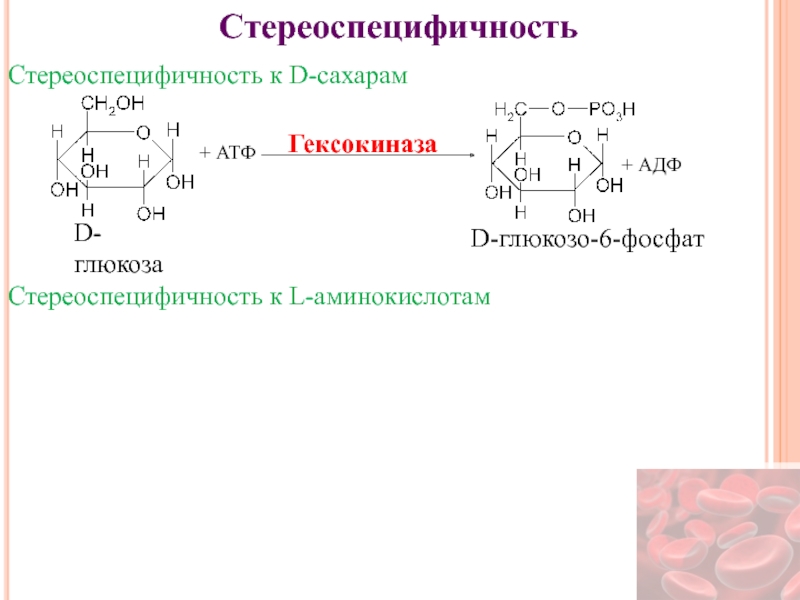
Слайд 21Стереоспецифичность
Стереоспецифичность к D-сахарам
+ АТФ
+ АДФ
Гексокиназа
D-глюкоза
D-глюкозо-6-фосфат
Стереоспецифичность к L-аминокислотам
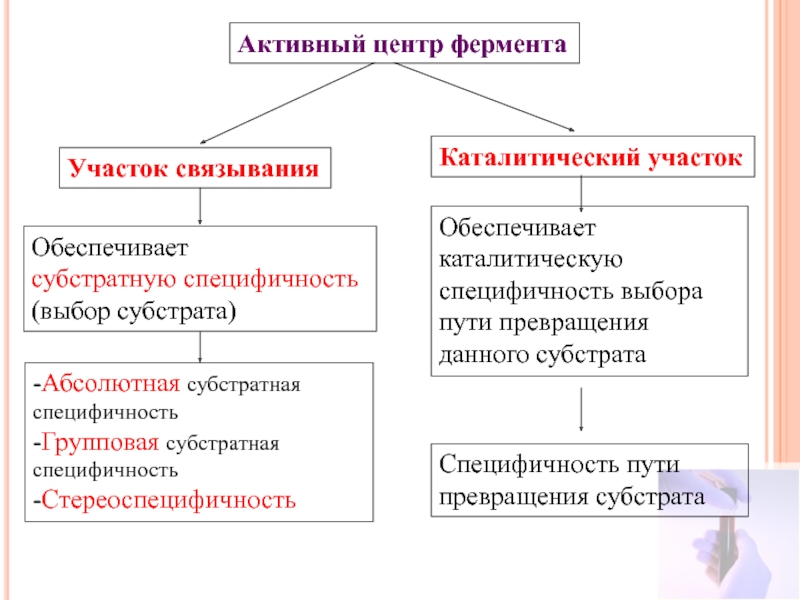
Слайд 22Активный центр фермента
Участок связывания
Каталитический участок
Обеспечивает
субстратную специфичность
(выбор субстрата)
-Абсолютная субстратная специфичность
-Групповая субстратная
-Стереоспецифичность
Обеспечивает каталитическую специфичность выбора пути превращения данного субстрата
Специфичность пути превращения субстрата
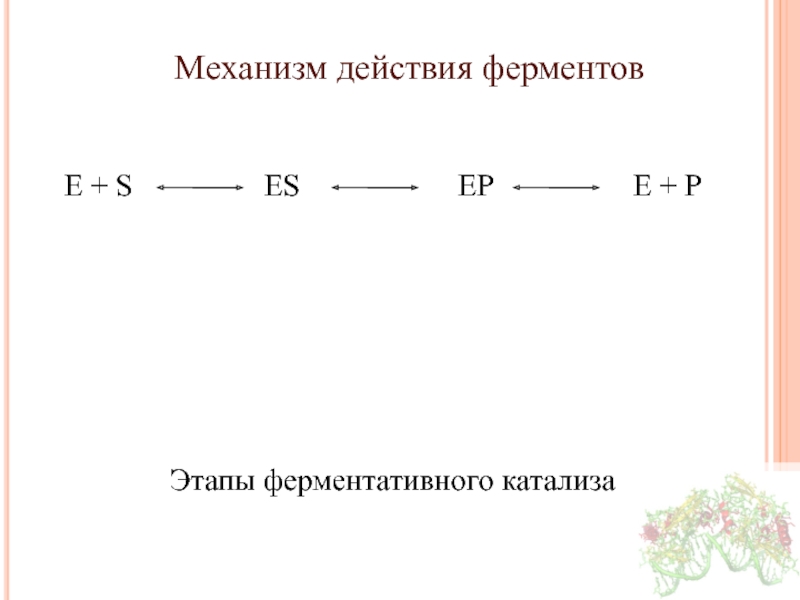
Слайд 25Механизм действия ферментов
Изменение свободной энергии в ходе химической реакции, некатализируемой и
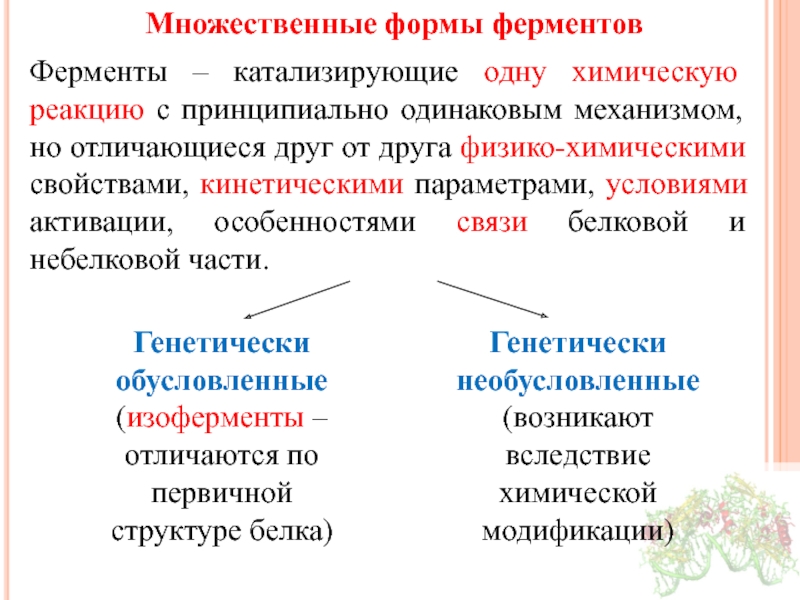
Слайд 27Множественные формы ферментов
Ферменты – катализирующие одну химическую реакцию с принципиально одинаковым
Генетически обусловленные (изоферменты – отличаются по первичной структуре белка)
Генетически необусловленные (возникают вследствие химической модификации)