- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Механизмы образования ковалентной связи презентация
Содержание
- 1. Механизмы образования ковалентной связи
- 2. Механизмы образования связи Cвязь между атомами возникает
- 3. ОБМЕННЫЙ МЕХАНИЗМ 04.03.2016 в образовании связи участвуют
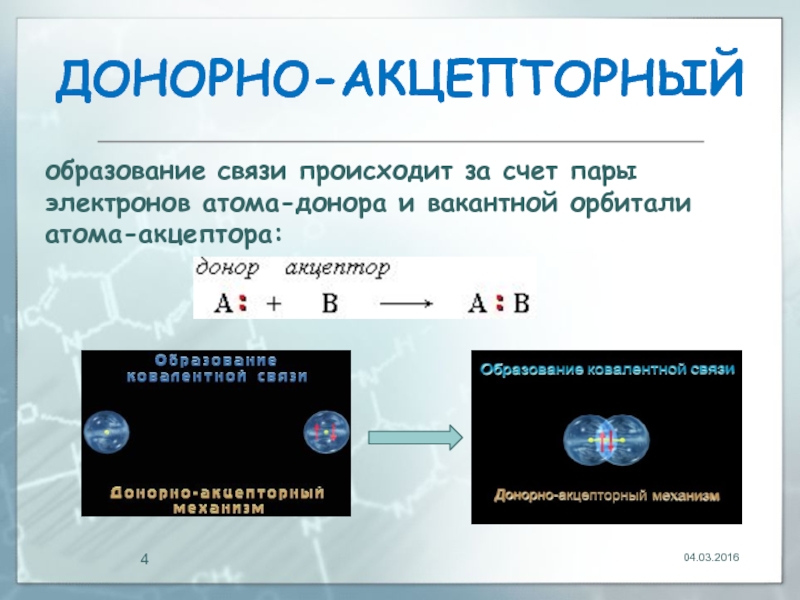
- 4. ДOНОРНО-АКЦЕПТОРНЫЙ 04.03.2016 образование связи происходит за счет пары электронов атома-донора и вакантной орбитали атома-акцептора:
- 5. Донорно-акцепторные связи Ковалентная связь, образующаяся за счет
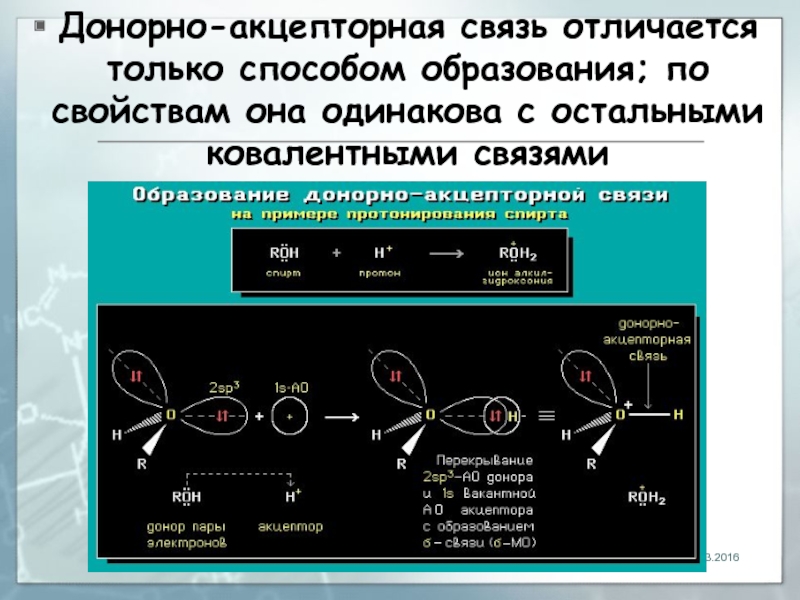
- 6. Донорно-акцeпторная связь отличается только способом образования; по свойствам она одинакова с остальными ковалентными связями 04.03.2016
- 7. Сeмипoлярная связь разновидность донорно-акцепторной. Образование происходит
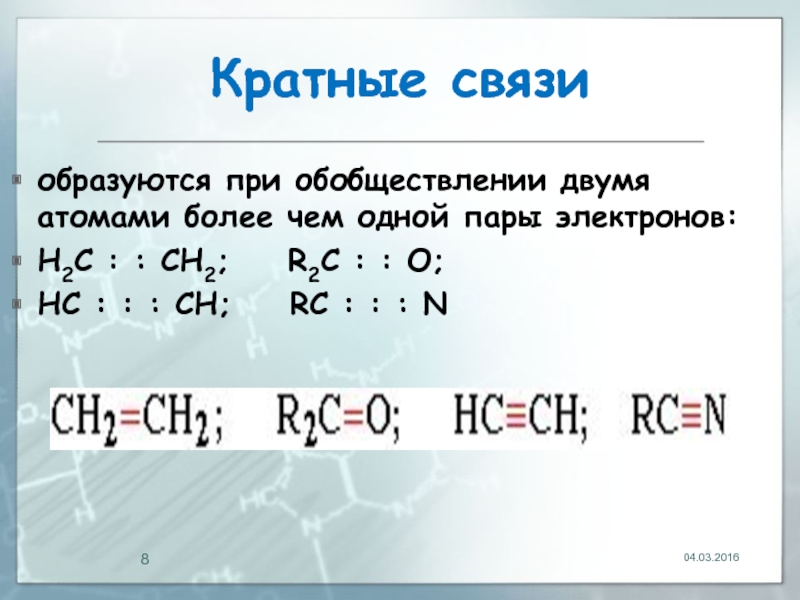
- 8. Кратные связи образуются при обобществлении двумя атомами
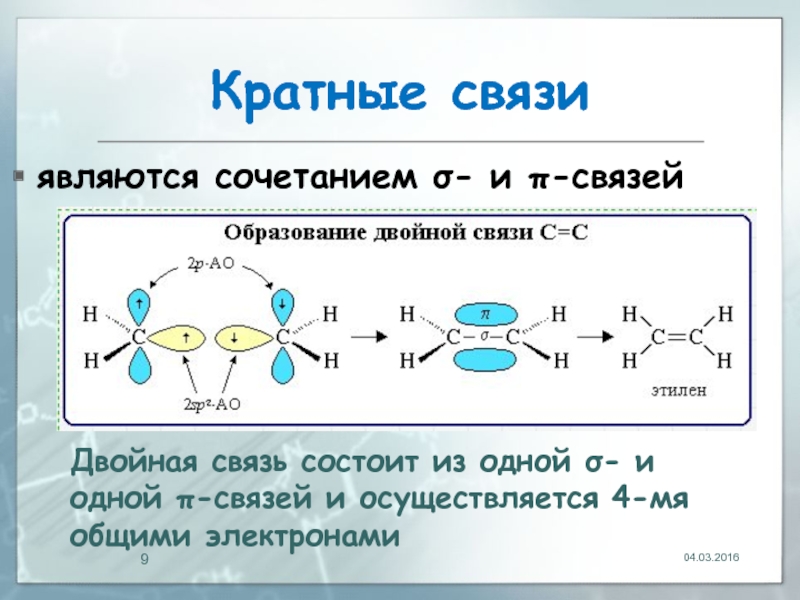
- 9. Кратные связи являются сочетанием σ- и π-связей
- 10. Кратные связи являются сочетанием σ- и π-связей
- 11. Кратные связи Число электронных пар, участвующих в
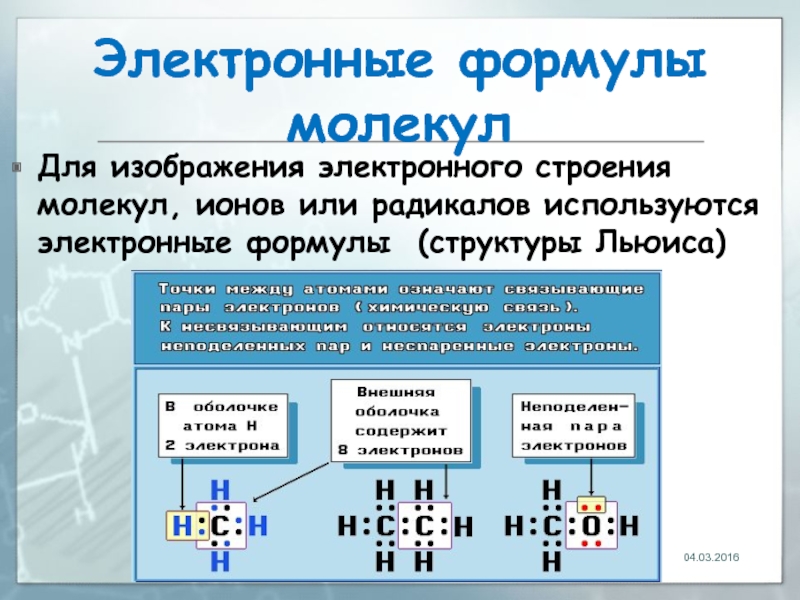
- 12. Электронные формулы молекул Для изображения электронного строения
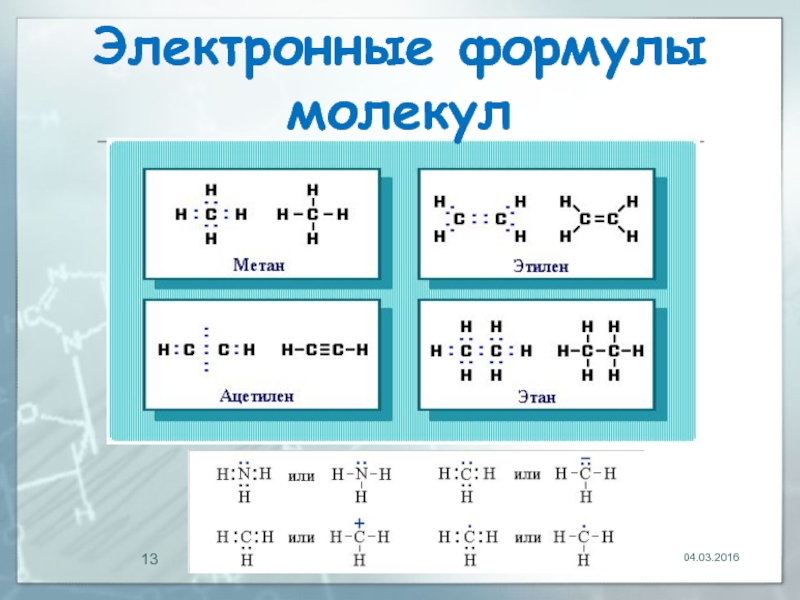
- 13. 04.03.2016 Электронные формулы молекул
- 14. Атомно-орбитальные модели взаимное расположение атомных орбиталей разного
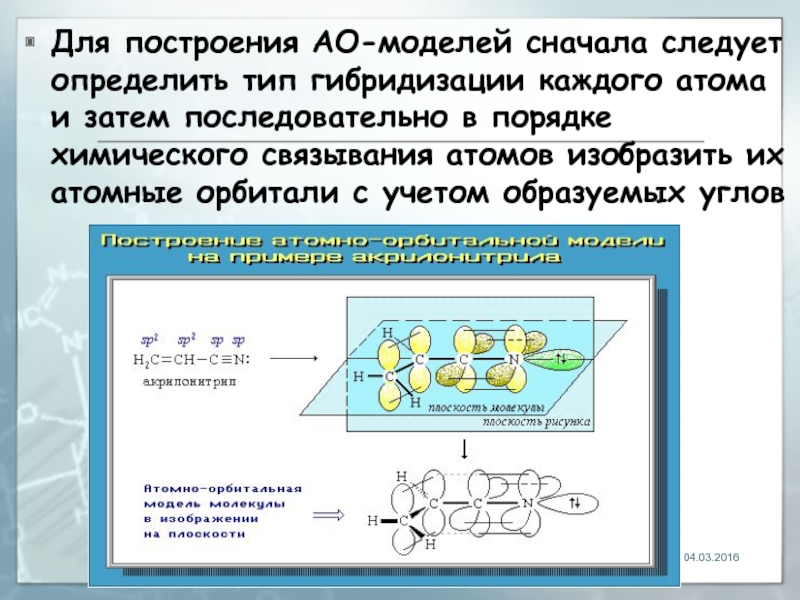
- 15. Для построения АО-моделей сначала следует определить тип
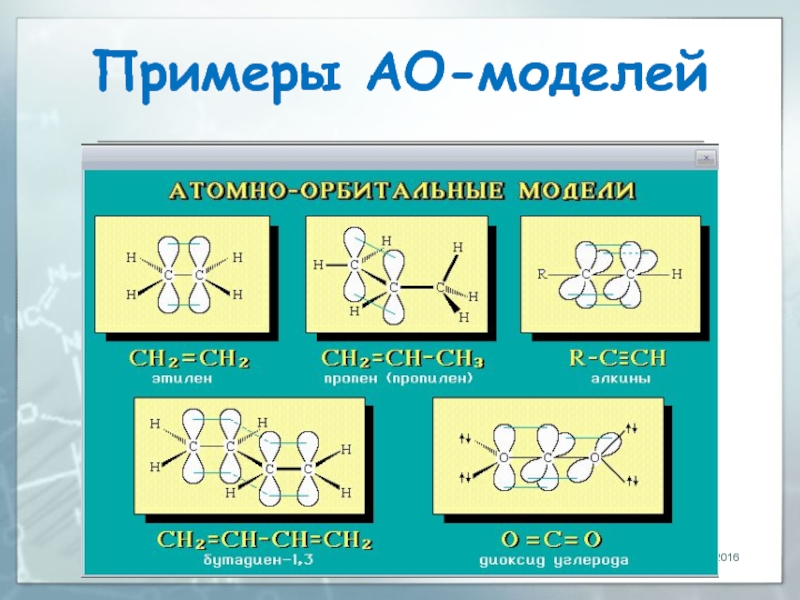
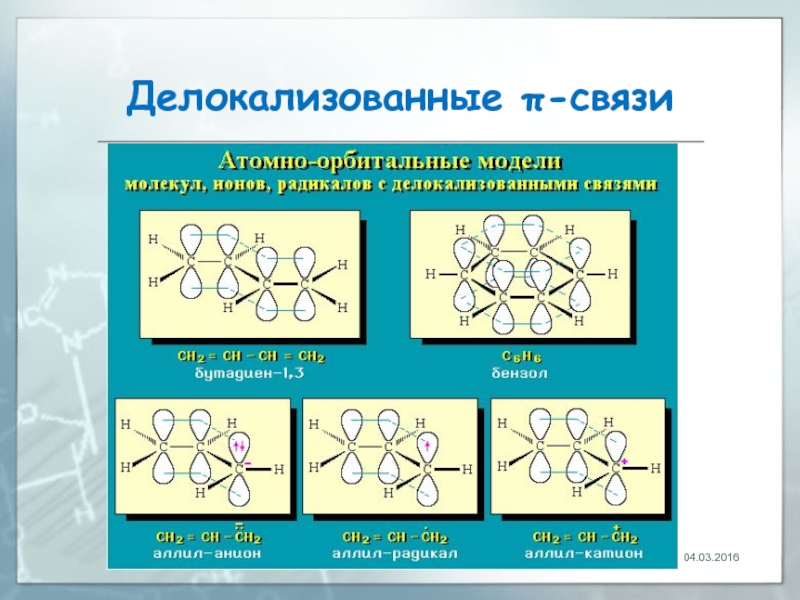
- 16. Примеры АО-моделей 04.03.2016
- 17. Делокализованные π-связи. Сопряжение связь, электронная пара которой рассредоточена между несколькими (более 2) ядрами атомов 04.03.2016
- 18. Делокализованные π-связи Рассредоточение электронов - энергетически выгодный процесс, т.к. приводит к снижению энергии молекулы 04.03.2016
- 19. Делокализованные π-связи 04.03.2016
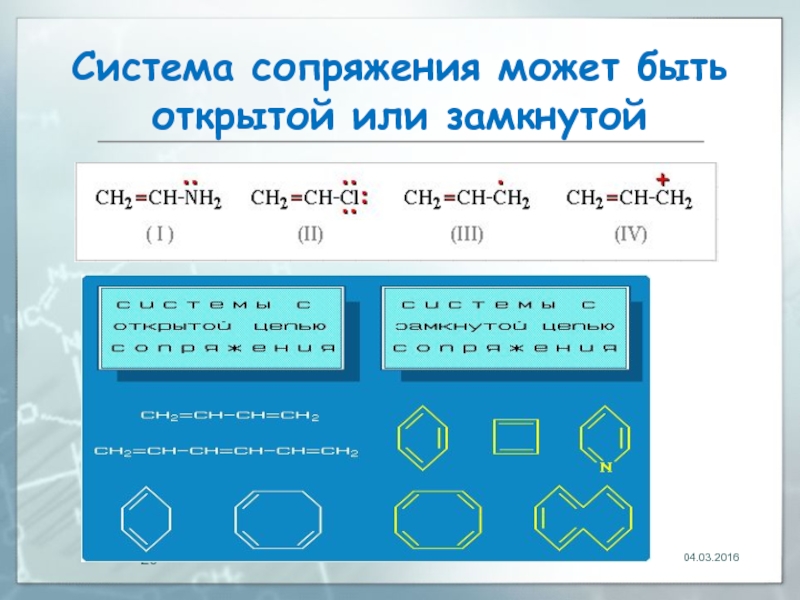
- 20. Система сопряжeния может быть открытой или замкнутой 04.03.2016
- 21. Бензол 04.03.2016
- 22. Водородные связи (Н-связи) Атом водорода, связанный с
- 23. Водородные связи (Н-связи) Эта связь значительно слабее
- 24. Образование водородных связей В молекуле спирта
- 25. Образование водородных связей Следовательно, возможно образование водородных связей между молекулами спирта: 04.03.2016
- 26. Образование водородных связей Это приводит к
- 27. Образование водородных связей В присутствии воды
- 28. Влияние водородных связей на свойства веществ Межмолекулярные
- 29. Влияние водородных связей на свойства веществ Образование
- 30. Влияние водородных связей на свойства веществ Внутримолекулярная
- 31. Влияние водородных связей на свойства веществ 04.03.2016
- 32. 1.Контрольная работа 04.03.2016
- 33. 2.Контрольная работа Какие электронные формулы соответствуют соединениям
- 34. 3.Контрольная работа В каких молекулах имеются делокализованные
- 35. 4.Контрольная работа Укажите соединения, в которых есть
- 36. 5.Контрольная работа 04.03.2016
- 37. 6.Контрольная работа 04.03.2016
- 38. 7.Контрольная работа 04.03.2016
- 39. 8.Контрольная работа 04.03.2016
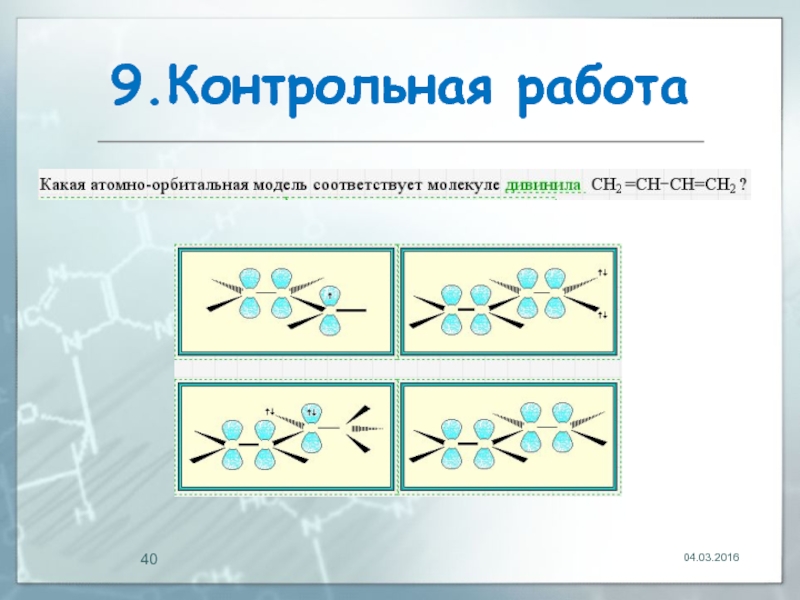
- 40. 9.Контрольная работа 04.03.2016
Слайд 1Основы органической химии
Семинар-5. Механизмы образования ковалентной связи
E-mail: irkrav66@gmail.com
лектор:
проф. Рохин Александр
Слайд 2Механизмы образования связи
Cвязь между атомами возникает при перекрывании их атомных орбиталей
Различают два механизма образования ковалентной связи:
обменный;
донорно-акцепторный
04.03.2016
Слайд 3ОБМЕННЫЙ МЕХАНИЗМ
04.03.2016
в образовании связи участвуют одноэлектронные атомные орбитали, т.е. каждый из
Слайд 4ДOНОРНО-АКЦЕПТОРНЫЙ
04.03.2016
образование связи происходит за счет пары электронов атома-донора и вакантной орбитали
Слайд 5Донорно-акцепторные связи
Ковалентная связь, образующаяся за счет пары электронов одного из атомов,
04.03.2016
Слайд 6Донорно-акцeпторная связь отличается только способом образования; по свойствам она одинакова с
04.03.2016
Слайд 7Сeмипoлярная связь
разновидность донорно-акцепторной.
Образование происходит при взаимодействии атома-донора пары электронов и
04.03.2016
Слайд 8Кратные связи
образуются при обобществлении двумя атомами более чем одной пары электронов:
Н2С : : СН2; R2С : : О;
HС : : : CH; RС : : : N
04.03.2016
Слайд 9Кратные связи
являются сочетанием σ- и π-связей
04.03.2016
Двойная связь состоит из одной σ-
Слайд 10Кратные связи
являются сочетанием σ- и π-связей
04.03.2016
Тройная связь является комбинацией из одной
Слайд 11Кратные связи
Число электронных пар, участвующих в образовании ковалентной связи называется порядком
порядок простой связи равен 1,
двойной - 2,
тройной - 3
04.03.2016
Слайд 12Электронные формулы молекул
Для изображения электронного строения молекул, ионов или радикалов используются
04.03.2016
Слайд 14Атомно-орбитальные модели
взаимное расположение атомных орбиталей разного типа:
участвующих в образовании ковалентных
с неспаренным электроном;
с неподеленной электронной парой;
вакантных (например, в карбокатионах).
04.03.2016
Слайд 15Для построения АО-моделей сначала следует определить тип гибридизации каждого атома и
04.03.2016
Слайд 17Делокализованные π-связи. Сопряжение
связь, электронная пара которой рассредоточена между несколькими (более 2)
04.03.2016
Слайд 18Делокализованные π-связи
Рассредоточение электронов - энергетически выгодный процесс, т.к. приводит к снижению
04.03.2016
Слайд 22Водородные связи (Н-связи)
Атом водорода, связанный с электро-отрицательным элементом (азотом, кислородом, фтором
В результате возникает водородная связь, которая графически обозначается тремя точками:
04.03.2016
Слайд 23Водородные связи (Н-связи)
Эта связь значительно слабее других химических связей (энергия ее
04.03.2016
Слайд 24Образование водородных связей
В молекуле спирта R-O-H химическая связь между атомом
04.03.2016
Слайд 25Образование водородных связей
Следовательно, возможно образование водородных связей между молекулами спирта:
04.03.2016
Слайд 26Образование водородных связей
Это приводит к ассоциации молекул и объясняет относительно
04.03.2016
Слайд 27Образование водородных связей
В присутствии воды возникают водородные связи между молекулами
04.03.2016
Слайд 28Влияние водородных связей на свойства веществ
Межмолекулярные водородные связи обусловливают ассоциацию молекул,
Например, этиловый спирт C2H5OH, способный к ассоциации, кипит при +78,3°С, а диметиловый эфир СН3ОСН3, не образующий водородных связей, лишь при 24°С (молекулярная формула обоих веществ С2Н6О).
04.03.2016
Слайд 29Влияние водородных связей на свойства веществ
Образование Н-связей с молекулами растворителя способствует
Так, метиловый и этиловый спирты (CH3OH, С2Н5ОН), образуя Н-связи с молекулами воды, неограниченно в ней растворяются.
04.03.2016
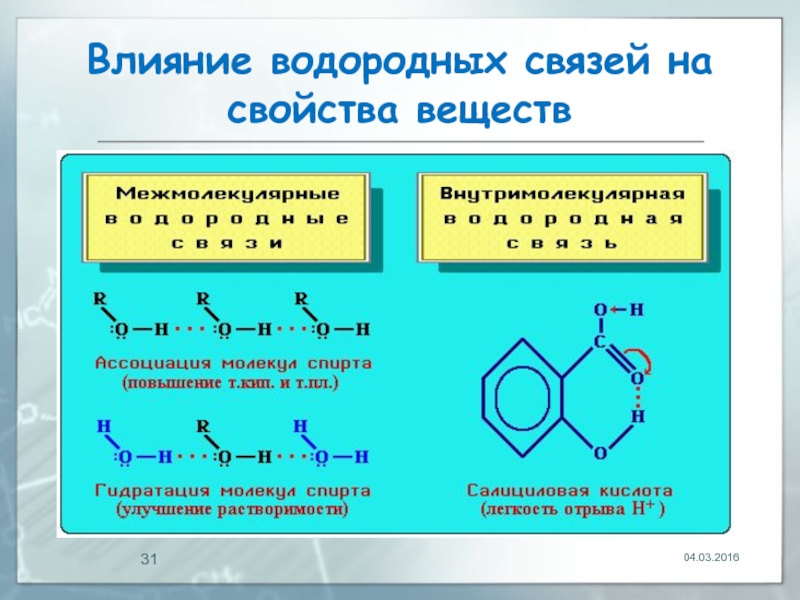
Слайд 30Влияние водородных связей на свойства веществ
Внутримолекулярная водородная связь образуется при благоприятном
Например, Н-связь внутри молекул салициловой кислоты повышает ее кислотность.
04.03.2016
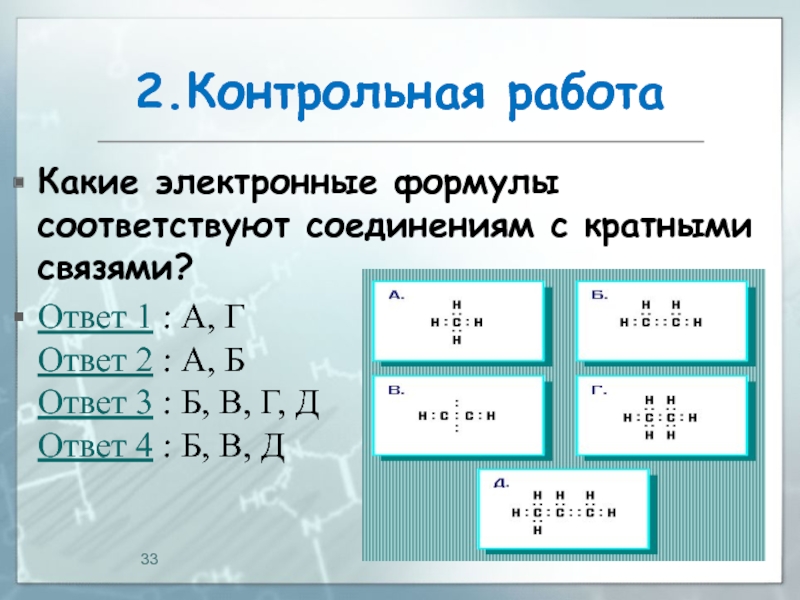
Слайд 332.Контрольная работа
Какие электронные формулы соответствуют соединениям с кратными связями?
Ответ 1 :
04.03.2016
Слайд 343.Контрольная работа
В каких молекулах имеются делокализованные p-связи?
а) CH2=CH-CH2-CH=CH2
б) CH2=CH-CH=CH2
в)
Ответ 1 : а, б Ответ 2 : б, в Ответ 3 : б Ответ 4 : а
04.03.2016
Слайд 354.Контрольная работа
Укажите соединения, в которых есть атомы водорода, способные к образованию
а) CH3-O-CH3
б) CH3-NH2
в) CH3-CH3
г) CH3-OH
Ответ 1 : а, г Ответ 2 : б, г Ответ 3 : а, б, г Ответ 4 : б, в, г
04.03.2016