- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Коллоидная химия. Введение презентация
Содержание
- 1. Коллоидная химия. Введение
- 2. Коллоидная химия (от греч. κόλλα — клей) - физическая
- 3. Основные понятия в коллоидной химии Дисперсные системы
- 5. Признаками дисперсных систем являются: - гетерогенность, т. е.
- 6. Степень раздробленности дисперсной фазы характеризуется дисперсностью D.
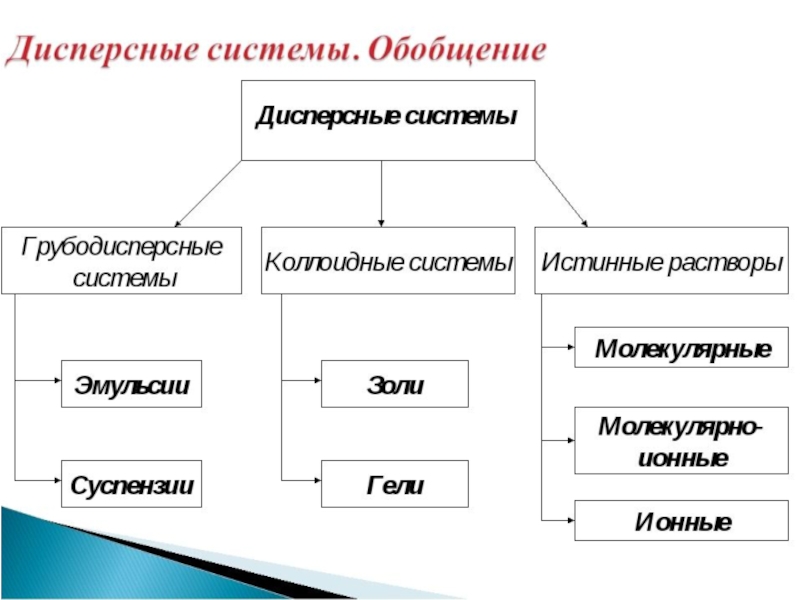
- 7. Классификация дисперсных систем 1а. Классификация дисперсных систем
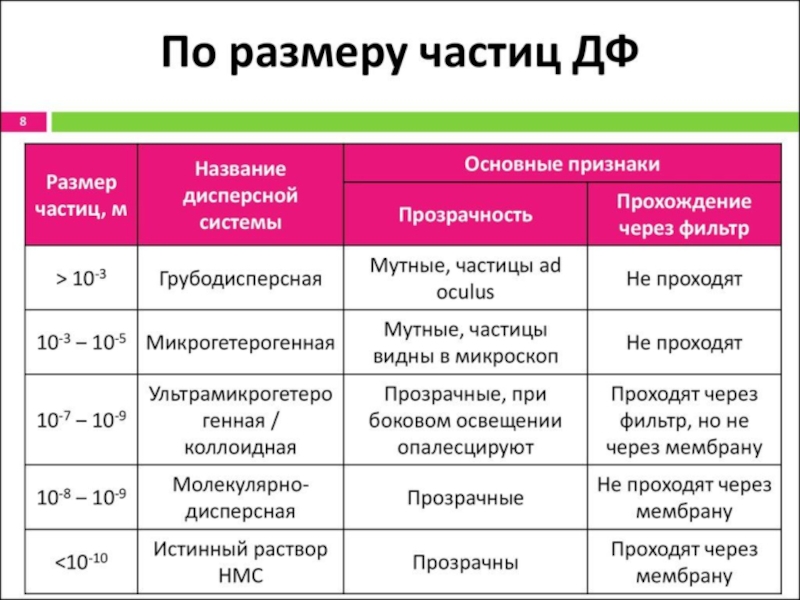
- 8. 1б. Классификация дисперсных систем по размерам
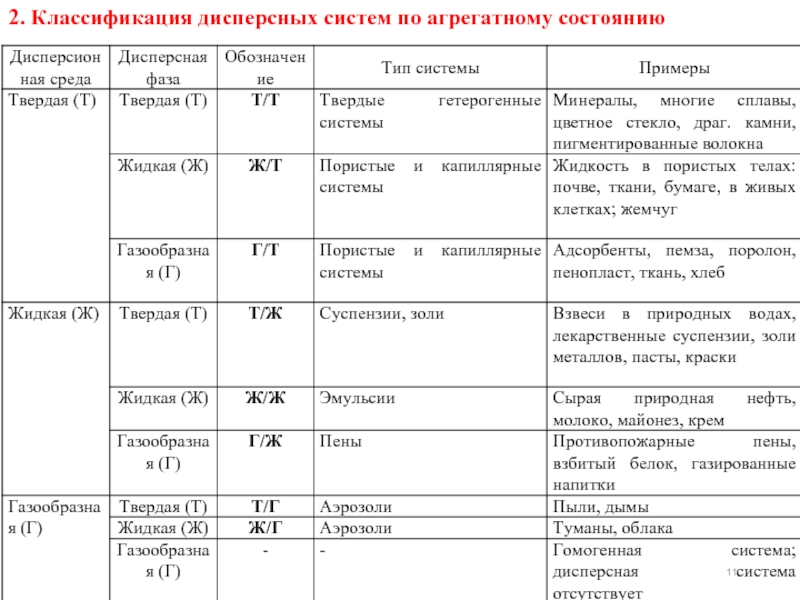
- 11. 2. Классификация дисперсных систем по агрегатному состоянию
- 13. 3. Классификация по характеру взаимодействия частиц со
Слайд 2Коллоидная химия (от греч. κόλλα — клей) - физическая химия поверхностных явлений и
Предметом изучения коллоидной химии являются гетерогенные смеси веществ (дисперсные системы), их свойства, процессы, протекающие в этих системах.
Задачи коллоидной химии – прогнозирование направления и изучение особенностей протекания физико-химических процессов в дисперсных системах.
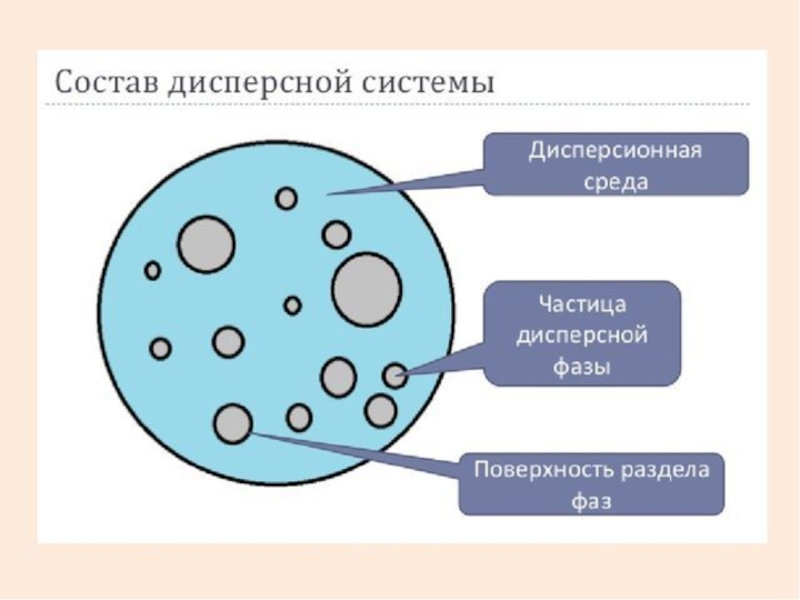
Слайд 3Основные понятия в коллоидной химии
Дисперсные системы – это двух- или в
Дисперсная фаза – это та часть дисперсной системы, которая раздроблена и распределена в дисперсионной среде.
Дисперсионная среда – это сплошная фаза, в которой распределено раздробленное вещество дисперсной фазы.
Слайд 5Признаками дисперсных систем являются:
- гетерогенность, т. е. наличие поверхности раздела между частицами
- дисперсность, т. е. раздробленность.
Различия дисперсных систем и истинных растворов
Слайд 6Степень раздробленности дисперсной фазы характеризуется дисперсностью D.
Дисперсность – это величина,
Слайд 7Классификация дисперсных систем
1а. Классификация дисперсных систем по степени дисперсности
- грубодисперсные системы
- тонкодисперсные (коллоидные системы) с размером частиц 10-9–10-5 м;
- молекулярно-дисперсные (истинные растворы) с размером частиц менее 10-9 м.
Слайд 133. Классификация по характеру взаимодействия частиц со средой
Лиофильные системы характеризуются тем, что
Лиофобные системы не образуют сольватной оболочки из дисперсионной среды вокруг частиц дисперсной фазы. В таких системах взаимодействие между частицами различных фаз значительно слабее. Значение межфазного поверхностного натяжения велико, вследствие чего система проявляет тенденции к самопроизвольному укрупнению частиц дисперсной фазы. Такие системы образуют неорганические и органические вещества плохо растворимые в данной среде.