- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Классы неорганических соединений презентация
Содержание
- 1. Классы неорганических соединений
- 2. Сложные вещества Оксиды Кислоты Основания Соли Основные
- 3. Вещества, образованные атомами двух элементов, одним из которых является кислород Оксиды
- 4. Вещества, молекулы которых состоят из одного или
- 5. Вещества, образованные атомами металлов и гидроксогруппами. Основания
- 6. Вещества, образованные атомами металлов и кислотными остатками. Соли
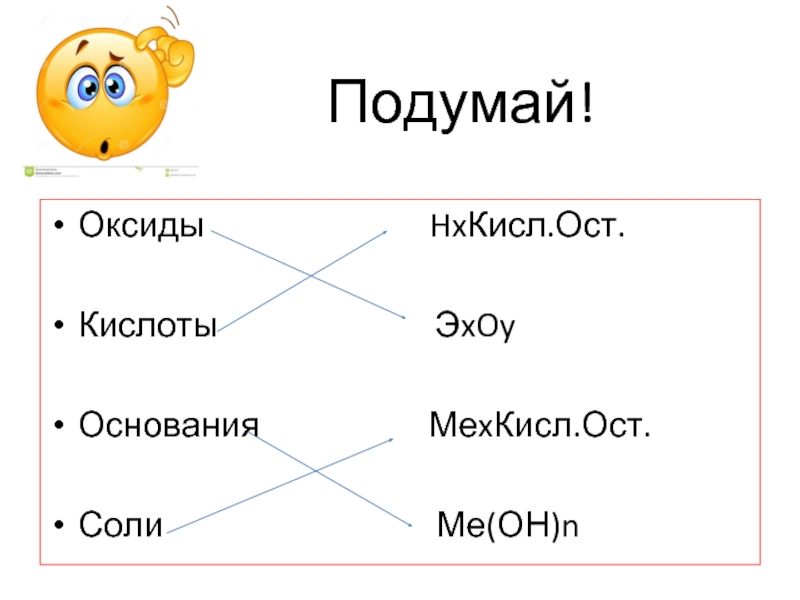
- 7. Подумай! Оксиды
- 8. Даны вещества: Na2O, H3PO4, KNO3, Ca(OH)2, AlCl3,
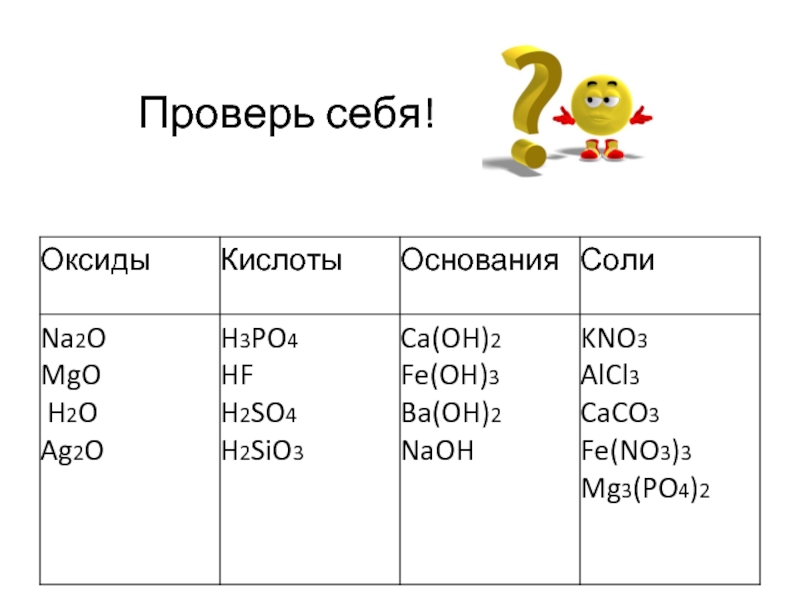
- 9. Проверь себя!
- 10. Химические свойства неорганических веществ
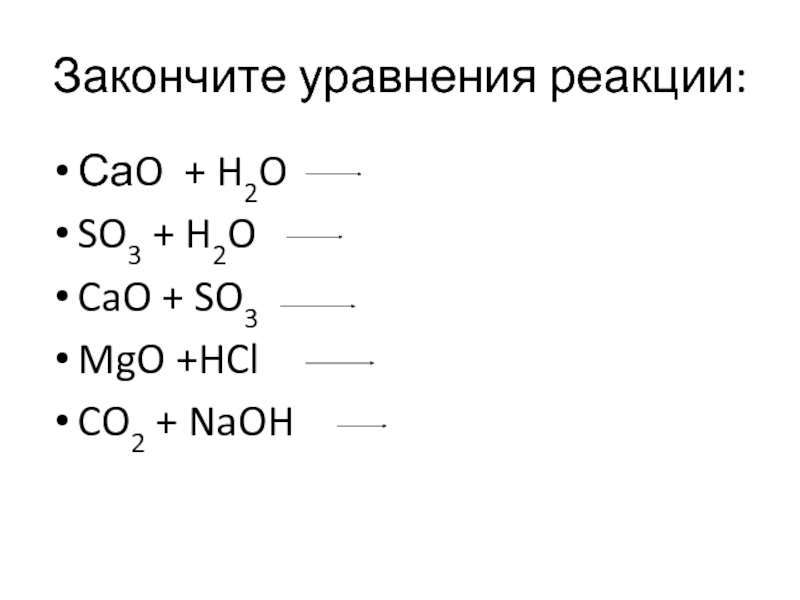
- 11. Закончите уравнения реакции: СаO + H2O
- 12. Правильные ответы СаO + H2O
- 13. Закончите уравнения осуществимых реакций: H2SO4 + Ba(OH)2
- 14. Проверьте себя H2SO4 + Ba(OH)2
- 15. Допишите уравнения химических реакций Ba(OH)2 + HNO3
- 16. Химические свойства оснований Ba(OH)2 + 2HNO3
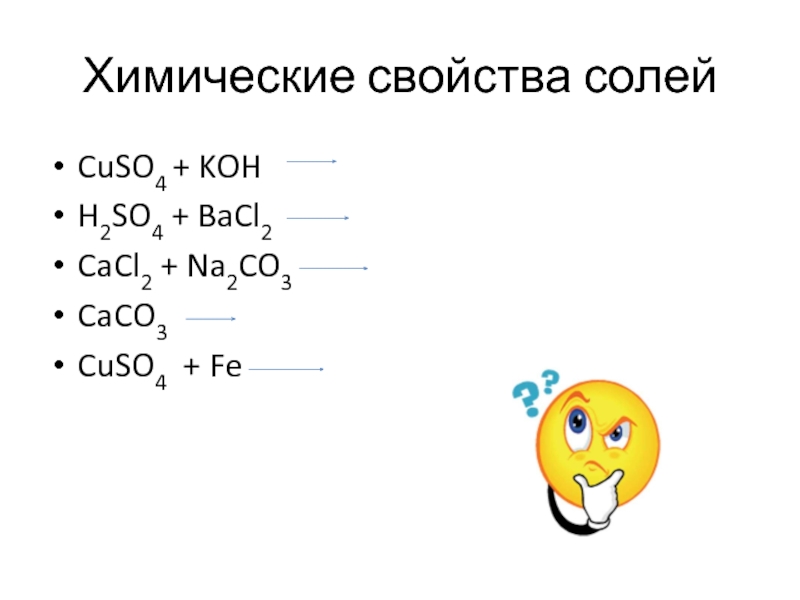
- 17. Химические свойства солей CuSO4 + KOH H2SO4
- 18. Проверь себя CuSO4 + 2KOH
- 19. ТЕСТ 1) Из предложенного перечня выберите основной
- 20. ОТВЕТЫ ТЕСТА 1) А 2) А 3)
- 21. Спасибо за работу!
Слайд 1Основные классы неорганических соединений
(повторение)
Основные классы неорганических соединений
Слайд 2Сложные вещества
Оксиды
Кислоты
Основания
Соли
Основные
Кислотные
Амфотерные
Бескислородные
Кислородсодержащие
Щелочи
Нерастворимые в воде
Средние
Кислые
Основные
Двойные
Слайд 4Вещества, молекулы которых состоят из одного или нескольких атомов водорода, способных
замещаться на атомы металлов, и кислотных остатков.
Кислоты
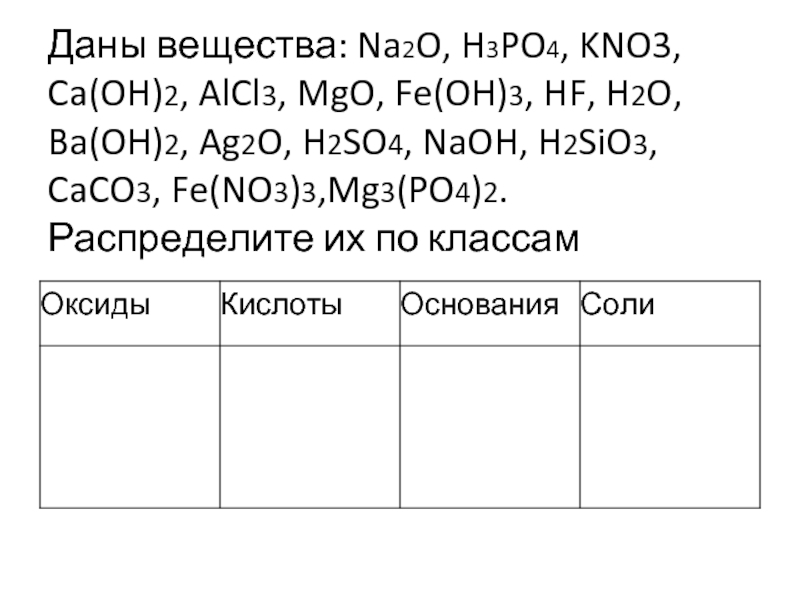
Слайд 8Даны вещества: Na2O, H3PO4, KNO3, Ca(OH)2, AlCl3, MgO, Fe(OH)3, HF, H2O,
Ba(OH)2, Ag2O, H2SO4, NaOH, H2SiO3, CaCO3, Fe(NO3)3,Mg3(PO4)2.Распределите их по классам
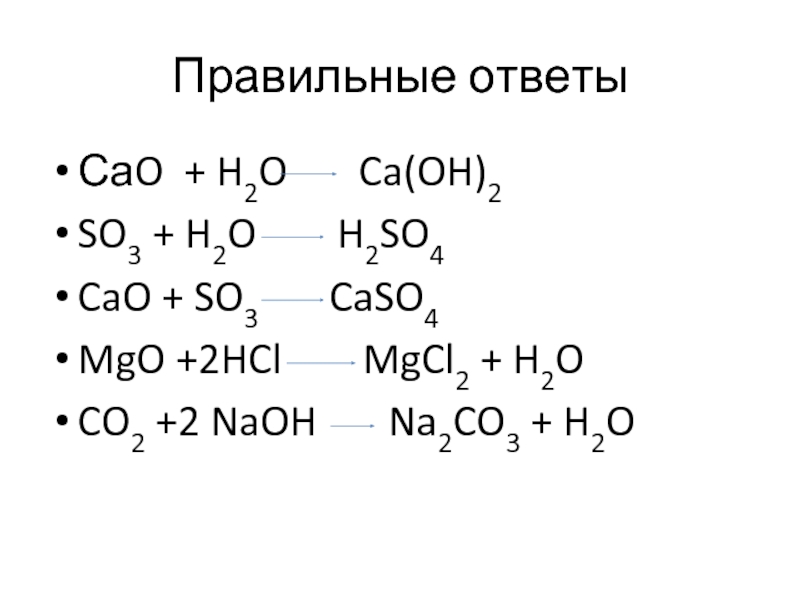
Слайд 12Правильные ответы
СаO + H2O Ca(OH)2
SO3 + H2O
H2SO4
CaO + SO3 CaSO4
MgO +2HCl MgCl2 + H2O
CO2 +2 NaOH Na2CO3 + H2O
CaO + SO3 CaSO4
MgO +2HCl MgCl2 + H2O
CO2 +2 NaOH Na2CO3 + H2O
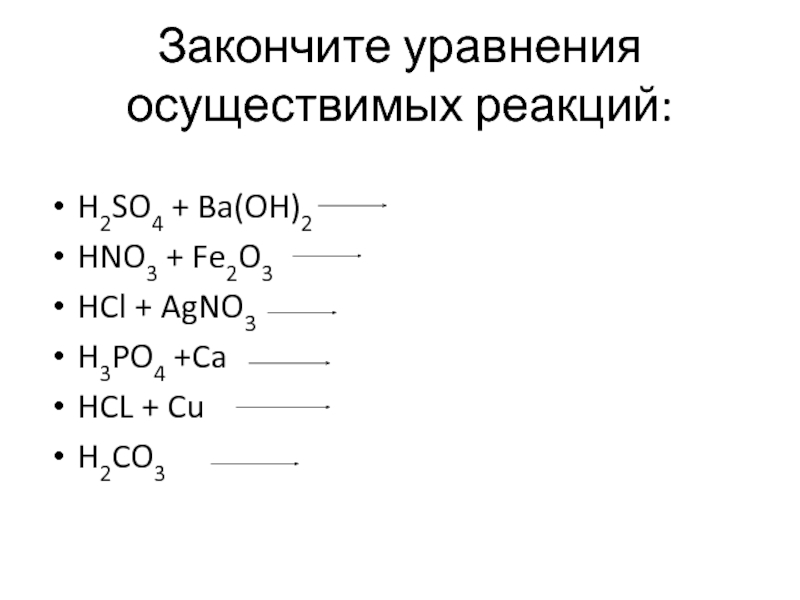
Слайд 13Закончите уравнения осуществимых реакций:
H2SO4 + Ba(OH)2
HNO3 + Fe2O3
HCl +
AgNO3
H3PO4 +Ca
HCL + Cu
H2CO3
H3PO4 +Ca
HCL + Cu
H2CO3
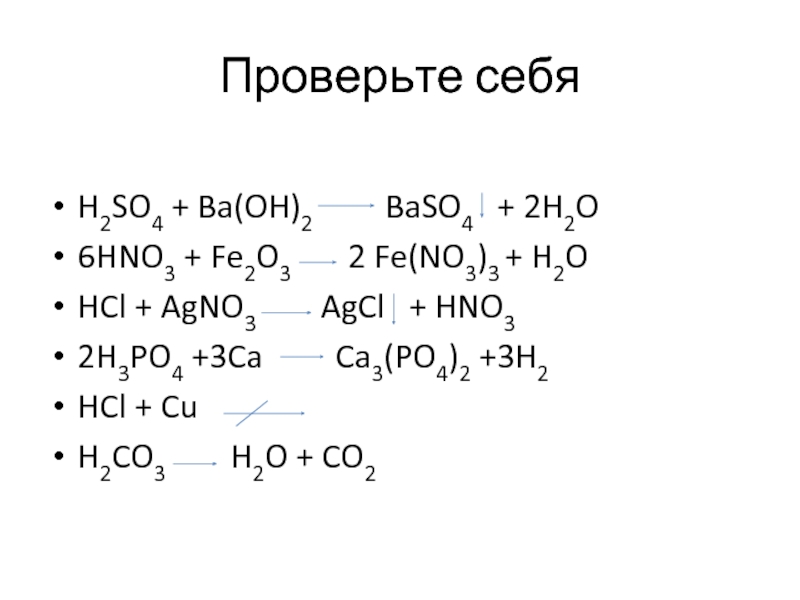
Слайд 14Проверьте себя
H2SO4 + Ba(OH)2 BaSO4 +
2H2O
6HNO3 + Fe2O3 2 Fe(NO3)3 + H2O
HCl + AgNO3 AgCl + HNO3
2H3PO4 +3Ca Ca3(PO4)2 +3H2
HCl + Cu
H2CO3 H2O + CO2
6HNO3 + Fe2O3 2 Fe(NO3)3 + H2O
HCl + AgNO3 AgCl + HNO3
2H3PO4 +3Ca Ca3(PO4)2 +3H2
HCl + Cu
H2CO3 H2O + CO2
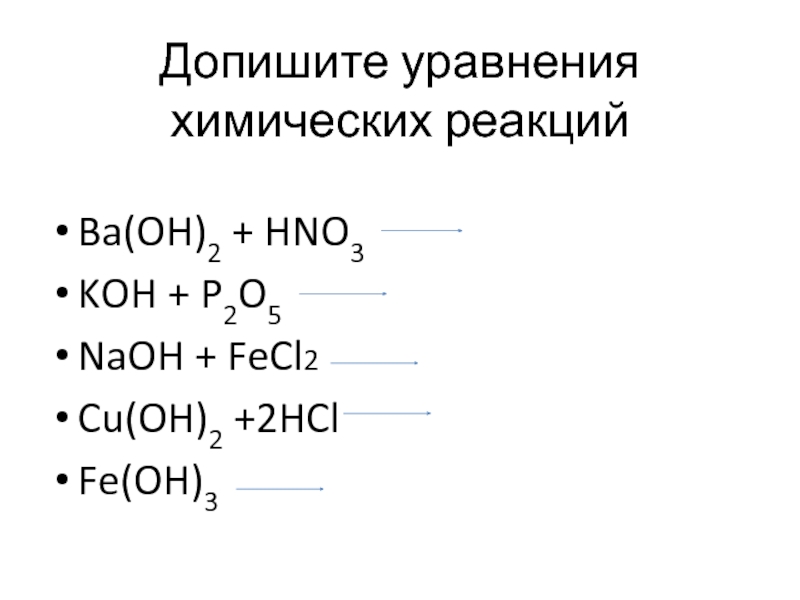
Слайд 15Допишите уравнения химических реакций
Ba(OH)2 + HNO3
KOH + P2O5
NaOH +
FeCl2
Cu(OH)2 +2HCl
Fe(OH)3
Cu(OH)2 +2HCl
Fe(OH)3
Слайд 16Химические свойства оснований
Ba(OH)2 + 2HNO3 Ba(NO)2 + 2H2O
6KOH +
P2O5 2 K3PO4 + 3H2O
2NaOH + FeCl2 Fe(OH)2 + 2NaCl
Cu(OH)2 +2HCL CuCl2 +2H2O
2Fe(OH)3 Fe2O3 + 3H2O
2NaOH + FeCl2 Fe(OH)2 + 2NaCl
Cu(OH)2 +2HCL CuCl2 +2H2O
2Fe(OH)3 Fe2O3 + 3H2O
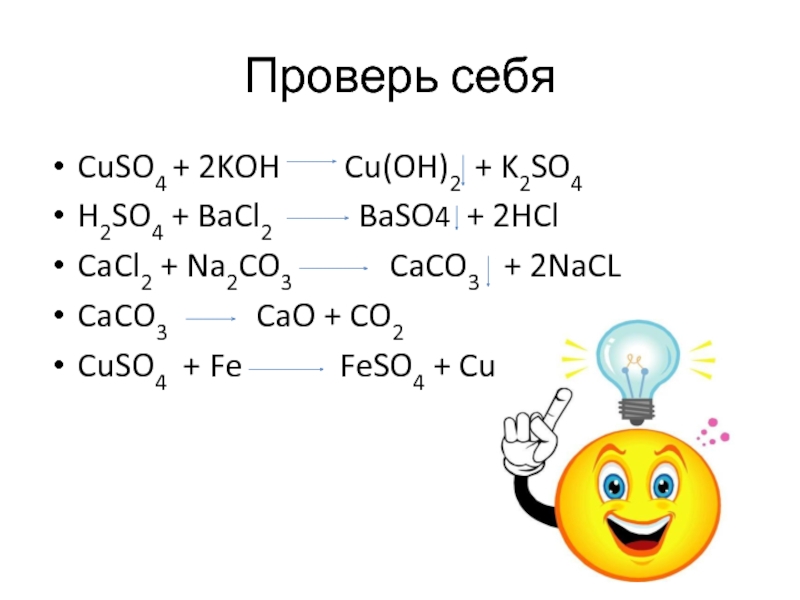
Слайд 18Проверь себя
CuSO4 + 2KOH Cu(OH)2 + K2SO4
H2SO4 +
BaCl2 BaSO4 + 2HCl
CaCl2 + Na2CO3 CaCO3 + 2NaCL
CaCO3 CaO + CO2
CuSO4 + Fe FeSO4 + Cu
CaCl2 + Na2CO3 CaCO3 + 2NaCL
CaCO3 CaO + CO2
CuSO4 + Fe FeSO4 + Cu
Слайд 19ТЕСТ
1) Из предложенного перечня выберите основной оксид
а) K2O
б) SO3 в) CO2
2) В результате взаимодействия с водой Na2O образуется
а) основание б) кислота в) соль
3) Какая из веществ в быту называется поваренной солью
а) Na2CO3 б) NaNO3 в) NaCl г) Na3PO4
4) Какой металл не реагирует с соляной кислотой
а) Mg б) Ag в) Fe
5)Что из перечисленного подходит гидроксиду натрия
а) щелочь б) двухосновная в) нерастворима в воде
6) Вещества какой пары могут реагировать между собой
а) СO2 + HCl б) CaO + HCl в) CaO + NaOH
2) В результате взаимодействия с водой Na2O образуется
а) основание б) кислота в) соль
3) Какая из веществ в быту называется поваренной солью
а) Na2CO3 б) NaNO3 в) NaCl г) Na3PO4
4) Какой металл не реагирует с соляной кислотой
а) Mg б) Ag в) Fe
5)Что из перечисленного подходит гидроксиду натрия
а) щелочь б) двухосновная в) нерастворима в воде
6) Вещества какой пары могут реагировать между собой
а) СO2 + HCl б) CaO + HCl в) CaO + NaOH
Слайд 20ОТВЕТЫ ТЕСТА
1) А
2) А
3) В
4) Б
5) А
6) Б
Критерии оценки:
1.6 правильных ответов
– 5
2.5 правильных ответов – 4
3.4 правильных ответа – 3
2.5 правильных ответов – 4
3.4 правильных ответа – 3