- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Кислоты. Соли (8 класс) презентация
Содержание
- 1. Кислоты. Соли (8 класс)
- 2. Соли
- 3. Соли
- 4. Исключение соли аммония, в которых с кислотными
- 5. Средними или нормальными солями называют соли, которые
- 6. Кислыми солями называют соли, которые образуются при
- 7. Основными солями называют соли, которые это продукты
- 8. Основными солями называют соли, которые это продукты
- 9. Двойными солями называют соли, которые содержат два
- 10. Обжиг минерала алунита K2SO4•Al2(SO4)3•Al(OH)3 с последующим выщелачиванием
- 11. Смешанными солями называют соли, которые содержат два
- 12. Комплексными солями называют соли, которые образуются в
- 13. Соли
- 14. 3. Взаимодействие солей с кислотами, щелочами, металлами,
- 15. Соли
- 16. Соли
Слайд 2
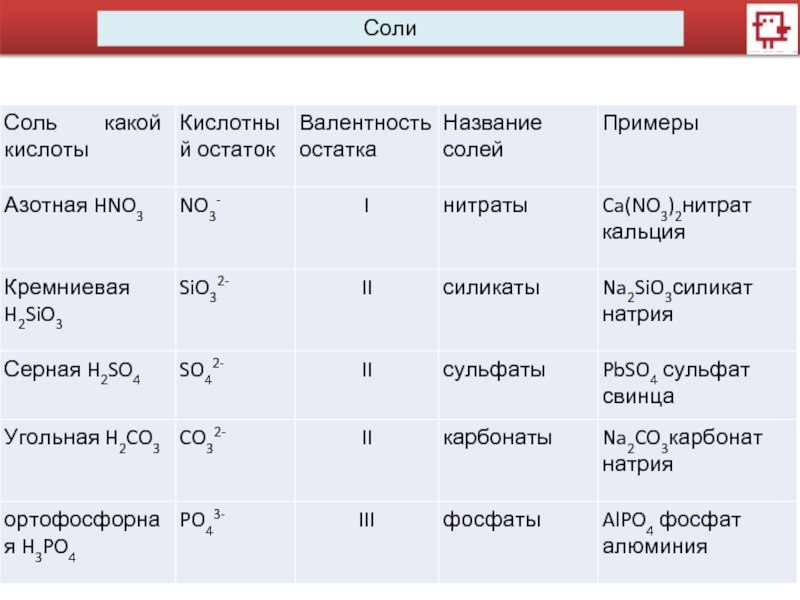
Соли
Соли – это сложные вещества, образованные атомами металлов и кислотными остатками.
Fe + 2HCl = FeCl2 + H2
Mg + H2SO4 = MgSO4 + H2
Fe2O3 + 6HCl = 2FeCl3 + 3H2O
Слайд 4Исключение соли аммония, в которых с кислотными остатками связаны не атомы
Соли аммония - это сложные вещества, в состав которых входят ионы аммония NH4+, соединённые с кислотными остатками.
Например,
NH4Cl – хлорид аммония
(NH4)2SO4 - сульфат аммония
NH4NO3 – нитрат аммония
(NH4)3PO4 – ортофосфат аммония
(NH4)2HPO4 – гидроортофосфат аммония
NH4H2PO4 – дигидроортофосфат аммония
Соли
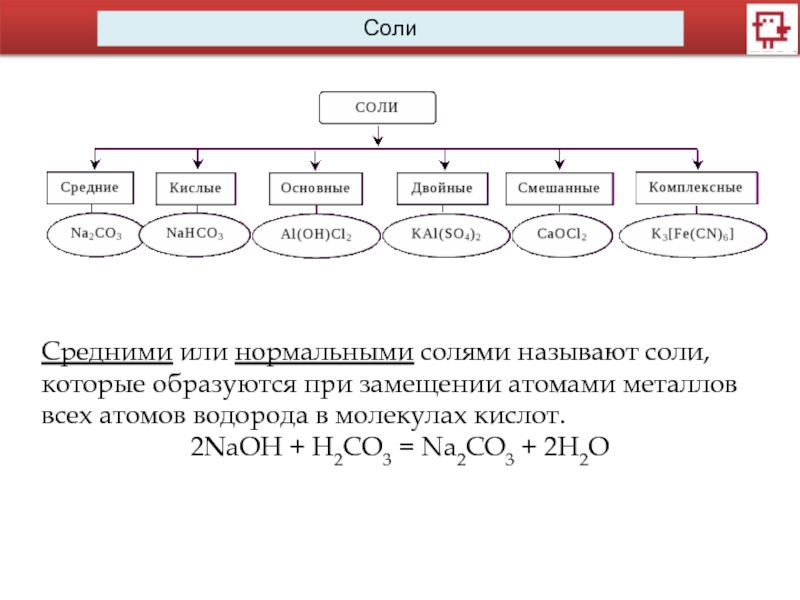
Слайд 5Средними или нормальными солями называют соли, которые образуются при замещении атомами
2NaOH + H2CO3 = Na2CO3 + 2H2O
Соли
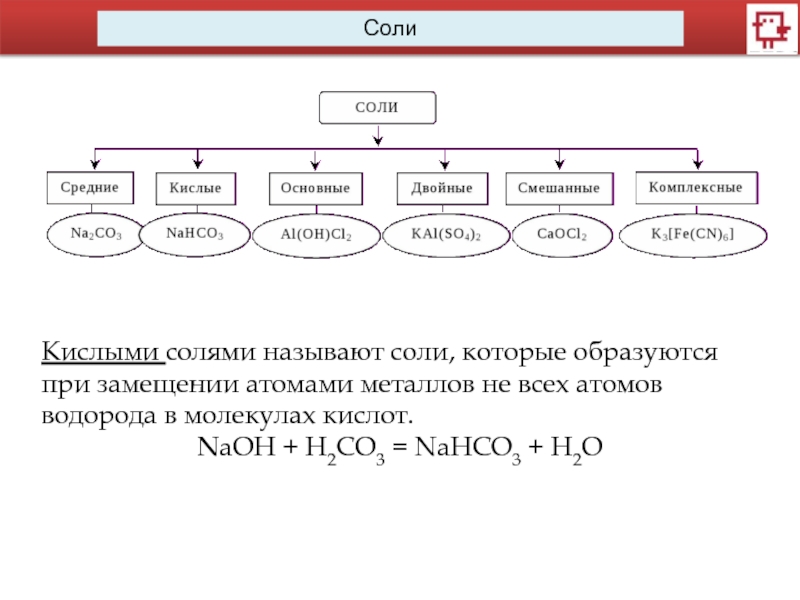
Слайд 6Кислыми солями называют соли, которые образуются при замещении атомами металлов не
NaOH + H2CO3 = NaНCO3 + H2O
Соли
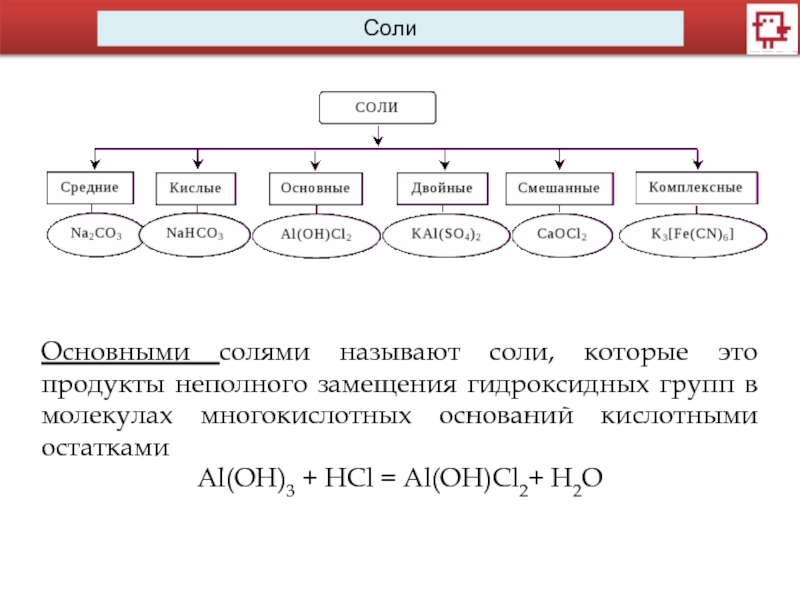
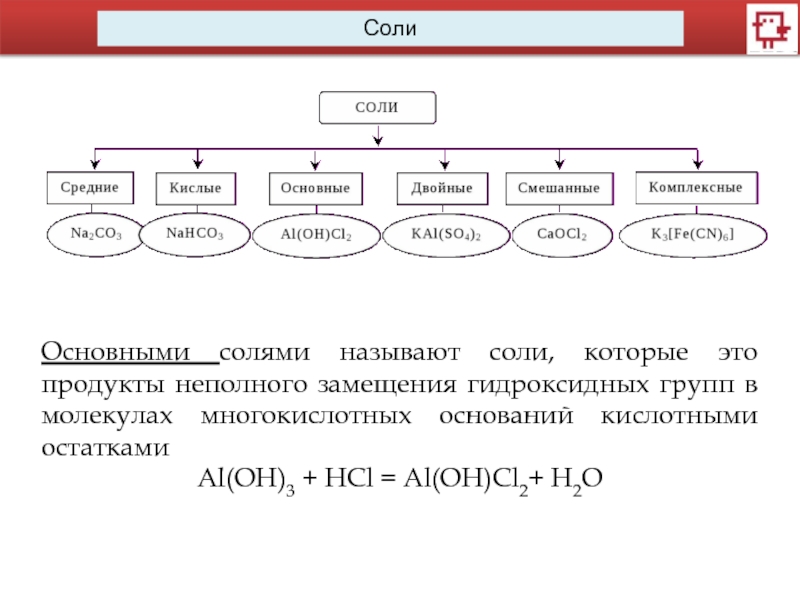
Слайд 7Основными солями называют соли, которые это продукты неполного замещения гидроксидных групп
Al(OH)3 + HCl = Al(OH)Cl2+ H2O
Соли
Слайд 8Основными солями называют соли, которые это продукты неполного замещения гидроксидных групп
Al(OH)3 + HCl = Al(OH)Cl2+ H2O
Соли
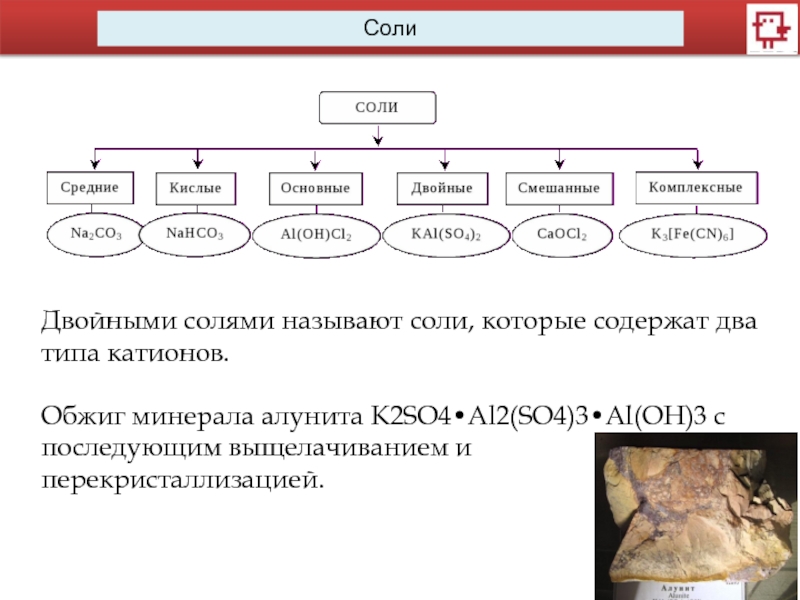
Слайд 9Двойными солями называют соли, которые содержат два типа катионов.
Обжиг минерала алунита
Соли
Слайд 10Обжиг минерала алунита K2SO4•Al2(SO4)3•Al(OH)3 с последующим выщелачиванием и перекристаллизацией.
Совместная кристаллизация сульфатов
Соли
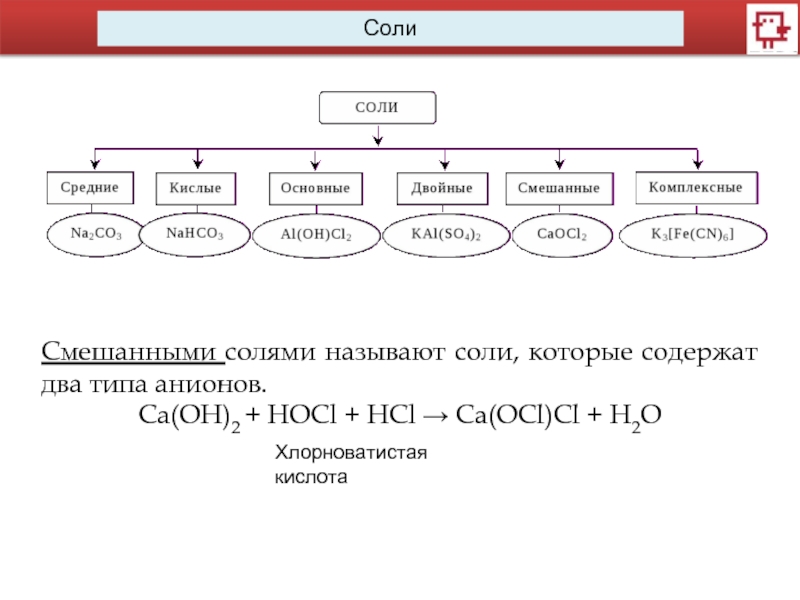
Слайд 11Смешанными солями называют соли, которые содержат два типа анионов.
Ca(OH)2 +
Соли
Хлорноватистая кислота
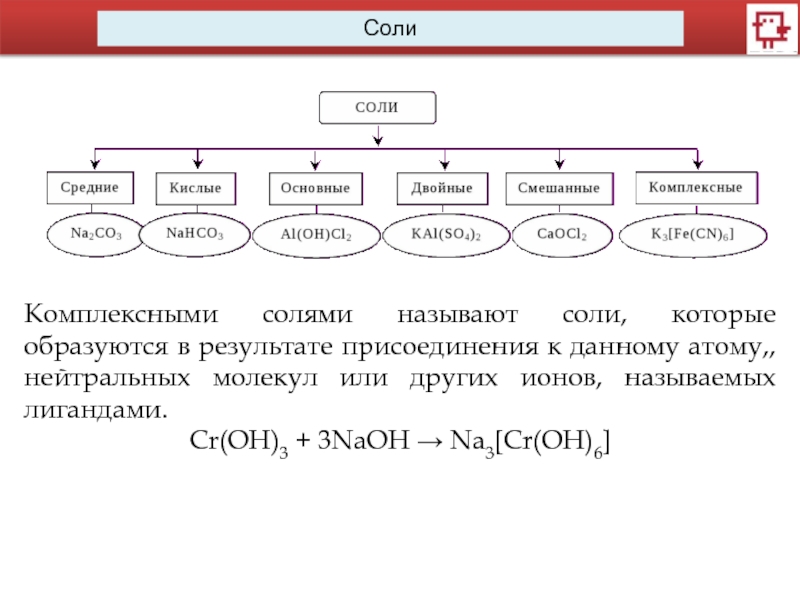
Слайд 12Комплексными солями называют соли, которые образуются в результате присоединения к данному
Cr(OH)3 + 3NaOH → Na3[Cr(OH)6]
Соли
Слайд 13
Соли
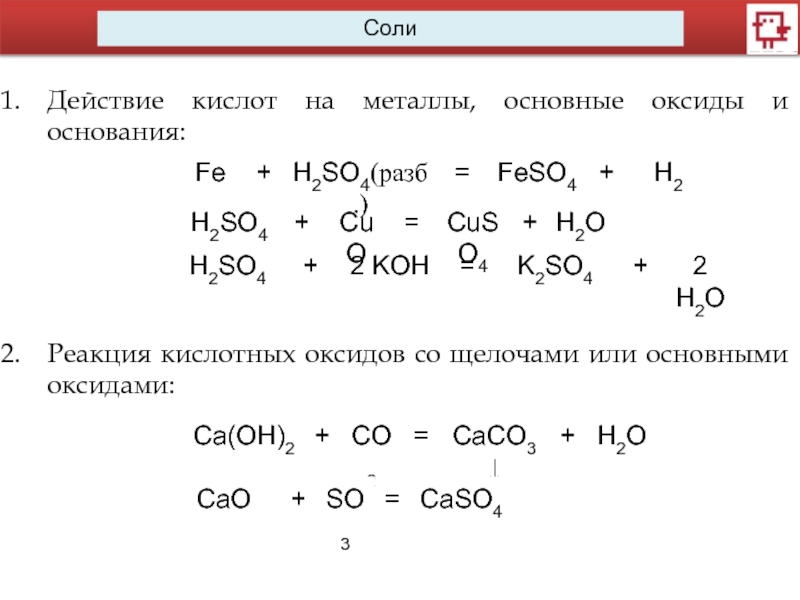
Действие кислот на металлы, основные оксиды и основания:
Реакция кислотных оксидов
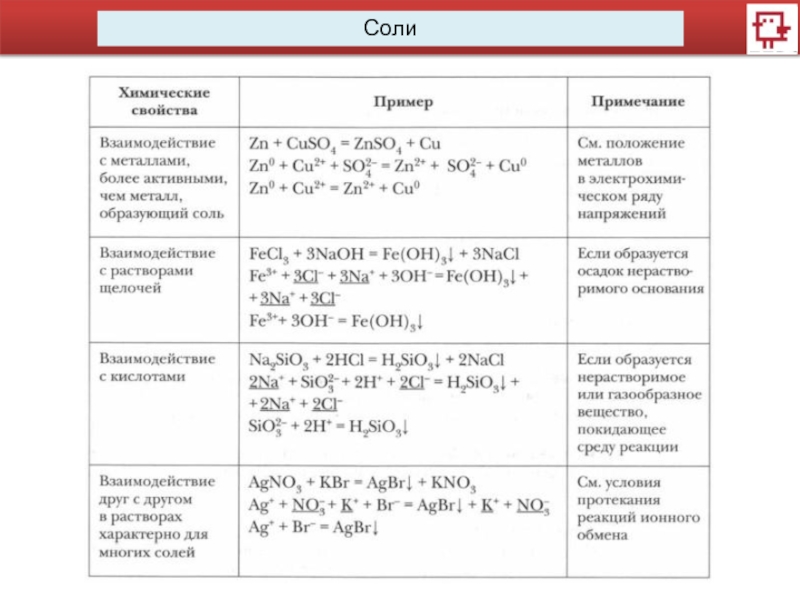
Слайд 143. Взаимодействие солей с кислотами, щелочами, металлами, нелетучими кислотными оксидами и
Ca3(PO4)2 +3H2SO4 = 3CaSO4 +2H3PO4
Fe2(SO4)3 + 6NaOH = 2Fe(OH)3 + 3Na2SO4
CuSO4 + Fe = FeSO4 + Cu
CaCO3 + SiO2 = CaSiO3 + CO2
Al2(SO4)3 + 3BaCl2 = 3BaSO4 +2AlCl3
4. Взаимодействие металлов с неметаллами:
Соли
Слайд 16
Соли
C какими из перечисленных ниже металлов будет взаимодействовать соляная кислота: 1)
Составьте уравнения реакций между серной кислотой и следующими веществами: а) магнием; б) оксидом магния; в) оксидом алюминия; г) оксидом калий; д) цинком.
Дайте названия следующим соединениям (солям): а) KCl; б) CaCO3; в) K3PO4; г) H2CO3; д) FeSO4; е) Fe2(SO4)3; ж) Cu(NO3)2.
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: