- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Ионное произведение воды. Водородный показатель презентация
Содержание
- 1. Ионное произведение воды. Водородный показатель
- 2. Содержание Электролитическая диссоциация воды Ионное произведение
- 3. Диссоциация воды Упрощенная запись уравнения диссоциации воды
- 4. Ионное произведение воды Kw
- 5. Концентрации ионов H+ и OH−
- 6. Водородный показатель рН pH =
- 7. Расчет рН 0,01 М раствора HBrO
- 8. Расчет рН 0,01 М раствора аммиака
- 9. Нейтральная среда
- 10. Значения рН в различных средах
- 11. Схема измерения рН раствора
- 12. Прибор для измерения рН рН-метр
- 13. Индикатор фенолфталеин преобладает молекулярная форма
- 14. Индикатор метиловый оранжевый преобладает
- 15. Кислотно-основные индикаторы
- 16. Ацетатный буферный раствор - – смесь уксусной
- 17. Аммиачный буферный раствор – – водный
- 18. Заключение Электропроводность чистой воды обусловлена ее автопротолизом.
- 19. Рекомендуемая литература Никольский А.Б., Суворов А.В.
Слайд 1ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА
ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА
Лекция 9
ИОННОЕ ПРОИЗВЕДЕНИЕ ВОДЫ.
ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ
Слайд 2Содержание
Электролитическая диссоциация воды
Ионное произведение воды
Водородный показатель (рН)
Определение рН водных растворов
Буферные растворы
Модуль
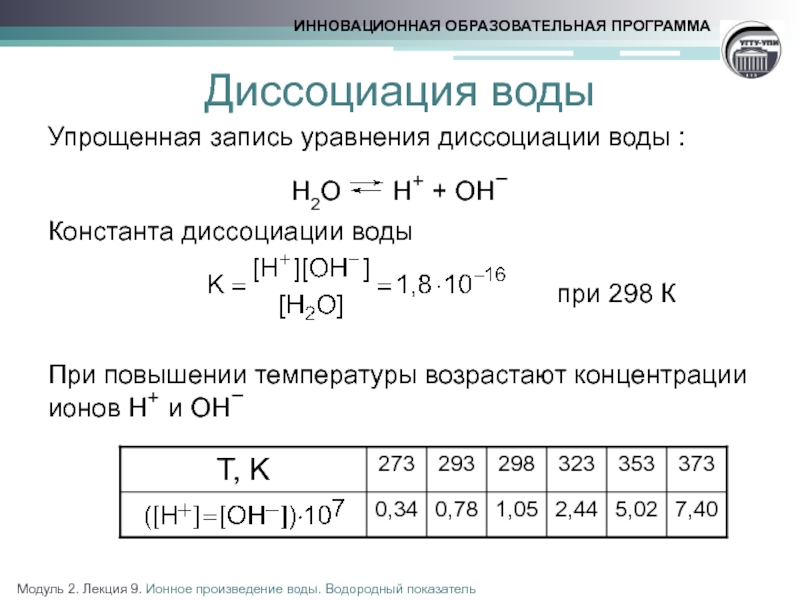
Слайд 3Диссоциация воды
Упрощенная запись уравнения диссоциации воды :
H2O H+ + OH−
Константа диссоциации воды
при 298 К
При повышении температуры возрастают концентрации
ионов H+ и OH−
Модуль 2. Лекция 9. Ионное произведение воды. Водородный показатель
Слайд 4Ионное произведение воды Kw
При повышении температуры Kw увеличивается
Модуль 2. Лекция 9. Ионное произведение воды. Водородный показатель
Слайд 5Концентрации ионов H+ и OH−
Расчет [H+] и [OH-] в 0,01
NaOH = Na+ + OH-
Модуль 2. Лекция 9. Ионное произведение воды. Водородный показатель
Слайд 6
Водородный показатель рН
pH = -lg [H+]
Расчет рН 0,01 М раствора
HCl = H+ + Cl−
Расчет рН 0,1 М раствора гидроксида калия
КОН = К+ + ОН-
Модуль 2. Лекция 9. Ионное произведение воды. Водородный показатель
Слайд 7Расчет рН 0,01 М раствора HBrO
HBrO - слабый электролит
[H+] = [BrO−]
Модуль 2. Лекция 9. Ионное произведение воды. Водородный показатель
Слайд 8Расчет рН 0,01 М раствора аммиака
Гидрат аммиака
Модуль 2. Лекция 9. Ионное произведение воды. Водородный показатель
рН=14 – 3,4 = 10,6
Слайд 9
Нейтральная среда
Кислая среда
Щелочная среда
Количественные
характеристики среды
Модуль 2. Лекция 9. Ионное произведение воды.
Слайд 10Значения рН в различных средах
Модуль 2. Лекция
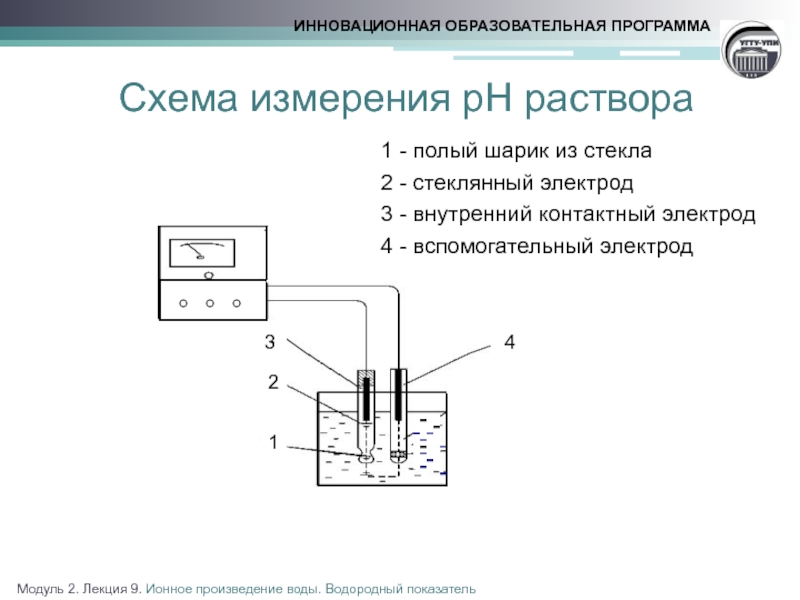
Слайд 11Схема измерения рН раствора
1 - полый шарик из стекла
2 - стеклянный электрод
3 - внутренний контактный электрод
4 - вспомогательный электрод
3
2
1
4
Модуль 2. Лекция 9. Ионное произведение воды. Водородный показатель
Слайд 12Прибор для измерения рН
рН-метр «ЭКСПЕРТ-рН»
Модуль 2. Лекция 9. Ионное произведение воды.
Слайд 13Индикатор фенолфталеин
преобладает
молекулярная форма
преобладает
ионная форма
HInd H+ +
бесцветный малиновый
Модуль 2. Лекция 9. Ионное произведение воды. Водородный показатель
Слайд 14Индикатор метиловый оранжевый
преобладает
молекулярная форма
преобладает
ионная форма
1
в нейтральной и
щелочной среде
рН
HInd H+ + Ind−
красный желтый
Модуль 2. Лекция 9. Ионное произведение воды. Водородный показатель
в кислой среде
Слайд 15Кислотно-основные индикаторы
метиловый оранжевый
лакмус
фенолфталеин
универсальный индикатор
рН
0
Модуль 2. Лекция 9. Ионное произведение воды. Водородный показатель
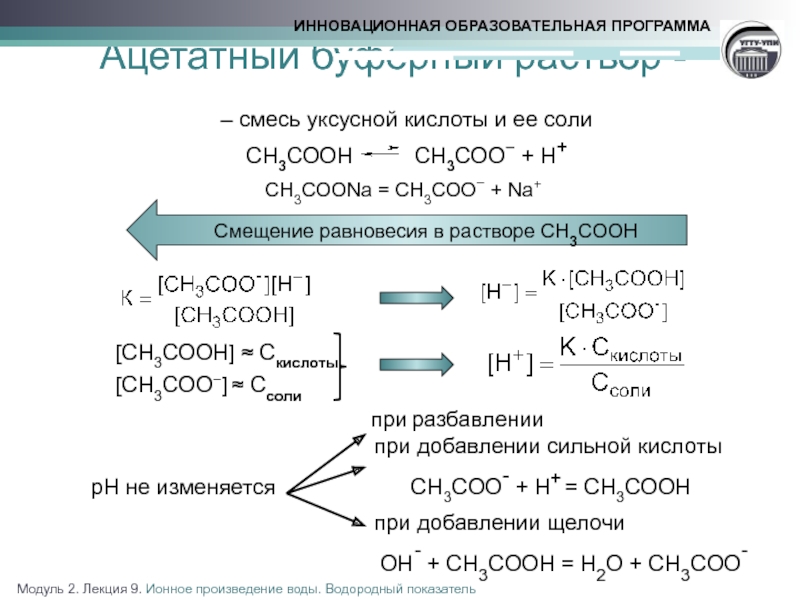
Слайд 16Ацетатный буферный раствор -
– смесь уксусной кислоты и ее соли
СН3СООН
СН3СООNa = СН3СОО− + Na+
[CH3COOH] ≈ Cкислоты
[CH3COO−] ≈ Ссоли
при разбавлении
при добавлении сильной кислоты
рН не изменяется CH3COO- + H+ = CH3COOH
при добавлении щелочи
OH‑ + CH3COOH = H2O + CH3COO‑
Смещение равновесия в растворе CH3COOH
Модуль 2. Лекция 9. Ионное произведение воды. Водородный показатель
Слайд 17
Аммиачный буферный раствор –
– водный раствор аммиака с добавлением соли аммония
при разбавлении
при добавлении сильной кислоты
pH не изменяется + H+ =
при добавлении щелочи
=
Модуль 2. Лекция 9. Ионное произведение воды. Водородный показатель
Смещение ионного равновесия в растворе аммиака
Слайд 18Заключение
Электропроводность чистой воды обусловлена ее автопротолизом. Вода проявляет свойства слабого электролита
Для
Водородный показатель рН является количественной характеристикой кислотности или щелочности среды
Определение рН проводят с помощью приборов (рН-метров); для приблизительной оценки рН используют кислотно-основные индикаторы
Буферные растворы применяют для создания и сохранения постоянства значений рН раствора в определенном диапазоне
Модуль 2. Лекция 9. Ионное произведение воды. Водородный показатель
Слайд 19Рекомендуемая литература
Никольский А.Б., Суворов А.В. Химия. - СПб: Химиздат, 2001
Степин
Карапетьянц М.Х. Общая и неорганическая химия. - М.: Химия, 2000
Угай Я.А. Общая и неорганическая химия. - М.: Высш. шк., 2007
Неорганическая химия. В 3 т. Т. 1: Физико-химические основы неорганической химии. Под ред. Ю. Д. Третьякова. - М.: Академия, 2004
Гаршин А.П. Неорганическая химия в схемах, рисунках, таблицах, формулах, химических реакциях. - СПб.: Лань, 2000
Модуль 2. Лекция 9. Ионное произведение воды. Водородный показатель



![Концентрации ионов H+ и OH− Расчет [H+] и [OH-] в 0,01 М растворе NaOHNaOH =](/img/tmb/5/481571/2593ae3f360e0f5fdf4a9b32d4c7b597-800x.jpg)
![Водородный показатель рНpH = -lg [H+] Расчет рН 0,01 М раствора соляной кислоты](/img/tmb/5/481571/0e253b80c3dd41970c342a38bbd4197c-800x.jpg)