- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Химический элемент сера презентация
Содержание
- 3. Физические свойства серы Твёрдое кристаллическое вещество желтого
- 4. Нахождение серы в природе Сера является на
- 5. Сера также встречается в виде сульфатов - солей серной кислоты - мирабилит
- 6. Пирит – «огненный камень» (соединение серы в природе)
- 7. В древности и в средние века
- 8. Сера входит в состав белков. Особенно много
- 9. Серой богаты бобовые растения (горох, чечевица), овсяные хлопья, яйца
- 11. Ромбическая сера Ромбическая (α-сера) – S8,
- 12. Моноклинная сера Моноклинная (β –сера)- S8,
- 13. Пластическая сера Пластическая сера- коричневая резиноподобная (аморфная)
- 14. Химические свойства серы (восстановительные) Сера проявляет в
- 15. Химические свойства серы (окислительные) S0 + 2ē
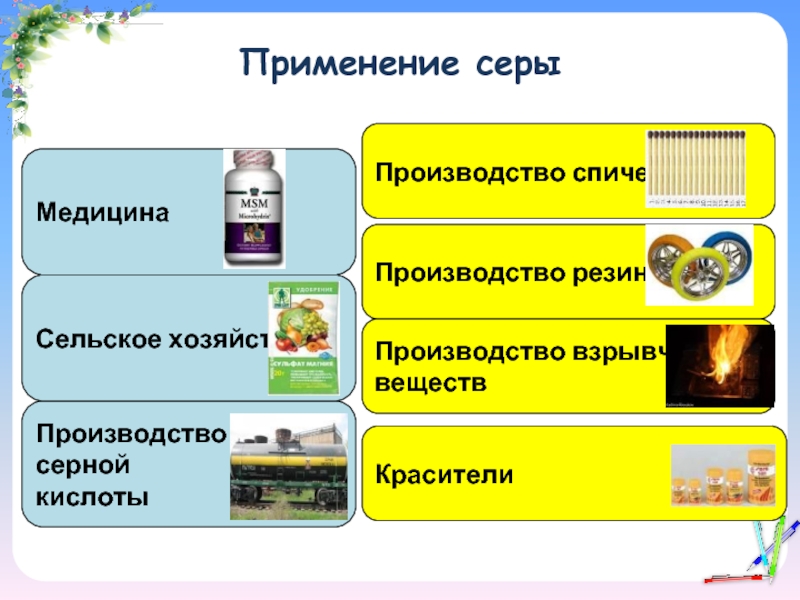
- 16. Применение серы Медицина Производство серной кислоты
Слайд 2 Валентные состояния атома серы S
Валентность II,
ст. окисления -2
3s 3p 3d
Валентность IV,
Ст. окисления +4
Валентность VI,
Ст. окисления +6
Н2S
SО2
Н2SО4
Слайд 3Физические свойства серы
Твёрдое кристаллическое вещество желтого цвета, без запаха
Плохо проводит теплоту
и не проводит электрический ток
Сера в воде практически не растворяется
Температура плавления 1200С
Сера в воде практически не растворяется
Температура плавления 1200С
Слайд 4Нахождение серы в природе
Сера является на 16-м месте по распространённости в земной
коре. Встречается в свободном (самородном) состоянии и связанном виде.
Слайд 7
В древности и в средние века серу добывали, вкапывая в землю
большой глиняный горшок, на который ставили другой, с отверстием в дне. Последний заполняли породой, содержащей серу, и затем нагревали. Сера плавилась и стекала в нижний горшок.
В настоящее время серу получают главным образом путём выплавки самородной серы непосредственно в местах её залегания под землёй. Серные руды добывают разными способами — в зависимости от условий залегания. Залежам серы почти всегда сопутствуют скопления ядовитых газов — соединений серы. К тому же нельзя забывать о возможности её самовозгорания.
Слайд 8Сера входит в состав белков. Особенно много серы в белках волос,
рогов, шерсти. Кроме этого сера является составной частью биологически активных веществ: витаминов и гормонов. При недостатке серы в организме наблюдается хрупкость и ломкость костей, выпадение волос.
Сера в природе
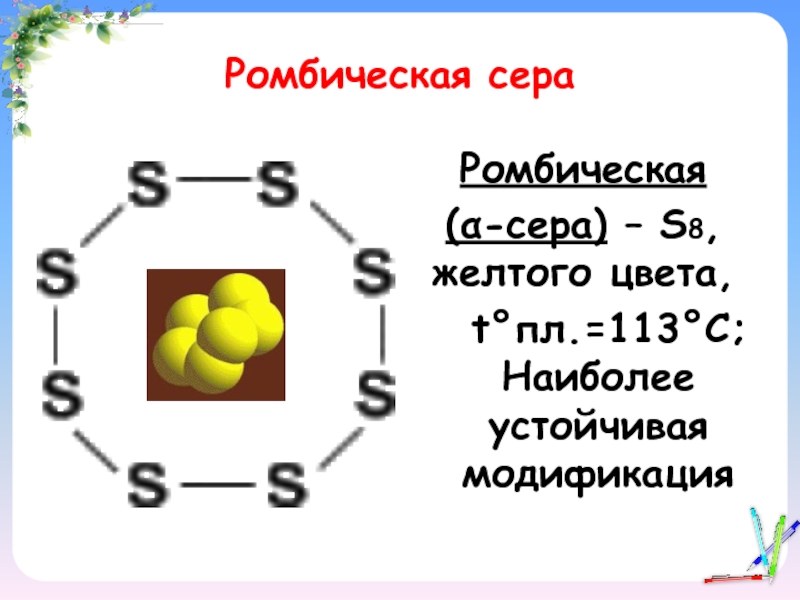
Слайд 11Ромбическая сера
Ромбическая
(α-сера) – S8, желтого цвета,
t°пл.=113°C; Наиболее устойчивая
модификация
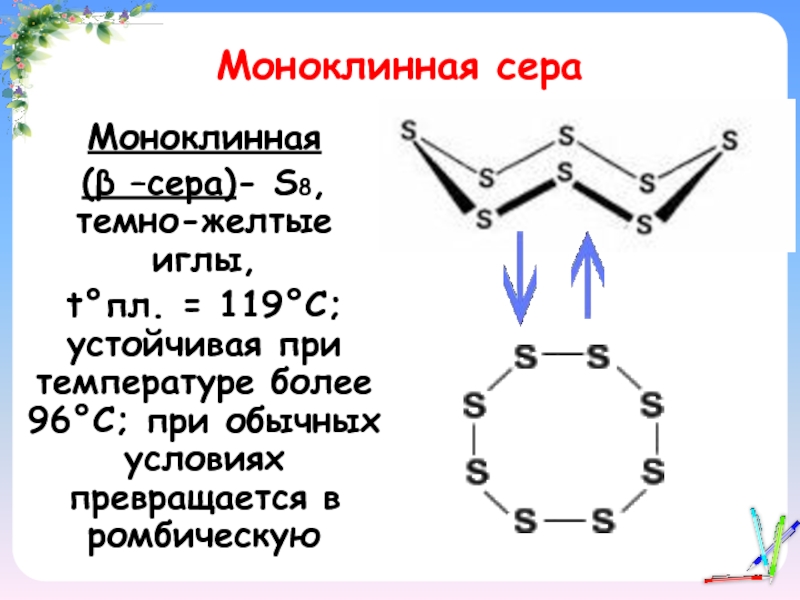
Слайд 12Моноклинная сера
Моноклинная
(β –сера)- S8, темно-желтые иглы,
t°пл. = 119°C; устойчивая при
температуре более 96°С; при обычных условиях превращается в ромбическую
Слайд 13Пластическая сера
Пластическая сера- коричневая резиноподобная (аморфная) масса.
Она неустойчива и через некоторое
время становится хрупкой, приобретёт желтый цвет, т.е
превращается в ромбическую серу
превращается в ромбическую серу
Слайд 14Химические свойства серы (восстановительные)
Сера проявляет в реакциях с сильными окислителями:
S
- 2ē → S+2; S - 4ē → S+4; S - 6ē → S+6
1) C кислородом:
S + O2 t°→ S+4O2
2S + 3O2 t°;Рt→ 2S+6O3
2) С галогенами (кроме йода)
S + Cl2 → S+2Cl2
3) С кислотами - окислителями:
S + 2H2SO4(конц) → 3S+4O2 + 2H2O
S + 6HNO3(конц) → H2S+6O4 + 6NO2 + 2H2O
1) C кислородом:
S + O2 t°→ S+4O2
2S + 3O2 t°;Рt→ 2S+6O3
2) С галогенами (кроме йода)
S + Cl2 → S+2Cl2
3) С кислотами - окислителями:
S + 2H2SO4(конц) → 3S+4O2 + 2H2O
S + 6HNO3(конц) → H2S+6O4 + 6NO2 + 2H2O
Слайд 15Химические свойства серы (окислительные)
S0 + 2ē → S-2
4) Сера реагирует со
щелочными металлами без нагревания:
2Na + S → Na2S
c остальными металлами (кроме Au, Pt) - при повышенной t°:
2Al + 3S –t°→ Al2S3
Cu + S –t°→ CuS
5) С некоторыми неметаллами сера образует бинарные соединения:
H2 + S → H2S
2P + 3S → P2S3
C + 2S → CS2
2Na + S → Na2S
c остальными металлами (кроме Au, Pt) - при повышенной t°:
2Al + 3S –t°→ Al2S3
Cu + S –t°→ CuS
5) С некоторыми неметаллами сера образует бинарные соединения:
H2 + S → H2S
2P + 3S → P2S3
C + 2S → CS2