- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Химический элемент хлор презентация
Содержание
- 1. Химический элемент хлор
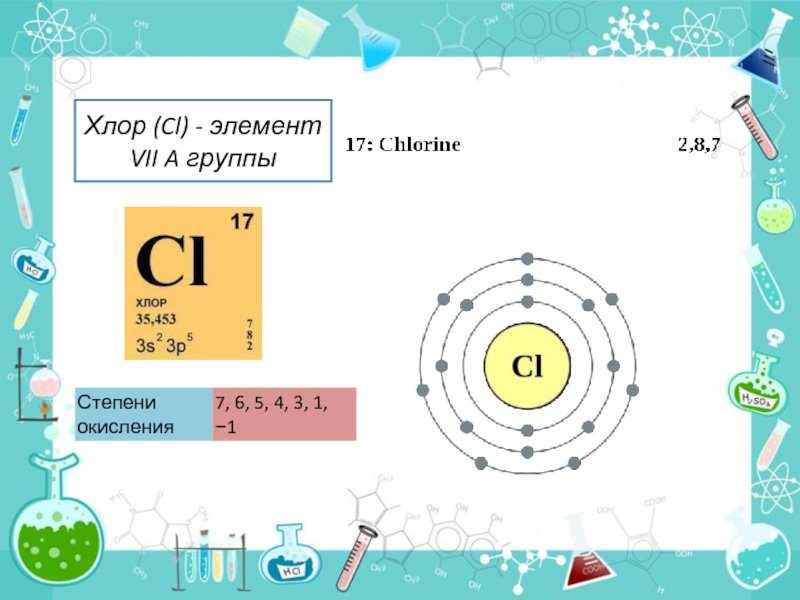
- 2. Хлор (Cl) - элемент VII A группы
- 3. История открытия Впервые хлор был получен в 1772 г. Шееле:
- 4. Распространение в природе Хлор – активный элемент
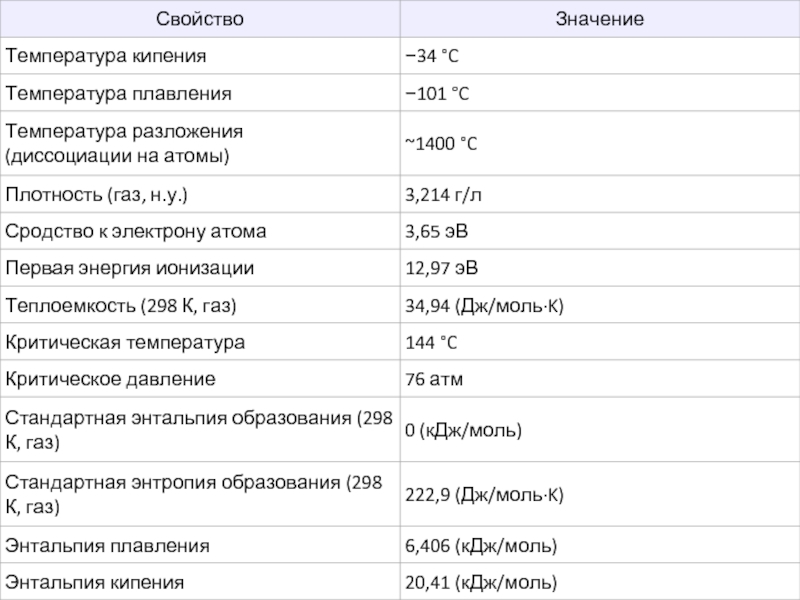
- 6. Физические свойства При н.у. хлор -ядовитый газ желтовато-зелёного цвета, с
- 8. Химические свойства В колбу с хлором капнули
- 9. Хлор очень сильный окислитель Cl2+2Na=2NaCl
- 10. Применения хлора В производстве пластикатов, синтетического каучука и
- 11. Оконный профиль изготовленный из хлорсодержащих полимеров Основным компонентом отбеливателей является хлорная вода
- 12. Хлор — токсичный удушливый газ, при попадании
Слайд 3История открытия
Впервые хлор был получен в 1772 г. Шееле:
4HCl + MnO2 = Cl2 + MnCl2 + 2H2O
Однако Шееле
И только Дэви удалось электролизом разложить поваренную соль на натрий и хлор.
Слайд 4Распространение в природе
Хлор – активный элемент
В природе он встречается только в
сильвина KCl,
сильвинита KCl · NaCl,
бишофита MgCl2 · 6H2O,
карналлита KCl · MgCl2 · 6Н2O,
каинита KCl · MgSO4 · 3Н2О.
Самые большие запасы хлора содержатся в составе солей вод морей и океанов.
В организме человека и животных хлор содержится в основном в межклеточных жидкостях (в том числе в крови) и играет важную роль в регуляции осмотических процессов, а также в процессах, связанных с работой нервных клеток.
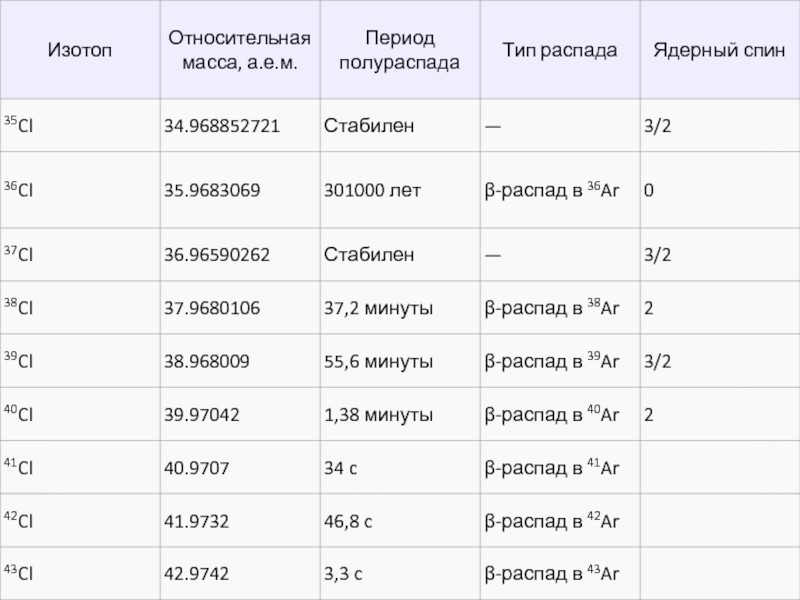
В природе встречаются 2 стабильных изотопа хлора: с массовым числом 35 и 37.
Слайд 6Физические свойства
При н.у. хлор -ядовитый газ желтовато-зелёного цвета, с резким, удушающим запахом.
По электропроводности жидкий хлор
Слайд 8Химические свойства
В колбу с хлором капнули несколько капель концентрированного раствора аммиака.
В условиях нашего опыта хлористый азот моментально разлагается, чем и объясняется треск и маленькие вспышки в колбе
В результате взаимодействия хлора с аммиаком образуется NСl3 (хлористый азот, взрывчатая желтая маслянистая жидкость) по уравнению:
4NН3 + ЗСl2 = NСl3 + ЗNН4Сl
Слайд 10Применения хлора
В производстве пластикатов, синтетического каучука и др.
Для отбеливания в текстильной и
Производство веществ, убивающих вредных для посевов насекомых, но безопасные для растений.
Использовался как боевое отравляющее вещество (слезоточивый газ), а так же для производства других боевых отравляющих веществ: иприт, фосген.
Для обеззараживания воды — «хлорирования».
В пищевой промышленности зарегистрирован в качестве пищевой добавки E925.
В химическом производстве ядов, лекарств, удобрений.
В металлургии для производства чистых металлов: титана, олова, тантала, ниобия.
Как индикатор солнечных нейтрино в хлор-аргонных детекторах.
Слайд 11Оконный профиль изготовленный из хлорсодержащих полимеров
Основным компонентом отбеливателей является хлорная вода
Слайд 12Хлор — токсичный удушливый газ, при попадании в лёгкие вызывает ожог лёгочной ткани, удушье.
Раздражающее действие
Хлор был одним из первых химических отравляющих веществ, использованных Германией в Первую мировую войну.
При работе с хлором следует пользоваться защитной спецодеждой, противогазом, перчатками. Н
а короткое время защитить органы дыхания от попадания в них хлора можно тряпичной повязкой, смоченной раствором сульфита натрия Na2SO3 или тиосульфата натрия Na2S2O3.
© Wikipedia.org