- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Химические свойства солей презентация
Содержание
- 1. Химические свойства солей
- 2. № 1 № 2 № 3
- 3. Что общего между всеми этими картинками??? ХИМИЧЕСКИЕ СВОЙСТВА СОЛЕЙ. ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ
- 4. ХИМИЧЕСКИЕ СВОЙСТВА СОЛЕЙ § 47 Таблица 14
- 5. ЭТО НУЖНО ЗАПОМНИТЬ!!! Соли взаимодействуют с металлами
- 6. ПОЛУЧЕНИЕ СОЛЕЙ КИСЛОТА + МЕТАЛЛ, ОКСИД МЕ,
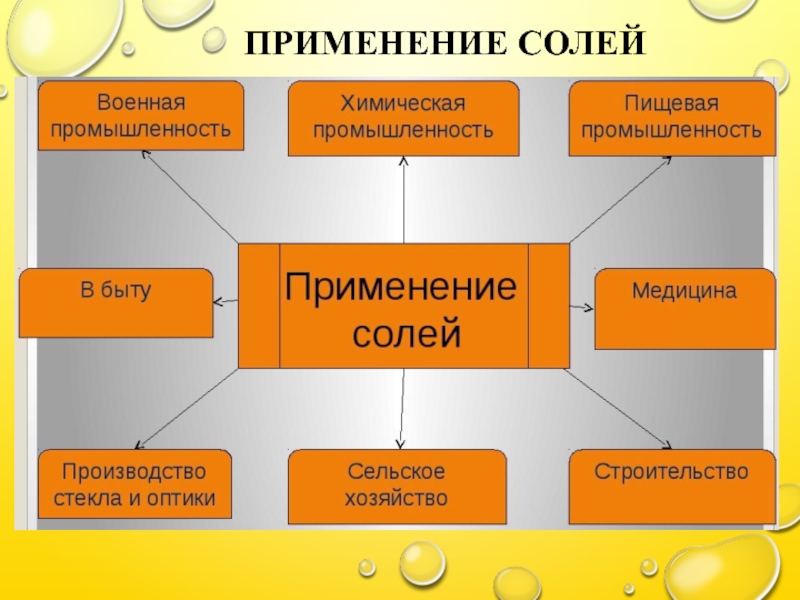
- 7. ПРИМЕНЕНИЕ СОЛЕЙ
- 8. ЗАКРЕПЛЕНИЕ Учебник § 47 № 1
- 9. НАПИШИТЕ УРАВНЕНИЕ РЕАКЦИИ ВЗАИМОДЕЙСТВИЯ АЛЮМИНИЯ С СЕРНОЙ КИСЛОТОЙ
- 10. ВЫБЕРИТЕ ИЗ ПЕРЕЧНЯ ТОЛЬКО СОЛИ И
- 11. ПЕРЕЧИСЛИТЕ, С КАКИМИ ВЕЩЕСТВАМИ ВЗАИМОДЕЙСТВУЮТ КИСЛОТЫ? ПРИ КАКИХ УСЛОВИЯХ ПРОИСХОДЯТ ЭТИ РЕАКЦИИ?
- 12. ЧТО ТАКОЕ ИНДИКАТОРЫ? ДЛЯ ЧЕГО ОНИ
- 13. ЧТО ТАКИЕ ОСНОВАНИЯ (ГИДРОКСИДЫ)? КАКИЕ ОСНОВАНИЯ (ГИДРОКСИДЫ) БЫВАЮТ?
- 14. НАПИШИТЕ УРАВНЕНИЕ ХИМИЧЕСКОЙ РЕАКЦИИ ВЗАИМОДЕЙСТВИЕ ГИДРОКСИДА КАЛИЯ С УГЛЕКИСЛЫМ ГАЗОМ
- 15. КАКИЕ СПОСОБЫ ПОЛУЧЕНИЯ ОСНОВАНИЙ (ГИДРОКСИДОВ) ВЫ МОЖЕТЕ ПРЕДЛОЖИТЬ?
Слайд 4ХИМИЧЕСКИЕ СВОЙСТВА СОЛЕЙ
§ 47
Таблица 14
FeSO4 + Cu
Реакция не идет, медь правее
FeCI3 + 3NaOH → Fe(OH)3↓ + 3NaCI
BaCI2 + Na2SO4 → BaSO4↓ + NaCI
H2O
CO2↑
СaO+ CO2↑
Слайд 5ЭТО НУЖНО ЗАПОМНИТЬ!!!
Соли взаимодействуют с металлами если, металл вступающий в химическую
Соли взаимодействуют с щелочами если, в результате реакции образуется нерастворимое вещество (осадок)
Соли взаимодействуют с кислотами если, соль образована более слабой кислотой чем та кислота, которая с ней вступает в реакцию. Соль образована летучей кислотой.
Соли взаимодействуют друг с другом если, в результате реакции образуется нерастворимое вещество (соль)
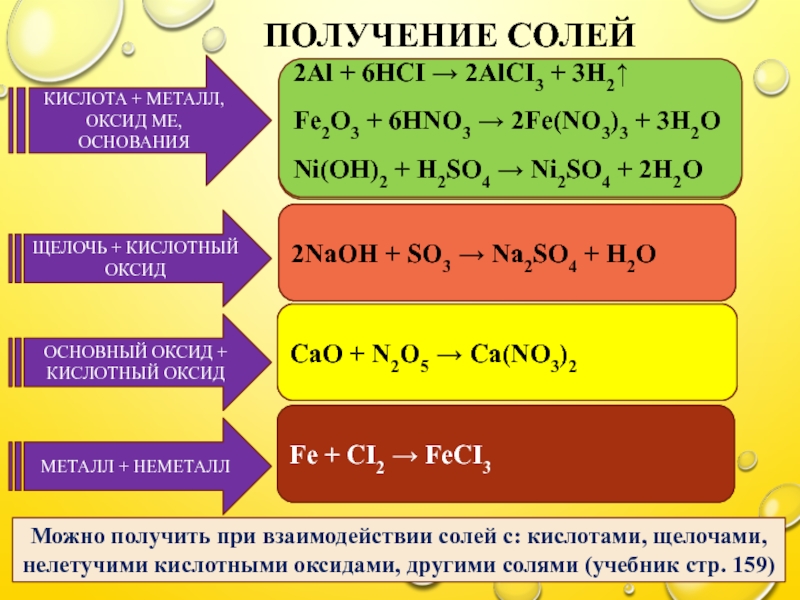
Слайд 6ПОЛУЧЕНИЕ СОЛЕЙ
КИСЛОТА + МЕТАЛЛ, ОКСИД МЕ, ОСНОВАНИЯ
Al + HCI → …
Fe2O3
Ni(OH)2 + H2SO4 → …
2Al + 6HCI → 2AlCI3 + 3H2↑
Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O
Ni(OH)2 + H2SO4 → Ni2SO4 + 2H2O
ЩЕЛОЧЬ + КИСЛОТНЫЙ ОКСИД
NaOH + SO3 → …
2NaOH + SO3 → Na2SO4 + H2O
ОСНОВНЫЙ ОКСИД + КИСЛОТНЫЙ ОКСИД
CaO + N2O5 → …
CaO + N2O5 → Ca(NO3)2
МЕТАЛЛ + НЕМЕТАЛЛ
Fe + CI2 → …
Fe + CI2 → FeCI3
Можно получить при взаимодействии солей с: кислотами, щелочами, нелетучими кислотными оксидами, другими солями (учебник стр. 159)