- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Химические свойства алкинов презентация
Содержание
- 1. Химические свойства алкинов
- 2. Цели урока: 1. Рассмотреть химические свойства алкинов:
- 3. 1. Повторение пройденного материала 2. Химические свойства алкинов 3. Применение алкинов 4.Закрепление
- 4. Тестирование 1. Общая формула гомологического ряда алкинов:
- 5. 2. Алкинам не свойственна изомерия: а)
- 6. 3.Укажите правильное название и точную характеристику алкина
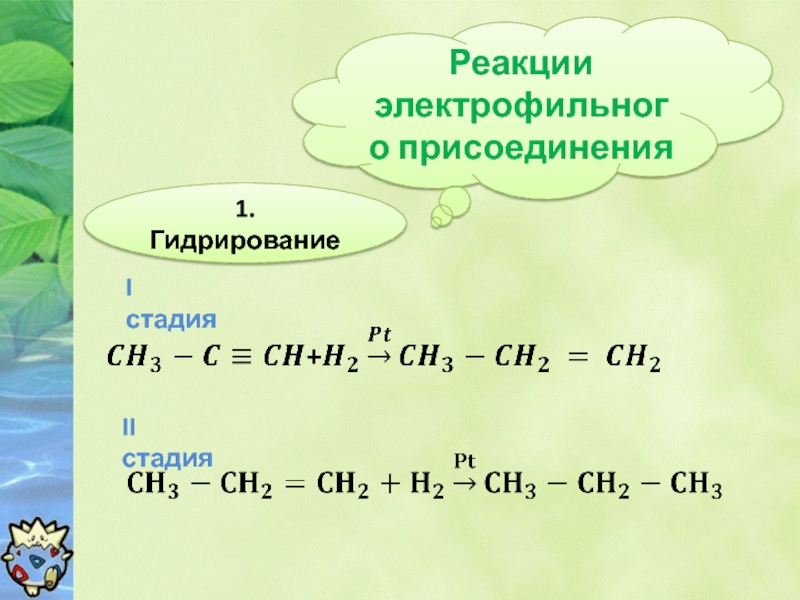
- 7. Реакции электрофильного присоединения 1. Гидрирование I стадия II стадия
- 8. Галогенирование (присоединение молекулы галогена-качественная реакция на алкины) I стадия II стадия
- 9. Гидрогалогенирования (присоединение галогенводорода) 2-бромпропен I стадия II стадия 2,2-дибромпропан По правилу Марковникова
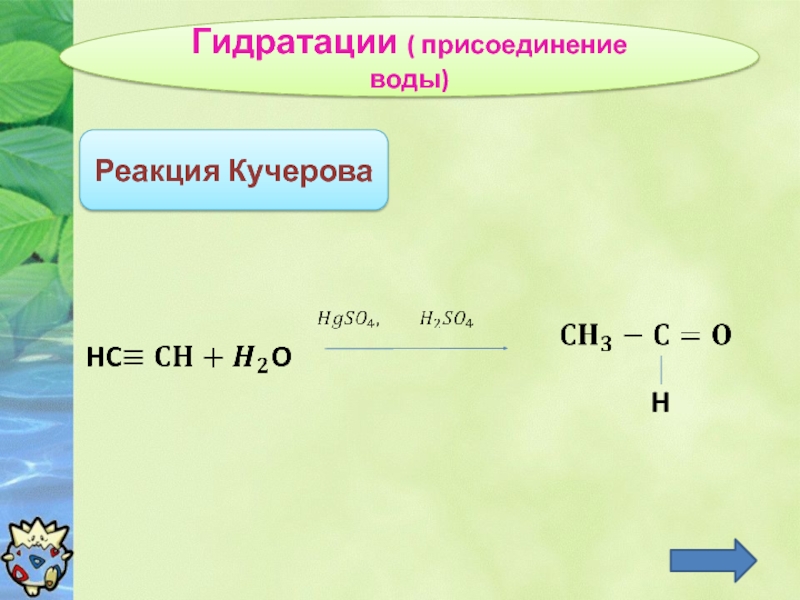
- 10. Гидратации ( присоединение воды) Реакция Кучерова H
- 11. В случае алкинов с более длинной цепью
- 12. Михаил Григорьевич Кучеров – русский химик-органик. Родился
- 13. Тримеризация При пропускании этина над активированным углем
- 14. Реакции окисления При полном сгорании ацетилена на
- 15. Кислотные свойства алкинов в терминальных алкинах (с
- 16. Алкины, как и алкены, обесцвечивают подкисленные растворы
- 17. Несколько иного типа реакция происходит между терминальными
- 18. Ацетилениды как соли слабых кислот легко разлагаются
- 19. Правило В.В.Марковникова: водород присоединяется к
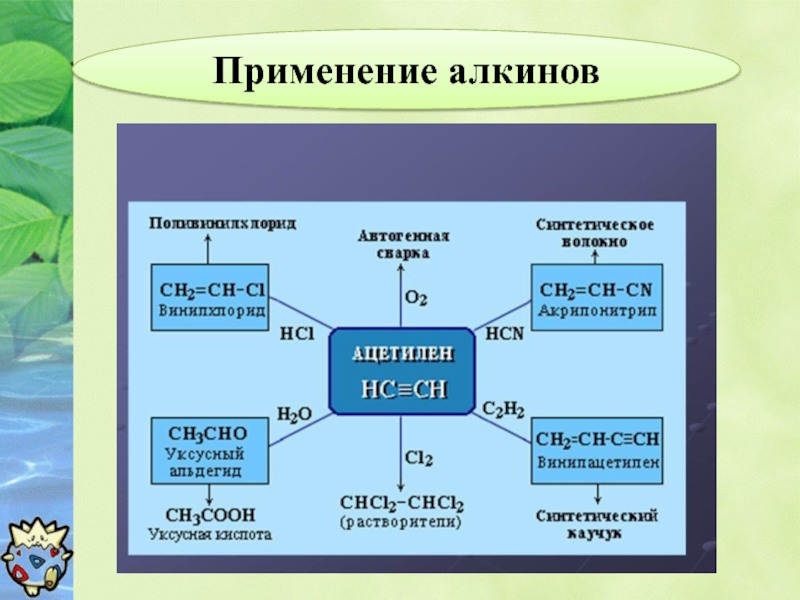
- 20. Применение алкинов
- 21. Расшифруйте следующую цепочку превращений. Назовите соединения А,Б
- 22. В-пропин Б-1,2-дибромпропан
- 23. Домашнее задание Пар. 13, упр. 9 Iв.а Iiв. б
Слайд 2Цели урока:
1. Рассмотреть химические свойства алкинов:
реакции присоединения
окисления
Тримеризации ацетилена в бензол
Кислотные
2. Применение алкинов
Слайд 31. Повторение пройденного материала
2. Химические свойства алкинов
3. Применение алкинов
4.Закрепление
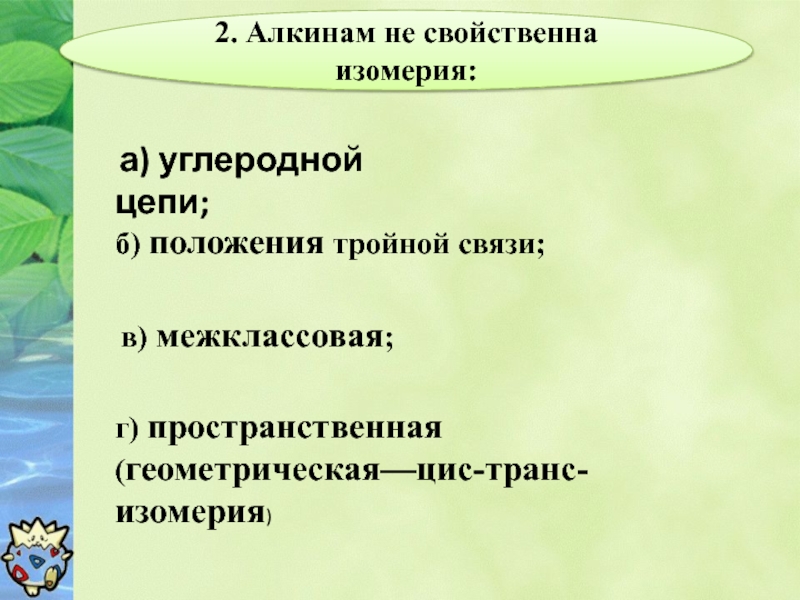
Слайд 52. Алкинам не свойственна изомерия:
а) углеродной цепи;
б) положения тройной связи;
в)
г) пространственная (геометрическая—цис-транс-изомерия)
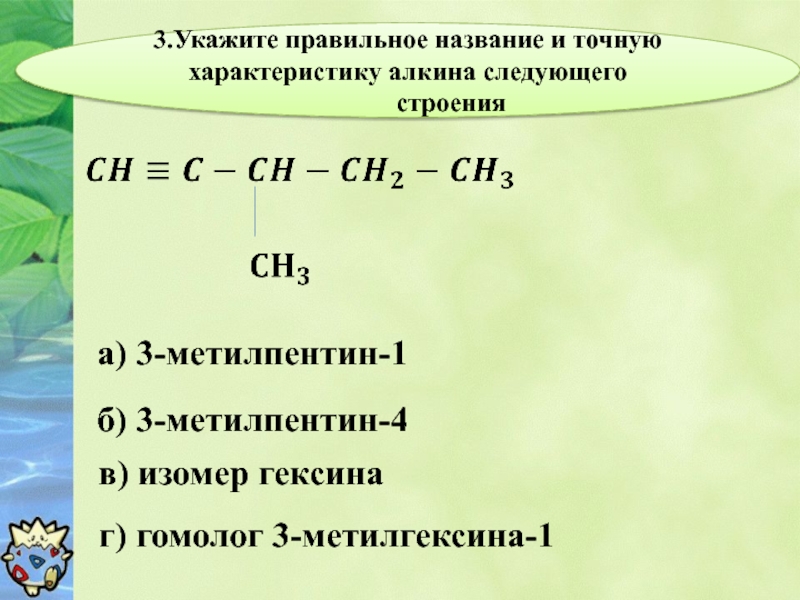
Слайд 63.Укажите правильное название и точную характеристику алкина следующего
а) 3-метилпентин-1
б) 3-метилпентин-4
в) изомер гексина
г) гомолог 3-метилгексина-1
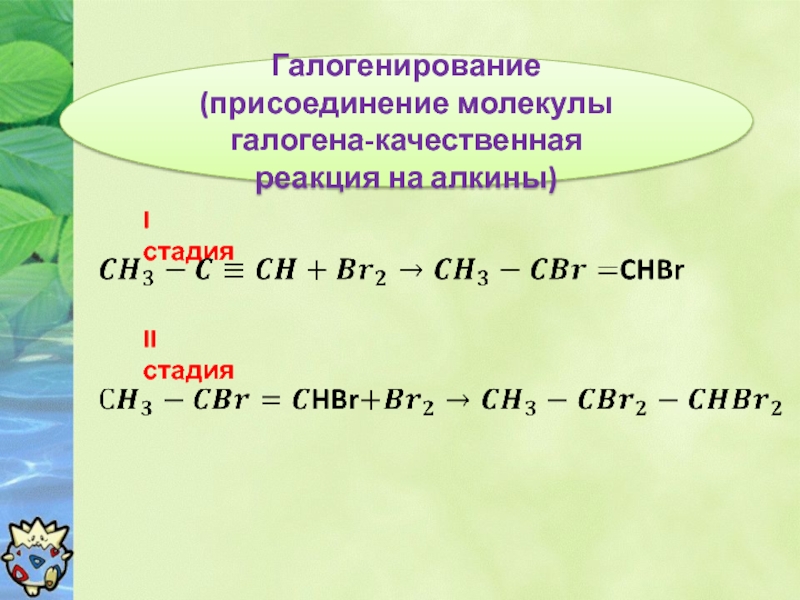
Слайд 8Галогенирование (присоединение молекулы галогена-качественная реакция на алкины)
I стадия
II стадия
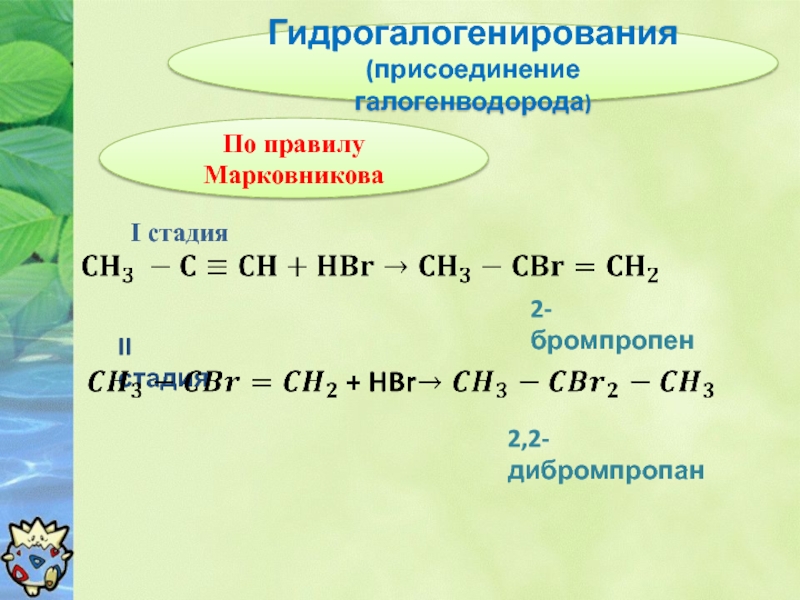
Слайд 9Гидрогалогенирования (присоединение галогенводорода)
2-бромпропен
I стадия
II стадия
2,2-дибромпропан
По правилу Марковникова
Слайд 11В случае алкинов с более длинной цепью в соответствии с правилом
OH
енол
кетон
Слайд 12Михаил Григорьевич Кучеров – русский химик-органик. Родился в имении отца под
Основные работы посвящены органическому синтезу. Получил (1873) дифенил и некоторые его производные. Исследовал (1875) условия превращения бромвинила в ацетилен. Открыл (1881) реакцию каталитической гидратации ацетиленовых углеводородов с образованием карбонильных соединений, в частности, превращения ацетилена в ацетальдегид в присутствии солей ртути (реакция Кучерова). За это открытие был удостоен (1885) премии Русского физико-химического общества. Реакция Кучерова была положена в основу промышленного способа получения ацетальдегида и уксусной кислоты. Показал (1909), что гидратацию ацетиленовых углеводородов можно проводить в присутствии солей магния, цинка, кадмия. Исследовал механизм этой реакции. Установил промежуточное образование металлорганических комплексов за счёт неполновалентного взаимодействия атомов металла соли и углеродных атомов с тройной связью.
Русское физико-химическое общество учредило в 1915 г. премию имени М. Г. Кучерова для начинающих исследователей-химиков.
Слайд 10
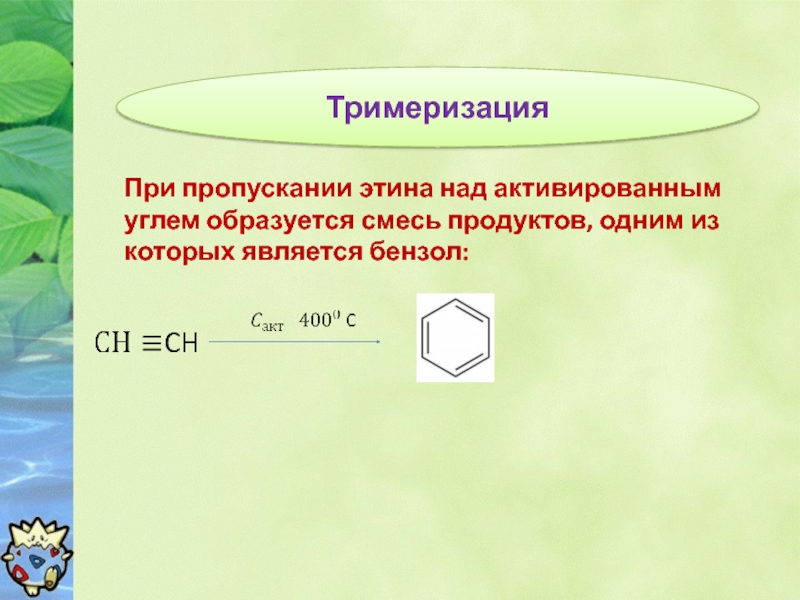
Слайд 13Тримеризация
При пропускании этина над активированным углем образуется смесь продуктов, одним из
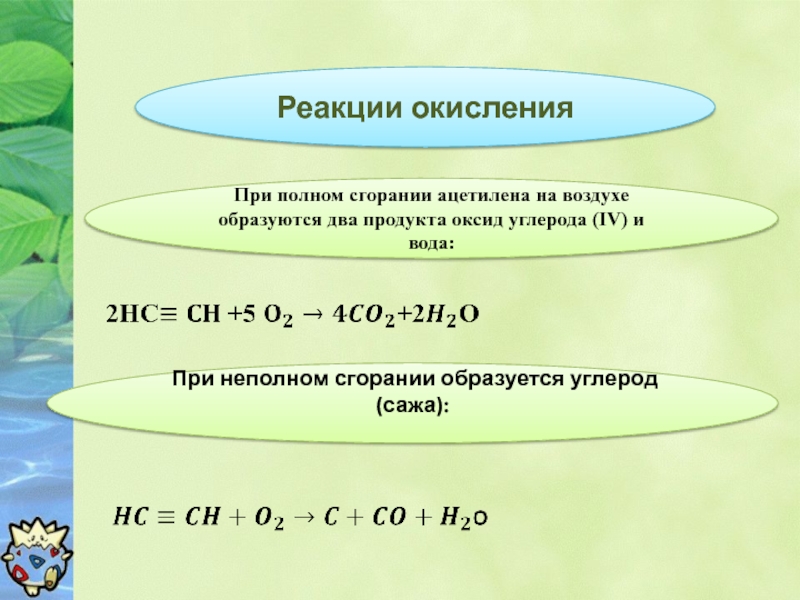
Слайд 14Реакции окисления
При полном сгорании ацетилена на воздухе образуются два продукта оксид
При неполном сгорании образуется углерод (сажа):
Слайд 15Кислотные свойства алкинов
в терминальных алкинах (с тройной связью на конце цепи)
Слайд 16 Алкины, как и алкены, обесцвечивают подкисленные растворы перманганата калия, при этом
Слайд 17Несколько иного типа реакция происходит между терминальными алкинами и аммиачными растворами
Бело-серый
желтый
Слайд 18Ацетилениды как соли слабых кислот легко разлагаются сильными кислотами при нагревании
Слайд 19Правило В.В.Марковникова:
водород присоединяется к наиболее гидрогенизированному атому углерода при