- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Характеристики атома. Электроотрицательность. Шкала Полинга. Изменения химических свойств элементов в ПСЭ. (Лекция 1.2) презентация
Содержание
- 1. Характеристики атома. Электроотрицательность. Шкала Полинга. Изменения химических свойств элементов в ПСЭ. (Лекция 1.2)
- 3. Основные характеристики атома
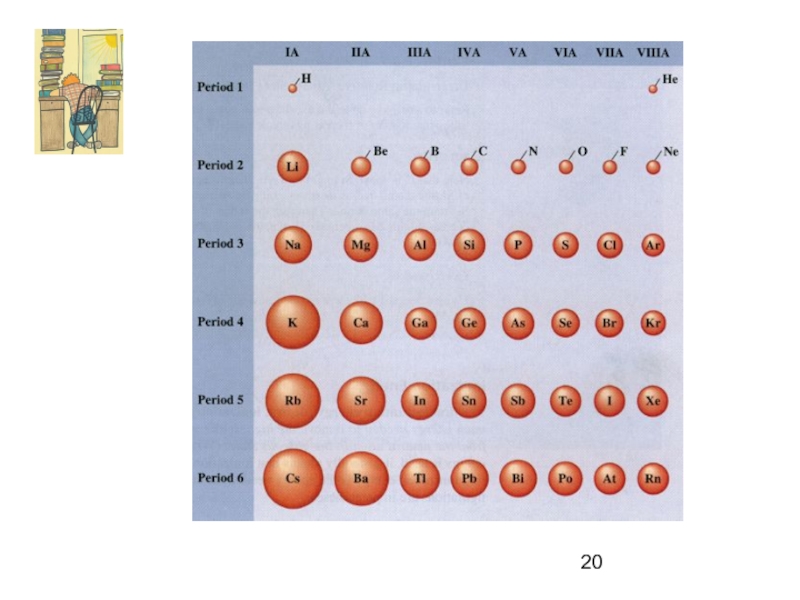
- 4. Атомный радиус (ra)
- 5. Энергия присоединения или отрыва электронов от
- 6. Относительная электроотрицательность (ОЭО) атомов характеризует способность
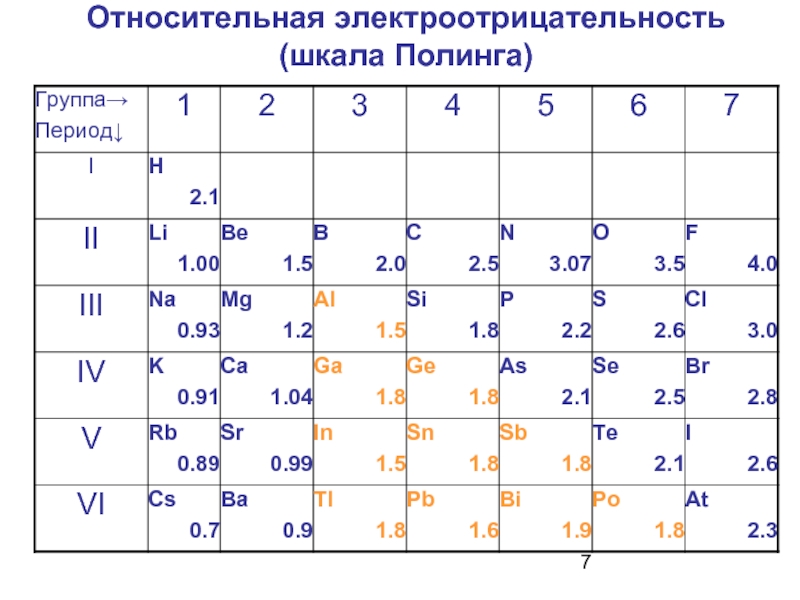
- 7. Относительная электроотрицательность (шкала Полинга)
- 9. Изменение свойств элементов и их соединений в периодах и группах
- 10. Химические свойства элемента зависят от способности атома
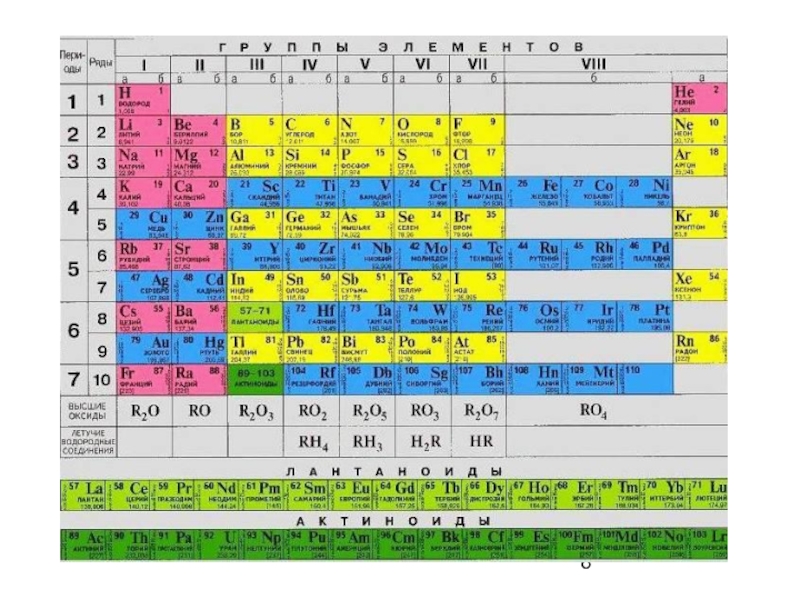
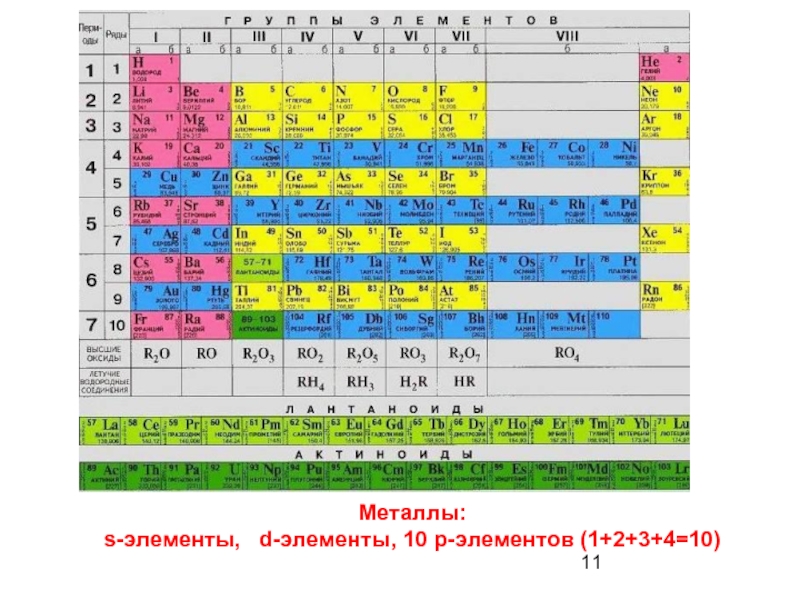
- 11. Металлы: s-элементы, d-элементы, 10 р-элементов (1+2+3+4=10)
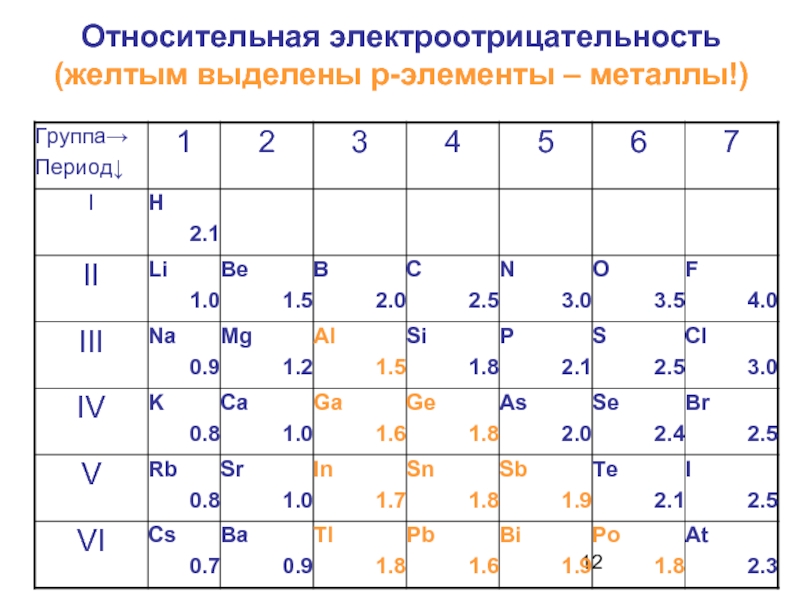
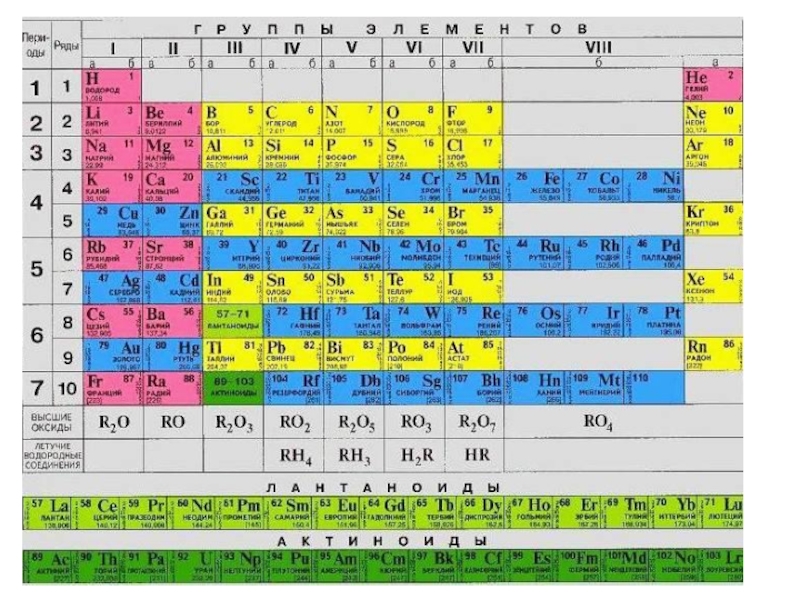
- 12. Относительная электроотрицательность (желтым выделены р-элементы – металлы!)
- 13. Значения электроотрицательности нужно! использовать для оценки направления смещения электронов при образовании молекул.
- 14. А-группы: Металлические свойства в периоде ослабевают,
- 15. Атомы металлов всегда отдают электроны и степень
- 16. Атомы металлов – только восстановители! Атомы неметаллов,
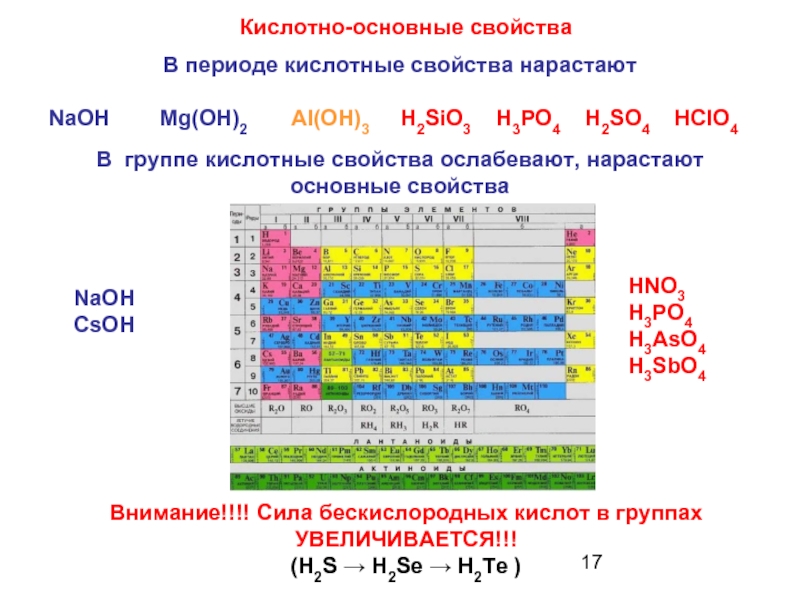
- 17. Кислотно-основные свойства В периоде кислотные свойства нарастают
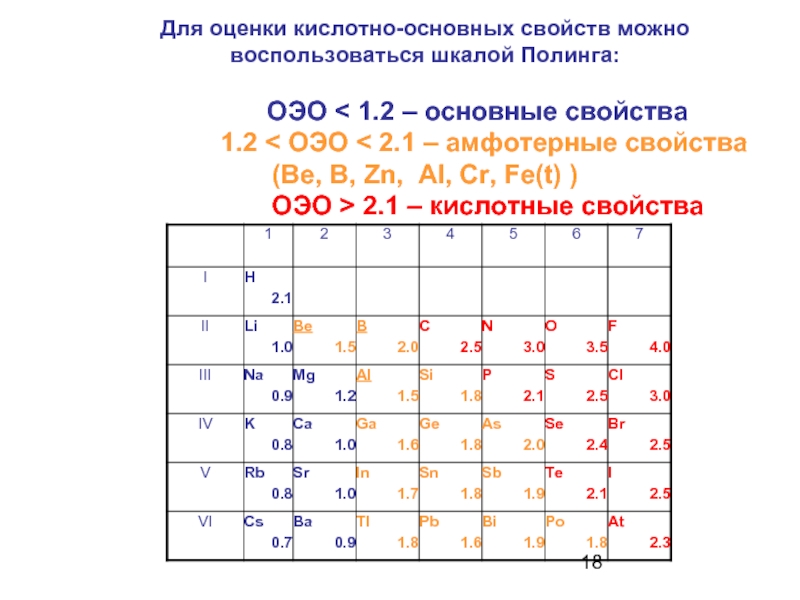
- 18. Для оценки кислотно-основных свойств можно воспользоваться шкалой
- 19. Характер изменений основных характеристик атома в ПСЭ
- 21. Тест №4 Основные характеристики атома (один вариант ответа)
- 22. 1. Химические элементы расположены в порядке возрастания
- 23. 2. В каком ряду химические элементы расположены
- 24. 3. Наибольший радиус имеют атомы: 1)
- 25. 4. В каком ряду содержатся только те
- 26. 5. Аллотропными модификациями являются: 1)азот и
- 27. 6. Графит и алмаз — это:
- 28. 7. Какие из перечисленных веществ являются различными аллотропными
- 29. 8.Какой химический элемент не
- 30. 9. Свойство химического элемента образовывать несколько простых веществ называют: 1)поливалентностью 2)гетерогенностью 3)аллотропией 4) изоморфизмом
- 31. 10. В порядке возрастания атомного радиуса химические
- 32. 11. В каком ряду химические элементы расположены
- 33. 12. В ряду элементов:
- 34. 13. Наименьшей электроотрицательностью обладает элемент:
- 35. 14. Наибольшей электроотрицательностью обладает элемент:
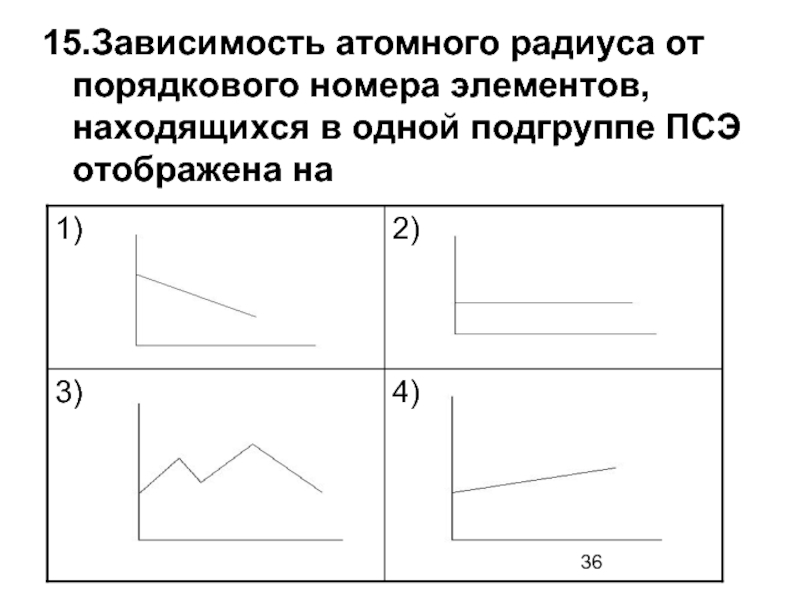
- 36. 15.Зависимость атомного радиуса от порядкового номера элементов,
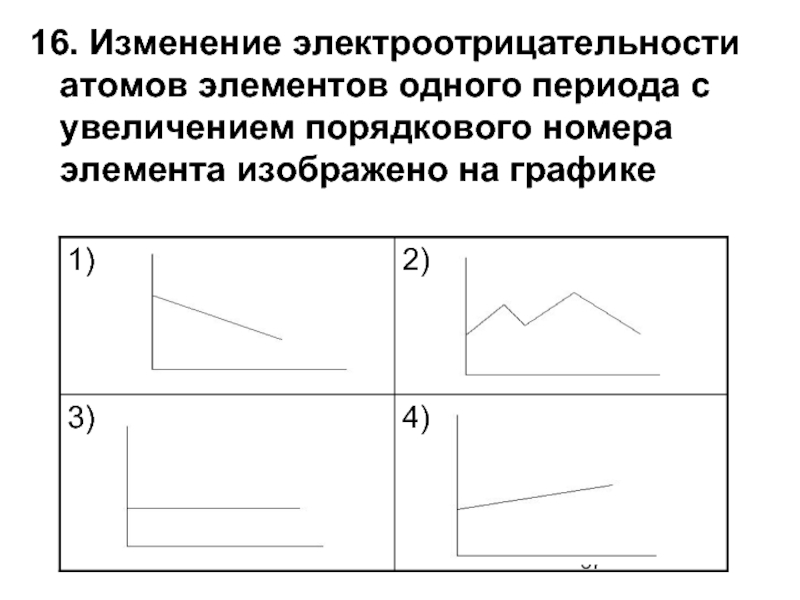
- 37. 16. Изменение электроотрицательности атомов элементов одного периода
- 38. 17. Увеличение электроотрицательности элементов, расположенных в одной
- 39. 18. Состав ядер изотопов 12С и 13С
- 40. 19. Элементы расположены в порядке уменьшения их
- 41. 20. Наименьший радиус имеет атом: 1)
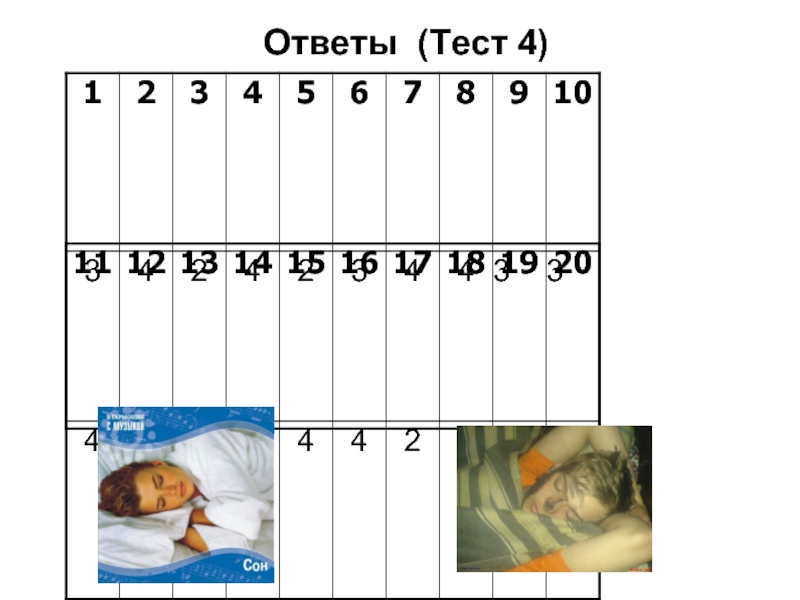
- 42. Ответы (Тест 4)
- 43. Тест 5 Изменение свойств элементов
- 45. В малых периодах расположены элементы (2 варианта
- 46. 2. Укажите физический смысл номера группы в
- 47. 3. Неметаллические свойства атомов элементов постепенно нарастают
- 48. 4. В одном периоде находятся элементы:
- 49. 5. Общую формулу летучих водородных соединений ЭН3
- 50. 6. Какова общая формула летучих водородных соединений
- 51. 7. Укажите общую формулу высших оксидов элементов
- 52. 8. Общую формулу высших оксидов Э2О7 имеют
- 53. 9. Укажите символы элементов, формула высших оксидов
- 54. 10. В больших периодах расположены элементы
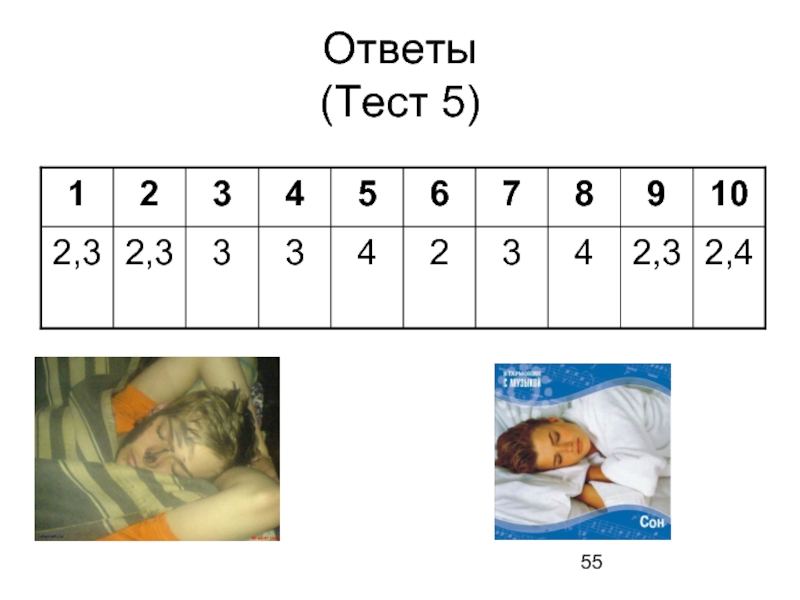
- 55. Ответы (Тест 5)
- 56. Тест 6 Изменение свойств элементов
- 57. Укажите атомный номер элемента, образующего высший оксид
- 58. 2. Электроотрицательность последовательно возрастает в ряду атомов,
- 59. 3. Укажите ряд, в котором символы элементов
- 60. 4. С последовательным возрастанием неметаллических свойств атомов
- 61. 5. Укажите электронную конфигурацию атома элемента с
- 62. 6. Укажите электронную конфигурацию атома элемента с
- 63. 7. Энергия сродства к электрону наибольшая у
- 64. 8. Энергия сродства к электрону последовательно возрастает
- 65. 9. Укажите электронную конфигурацию атома элемента с наиболее выраженными металлическими свойствами: 1s22s22p6 1s22s22p63s23p63d34s2 1s22s22p5 1s22s22p63s23p4
- 66. 10. Укажите электронную конфигурацию атома элемент с
- 67. Ответы (Тест 6)
- 68. Спасибо за внимание!
Слайд 1Лекция 1-2
«Основные характеристики атома.
Электроотрицательность. Шкала Полинга.
Закономерности изменения химических
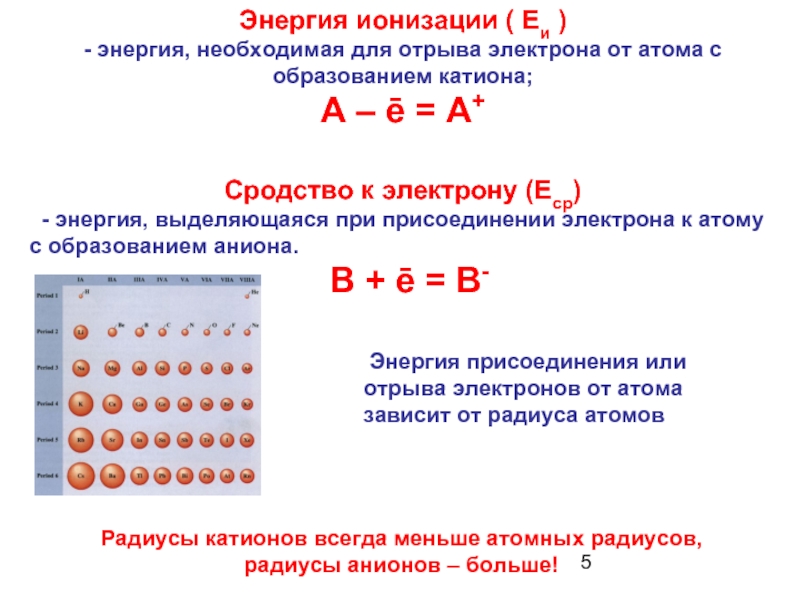
Слайд 5 Энергия присоединения или отрыва электронов от атома зависит от радиуса
Энергия ионизации ( Еи )
- энергия, необходимая для отрыва электрона от атома с образованием катиона;
А – ē = А+
Сродство к электрону (Еср)
- энергия, выделяющаяся при присоединении электрона к атому
с образованием аниона.
В + ē = В-
Радиусы катионов всегда меньше атомных радиусов,
радиусы анионов – больше!
Слайд 6Относительная электроотрицательность (ОЭО)
атомов характеризует способность атома притягивать к себе общие
Полинг принял:
ОЭО для Li = 1
ОЭО для F = 4
Слайд 10Химические свойства элемента зависят от способности атома отдавать (металлические свойства) или
1) заряда ядра
2) радиуса атома
3) электронной конфигурации внешнего и предвнешнего уровней
За металлические и неметаллические свойства борются две тенденции:
- при росте заряда ядра сила притяжения электронов растет
- но с увеличением числа электронов (от 4 до 7) идет приближение к устойчивой конфигурации ns2np6 и атом активнее присоединяет электроны
Слайд 13Значения электроотрицательности нужно! использовать для оценки направления смещения электронов при образовании
Слайд 14А-группы:
Металлические свойства в периоде ослабевают,
в группах нарастают, но!!!!
Б-группы:
У d-элементов электроны
d -уровень, поэтому радиус меняется незначительно и доминирующим фактором становится рост заряда!!!
Сравним:
29Cu→79Au
Слайд 15Атомы металлов всегда отдают электроны и степень окисления у них только
Атомы неметаллов могут иметь и положительную степень окисления и отрицательную (исключение составляет фтор - F).
Максимальная отрицательная степень окисления рассчитывается как разность числа 8 и номера группы.
Слайд 16Атомы металлов – только восстановители!
Атомы неметаллов, как правило, – окислители, но
2Р+3Н2→2РН3
4Р+5О2 →2Р2О5
Слайд 17Кислотно-основные свойства
В периоде кислотные свойства нарастают
NaOH Mg(OH)2
В группе кислотные свойства ослабевают, нарастают основные свойства
NaOH
CsOH
HNO3
H3PO4
H3AsO4
H3SbO4
Внимание!!!! Сила бескислородных кислот в группах УВЕЛИЧИВАЕТСЯ!!!
(H2S → H2Se → H2Te )
Слайд 18Для оценки кислотно-основных свойств можно воспользоваться шкалой Полинга:
Слайд 221. Химические элементы расположены в порядке возрастания их атомного радиуса в
1) Be,B,C,N
2) Rb,K,Na,Li
3) O,S,Se,Te
4) Mg,Al,Si,P
Слайд 232. В каком ряду химические элементы расположены в порядке возрастания их
1) Na,Mg,Al,Si
2) Li, Be, B, C
3) P,S, Cl ,Ar
4) F,O,N,C
Слайд 254. В каком ряду содержатся только те элементы, которые
имеют аллотропные формы?
1)
2) S, Si, CI
3) S, Р, Аг
4) О, С, Р
Слайд 265. Аллотропными модификациями являются:
1)азот и фосфор
2)кислород и озон
3) сера и селен
4)
Слайд 276. Графит и алмаз — это:
1)разные химические элементы
2)одно и то же
3)аллотропные видоизменения одного химического элемента
4)разные агрегатные состояния одного вещества.
Слайд 287. Какие из перечисленных веществ являются различными аллотропными видоизменениями одного элемента?
1) кремний
2) сажа и графит
3) белое золото и золото
4) белый фосфор и черный фосфор
Слайд 29
8.Какой химический элемент не образует аллотропных
модификаций?
1) Сера
2) Углерод
3)
4) Азот
Слайд 309. Свойство химического элемента образовывать несколько простых веществ называют:
1)поливалентностью
2)гетерогенностью
3)аллотропией
4) изоморфизмом
Слайд 3110. В порядке возрастания атомного радиуса химические элементы расположены в ряду:
1)
2) Rb, Na , К, Li
3) О, S, Se, Те
4) Al, Mg, Si, P
Слайд 3211. В каком ряду химические элементы расположены в порядке возрастания их
1) Al, Na, Si, Mg
2) Be, Li, В, С
3) S, P, Ar, CI
4) F, O, N, С
Слайд 3312. В ряду элементов:
азот
1) атомный радиус
2) число неспаренных электронов в атоме
3) число s-электронов в атоме
4) электроотрицательность
Слайд 3615.Зависимость атомного радиуса от порядкового номера элементов, находящихся в одной подгруппе
Слайд 3716. Изменение электроотрицательности атомов элементов одного периода с увеличением порядкового номера
Слайд 3817. Увеличение электроотрицательности элементов, расположенных в одной группе, с уменьшением их
1) уменьшением заряда ядря
2) уменьшением атомного радиуса
3) уменьшением общего числа электронов
4) уменьшением атомной массы элемента
Слайд 3918. Состав ядер изотопов 12С и 13С соответственно равен:
1) 12р+6n и
2) 12p+12n и 13р+13n
3) 6p+12n и 6p+13n
4) 6p+6n и 6p+7n
Слайд 4019. Элементы расположены в порядке уменьшения их атомного радиуса
1) F→ Br
2) H → F → Cl → Br
3) Br → Cl → F → H
4) H → Cl → Br → F
Слайд 43Тест 5
Изменение свойств элементов
и их соединений в периодах и
(несколько вариантов ответов)
Слайд 45 В малых периодах расположены элементы (2 варианта ответа)
только металлы
только s- и
только групп А
как главных, так и побочных групп
Слайд 462. Укажите физический смысл номера группы в периодической системе (2 варианта
равен числу электронных слоев в атоме
как правило, равен числу валентных электронов в атоме
для элементов групп А равен числу электронов внешнем электронном слое
равен общему числу электронов в атоме
Слайд 473. Неметаллические свойства атомов элементов постепенно нарастают в ряду:
В, С,
Si, C, B
Si, C, N
C, Si, N
Слайд 484. В одном периоде находятся элементы:
с подобными химическими свойствами атомов;
с
с одинаковым числом электронных слоев в атоме;
с одинаковой энергией ионизации атома.
Слайд 495. Общую формулу летучих водородных соединений
ЭН3 имеют элементы группы:
II А
III
IV А
V А
Слайд 539. Укажите символы элементов, формула высших оксидов которых Э2О3 (2 варианта
Ca
B
Sc
S
Слайд 5410. В больших периодах расположены элементы
(2 варианта ответа):
только d-
элементы s-, р., d- и f-семейств
только А групп
как А, так и В групп
Слайд 57 Укажите атомный номер элемента, образующего высший оксид и летучее водородное соединение
1
14
15
23
Слайд 582. Электроотрицательность последовательно возрастает в ряду атомов, символы которых:
C, N, Si
C,
N, C, Si
Si, C, N
Слайд 593. Укажите ряд, в котором символы элементов указаны в порядке возрастания
N, С, Si
Si, C, N
C, Si, N
C, N, Si
Слайд 604. С последовательным возрастанием неметаллических свойств атомов химических элементов электроотрицательность:
уменьшается
не изменяется
увеличивается
изменяется периодически
Слайд 615. Укажите электронную конфигурацию атома элемента с наиболее выраженными металлическими свойствами
ns2
ns2np2
ns2np4
ns2np5
Слайд 626. Укажите электронную конфигурацию атома элемента с наиболее выраженными неметаллическими свойствами
ns2np5
ns2np4
ns2np2
ns2
Слайд 648. Энергия сродства к электрону последовательно возрастает в ряду атомов элементов),
Р, S, Сl
Р, Cl, S
Сl, S, Р
S, Р, Сl
Слайд 659. Укажите электронную конфигурацию атома элемента с наиболее выраженными металлическими свойствами:
1s22s22p6
1s22s22p63s23p63d34s2
1s22s22p5
1s22s22p63s23p4
Слайд 6610. Укажите электронную конфигурацию атома элемент с наиболее выраженными неметаллическими свойствам
[Ne]
[Ne] 3s23р2
[Ne]3s23p4
[Ne] 3s23p3



















































![10. Укажите электронную конфигурацию атома элемент с наиболее выраженными неметаллическими свойствам[Ne] 3s23p5 [Ne] 3s23р2[Ne]3s23p4[Ne] 3s23p3](/img/tmb/3/211531/d66d7bd5100835b12a9d5a1d9272b8a3-800x.jpg)