- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Характеристика элемента по его положению в периодической системе химических элементов Д.И.Менделеева презентация
Содержание
- 1. Характеристика элемента по его положению в периодической системе химических элементов Д.И.Менделеева
- 2. Характеристика элемента по его положению в периодической системе химических элементов Д.И.Менделеева. ТБ 02.09.2017
- 3. Химический элемент Химический элемент – это атомы одного вида (одинаковые атомы) Атомы углерода Атомы алюминия
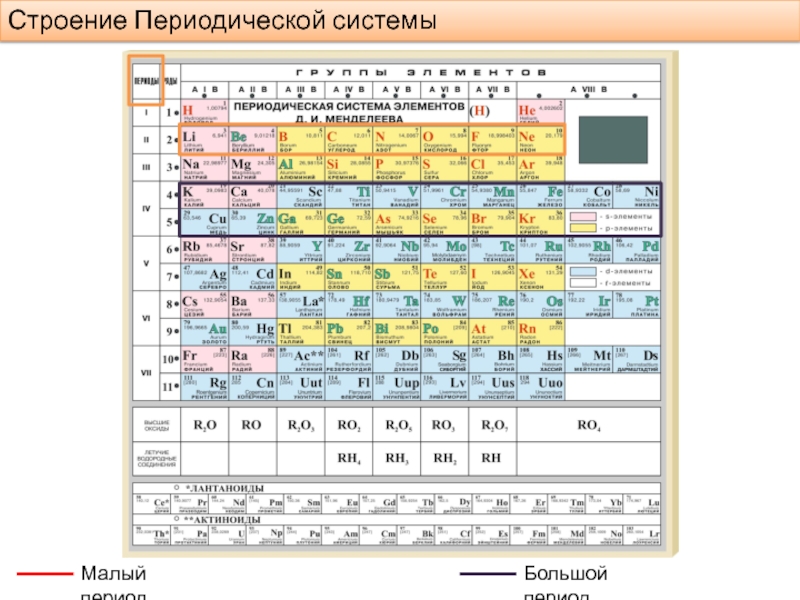
- 4. Строение Периодической системы Малый период Большой период
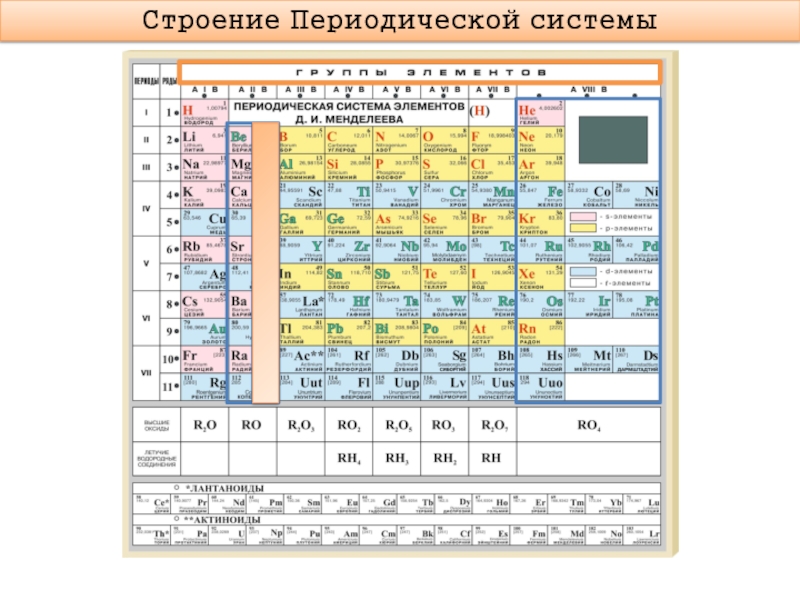
- 5. Строение Периодической системы
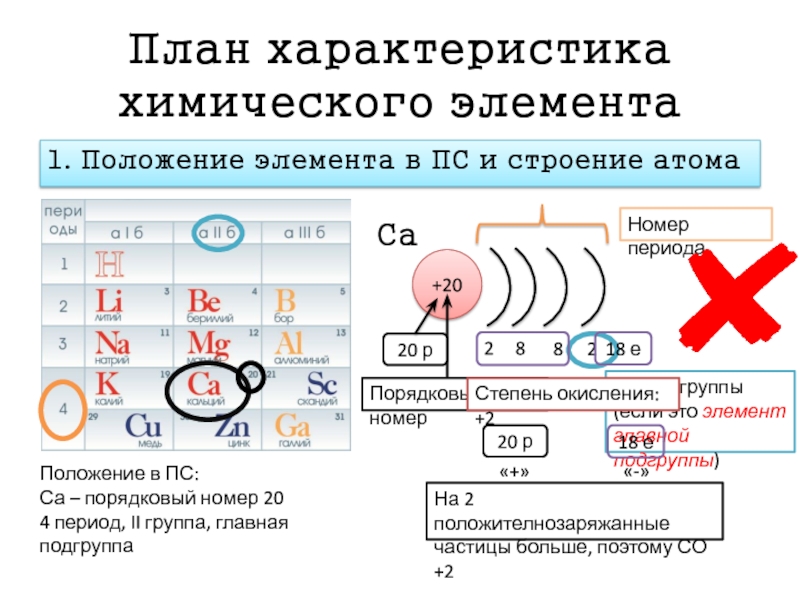
- 6. План характеристика химического элемента 1. Положение элемента
- 7. План характеристика химического элемента 2. Характеристика простого
- 8. План характеристика химического элемента 3. Сравнение свойств
- 9. 3. Сравнение свойств простого вещества со свойствами
- 10. 3. Сравнение свойств простого вещества со свойствами
- 11. План характеристика химического элемента 4. Сравнение свойств
- 12. 4. Сравнение свойств простого вещества со свойствами
- 13. 4. Сравнение свойств простого вещества со свойствами
- 14. План характеристика химического элемента 5. Состав высшего
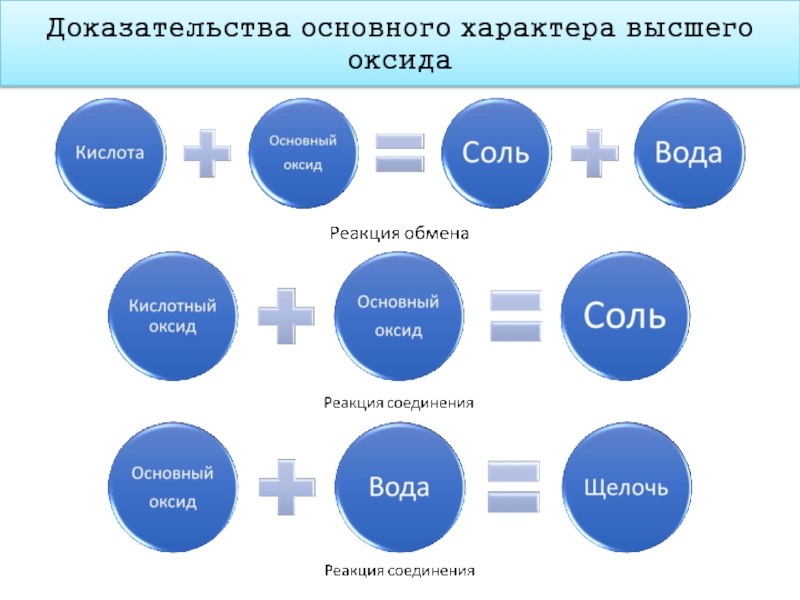
- 15. Доказательства основного характера высшего оксида
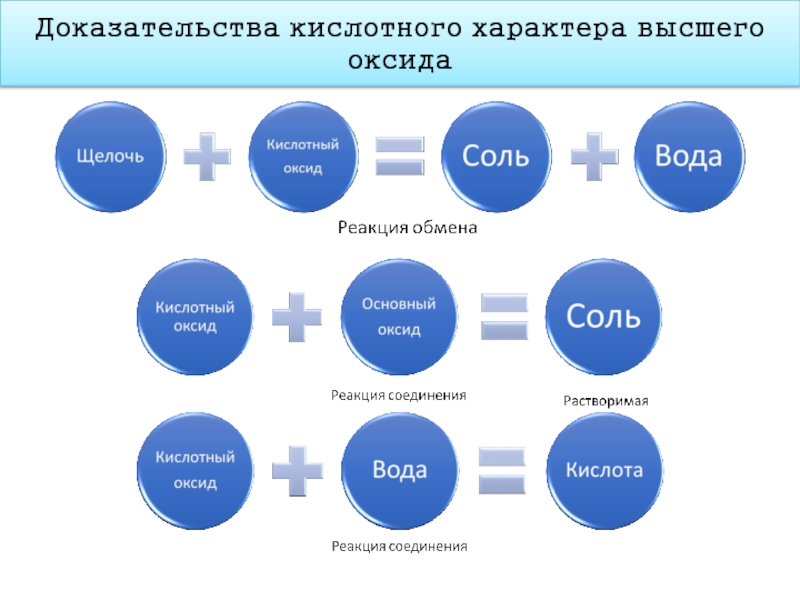
- 16. Доказательства кислотного характера высшего оксида
- 17. 6. Состав высшего гидроксида, его характер (кислородсодержащая
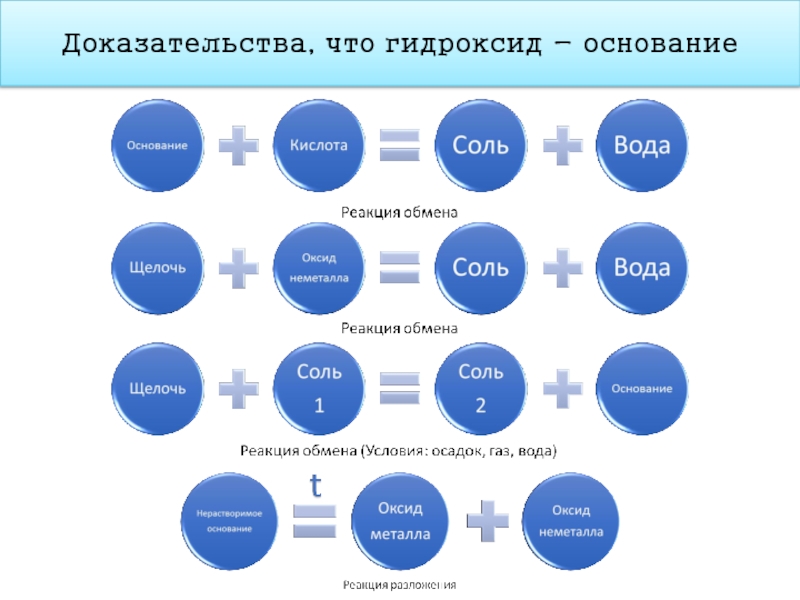
- 18. Доказательства, что гидроксид - основание
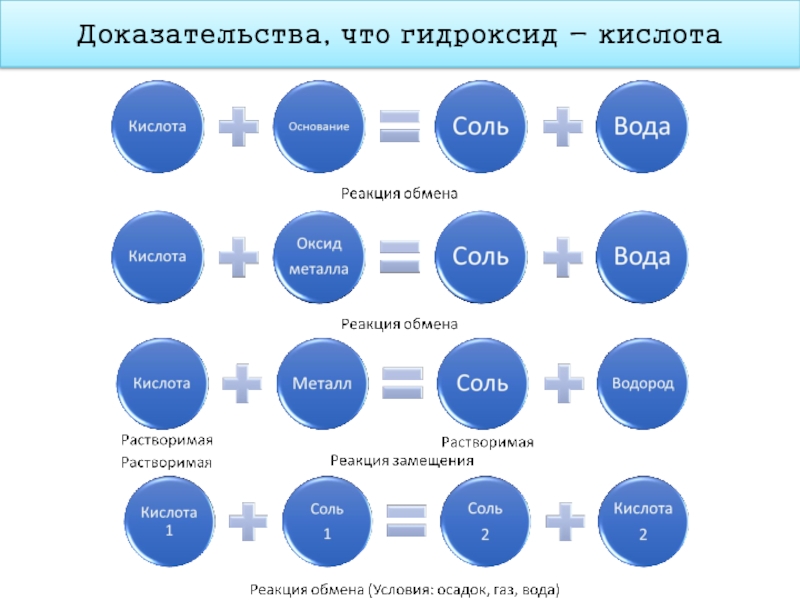
- 19. Доказательства, что гидроксид - кислота
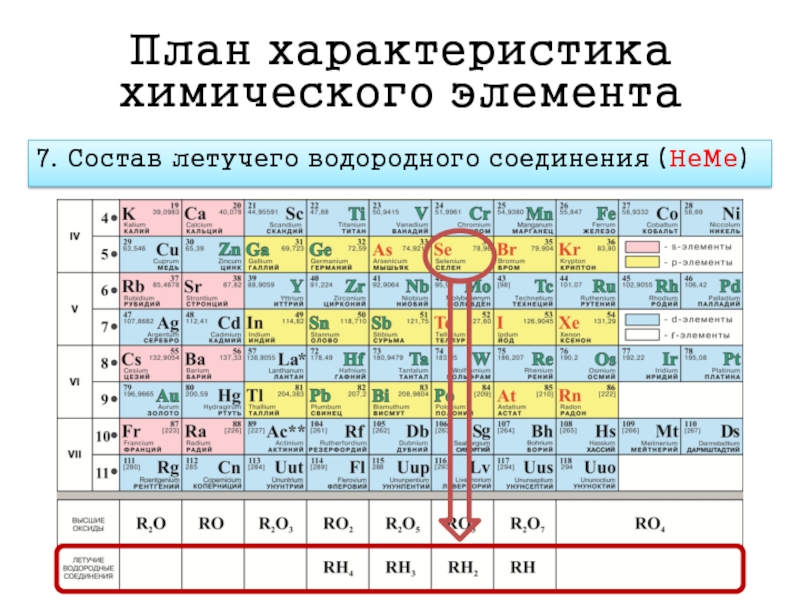
- 20. План характеристика химического элемента 7. Состав летучего водородного соединения (НеМе)
- 24. Подготовка к с.р. Работа на 15 минут
Слайд 2Характеристика элемента по его положению в периодической системе химических элементов Д.И.Менделеева.
02.09.2017
Слайд 3Химический элемент
Химический элемент – это атомы одного вида (одинаковые атомы)
Атомы углерода
Атомы
Слайд 6План характеристика химического элемента
1. Положение элемента в ПС и строение атома
Положение
Са – порядковый номер 20
4 период, II группа, главная подгруппа
+20
2
8
8
2
Са
Номер периода
Номер группы
(если это элемент
главной подгруппы)
Порядковый номер
Степень окисления: +2
18 е
20 р
20 р
18 е
«+»
«-»
На 2 положителнозаряжанные
частицы больше, поэтому СО +2
Слайд 7План характеристика химического элемента
2. Характеристика простого вещества (Ме/НеМе)
Металлы
Неметаллы
Только для элементов главных
В побочных подгруппах все элементы – металлы!!!
В 5
Бор
At 85
Астат
Слайд 8План характеристика химического элемента
3. Сравнение свойств простого вещества со
свойствами простых веществ
Ca
Mg
Sr
Цинк – элемент побочной подгруппы
Магний, кальций и стронций – элементы
главной подгруппы
Именно их и сравниваем:
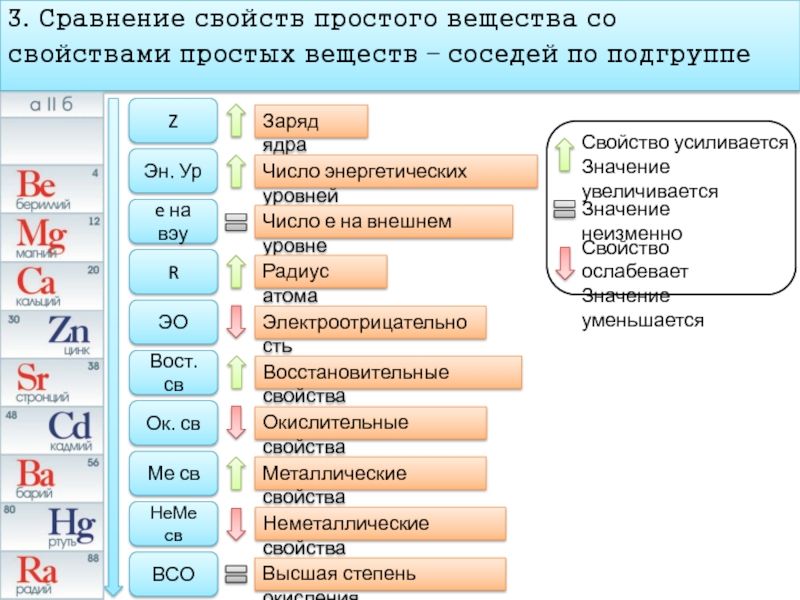
Слайд 93. Сравнение свойств простого вещества со
свойствами простых веществ – соседей по
Z
Эн. Ур
e на вэу
R
ЭО
Вост. св
Ок. св
Ме св
НеМе св
ВСО
Заряд ядра
Число энергетических уровней
Число е на внешнем уровне
Радиус атома
Электроотрицательность
Восстановительные свойства
Окислительные свойства
Металлические свойства
Неметаллические свойства
Высшая степень окисления
Свойство усиливается
Значение увеличивается
Значение неизменно
Свойство ослабевает
Значение уменьшается
Слайд 103. Сравнение свойств простого вещества со
свойствами простых веществ – соседей по
Z
Эн. Ур
e на вэу
R
ЭО
Вост. св
Ок. св
Ме св
НеМе св
ВСО
Свойство усиливается
Значение увеличивается
Значение неизменно
Свойство ослабевает
Значение уменьшается
Ca
Mg
Sr
Ca
Mg
Sr
Ca
Mg
Sr
Ca
Mg
Sr
Ca
Mg
Sr
Ca
Mg
Sr
Ca
Mg
Sr
Ca
Mg
Sr
Ca
Mg
Sr
Ca
Mg
Sr
Слайд 11План характеристика химического элемента
4. Сравнение свойств простого вещества со
свойствами простых веществ
Ca
K
Sc
Калий, кальций и скандий – элементы
одного периода
Именно их и сравниваем:
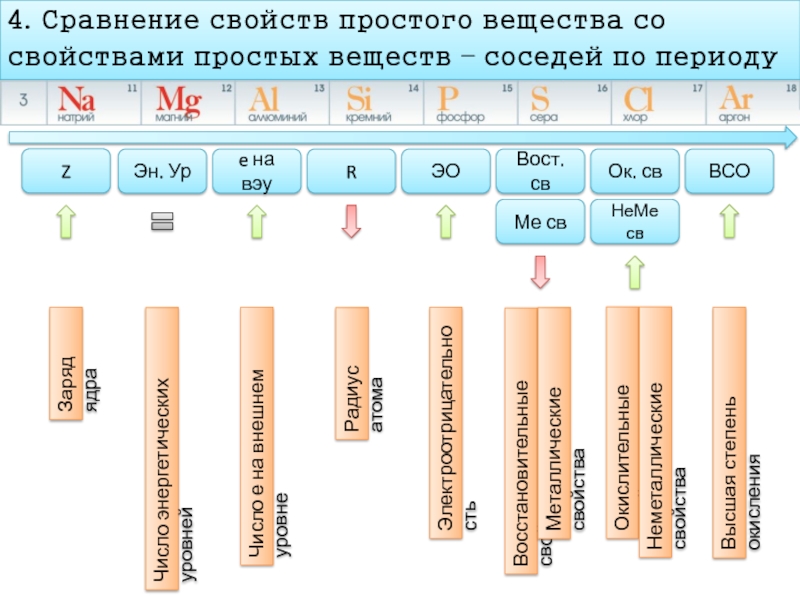
Слайд 124. Сравнение свойств простого вещества со
свойствами простых веществ – соседей по
Z
Эн. Ур
e на вэу
R
ЭО
Вост. св
Ок. св
Ме св
НеМе св
ВСО
Заряд ядра
Число энергетических уровней
Число е на внешнем уровне
Радиус атома
Электроотрицательность
Восстановительные свойства
Окислительные свойства
Металлические свойства
Неметаллические свойства
Высшая степень окисления
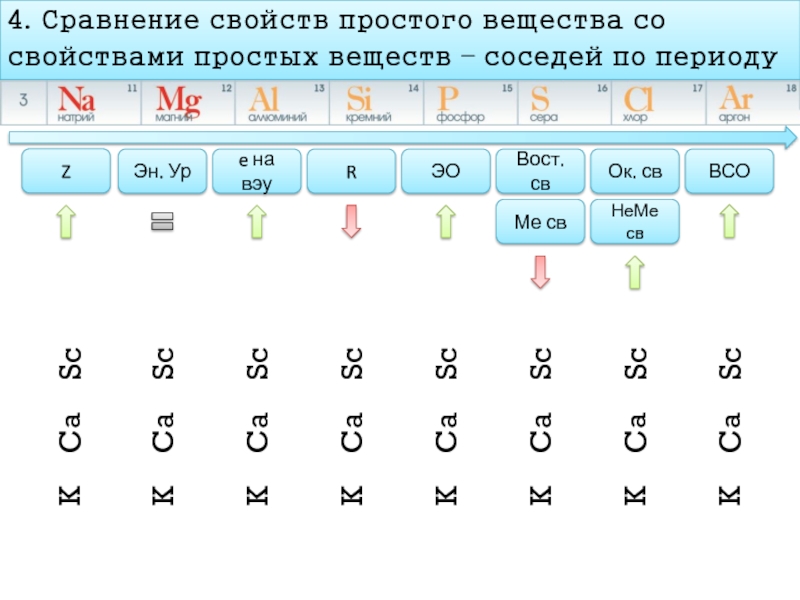
Слайд 134. Сравнение свойств простого вещества со
свойствами простых веществ – соседей по
Z
Эн. Ур
e на вэу
R
ЭО
Вост. св
Ок. св
Ме св
НеМе св
ВСО
Ca
K
Sc
Ca
K
Sc
Ca
K
Sc
Ca
K
Sc
Ca
K
Sc
Ca
K
Sc
Ca
K
Sc
Ca
K
Sc
Слайд 14План характеристика химического элемента
5. Состав высшего оксида, его характер (основный, кислотный,
Слайд 176. Состав высшего гидроксида, его характер (кислородсодержащая кислота, основание, амфотерный гидроксид)
План
Гидроксид Ме - основание
Гидроксид НеМе – кислородсодержащая кислота
Гидроксид Ме – амфотерный гидроксид
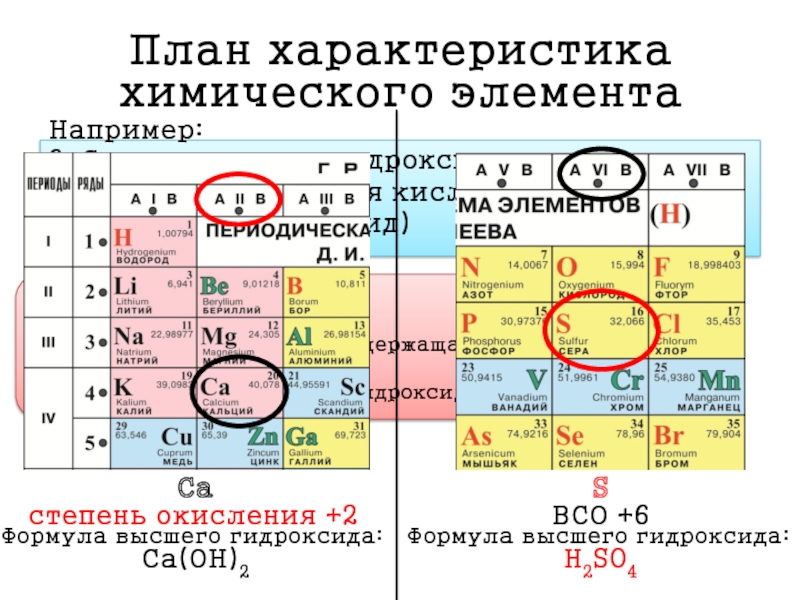
Например:
Са
степень окисления +2
Формула высшего гидроксида:
Са(ОН)2
S
ВСО +6
Формула высшего гидроксида:
H2SO4
Слайд 24Подготовка к с.р.
Работа на 15 минут
Дано распределение е в атоме. Определить
Написать уравнения реакций простого вещества с тремя другими простыми веществами. Составить электронный баланс. Указать окислитель и восстановитель
Дан оксид. Дан перечень других веществ. Выяснить, с какими веществами из перечня взаимодействует данный оксид. Записать уравнения возможных реакций.