- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Гидроксилпроизводные углеводородов презентация
Содержание
- 1. Гидроксилпроизводные углеводородов
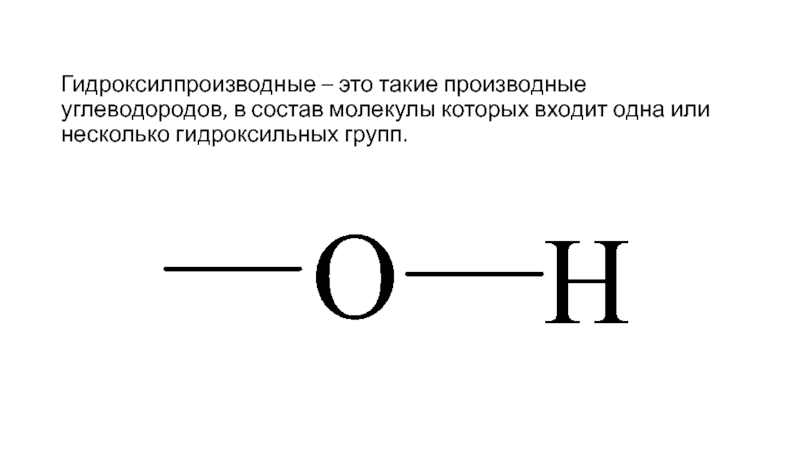
- 2. Гидроксилпроизводные – это такие производные углеводородов, в
- 3. Классификация В зависимости от количества гидроксильных групп
- 4. Номенклатура
- 5. классификация Таким образом получаем, что различают
- 6. классификация Гидроксилпроизводные алкиларенов с гидроксильной группой в
- 7. классификация Трёхатомные и многоатомные спирты Гидроксилпроизводные ароматическихуглеводородов - фенолы
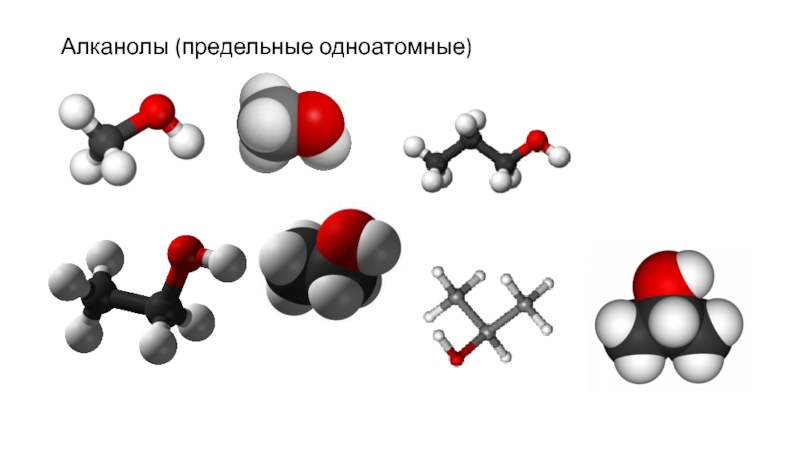
- 8. Алканолы (предельные одноатомные)
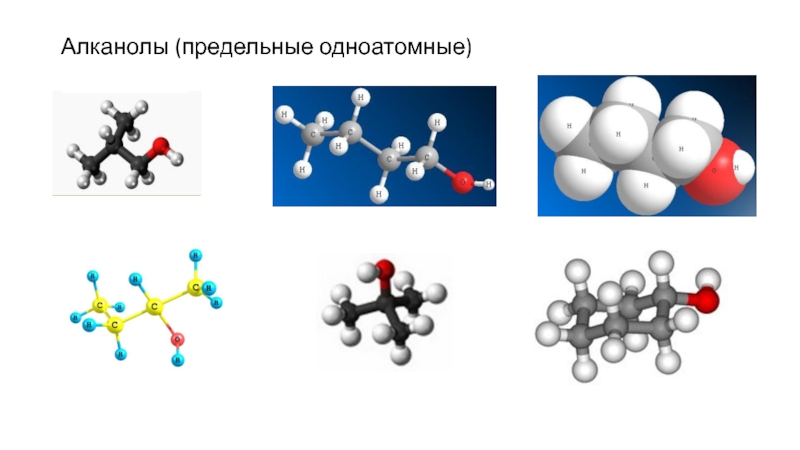
- 9. Алканолы (предельные одноатомные)
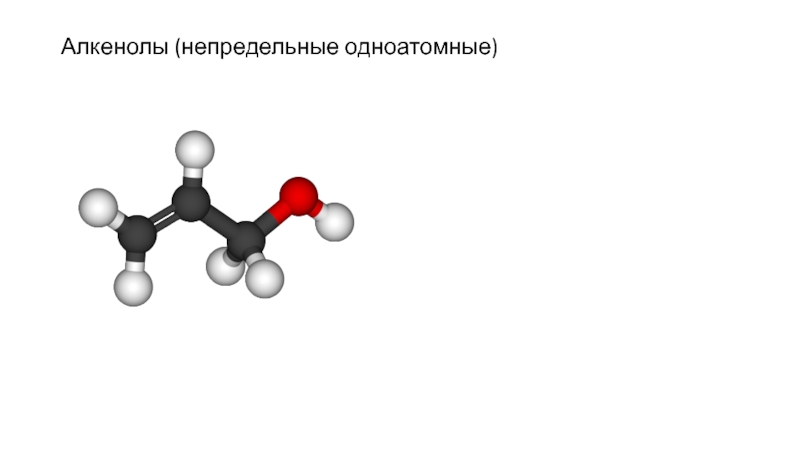
- 10. Алкенолы (непредельные одноатомные)
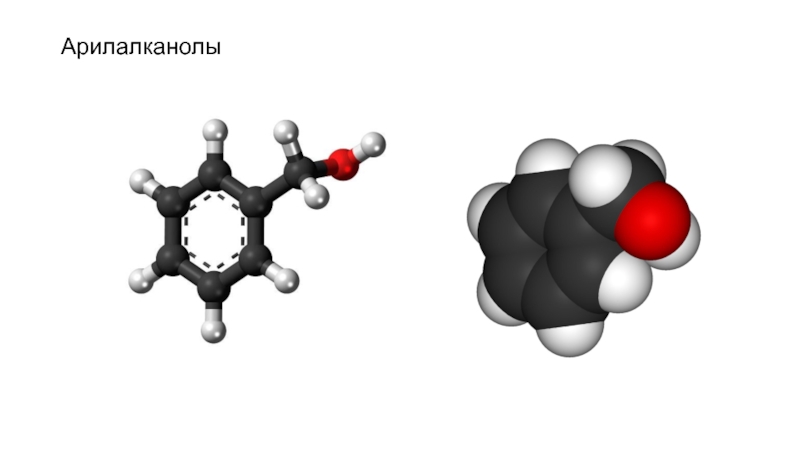
- 11. Арилалканолы
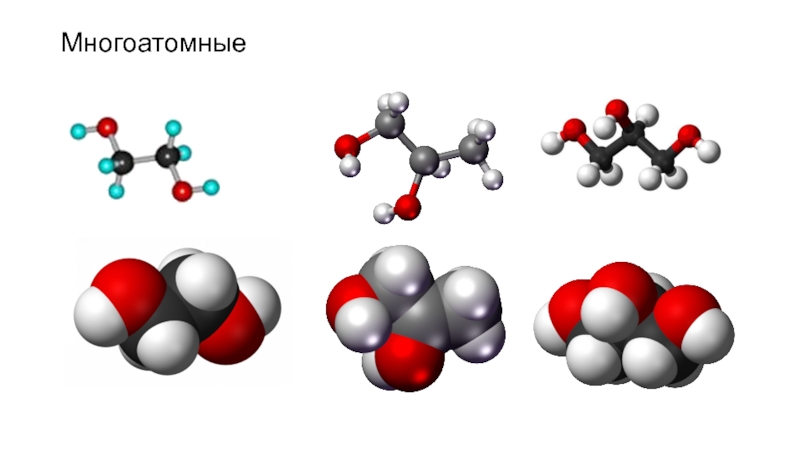
- 12. Многоатомные
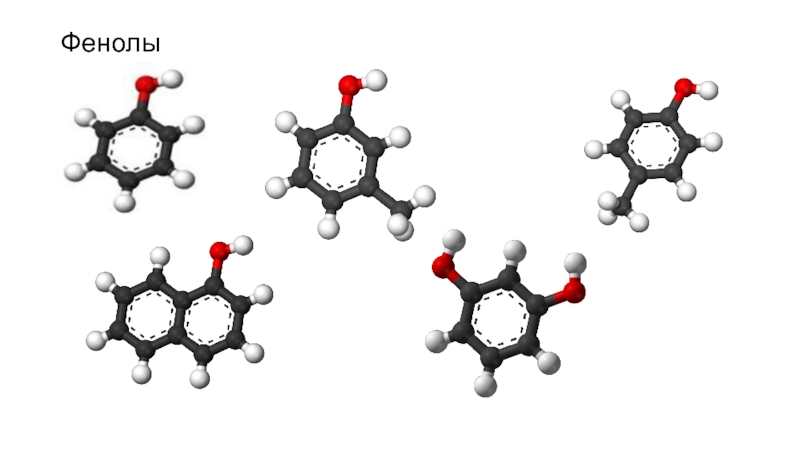
- 13. Фенолы
- 14. Спирты
- 15. Спирты - это производные углеводородов, содержащие одну или несколько гидроксильных групп (-O-H) R-OH
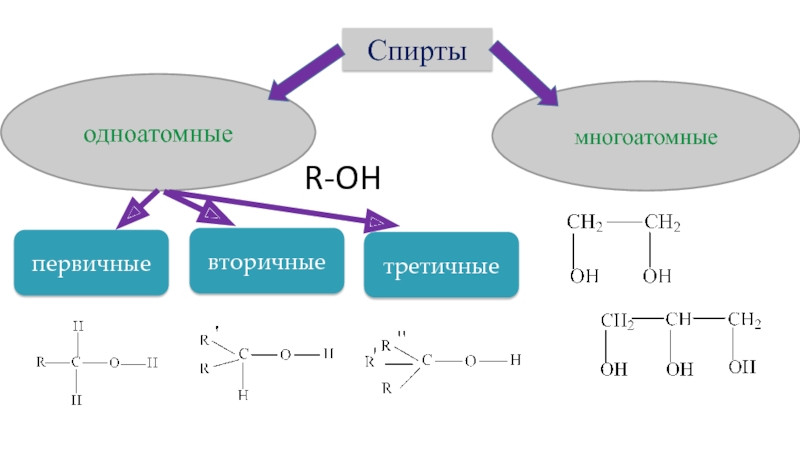
- 16. Классификация спиртов
- 17. третичные R-OH
- 18. Номенклатура спиртов
- 19. Название углеводородного радикала и окончание ОЛ CH3-OH
- 20. Этандиол-1,2 этиленгликоль Пропантриол-1,2,3 глицерин Гексангексаол-1,2,3,4,5,6 сорбит циклогексанол
- 21. Методы получения спиртов ЩЕЛОЧНОЙ ГИДРОЛИЗ ГАЛОГЕНУГЛЕВОДОРОДОВ: при
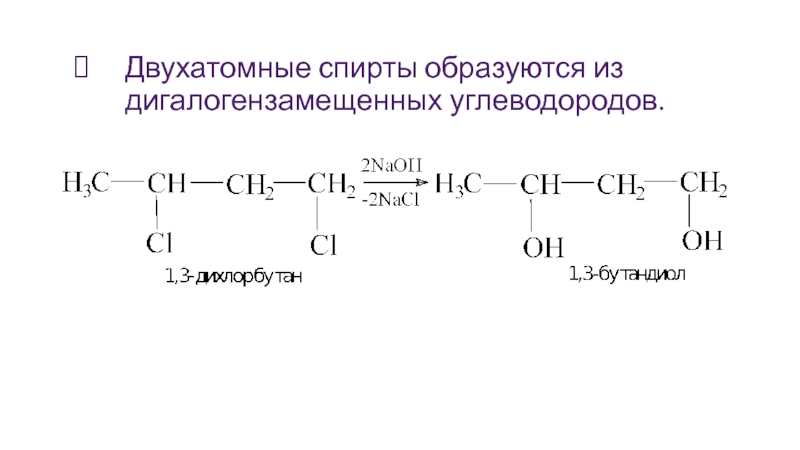
- 22. Двухатомные спирты образуются из дигалогензамещенных углеводородов.
- 23. 2. Гидратация непредельных углеводородов При нагревании алкенов
- 24. 2. Гидратация непредельных углеводородов При нагревании алкинов
- 25. 3. ВОССТАНОВЛЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ Из монофункциональных
- 26. 3. ВОССТАНОВЛЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ Из многофункциональных
- 27. 4. Синтез спиртов с помощью реактивов Гриньяра:
- 28. Этанол получают из пищевого и непищевого органического сырья путем сбраживания: глюкоза ферменты
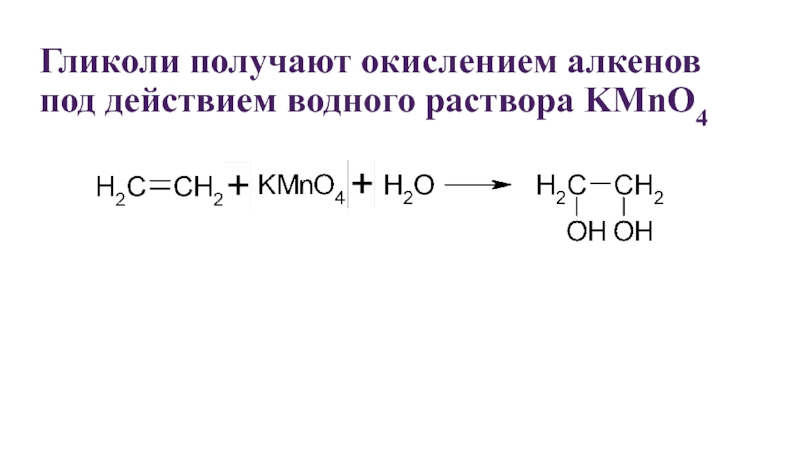
- 29. Гликоли получают окислением алкенов под действием водного раствора KMnO4
- 30. Получение смеси спиртов - синтола Условия: Нагревание,
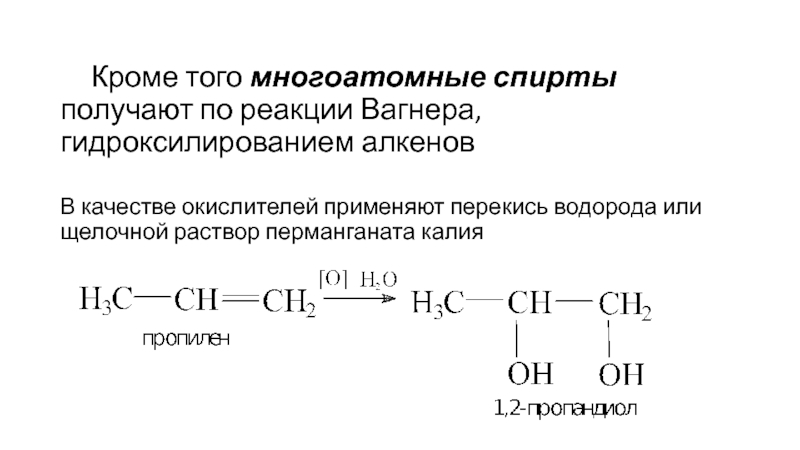
- 31. Кроме того многоатомные спирты получают по реакции
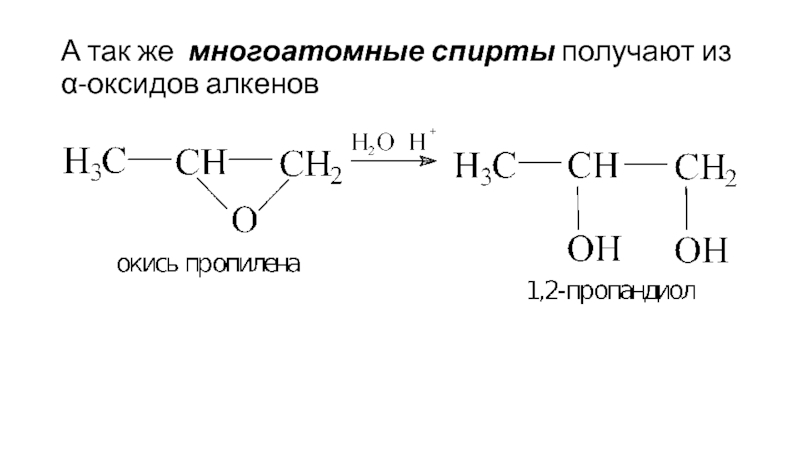
- 32. А так же многоатомные спирты получают из α-оксидов алкенов
- 33. Физические свойства спиртов Молекулы спиртов ассоциированы за
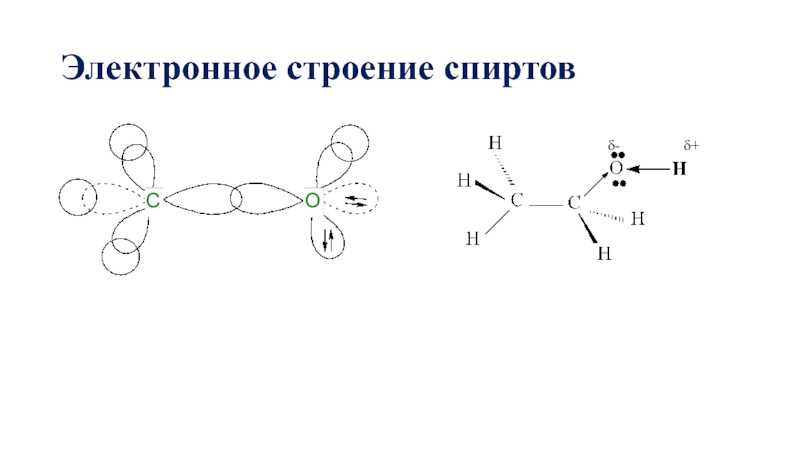
- 34. Электронное строение спиртов δ-
- 35. Химические свойства спиртов Спирты очень слабые электролиты
- 36. I. Реакции с участием водорода гидроксильной
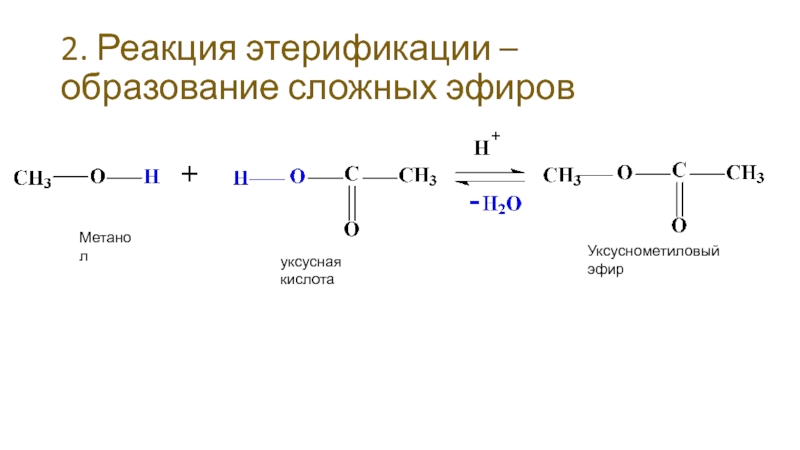
- 37. 2. Реакция этерификации – образование сложных эфиров
- 38. II. Реакции с отщеплением или замещением гидроксильной
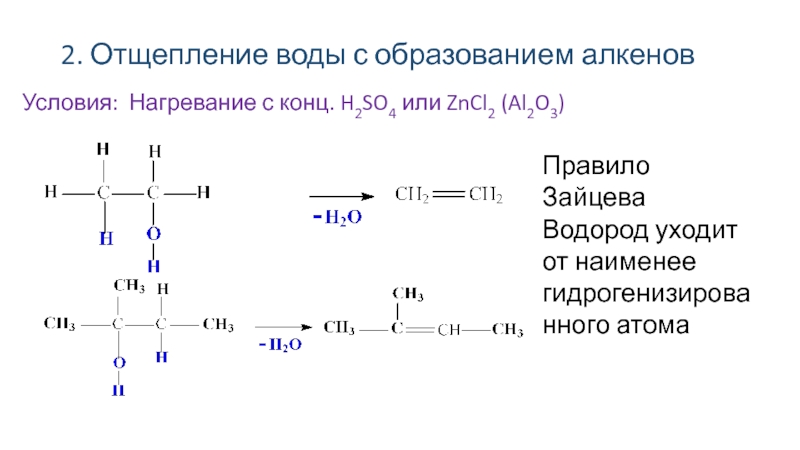
- 39. 2. Отщепление воды с образованием алкенов Условия: Нагревание с конц. H2SO4 или ZnCl2 (Al2O3)
- 40. 3. Межмолекулярная дегидратация Условия: нагревание избытка спирта
- 41. 4. Замена гидроксила на аминогруппу Условия: 3000С,
- 42. III. Реакции окисления, в которых одновременно принимают
- 43. 1. Дегидрогенизация (отщепление водорода) Условие: пропускание паров
- 44. 2. Окисление Условия : сильные окислители (H2SO4
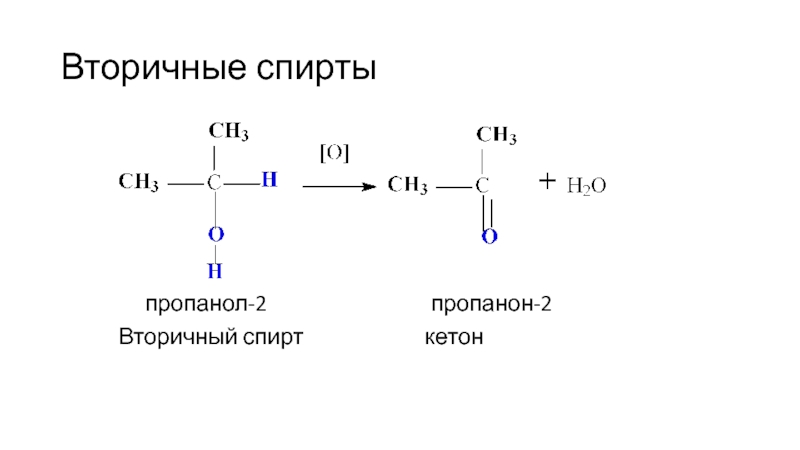
- 45. Вторичные спирты
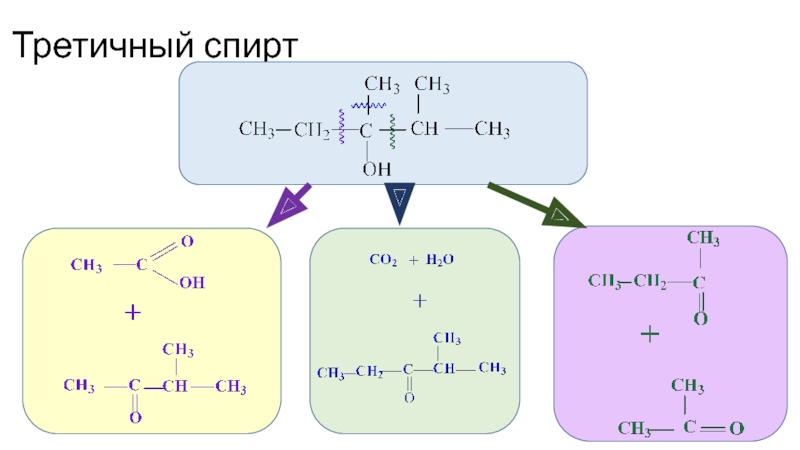
- 46. Третичный спирт
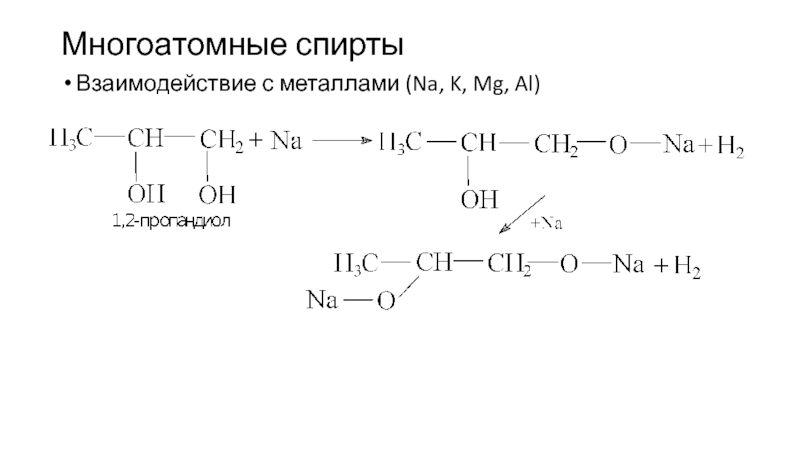
- 47. Многоатомные спирты Взаимодействие с металлами (Na, K, Mg, Al)
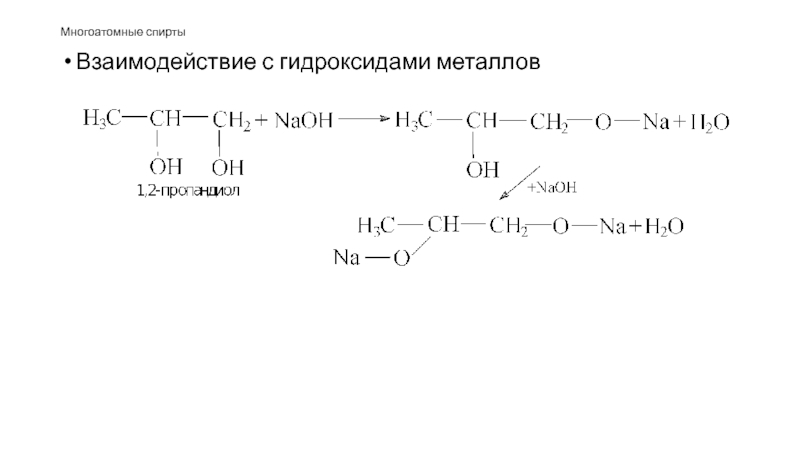
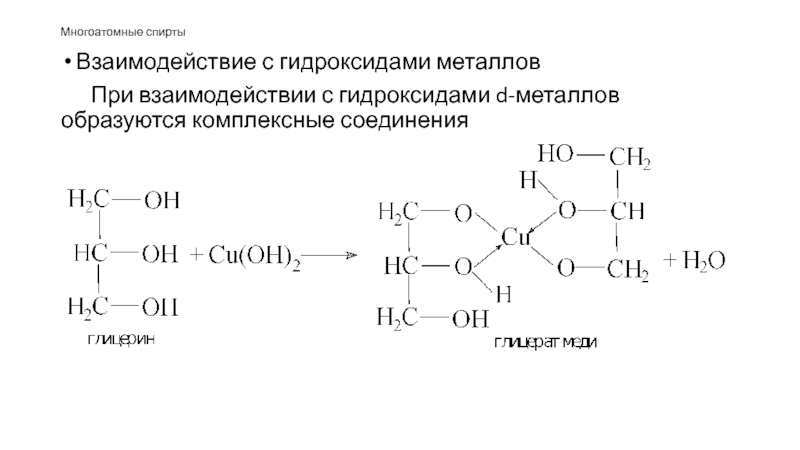
- 48. Многоатомные спирты Взаимодействие с гидроксидами металлов
- 49. Многоатомные спирты Взаимодействие с гидроксидами металлов При взаимодействии с гидроксидами d-металлов образуются комплексные соединения
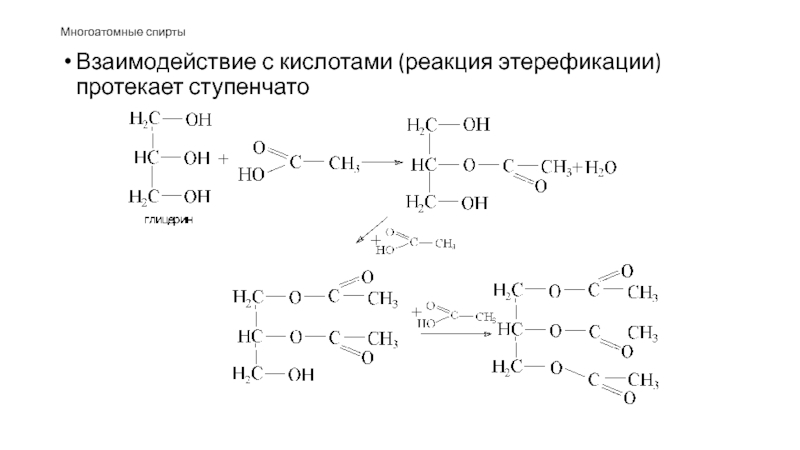
- 50. Многоатомные спирты Взаимодействие с кислотами (реакция этерефикации) протекает ступенчато
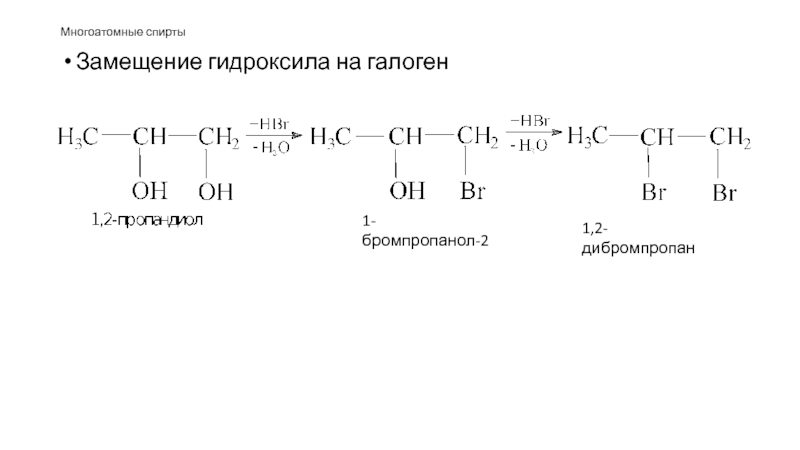
- 51. Многоатомные спирты Замещение гидроксила на галоген
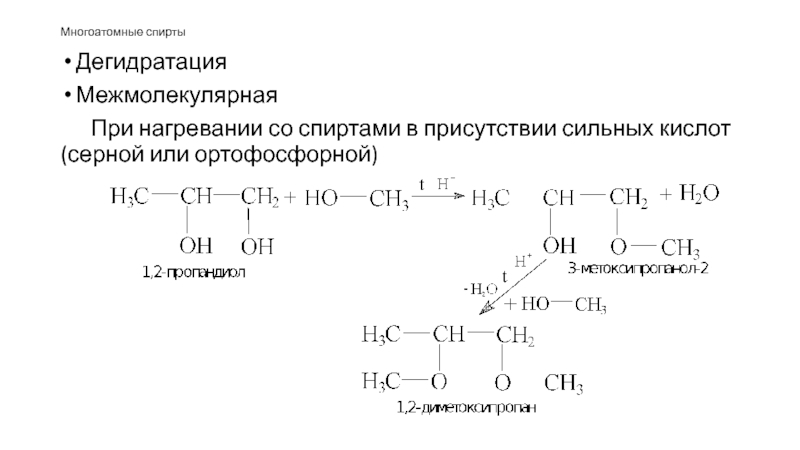
- 52. Дегидратация Межмолекулярная При нагревании со спиртами в присутствии сильных кислот (серной или ортофосфорной) Многоатомные спирты
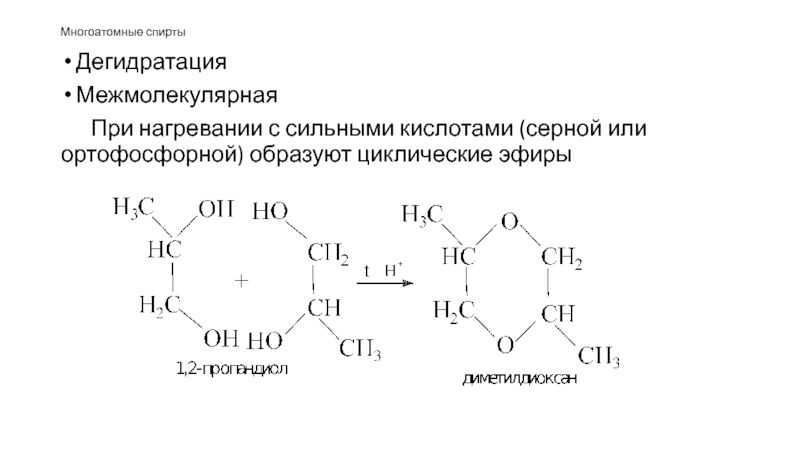
- 53. Дегидратация Межмолекулярная При нагревании с сильными кислотами (серной или ортофосфорной) образуют циклические эфиры Многоатомные спирты
- 54. Дегидратация Внутримолекулярная В случае гликолей с изолированными
- 55. Дегидратация Внутримолекулярная В случае гликолей с изолированными гидроксогруппами (β-гликоли) происходит образование непредельных спиртов Многоатомные спирты
- 56. Дегидратация Особым образом происходит этот процесс в
- 57. Окисление В общем виде окисление многоатомных спиртов
- 58. Окисление Особым образом протекает окисление пинаколинов тетраацетатом свинца и периодатами Многоатомные спирты
- 59. Отдельные представители спиртов
- 60. Метанол (метиловый спирт, древесный спирт, карбинол)
- 61. Метанол -жидкость без цвета с температурой кипения
- 62. ПРИМЕНЕНИЕ метилового спирта
- 63. метанол Форм-альдегид (смолы) Уксусная кислота Изопрен
- 64. В газовой промышленности используется для борьбы с
- 65. Во многих странах метанол применяется в качестве
- 66. Метанол — опаснейший яд, приём внутрь 5—10 мл
- 67. Этиловый спирт (Этанол)
- 68. Этанол-бесцветная жидкость с характерным запахом и жгучим
- 69. Применение этанола
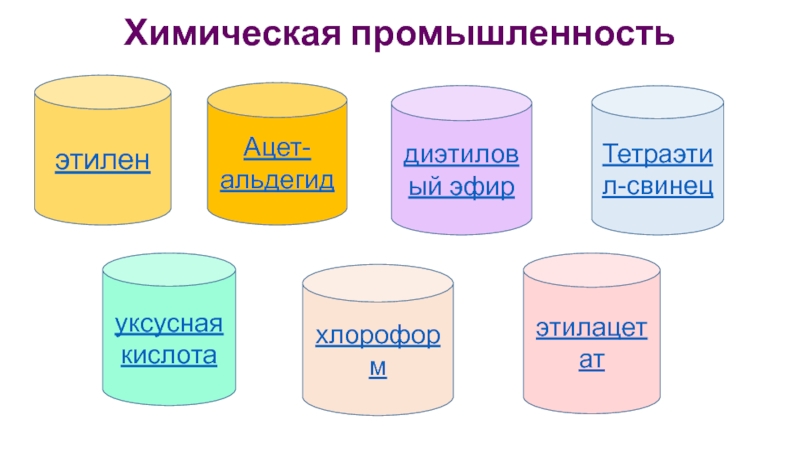
- 70. Химическая промышленность Ацет-альдегид диэтиловый эфир Тетраэтил-свинец уксусная кислота хлороформ этилацетат этилен
- 71. Растворитель В лакокрасочной промышленности, в производстве товаров
- 72. Парфюмерия и косметика Является универсальным растворителем различных
- 73. Этиловый спирт также используется как топливо.
- 74. В медицине антисептик; подсушивающие и дубящие свойства
- 75. Пищевая промышленность Является основным компонентом спиртных напитков.
- 76. Этиловый спирт по своему действию на организм
- 77. Этиленгликоль Прозрачная бесцветная
- 78. Применение Как компонент автомобильных антифризов и тормозных
- 79. В органическом синтезе для получения многих веществ
- 80. Этиленгликоль — горючее вещество. Температура вспышки паров 120 °C
- 81. Глицерин трехатомный предельный спирт. Бесцветная, вязкая,
- 82. Применяется в производстве взрывчатых веществ нитроглицерина.
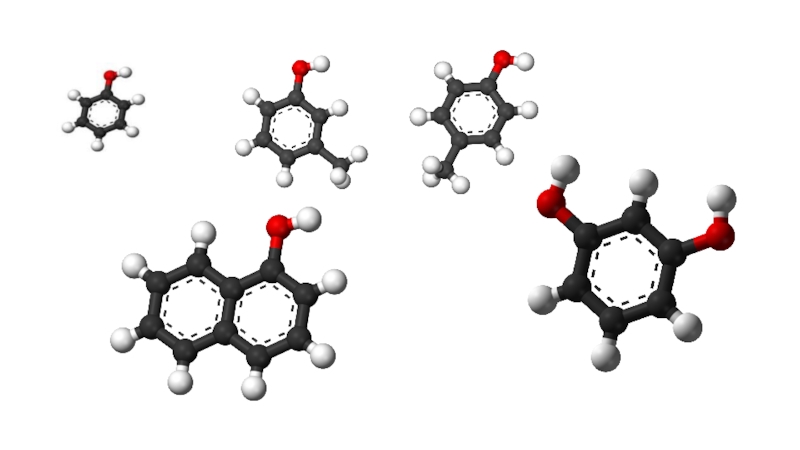
- 83. Гидроксилпроизводные ароматических углеводородов Фенолы
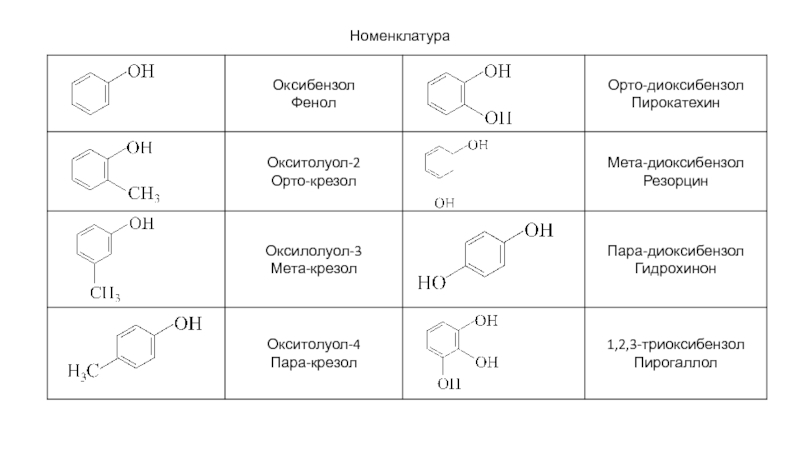
- 85. Номенклатура
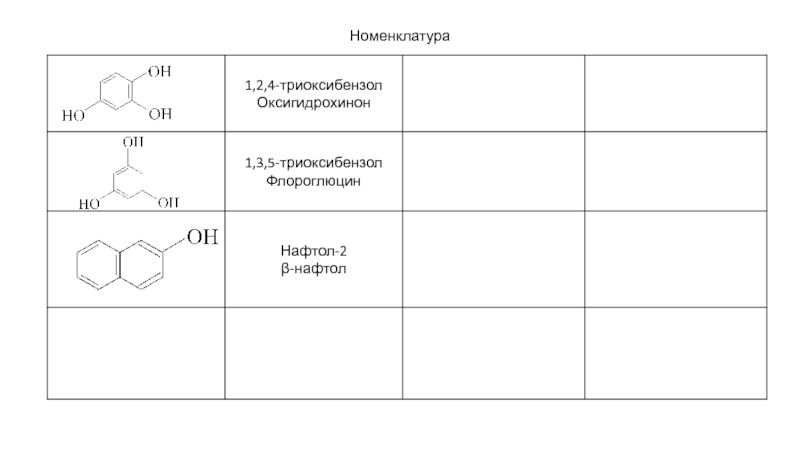
- 86. Номенклатура
- 87. Номенклатура
- 88. Изомерия Положения гидроксильных групп Строения и положения заместителей Межклассовая изомерия
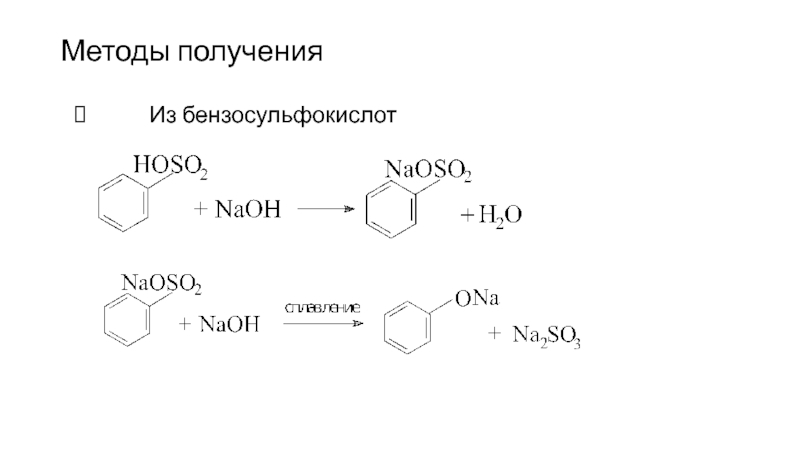
- 89. Методы получения Из бензосульфокислот
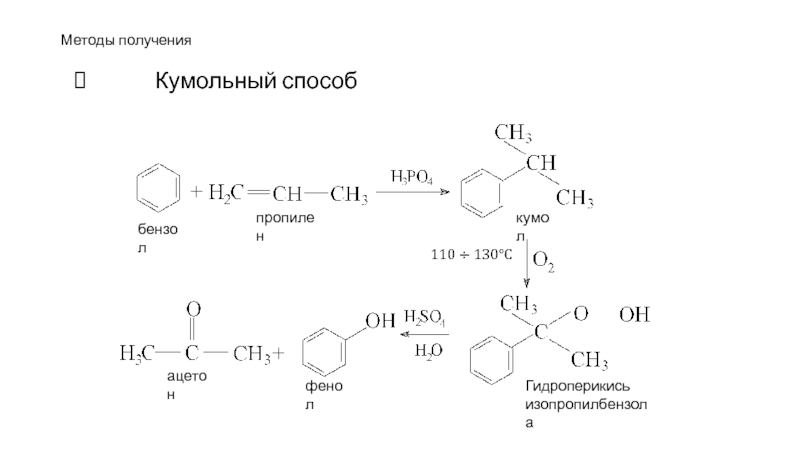
- 90. Методы получения Кумольный способ
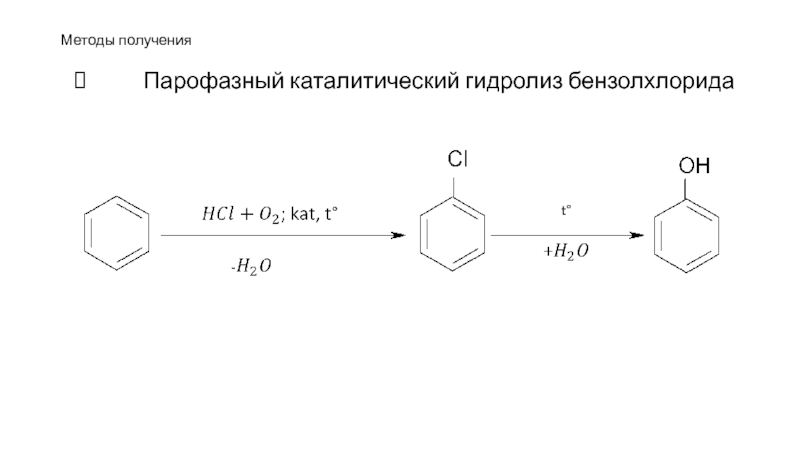
- 91. Методы получения Парофазный каталитический гидролиз бензолхлорида
- 92. Физические свойства и природа связей Фенолы при
- 93. Химические свойства Кислотность и реакции с участием
- 94. Химические свойства. Кислотность и реакции с участием
- 95. Химические свойства. Кислотность и реакции с участием атома кислорода. Алкилирование
- 96. Химические свойства. Кислотность и реакции с участием атома кислорода. Ацилирование
- 97. Химические свойства. Окисление.
- 98. Химические свойства. Реакции с электрофильными реагентами. Галогенирование.
- 99. Химические свойства. Реакции с электрофильными реагентами. Нитрование.
- 100. Химические свойства. Реакции с электрофильными реагентами. Сульфирование.
- 101. Химические свойства. Реакции с электрофильными реагентами. Ацилирование.
- 102. Химические свойства. Реакции с электрофильными реагентами. Алкилирование.
- 103. Химические свойства. Гидрирование.
Слайд 2Гидроксилпроизводные – это такие производные углеводородов, в состав молекулы которых входит
одна или несколько гидроксильных групп.
Слайд 3Классификация
В зависимости от количества гидроксильных групп различают:
Одноатомные;
Двухатомные;
Трех- и многоатомные.
В зависимости от
типа углеродного скелета различают:
Нециклические (ациклические);
Циклические.
В зависимости от наличия кратных связей различают:
Насыщенные;
Ненасыщенные.
Нециклические (ациклические);
Циклические.
В зависимости от наличия кратных связей различают:
Насыщенные;
Ненасыщенные.
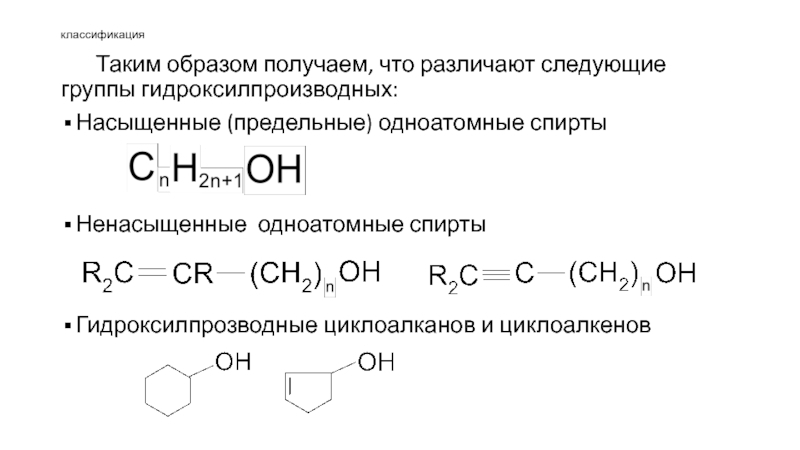
Слайд 5классификация
Таким образом получаем, что различают следующие группы гидроксилпроизводных:
Насыщенные (предельные) одноатомные
спирты
Ненасыщенные одноатомные спирты
Гидроксилпрозводные циклоалканов и циклоалкенов
Ненасыщенные одноатомные спирты
Гидроксилпрозводные циклоалканов и циклоалкенов
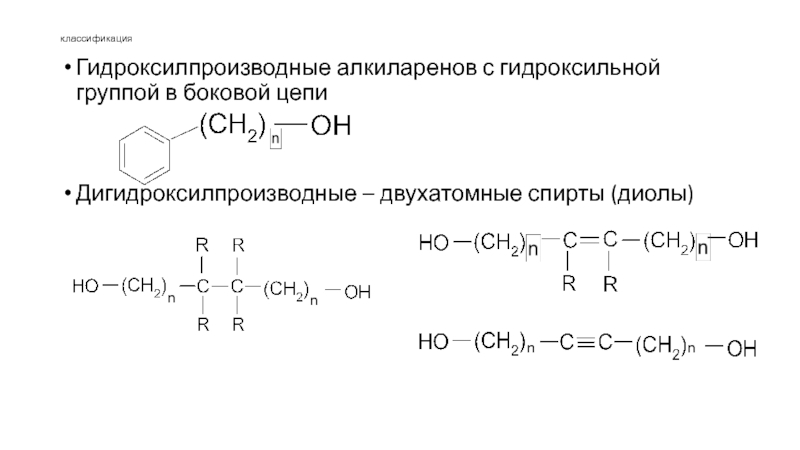
Слайд 6классификация
Гидроксилпроизводные алкиларенов с гидроксильной группой в боковой цепи
Дигидроксилпроизводные – двухатомные спирты
(диолы)
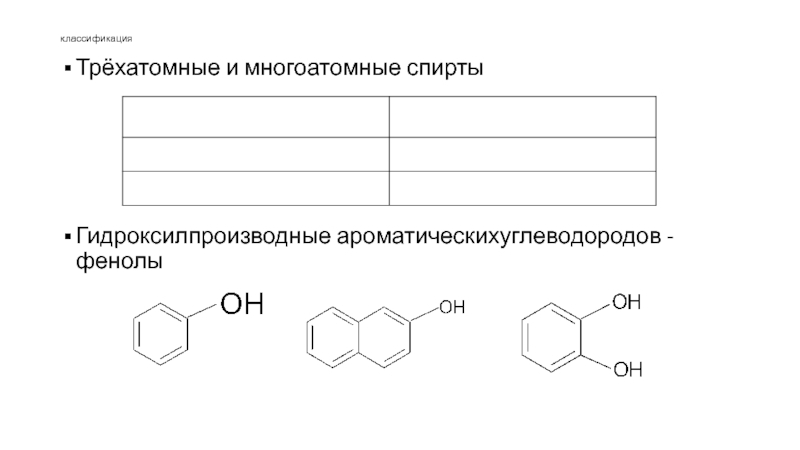
Слайд 7классификация
Трёхатомные и многоатомные спирты
Гидроксилпроизводные ароматическихуглеводородов - фенолы
Слайд 15Спирты - это производные углеводородов, содержащие одну или несколько гидроксильных групп
(-O-H)
R-OH
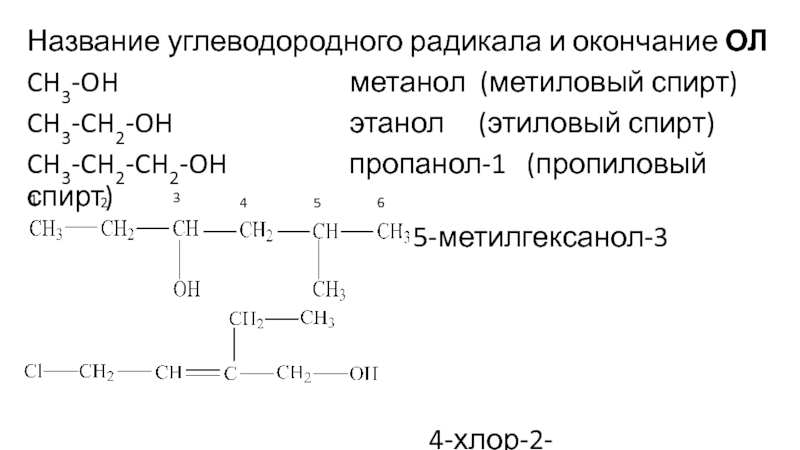
Слайд 19Название углеводородного радикала и окончание ОЛ
CH3-OH
метанол (метиловый спирт)
CH3-CH2-OH этанол (этиловый спирт)
CH3-CH2-CH2-OH пропанол-1 (пропиловый спирт)
5-метилгексанол-3
4-хлор-2-этилбутен-2-oл-1
CH3-CH2-OH этанол (этиловый спирт)
CH3-CH2-CH2-OH пропанол-1 (пропиловый спирт)
5-метилгексанол-3
4-хлор-2-этилбутен-2-oл-1
Слайд 20
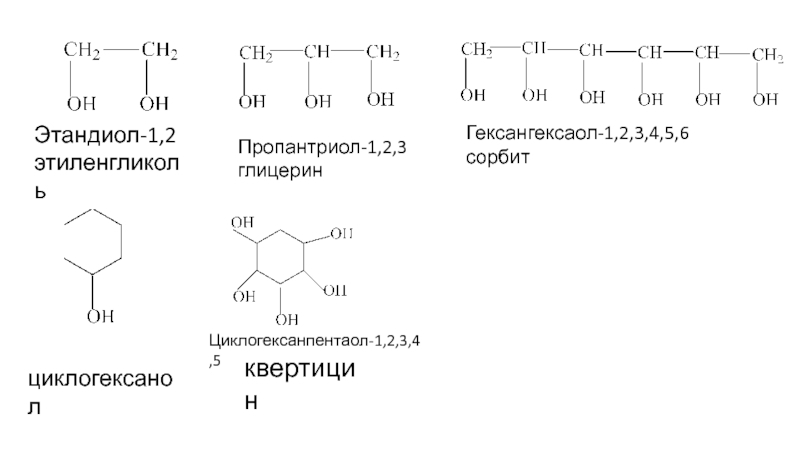
Этандиол-1,2
этиленгликоль
Пропантриол-1,2,3
глицерин
Гексангексаол-1,2,3,4,5,6
сорбит
циклогексанол
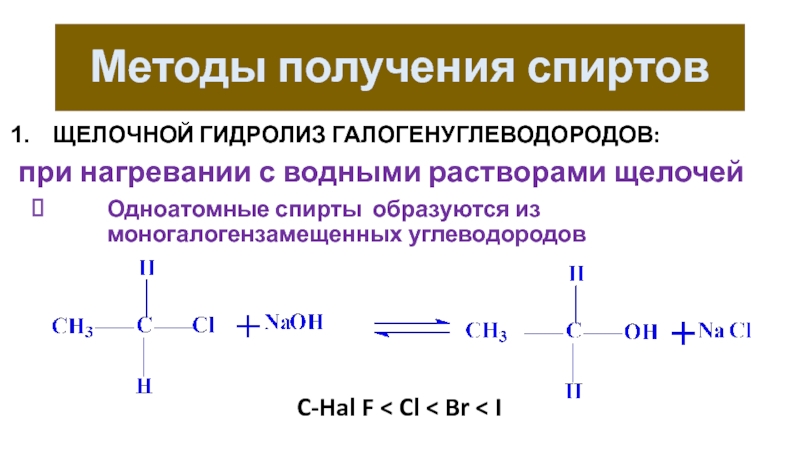
Слайд 21Методы получения спиртов
ЩЕЛОЧНОЙ ГИДРОЛИЗ ГАЛОГЕНУГЛЕВОДОРОДОВ:
при нагревании с водными растворами щелочей
Одноатомные спирты
образуются из моногалогензамещенных углеводородов
C-Hal F < Cl < Br < I
C-Hal F < Cl < Br < I
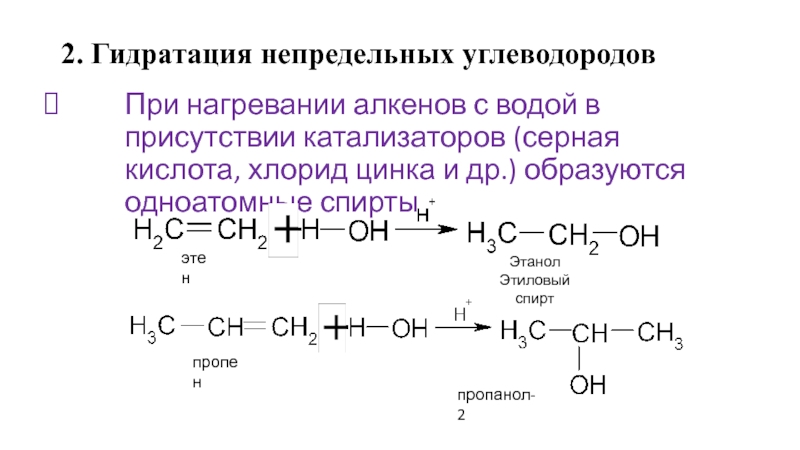
Слайд 232. Гидратация непредельных углеводородов
При нагревании алкенов с водой в присутствии катализаторов
(серная кислота, хлорид цинка и др.) образуются одноатомные спирты
Слайд 242. Гидратация непредельных углеводородов
При нагревании алкинов с водой в присутствии катализаторов
(серная кислота, хлорид цинка и др.) образуются двухатомные спирты
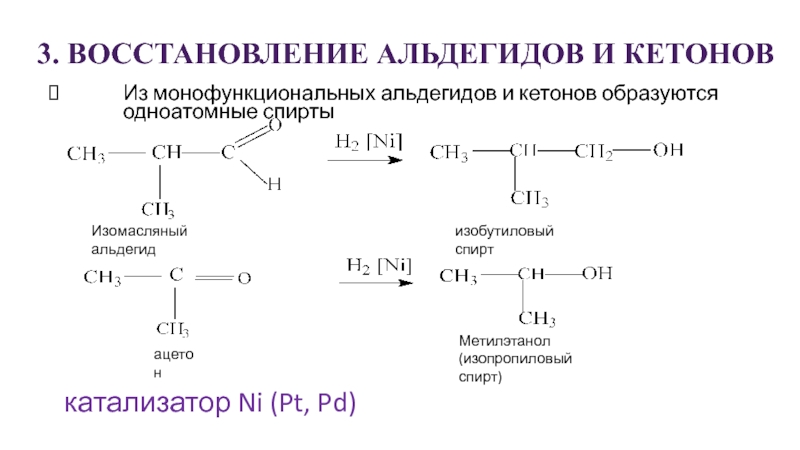
Слайд 253. ВОССТАНОВЛЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ
Из монофункциональных альдегидов и кетонов образуются одноатомные
спирты
катализатор Ni (Pt, Pd)
катализатор Ni (Pt, Pd)
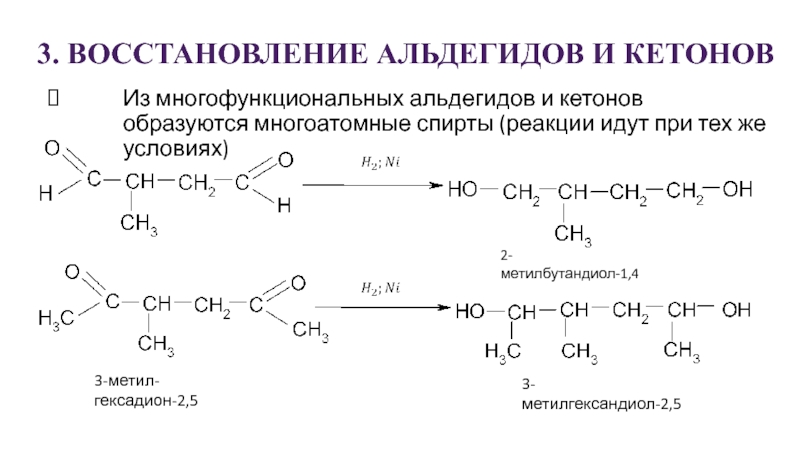
Слайд 263. ВОССТАНОВЛЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ
Из многофункциональных альдегидов и кетонов образуются многоатомные
спирты (реакции идут при тех же условиях)
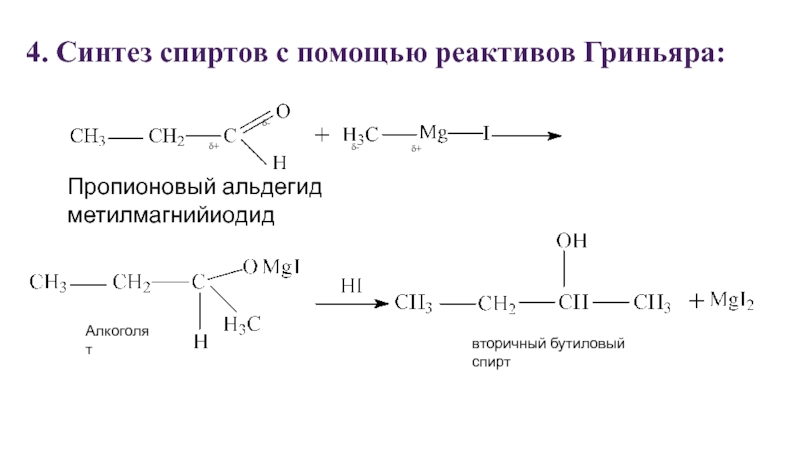
Слайд 274. Синтез спиртов с помощью реактивов Гриньяра:
Пропионовый альдегид метилмагнийиодид
δ+
δ-
δ-
δ+
Алкоголят
вторичный
бутиловый спирт
Слайд 28Этанол получают из пищевого и непищевого органического сырья путем сбраживания:
глюкоза
ферменты
Слайд 30Получение смеси спиртов - синтола
Условия: Нагревание, высокое давление,
катализатор (Fe, Co)
nCO
+2nH2 → CnH2n+1OH + (n-1)H2O
Слайд 31 Кроме того многоатомные спирты получают по реакции Вагнера, гидроксилированием алкенов
В качестве
окислителей применяют перекись водорода или щелочной раствор перманганата калия
Слайд 33Физические свойства спиртов
Молекулы спиртов ассоциированы за счет образования межмолекулярных водородных связей:
Низшие
и средние предельные одноатомные спирты, содержащие от одного до одиннадцати атомов углерода-жидкости.
Высшие спирты(начиная с С12Н25ОН) при комнатной температуре-твердые вещества.
Низшие спирты имеют характерный алкогольный запах и жгучий вкус, они хорошо растворимы в воде.
Высшие спирты(начиная с С12Н25ОН) при комнатной температуре-твердые вещества.
Низшие спирты имеют характерный алкогольный запах и жгучий вкус, они хорошо растворимы в воде.
Слайд 35Химические свойства спиртов
Спирты очень слабые электролиты (слабее воды)
CH3-CH2-O-H ↔CH3-CH2-O- + H+
Типы
реакций
Реакции с участием водорода гидроксильной группы.
Реакции с отщеплением или замещением гидроксилдьной группы
Реакции окисления
Реакции с участием водорода гидроксильной группы.
Реакции с отщеплением или замещением гидроксилдьной группы
Реакции окисления
Слайд 36I. Реакции с участием водорода
гидроксильной группы.
1. Замещение гидроксильного атома водорода
на металл. (Na,Mg,Al)
2R-O-H + 2Na →2R-O-Na + H2
Алкоголят натрия
CH3-CH2-O-Na +H2O→CH3-CH2-O-H +NaOH
2R-O-H + 2Na →2R-O-Na + H2
Алкоголят натрия
CH3-CH2-O-Na +H2O→CH3-CH2-O-H +NaOH
Слайд 38II. Реакции с отщеплением или замещением гидроксильной группы
1. Замещение гидроксила на
галоген:
CH3OH +PBr5 ↔ CH3Br + POBr3 + HBr
метанол бромметан
C3H7OH +SOCl2 ↔ C3H7Cl +SO2 + HCl
пропанол хлорпропан
C2H5OH + HBr ↔ C2H5Br + HOH
этанол бромэтан
CH3OH +PBr5 ↔ CH3Br + POBr3 + HBr
метанол бромметан
C3H7OH +SOCl2 ↔ C3H7Cl +SO2 + HCl
пропанол хлорпропан
C2H5OH + HBr ↔ C2H5Br + HOH
этанол бромэтан
Слайд 392. Отщепление воды с образованием алкенов
Условия: Нагревание с конц. H2SO4 или
ZnCl2 (Al2O3)
Слайд 403. Межмолекулярная дегидратация
Условия: нагревание избытка спирта с серной кислотой или пары
спирта при 2000С через порошок сульфата алюминия
CH3-CH2-O-H + H-O-CH2-CH3 →CH3–CH2-O-CH2-CH3 + HOH
Этанол диэтиловый эфир
CH3-CH2-O-H + H-O-CH2-CH3 →CH3–CH2-O-CH2-CH3 + HOH
Этанол диэтиловый эфир
Слайд 414. Замена гидроксила на аминогруппу
Условия: 3000С, Al2O3
R-O-H + NH3 →
R-NH2 + HOH
спирт амин
спирт амин
Слайд 42III. Реакции окисления, в которых одновременно принимают участие гидроксильная группа, α-водородные
атомы или соседние связи С-С
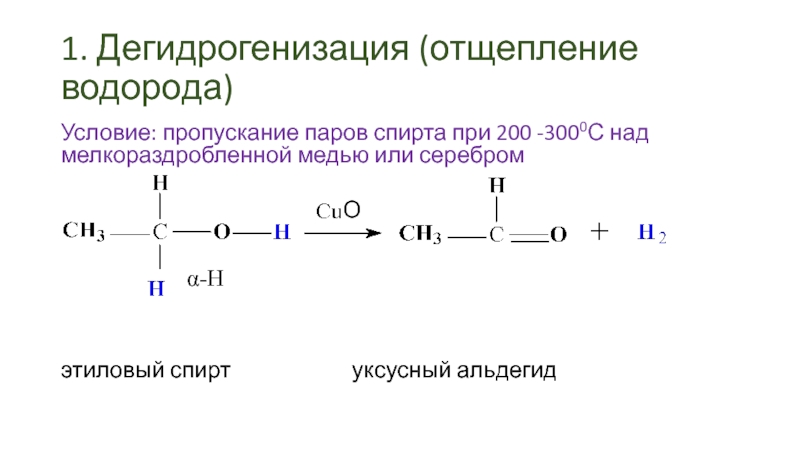
Слайд 431. Дегидрогенизация (отщепление водорода)
Условие: пропускание паров спирта при 200 -3000С над
мелкораздробленной медью или серебром
α-H
этиловый спирт уксусный альдегид
α-H
этиловый спирт уксусный альдегид
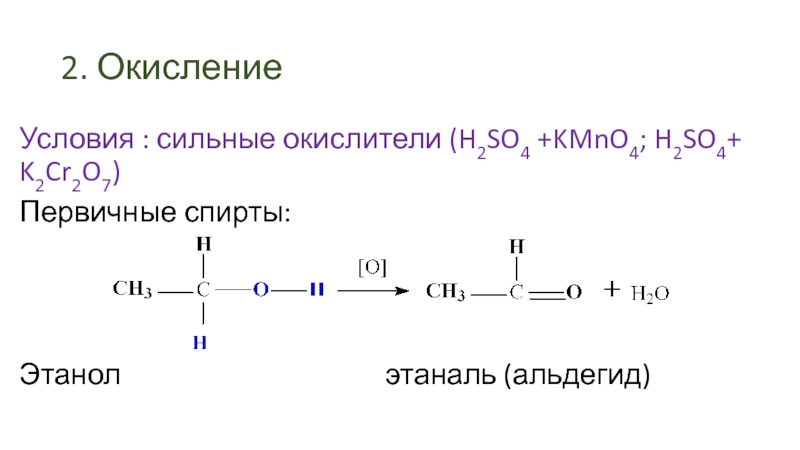
Слайд 442. Окисление
Условия : сильные окислители (H2SO4 +KMnO4; H2SO4+ K2Cr2O7)
Первичные спирты:
Этанол
этаналь (альдегид)
Слайд 49Многоатомные спирты
Взаимодействие с гидроксидами металлов
При взаимодействии с гидроксидами d-металлов образуются комплексные
соединения
Слайд 52Дегидратация
Межмолекулярная
При нагревании со спиртами в присутствии сильных кислот (серной или ортофосфорной)
Многоатомные
спирты
Слайд 53Дегидратация
Межмолекулярная
При нагревании с сильными кислотами (серной или ортофосфорной) образуют циклические эфиры
Многоатомные
спирты
Слайд 54Дегидратация
Внутримолекулярная
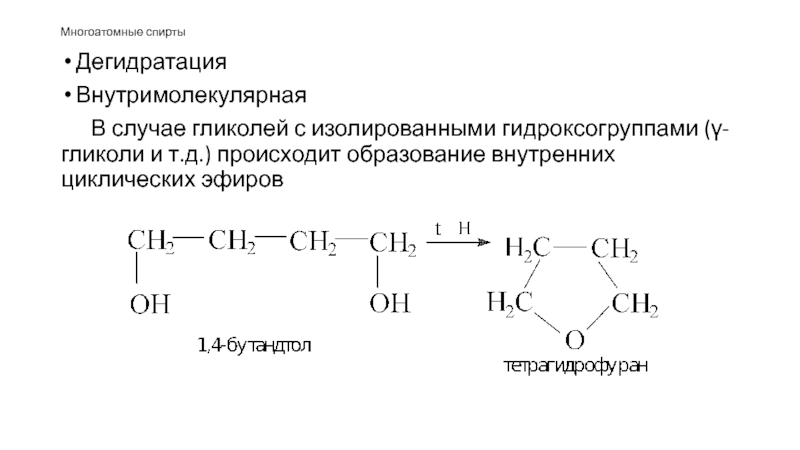
В случае гликолей с изолированными гидроксогруппами (γ-гликоли и т.д.) происходит образование
внутренних циклических эфиров
Многоатомные спирты
Слайд 55Дегидратация
Внутримолекулярная
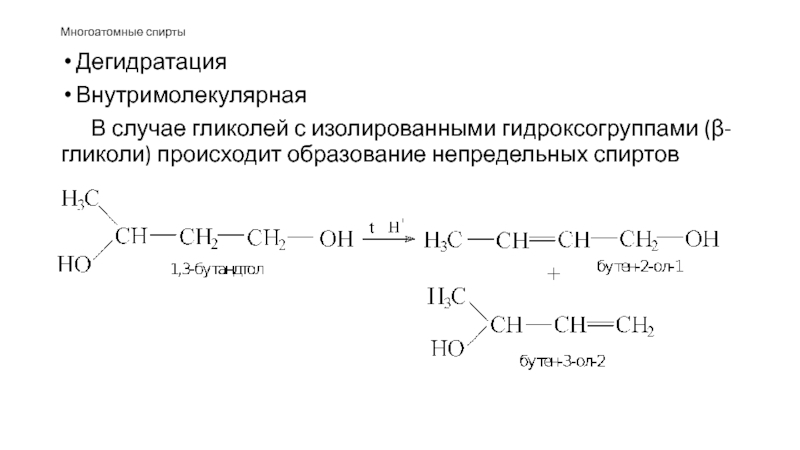
В случае гликолей с изолированными гидроксогруппами (β-гликоли) происходит образование непредельных спиртов
Многоатомные
спирты
Слайд 56Дегидратация
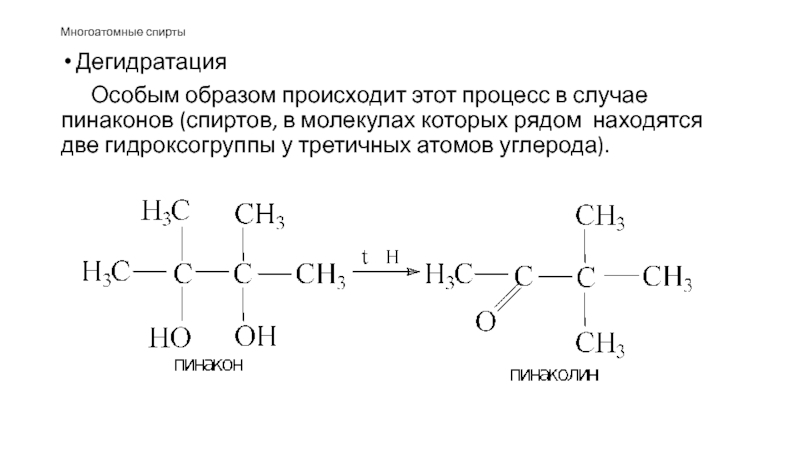
Особым образом происходит этот процесс в случае пинаконов (спиртов, в молекулах
которых рядом находятся две гидроксогруппы у третичных атомов углерода).
Многоатомные спирты
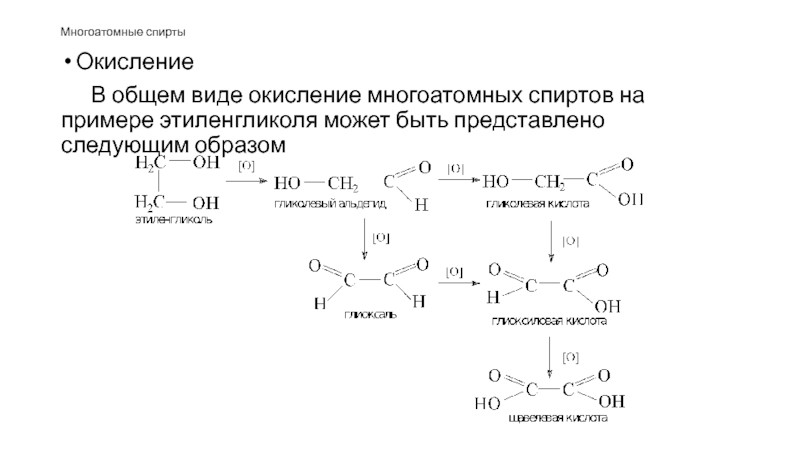
Слайд 57Окисление
В общем виде окисление многоатомных спиртов на примере этиленгликоля может быть
представлено следующим образом
Многоатомные спирты
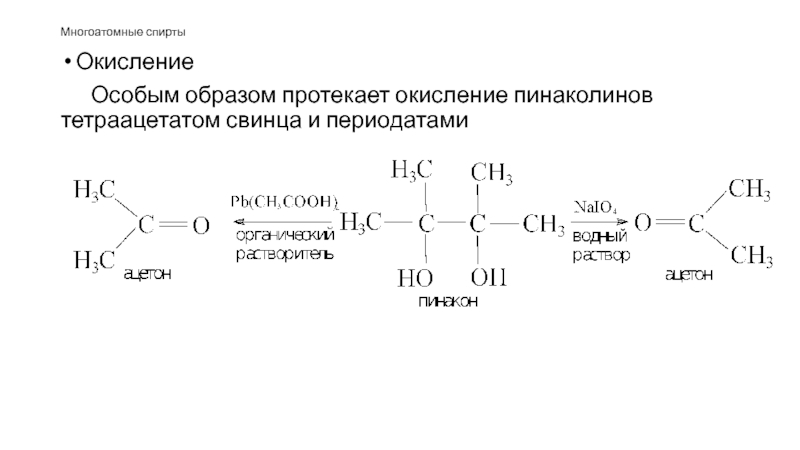
Слайд 58Окисление
Особым образом протекает окисление пинаколинов тетраацетатом свинца и периодатами
Многоатомные спирты
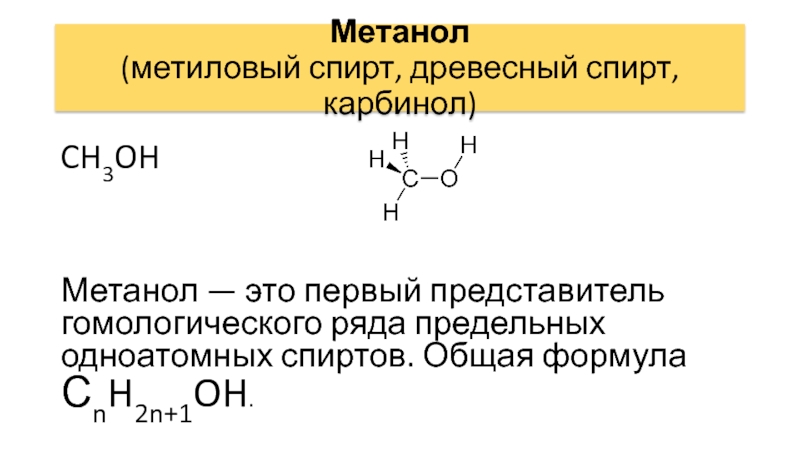
Слайд 60Метанол
(метиловый спирт, древесный спирт, карбинол)
CH3OH
Метанол — это первый представитель гомологического
ряда предельных одноатомных спиртов. Общая формула СnH2n+1OH.
Слайд 61Метанол
-жидкость без цвета с температурой кипения 64 0С,
с характерным запахом,
легче воды, горит бесцветным пламенем.
С воздухом в объёмных концентрациях 6,72—36,5 % образует взрывоопасные смеси (температура вспышки 15,6 °C).
Метанол смешивается в любых соотношениях с водой и большинством органических растворителей.
С воздухом в объёмных концентрациях 6,72—36,5 % образует взрывоопасные смеси (температура вспышки 15,6 °C).
Метанол смешивается в любых соотношениях с водой и большинством органических растворителей.
Слайд 63
метанол
Форм-альдегид
(смолы)
Уксусная кислота
Изопрен
Формалин
Эфиры
Растворитель в лакокрасочной промышленности
Топливные элементы
Добавка к моторному топливу
Слайд 64В газовой промышленности используется для борьбы с образованием гидратов.
(При добыче газа
гидраты могут образовываться в стволах скважин, промышленных коммуникациях и магистральных газопроводах. Отлагаясь на стенках труб, гидраты резко уменьшают их пропускную способность. )
Слайд 65Во многих странах метанол применяется в качестве добавки к этиловому спирту
при производстве парфюмерии.
В России использование метанола в потребительских товарах запрещено.
В России использование метанола в потребительских товарах запрещено.
Слайд 66Метанол — опаснейший яд, приём внутрь 5—10 мл метанола приводит к тяжёлому
отравлению и слепоте, а 30 граммов и более — к смерти.
ПДК метанола в воздухе рабочей зоны равна 5 мг/м³
(у этанола — 1000 мг/м³).
ПДК метанола в воздухе рабочей зоны равна 5 мг/м³
(у этанола — 1000 мг/м³).
Слайд 68Этанол-бесцветная жидкость с характерным запахом и жгучим вкусом, температурой кипения78 0С.
Легче воды. Смешивается с ней в любых отношениях. Легко воспламеняется, горит слабо светящимся голубоватым пламенем.
Слайд 70Химическая промышленность
Ацет-альдегид
диэтиловый эфир
Тетраэтил-свинец
уксусная кислота
хлороформ
этилацетат
этилен
Слайд 71Растворитель
В лакокрасочной промышленности,
в производстве товаров бытовой химии (в чистящих и моющих
средствах, в особенности для ухода за стеклом и сантехникой) ;
является компонентом антифризов и стеклоомывателей;
получение репеллентов
является компонентом антифризов и стеклоомывателей;
получение репеллентов
Слайд 72Парфюмерия и косметика
Является универсальным растворителем различных веществ и основным компонентом духов,
аэрозолей.
Входит в состав зубных паст, шампуни, средств для душа.
Входит в состав зубных паст, шампуни, средств для душа.
Слайд 73Этиловый спирт также используется как топливо.
Применяется для консервирования биологических препаратов.
Является
наполнителем в спиртовых термометрах*.
Этанол
Т пл = -114,3 0С
Т кип = 78,4 0С
Ртуть
Т пл = +2,295 0С
Т кип = 626 0С
Слайд 74В медицине
антисептик;
подсушивающие и дубящие свойства 96%-го этилового спирта используются для обработки
операционного поля или для обработки рук хирурга;
растворитель для лекарственных средств, для приготовления настоек, экстрактов из растительного сырья и др.;
пеногаситель при подаче кислорода, искусственной вентиляции легких;
в согревающих компрессах;
компонент общей анестезии в ситуации дефицита медикаментозных средств;
противоядие при отравлении некоторыми токсичными метанолом и этиленгликолем.
растворитель для лекарственных средств, для приготовления настоек, экстрактов из растительного сырья и др.;
пеногаситель при подаче кислорода, искусственной вентиляции легких;
в согревающих компрессах;
компонент общей анестезии в ситуации дефицита медикаментозных средств;
противоядие при отравлении некоторыми токсичными метанолом и этиленгликолем.
Слайд 75Пищевая промышленность
Является основным компонентом спиртных напитков.
В небольших количествах содержится в ряде
напитков, получаемых брожением, но не причисляемых к алкогольным.
Растворитель для пищевых ароматизаторов.
Может быть использован как консервант для хлебобулочных изделий, а также в кондитерской промышленности.
Растворитель для пищевых ароматизаторов.
Может быть использован как консервант для хлебобулочных изделий, а также в кондитерской промышленности.
Слайд 76Этиловый спирт по своему действию на организм человека является:
Депресантом – психоактивным
веществом, угнетающим центральную нервную систему.
В зависимости от дозы, концентрации, пути попадания в организм и длительности воздействия этанол может обладать наркотическим и токсическим действием.
смертельная разовая доза — 4—12 граммов этанола на килограмм массы тела (на 50 кг от 500 г водки)
В зависимости от дозы, концентрации, пути попадания в организм и длительности воздействия этанол может обладать наркотическим и токсическим действием.
смертельная разовая доза — 4—12 граммов этанола на килограмм массы тела (на 50 кг от 500 г водки)
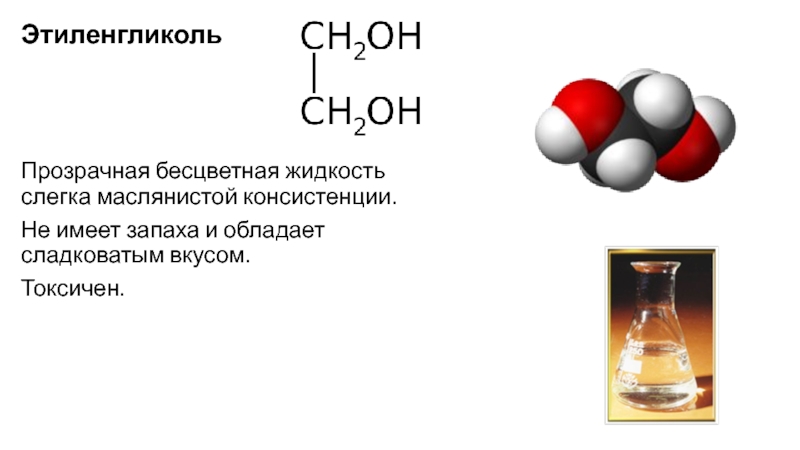
Слайд 77Этиленгликоль
Прозрачная бесцветная жидкость слегка маслянистой консистенции.
Не имеет запаха и
обладает сладковатым вкусом.
Токсичен.
Токсичен.
Слайд 78Применение
Как компонент автомобильных антифризов и тормозных жидкостей. Смесь 60 % этиленгликоля и
40 % воды замерзает при −45 °С. Коррозионно активен, поэтому применяется с ингибиторами коррозии;
В производстве целофана, полиуританов, лавсана и других полимеров.
В качестве теплоносителя в виде раствора в автомобилях, в системах жидкого охлаждения компьютеров;
Как растворитель красящих веществ;
В производстве целофана, полиуританов, лавсана и других полимеров.
В качестве теплоносителя в виде раствора в автомобилях, в системах жидкого охлаждения компьютеров;
Как растворитель красящих веществ;
Слайд 79В органическом синтезе для получения многих веществ и как высокотемпературный растворитель
Как
компонент жидкости «И», используемой для предотвращения обводнения авиационных топлив.
Для поглощения воды, для предотвращения образования гидрата метана.
Этиленгликоль является исходным сырьём для производства взрывчатого вещества нитрогликоля.
Компонент крема для обуви (1—2 %)
Входит в состав для мытья стёкол
Для поглощения воды, для предотвращения образования гидрата метана.
Этиленгликоль является исходным сырьём для производства взрывчатого вещества нитрогликоля.
Компонент крема для обуви (1—2 %)
Входит в состав для мытья стёкол
Слайд 80Этиленгликоль — горючее вещество. Температура вспышки паров 120 °C
Этиленгликоль токсичен. По степени воздействия
на организм относится к веществам 3-го класса опасности. Летальная доза при однократном употреблении составляет 100—300 мл.
Слайд 81Глицерин
трехатомный предельный спирт.
Бесцветная, вязкая, гигроскопичная, сладкая (гликос — сладкий) на вкус
жидкость.
Смешивается с водой в любых отношениях.
Смешивается с водой в любых отношениях.
Слайд 82Применяется
в производстве взрывчатых веществ нитроглицерина.
При обработке кожи.
Как компонент
некоторых клеев.
При производстве пластмасс глицерин используют в качестве пластификатора.
В производстве кондитерских изделий и напитков (как пищевая добавка E422).
При производстве пластмасс глицерин используют в качестве пластификатора.
В производстве кондитерских изделий и напитков (как пищевая добавка E422).
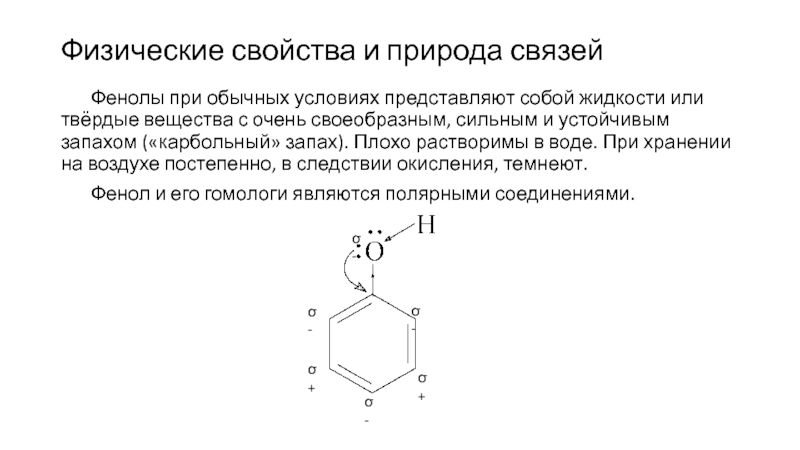
Слайд 92Физические свойства и природа связей
Фенолы при обычных условиях представляют собой жидкости
или твёрдые вещества с очень своеобразным, сильным и устойчивым запахом («карбольный» запах). Плохо растворимы в воде. При хранении на воздухе постепенно, в следствии окисления, темнеют.
Фенол и его гомологи являются полярными соединениями.
Фенол и его гомологи являются полярными соединениями.
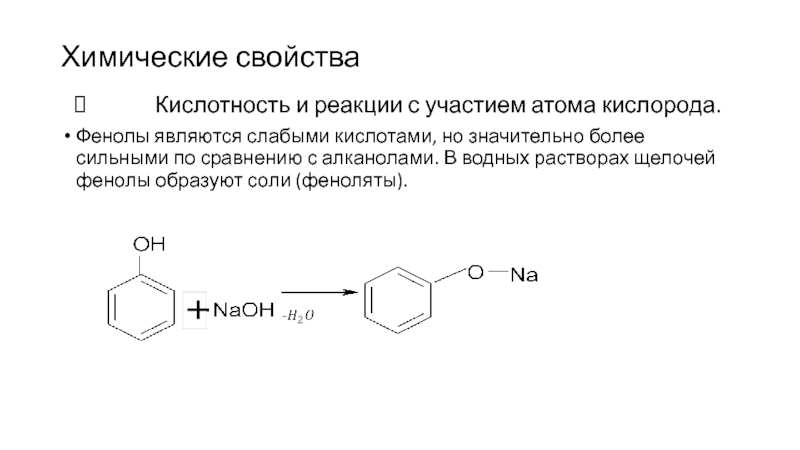
Слайд 93Химические свойства
Кислотность и реакции с участием атома кислорода.
Фенолы являются слабыми кислотами,
но значительно более сильными по сравнению с алканолами. В водных растворах щелочей фенолы образуют соли (феноляты).
Слайд 94Химические свойства. Кислотность и реакции с участием атома кислорода.
Фенолы имеют очень
характерную цветную реакцию: в водных растворах с FeCl3 они дают красно-фиолетовое окрашивание, которое исчезает после прибавления сильной кислоты или этанола.