- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Галогенопохідні вуглеводнів. Ізомерія органічних сполук. Просторова будова молекул презентация
Содержание
- 1. Галогенопохідні вуглеводнів. Ізомерія органічних сполук. Просторова будова молекул
- 2. Галогенпохідні вуглеводнів Галогенпохідними називаються похідні вуглеводнів,
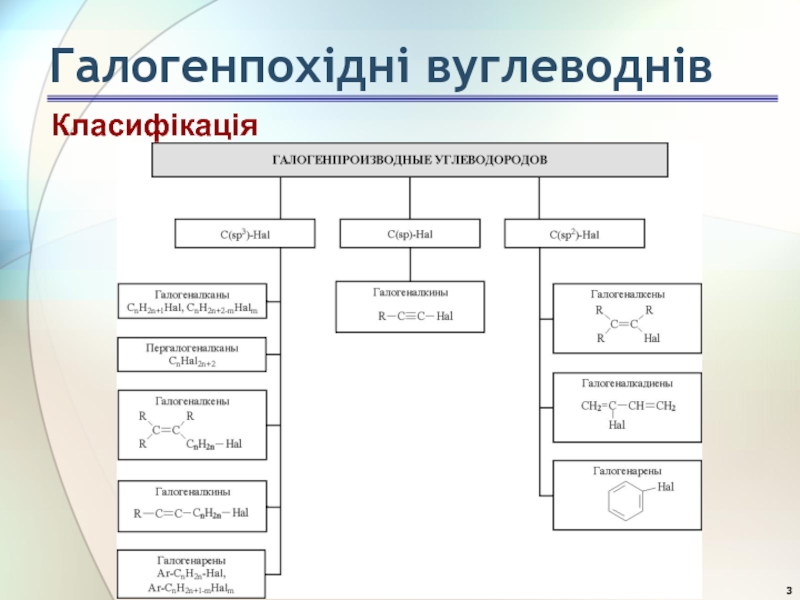
- 3. Класифікація Галогенпохідні вуглеводнів
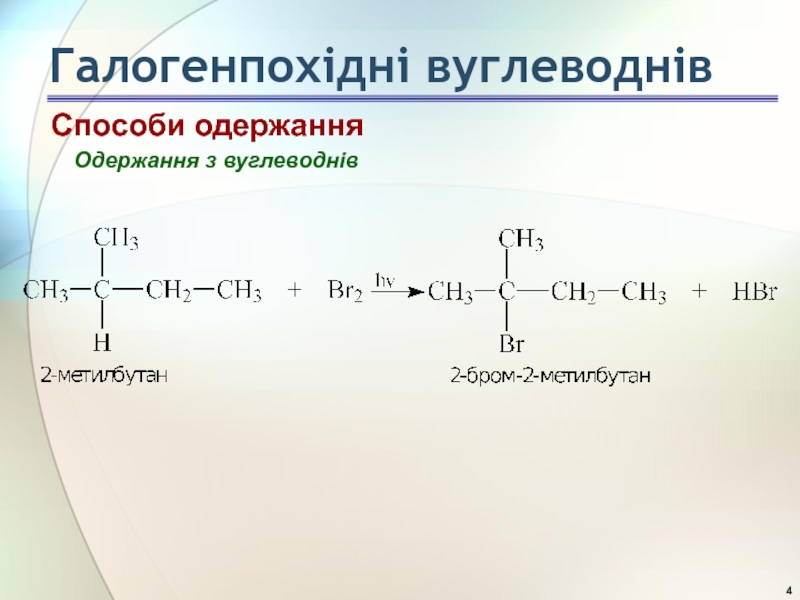
- 4. Способи одержання Одержання з вуглеводнів Галогенпохідні вуглеводнів
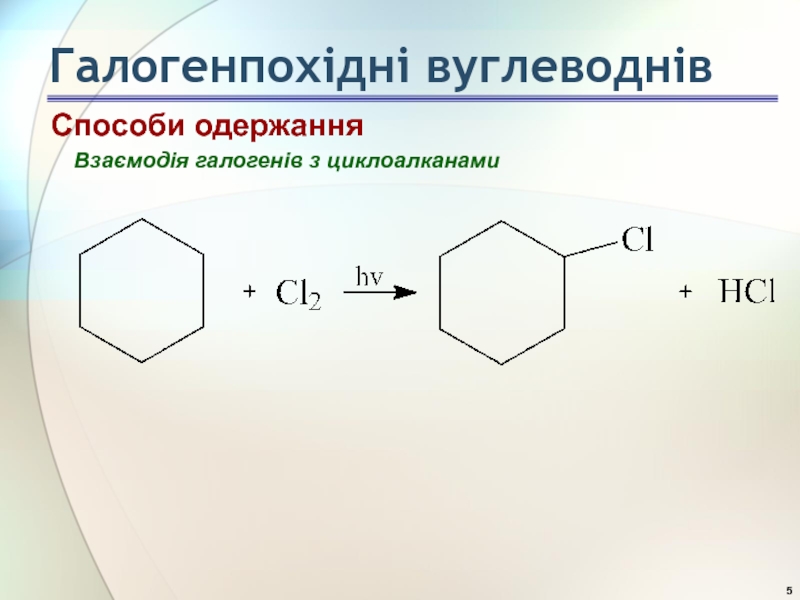
- 5. Взаємодія галогенів з циклоалканами Галогенпохідні вуглеводнів Способи одержання
- 6. Взаємодія галогенів з алкенами і алкінами Способи одержання Галогенпохідні вуглеводнів
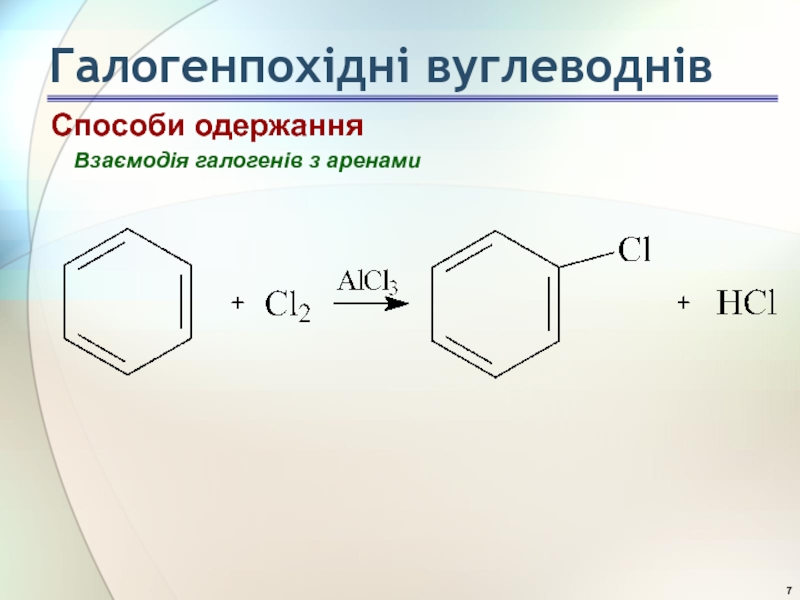
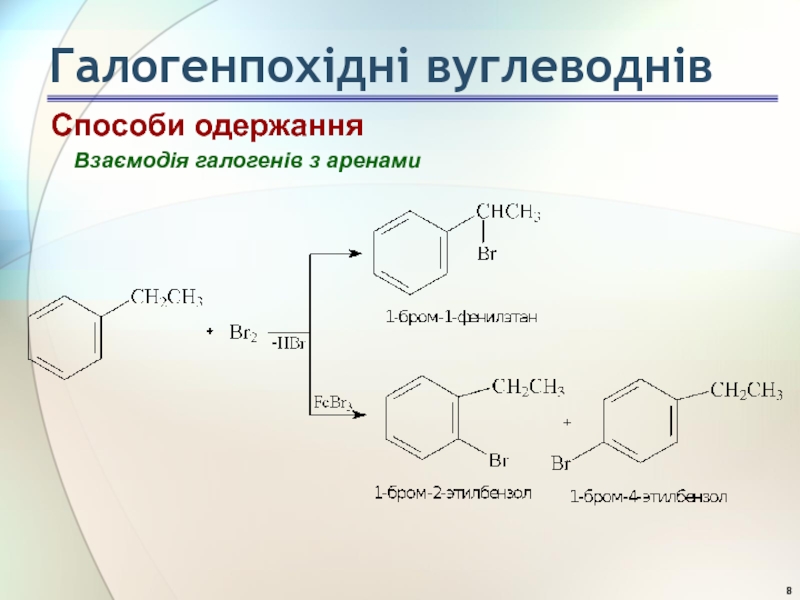
- 7. Способи одержання Взаємодія галогенів з аренами Галогенпохідні вуглеводнів
- 8. Взаємодія галогенів з аренами Галогенпохідні вуглеводнів Способи одержання
- 9. Взаємодія галогеноводнів з алкенами і алкінами
- 10. Способи одержання Взаємодія спиртів з галогеноводнями
- 11. Способи одержання Взаємодія спиртів з галогенідами
- 12. Способи одержання Взаємодія спиртів з тіонілхлоридом
- 13. Способи одержання Одержання з альдегідів і
- 14. Хімічні властивості Характеристика зв′язку C-Hal
- 15. Характеристика зв′язку C-Hal С—I >
- 16. Реакції нуклеофільного заміщення Реакції, в результаті
- 17. Реакції нуклеофільного заміщення Хімічні властивості Галогенпохідні вуглеводнів
- 18. Реакції нуклеофільного заміщення Взаємодія галогеналканів з
- 19. Реакції нуклеофільного заміщення Взаємодія галогеналканів с водними розчинами лугів Хімічні властивості Галогенпохідні вуглеводнів
- 20. Реакції нуклеофільного заміщення Взаємодія галогеналканів с
- 21. Швидкість реакції нуклеофільного заміщення
- 22. Нуклеофільна реакційна здатність реагента
- 23. Нуклеофільна реакційна здатність реагента NH3
- 24. Основність нуклеофільних реагентів I– < Br– < Cl– < F– Хімічні властивості Галогенпохідні вуглеводнів
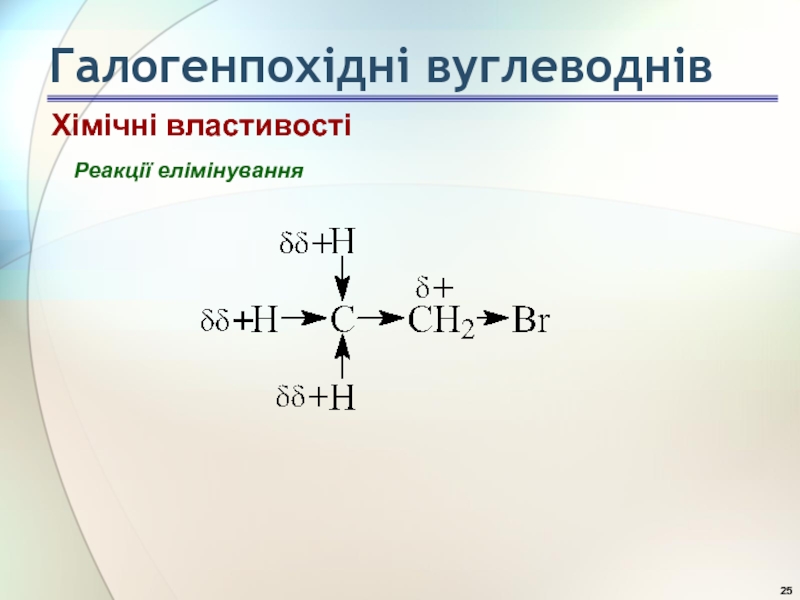
- 25. Реакції елімінування Хімічні властивості Галогенпохідні вуглеводнів
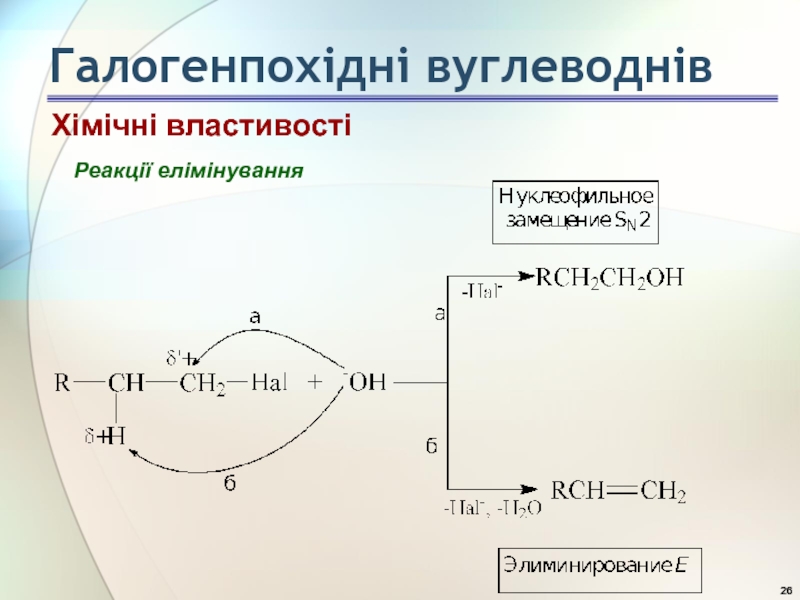
- 26. Реакції елімінування Хімічні властивості Галогенпохідні вуглеводнів
- 27. Реакції елімінування Хімічні властивості Галогенпохідні вуглеводнів
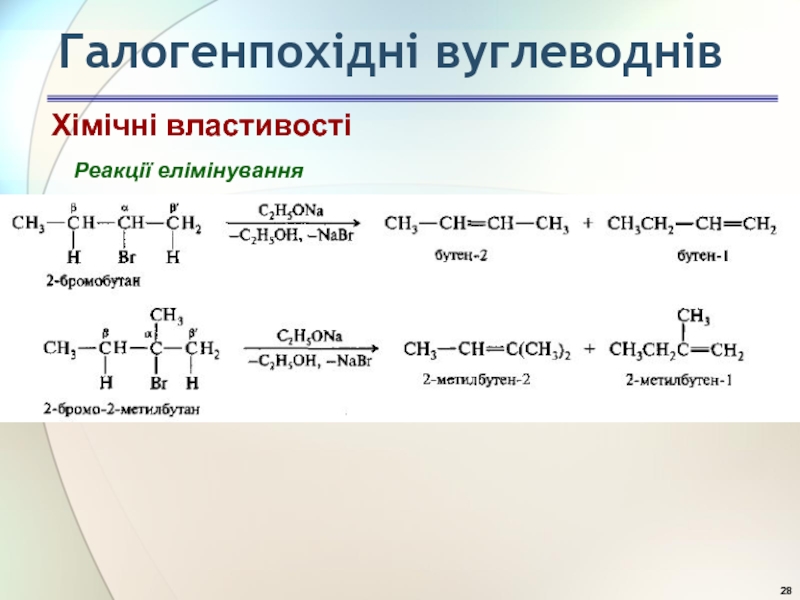
- 28. Реакції елімінування Хімічні властивості Галогенпохідні вуглеводнів
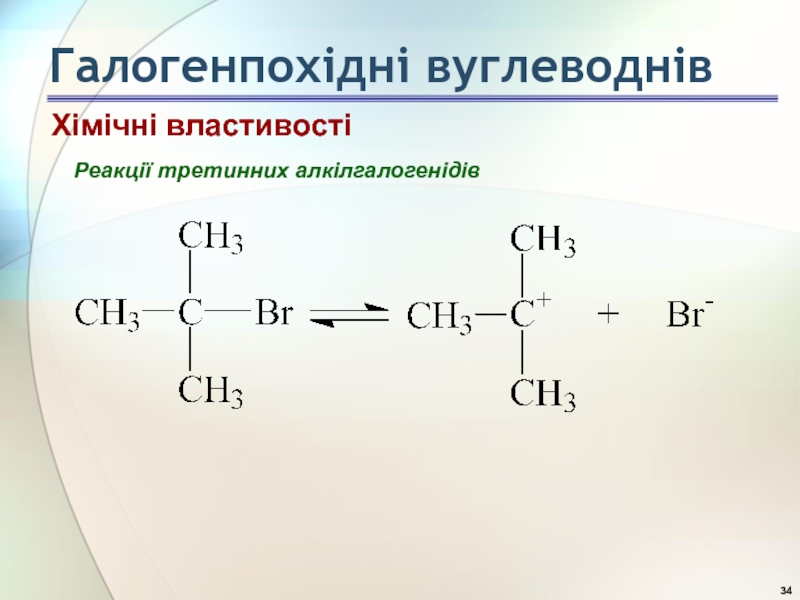
- 29. Реакції третинних алкілгалогенідів Хімічні властивості Галогенпохідні вуглеводнів
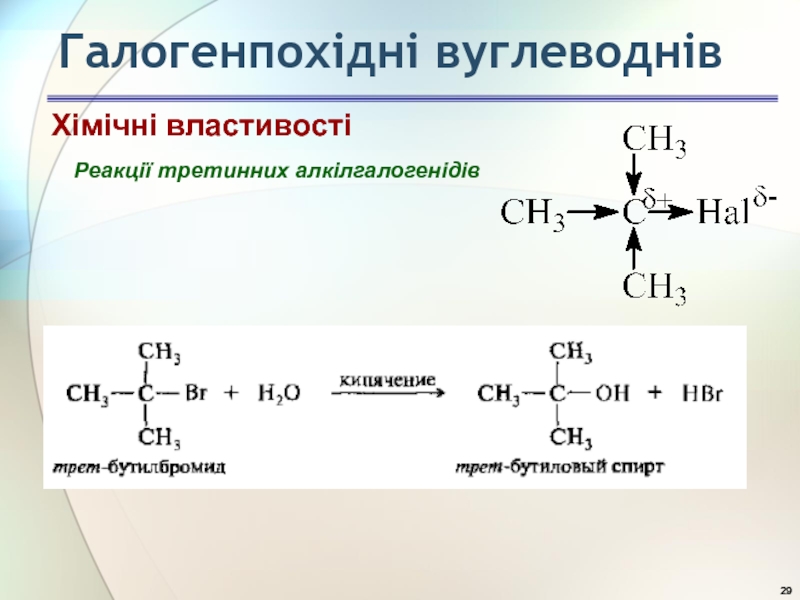
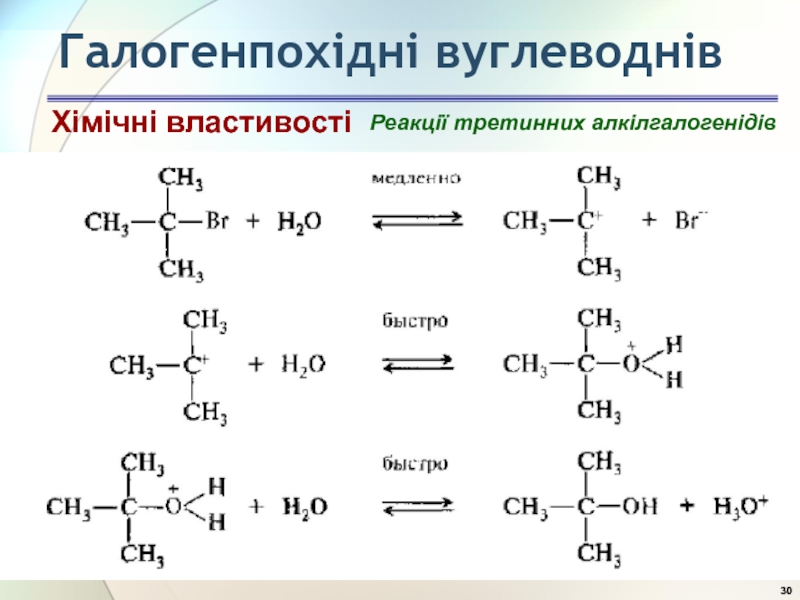
- 30. Галогенпохідні вуглеводнів Реакції третинних алкілгалогенідів Хімічні властивості
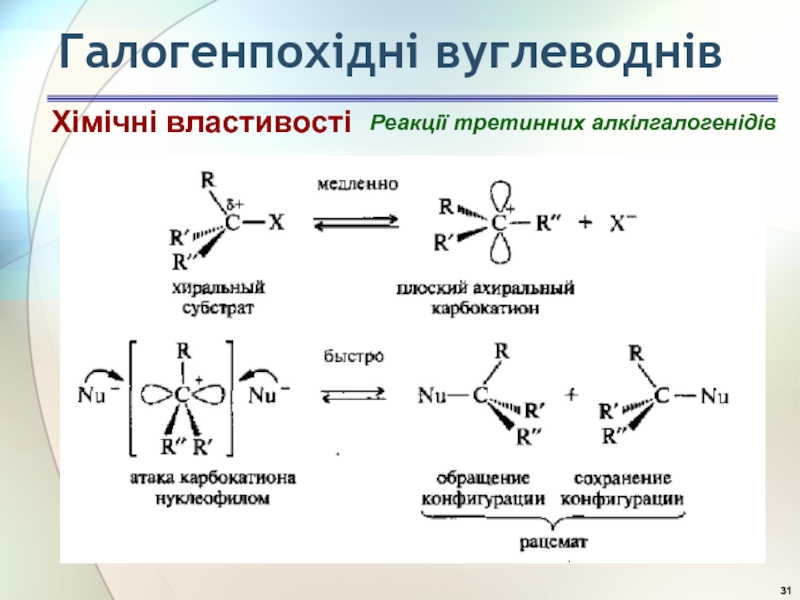
- 31. Галогенпохідні вуглеводнів Реакції третинних алкілгалогенідів Хімічні властивості
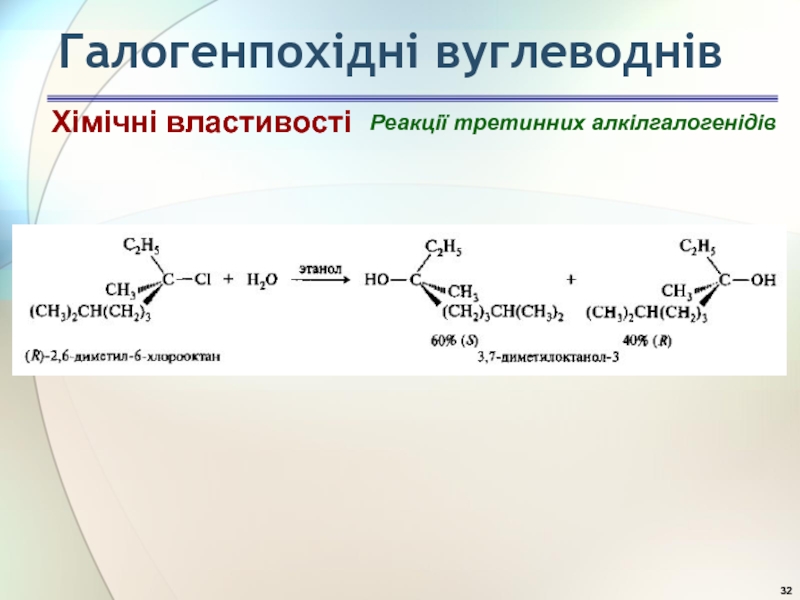
- 32. Галогенпохідні вуглеводнів Реакції третинних алкілгалогенідів Хімічні властивості
- 33. Реакції третинних алкілгалогенідів Хімічні властивості Галогенпохідні вуглеводнів
- 34. Реакції третинних алкілгалогенідів Хімічні властивості Галогенпохідні вуглеводнів
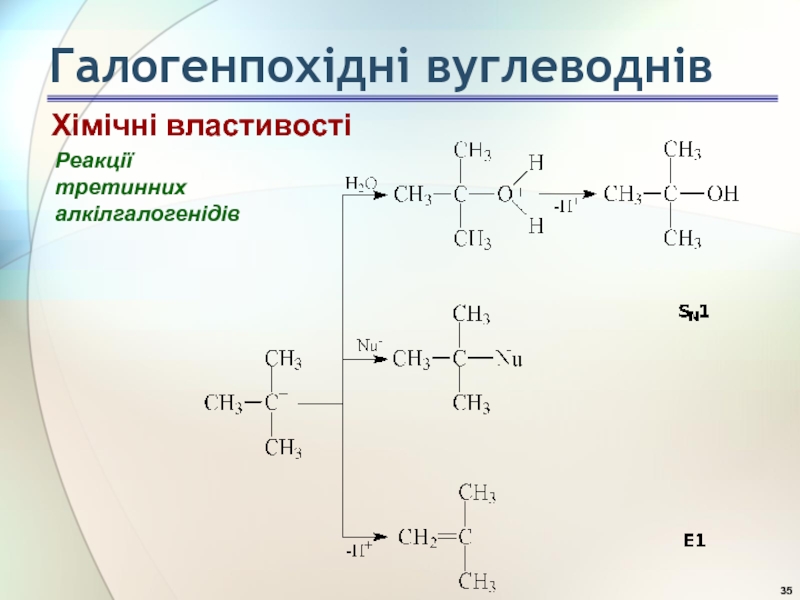
- 35. Реакції третинних алкілгалогенідів
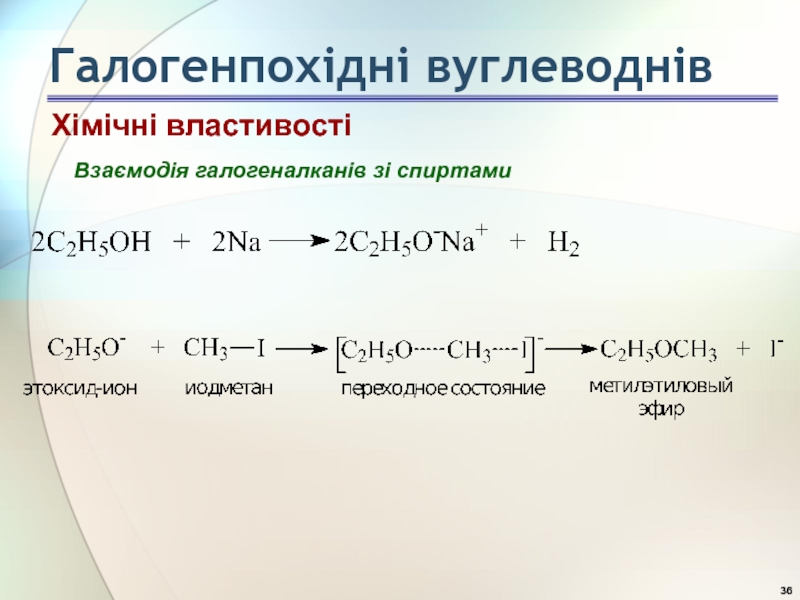
- 36. Взаємодія галогеналканів зі спиртами
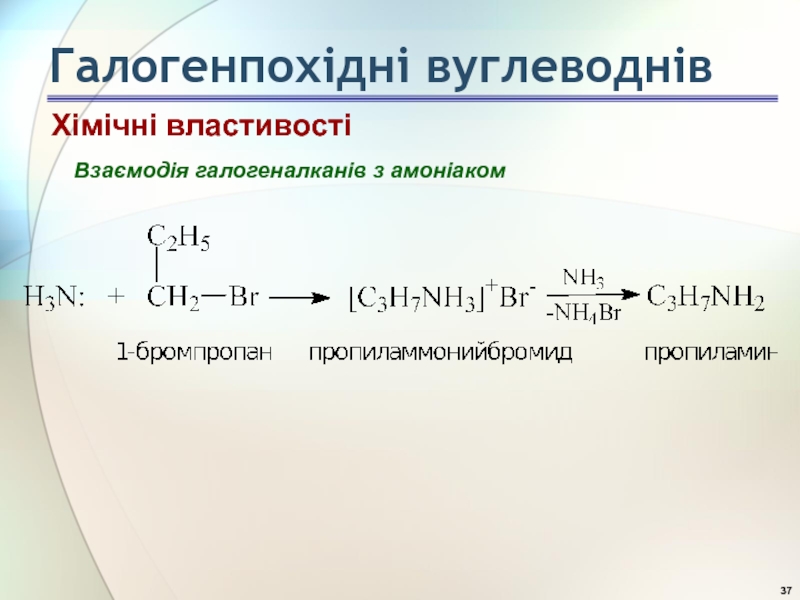
- 37. Взаємодія галогеналканів з амоніаком Хімічні властивості Галогенпохідні вуглеводнів
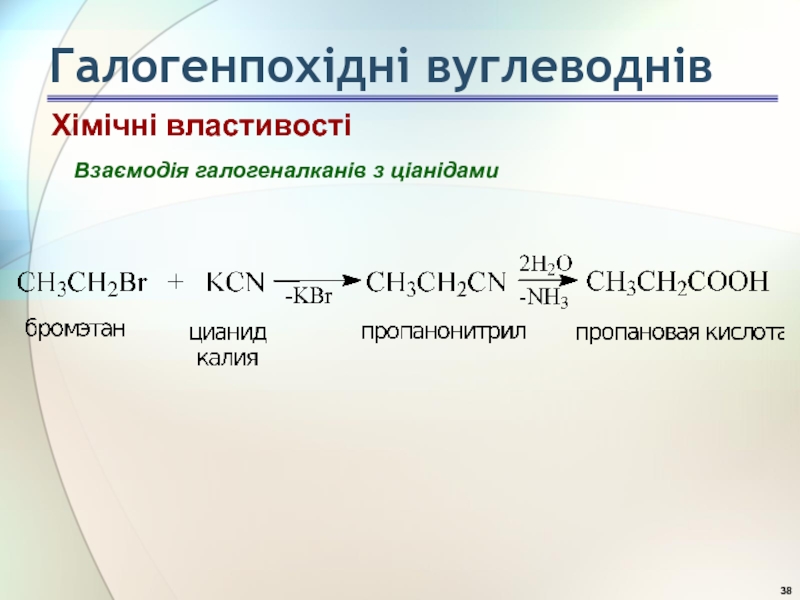
- 38. Взаємодія галогеналканів з ціанідами Хімічні властивості Галогенпохідні вуглеводнів
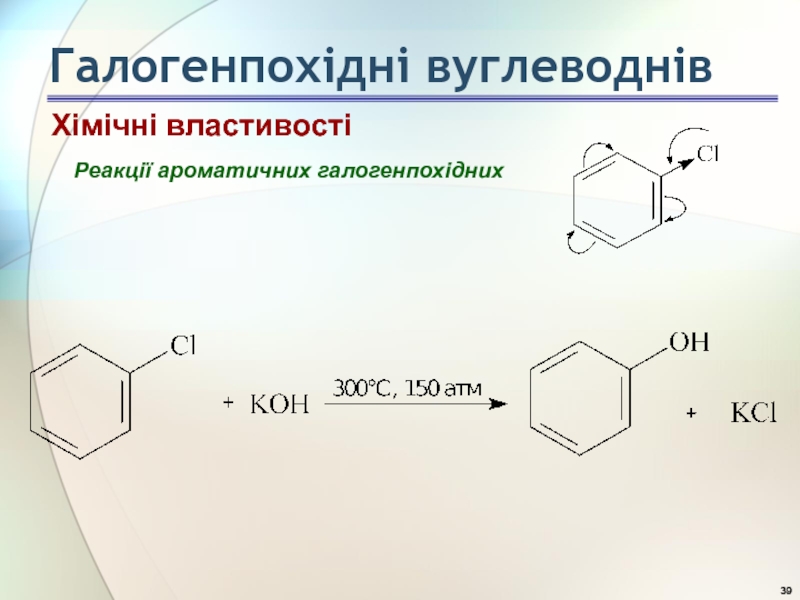
- 39. Реакції ароматичних галогенпохідних Хімічні властивості Галогенпохідні вуглеводнів
- 43. Просторова будова біологічно активних сполук.
- 44. Стереоізомерія Стереоізомери – це сполуки з однаковою
- 45. Стереоізомерія Конфігураційні стереоізомери характеризуються тим, що можуть
- 46. Стереоізомерія Конформація – просторове розташування атомів в
- 47. Конформації – деякі конформації більш стабільні за інші
- 48. Різна конфігурація
- 49. Геометрична ізомерія малеїнова кислота (цис-1,2-етан- дикарбонова кислота)
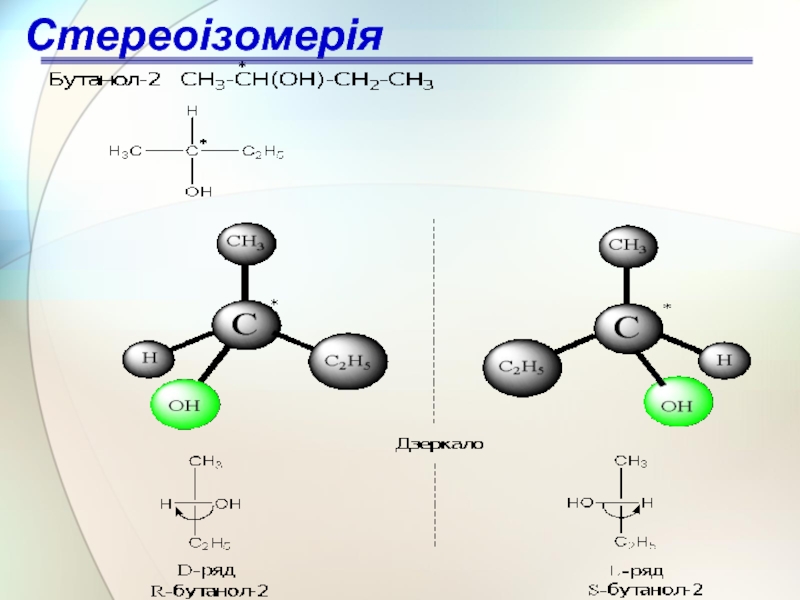
- 50. Енантіомери – це структури, що є дзеркальним
- 51. Стереоізомерія Н Br Cl I I Cl Br H
- 52. Оптична ізомерія S-α-амінопропіонова кислота R-α-амінопропіонова кислота Стереоізомерія
- 53. Стереоізомерія Оптична ізомерія S-α-амінопропіонова кислота R-α-амінопропіонова кислота
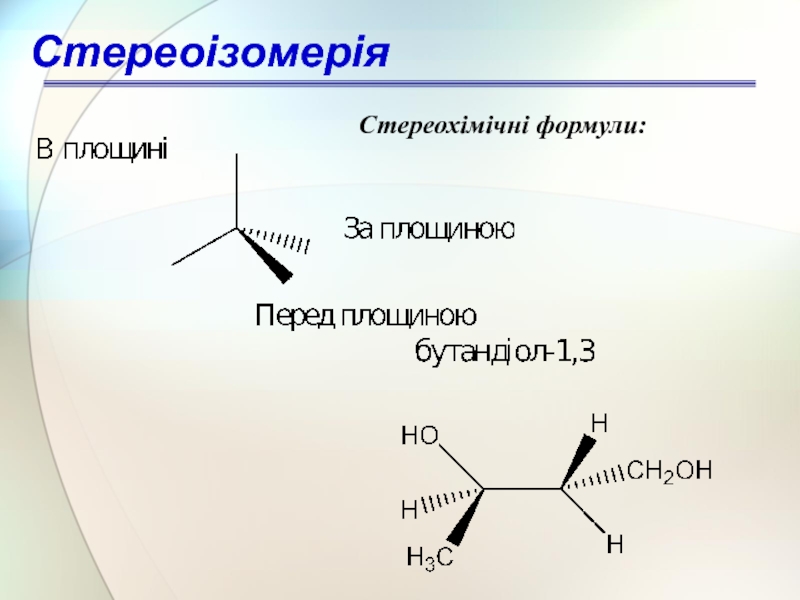
- 54. Стереохімічні формули: Стереоізомерія
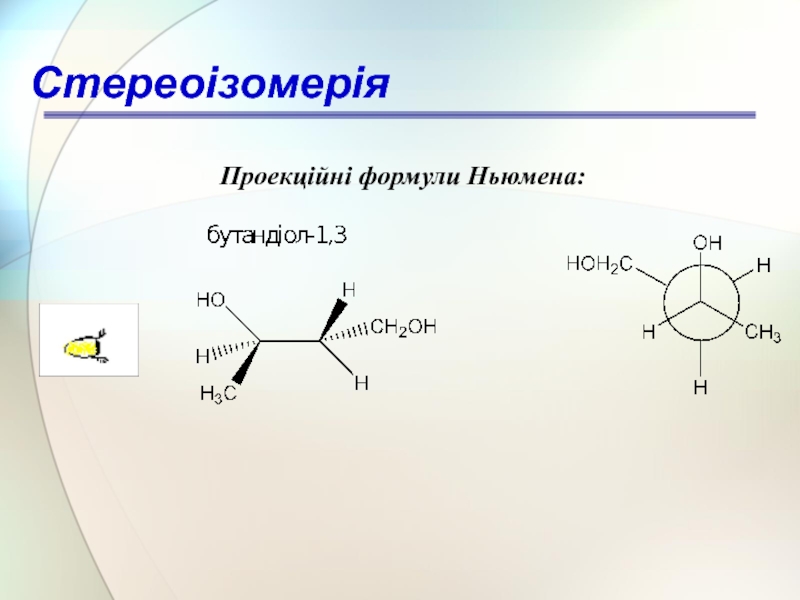
- 55. Проекційні формули Ньюмена: Стереоізомерія
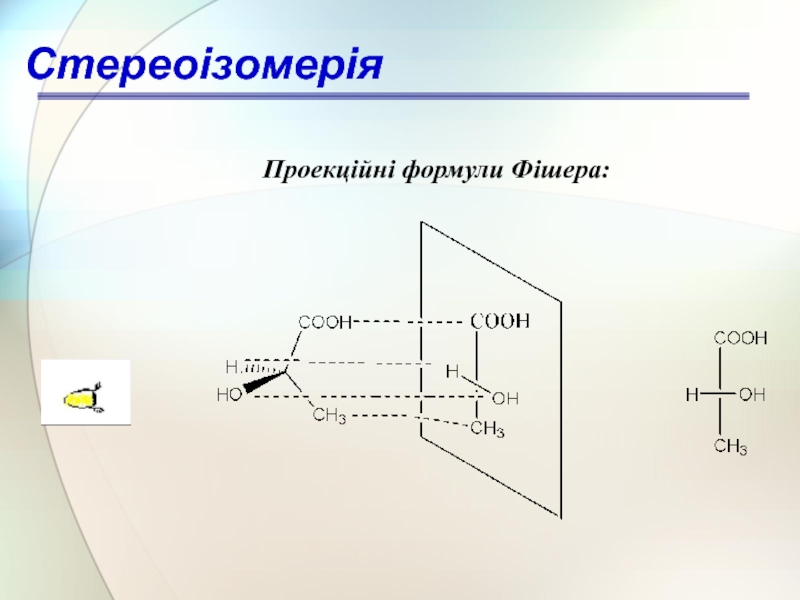
- 56. Проекційні формули Фішера: Стереоізомерія
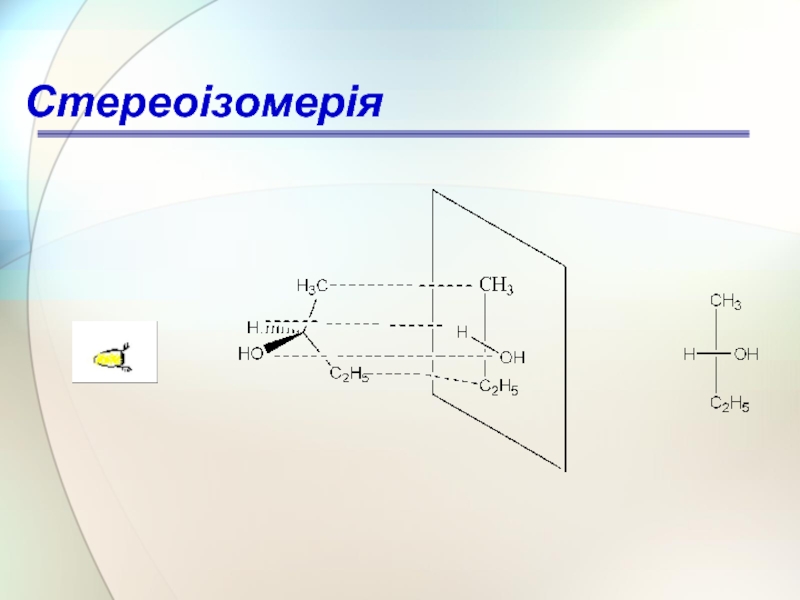
- 57. Стереоізомерія
- 58. Стереоізомерія
- 59. Просторова будова молекул і їх біологічна активність
- 60. Стереоізомерія
- 61. Стереоізомерія 1. Стереоспецифічність біологічно активних речовин. Всі
- 62. Стереоізомерія Активністю володіє S-ізомер, Рацемат є вдвічі менш активним 2R,4‘S,8‘S-ізомер – 100%
- 63. Стереоізомерія Домішка лише 1,1% Z-ізомера в статевому
- 64. Стереоізомерія Б) Іноді в дослідах in vitro
- 65. R-форма діуретика вдвічі активніша за S-форму
- 66. Стереоізомерія
- 67. Стереоізомерія Рацемічна суміш в 1,4 рази активніша
- 68. Дякую за увагу!
Слайд 1Галогенопохідні вуглеводнів.
Ізомерія органічних сполук. Просторова будова молекул.
скелетні
кулестержневі
сферичні
(Стюарта-Бріглеба)
Слайд 2Галогенпохідні вуглеводнів
Галогенпохідними називаються похідні вуглеводнів, в яких один або декілька атомів
Слайд 14
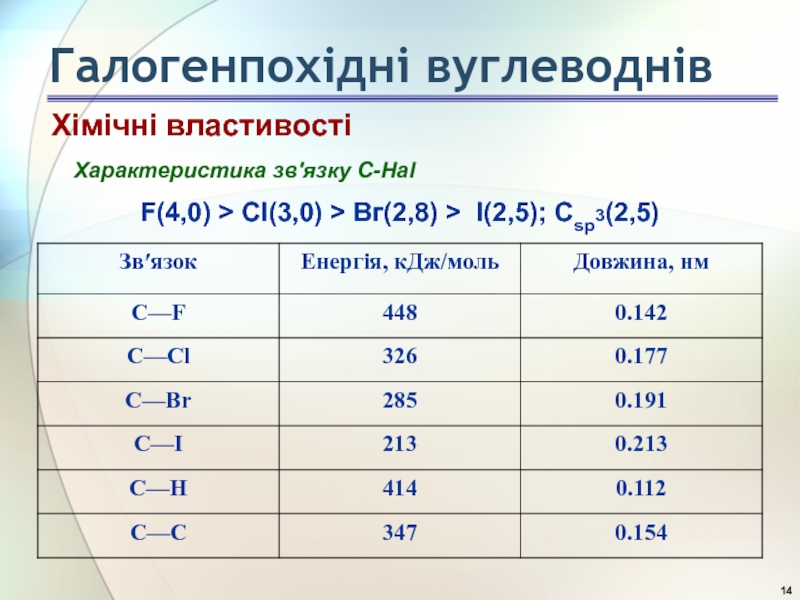
Хімічні властивості
Характеристика зв′язку C-Hal
F(4,0) > Сl(3,0) > Вг(2,8) > I(2,5); Сsp3(2,5)
Галогенпохідні
Слайд 15
Характеристика зв′язку C-Hal
С—I > С—Вr > C—CI > C—F
Хімічні властивості
Галогенпохідні
Слайд 16
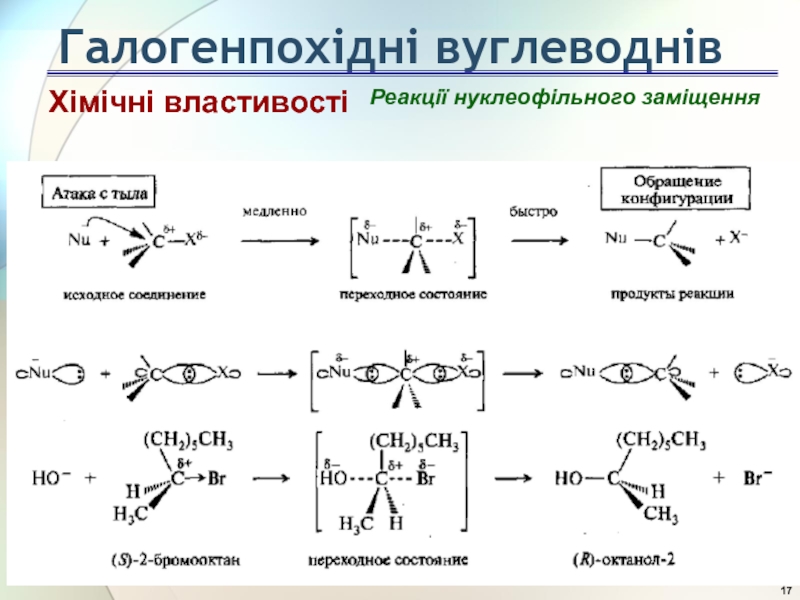
Реакції нуклеофільного заміщення
Реакції, в результаті яких в молекулі вихідної сполуки відбувається
Хімічні властивості
Галогенпохідні вуглеводнів
Слайд 18
Реакції нуклеофільного заміщення
Взаємодія галогеналканів з водними розчинами лугів
Хімічні властивості
Галогенпохідні вуглеводнів
Слайд 19
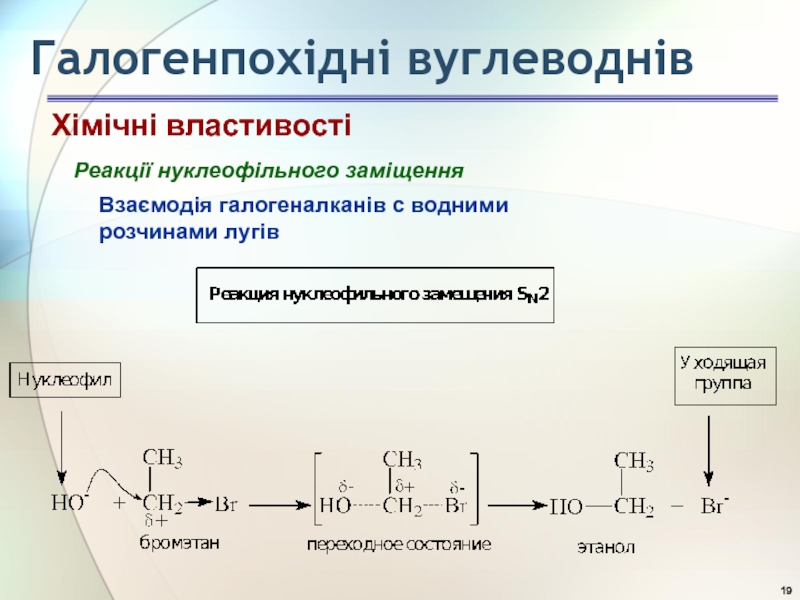
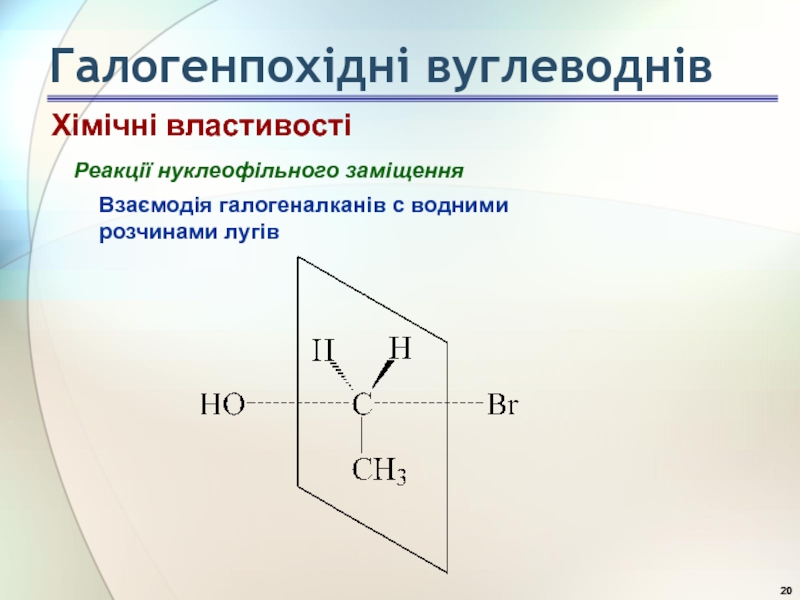
Реакції нуклеофільного заміщення
Взаємодія галогеналканів с водними розчинами лугів
Хімічні властивості
Галогенпохідні вуглеводнів
Слайд 20
Реакції нуклеофільного заміщення
Взаємодія галогеналканів с водними розчинами лугів
Хімічні властивості
Галогенпохідні вуглеводнів
Слайд 21
Швидкість реакції нуклеофільного заміщення залежить від таких факторів:
- нуклеофільної реакційної здатності
- основності нуклеофільного реагента;
- концентрації реагента;
- величини позитивного заряду на атакованому атомі Карбону в субстраті;
- енергії зв′язку і характері відхідної групи;
- будови радикалів, що зв′язані з атакованим атомом Карбону;
- природи розчинника
Реакції нуклеофільного заміщення
Хімічні властивості
Галогенпохідні вуглеводнів
Слайд 22
Нуклеофільна реакційна здатність реагента
Під нуклеофільною реакційною здатністю (нуклеофільною силою) прийнято
Хімічні властивості
Галогенпохідні вуглеводнів
Слайд 23
Нуклеофільна реакційна здатність реагента
NH3 > H2O > HF –CH3 > –NH2
–NH2 > NH3 –OH > H2O F– > HF
I– > Br– > Cl– > F–
CH3→O– > H—O– CH3→NH2 > H—NH2
Хімічні властивості
Галогенпохідні вуглеводнів
Слайд 24
Основність нуклеофільних реагентів
I– < Br– < Cl– < F–
Хімічні властивості
Галогенпохідні вуглеводнів
Слайд 44Стереоізомерія
Стереоізомери – це сполуки з однаковою будовою, тобто одним і тим
З позиції їх відносної стійкості стереоізомери поділяють на конфігураційні і конформаційні.
Слайд 45Стереоізомерія
Конфігураційні стереоізомери характеризуються тим, що можуть існувати у вигляді індивідуальних форм,
Конформаційні стереоізомери, або просто конформації, частіше всього виникають внаслідок обертання окремих фрагментів молекули навколо простих σ-зв’язків. Конформери можуть існувати тільки разом у вигляді множини геометричних форм молекули з різним взаємним розміщенням в просторі окремих атомів і атомних груп.
Слайд 46Стереоізомерія
Конформація – просторове розташування атомів в молекулі, яке може змінитися при
Конфігурація – просторове розташування атомів в молекулі, яке не може змінитися при обертанні і згині зв'язків.
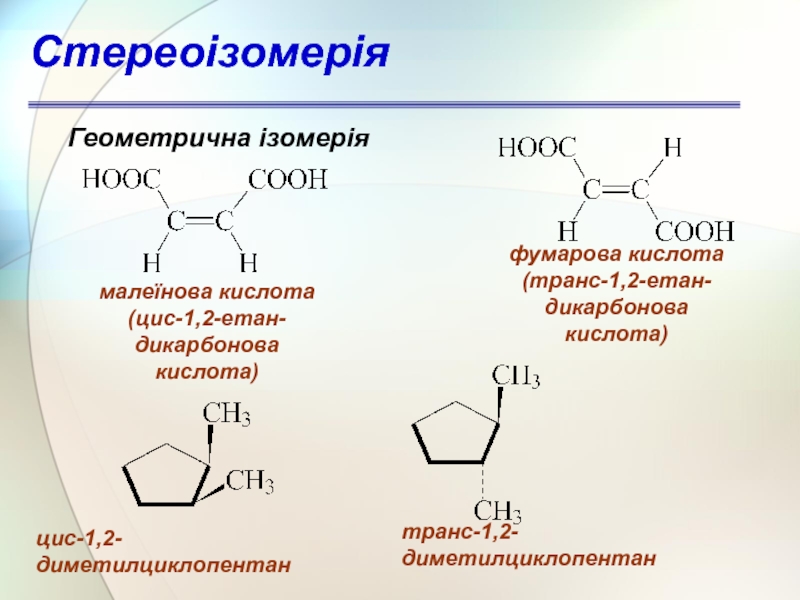
Слайд 49Геометрична ізомерія
малеїнова кислота
(цис-1,2-етан-
дикарбонова кислота)
фумарова кислота
(транс-1,2-етан-
дикарбонова кислота)
цис-1,2-диметилциклопентан
транс-1,2-диметилциклопентан
Стереоізомерія
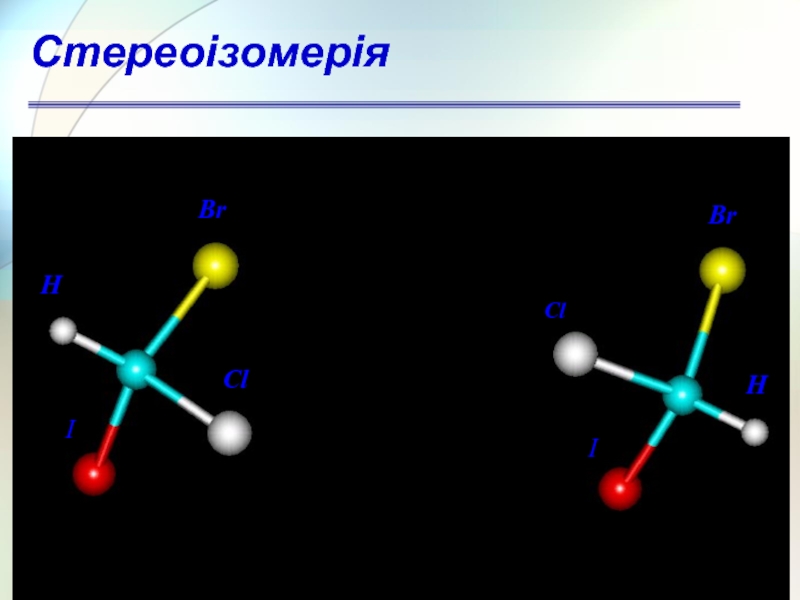
Слайд 50Енантіомери – це структури, що є дзеркальним відображенням один одного
Хіральність
Стереоізомерія
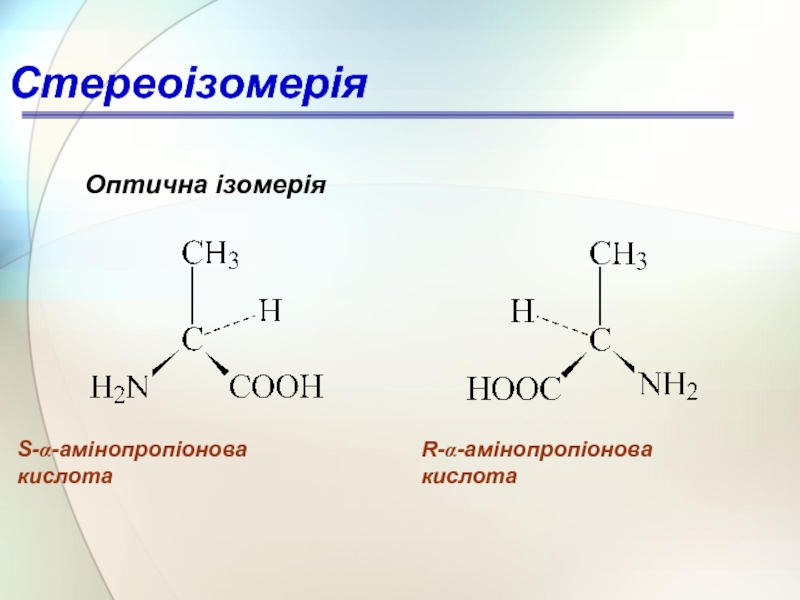
Слайд 53Стереоізомерія
Оптична ізомерія
S-α-амінопропіонова кислота
R-α-амінопропіонова кислота
Ізомерія — одне з найбільш особливих проявів специфіки
Слайд 59Просторова будова молекул і їх біологічна активність
В процесі еволюції живої природи
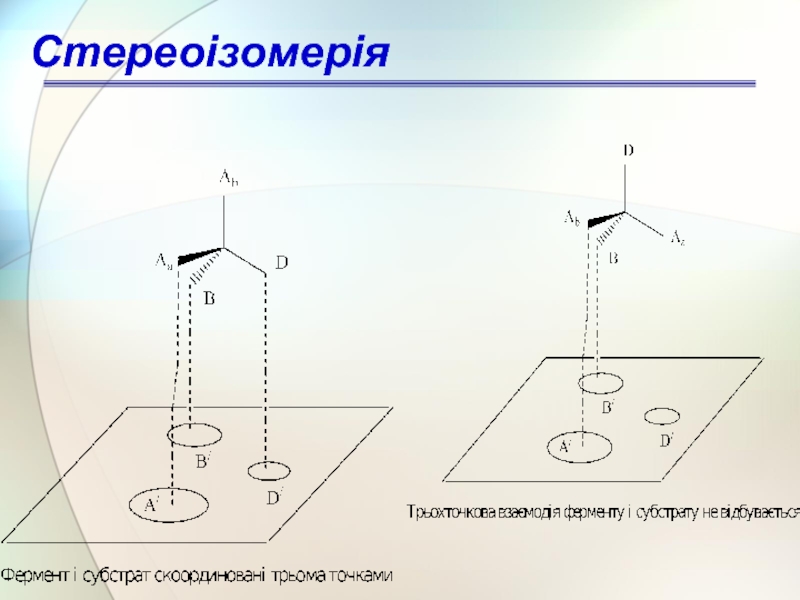
Стереоспецифічність ферментативних реакцій.
Відомо, що в процесі гліколізу вуглеводів під дією ферменту лактатдегідрогенази з двох енантіомерів молочної кислоти окисненню піддається тільки S-енантіомер – принцип трьох точкової взаємодії.
Стереоізомерія
Слайд 61Стереоізомерія
1. Стереоспецифічність біологічно активних речовин.
Всі білки побудовані з амінокислот L-ряду; в
2. Стереоспецифічність лікарських засобів.
Фармакологічна дія ліків здійснюється частіше всього в результаті взаємодії лікарського засобу з клітинним рецептором – принцип трьох точкової взаємодії.
А) В одних випадках більш активним є R-форма (R-форма діуретика мефрусиду більш як в два рази активніша за S-ізомер), в інших – навпаки (S-енантіомер β-адреноблокатора пропранолола (використовують при срцевій недостачі) є більш активним, ніж R-форма).
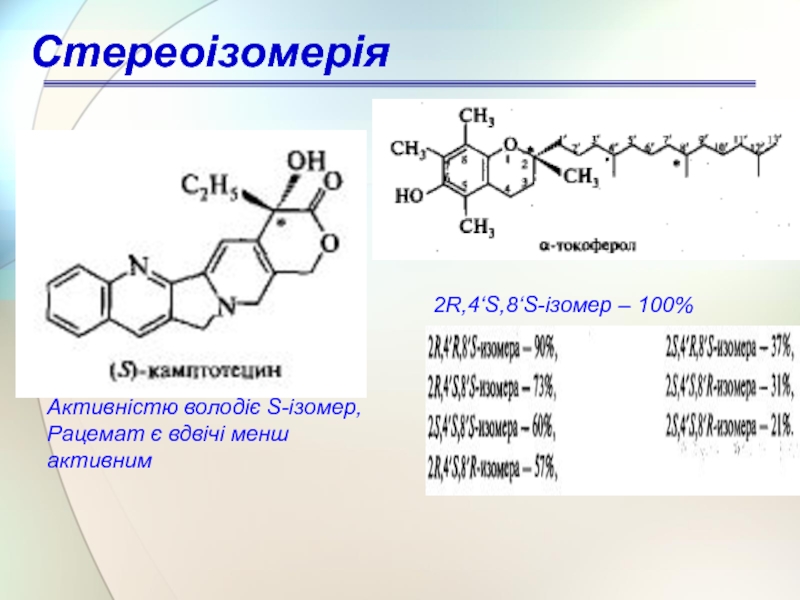
Слайд 62Стереоізомерія
Активністю володіє S-ізомер,
Рацемат є вдвічі менш активним
2R,4‘S,8‘S-ізомер – 100%
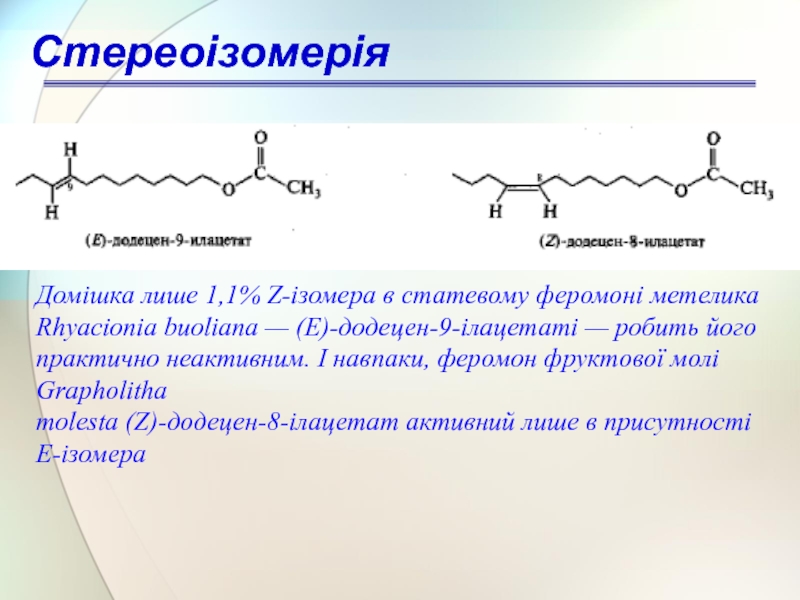
Слайд 63Стереоізомерія
Домішка лише 1,1% Z-ізомера в статевому феромоні метелика Rhyacionia buoliana —
molesta (Z)-додецен-8-ілацетат активний лише в присутності Е-ізомера
Слайд 64Стереоізомерія
Б) Іноді в дослідах in vitro більш активною є S-ізомери, тоді
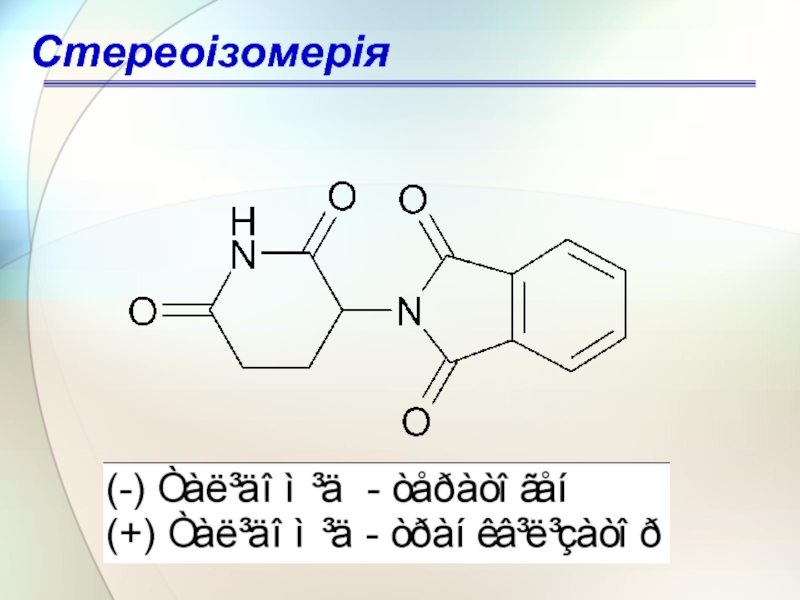
В) Трагічні випадки з не врахуванням фармакологічної активності стереоізомерів – препарат талідомід (Західна Німеччина) окрім снотворної дії, викликав сильну тератогенну і ембріотокисчну дію: ненормальний розвиток плоду у вагітних жінок, у новонароджених були недорозвинуті кінцівки – таку дію проявляв тільки S-ізомер.
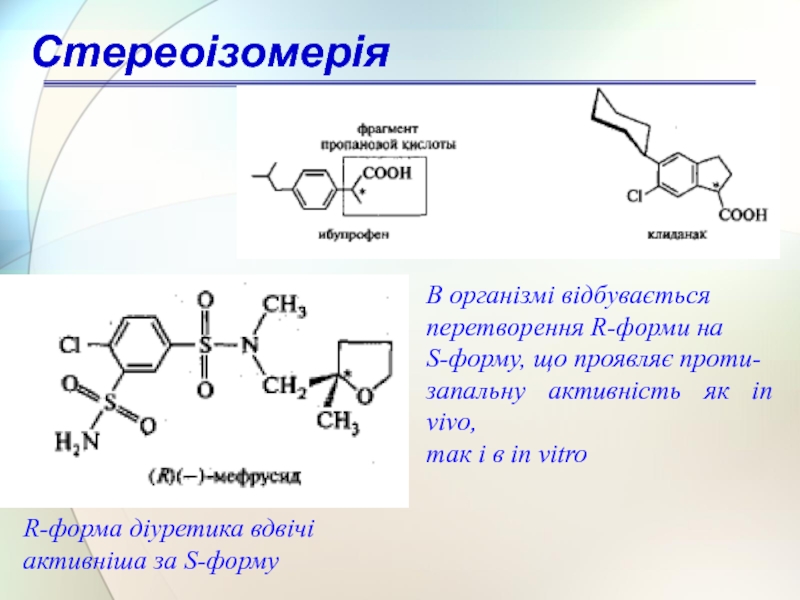
Слайд 65R-форма діуретика вдвічі
активніша за S-форму
Стереоізомерія
В організмі відбувається
перетворення R-форми на
S-форму, що проявляє проти-
запальну активність як in vivo,
так і в іn vitro
Слайд 67Стереоізомерія
Рацемічна суміш в 1,4 рази активніша
за правообертаючий ізомер, в 2,5 рази
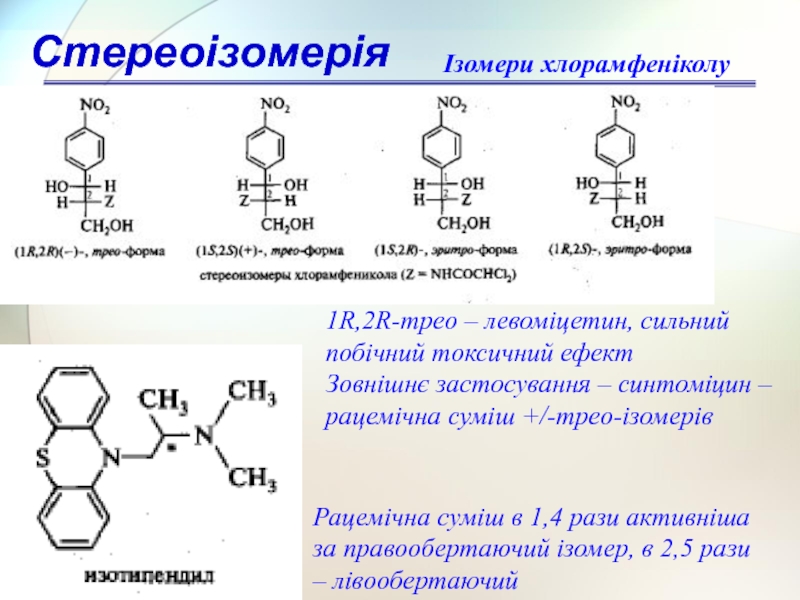
1R,2R-трео – левоміцетин, сильний
побічний токсичний ефект
Зовнішнє застосування – синтоміцин –
рацемічна суміш +/-трео-ізомерів
Ізомери хлорамфеніколу