- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Группа веществ, изолируемых из объектов путём минерализации биологического материала (Продолжение) презентация
Содержание
- 1. Группа веществ, изолируемых из объектов путём минерализации биологического материала (Продолжение)
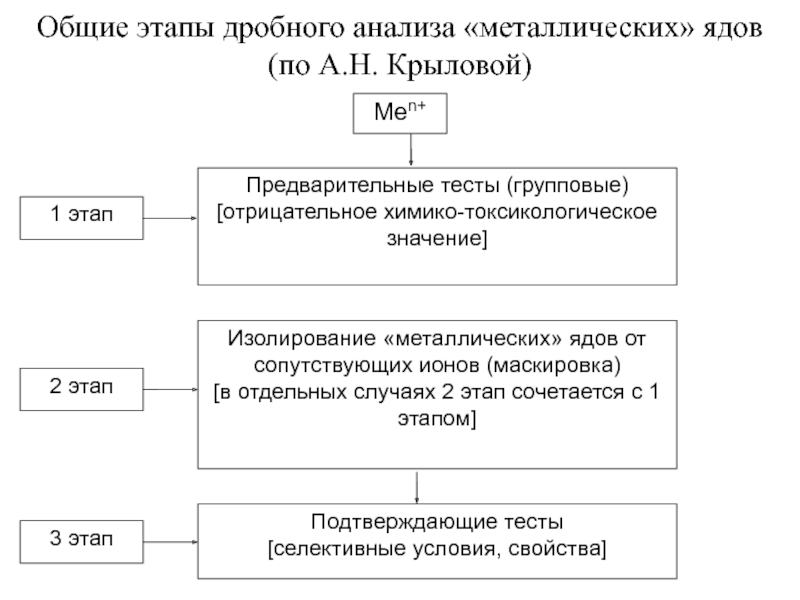
- 2. Общая характеристика, методологические
- 3. На современном этапе (с
- 4. История развития системных методов анализа
- 5. Аналитические группы (сероводородный метод анализа по Фрезениусу
- 6. б) Второй этап сероводородного метода включал дальнейшее
- 7. Сероводородный метод анализа соединений
- 8. В связи с перечисленными
- 9. Дробный метод анализа «металлических» ядов
- 10. Общее определение дробного метода анализа «металлических» ядов.
- 11. Основные достоинства метода. 1. Максимальное применение специфических
- 12. 4. Простота и доступность дробного метода для
- 13. Методологические аспекты дробного метода анализа.
- 14. Б. Основные приёмы маскировки мешающих ионов: 1.
- 15. б) фторидов: Fe + 6 NaF →
- 16. 2. Применение для маскировки мешающих (фоновых) металлов
- 17. 5. В целях маскировки посторонних ионов
- 18. 1) S C N N N N
- 19. 7. Применение определённой последовательности анализа отдельных «металлических»
- 20. Пример селективной экстракции на примере свинца.
- 21. 2 этап – На втором этапе производится
- 22. Приём селективной экстракции свинца из минерализата
- 23. 2 этап – реэкстрагирование свинца в водную
- 24. 2. Исследование минерализата на наличие свинца и
- 25. Men+ Общие этапы дробного анализа «металлических» ядов (по А.Н. Крыловой)
- 26. Схема исследования свинца и бария в минерализате
- 27. количественное определение ФЭК реэкстрагирование 0,1
- 28. нас. CH3COONH4 осадок (BaSO4) Качественное
- 29. Исследование минерализата (после отделения осадка) Mn2+
- 30. Cr 3+ Предварительная (отрицательное значение)
- 31. Ag+
- 32. Cu 2+ экстракция
- 33. Tl 3+ Предварительная (групповая
- 34. Bi 3+
- 35. Cd 2+ ДДТКNa экстракция
- 36. Zn 2+ Предварительная реакция (отрицательное
- 37. Спасибо за внимание!
Слайд 1Лекция 2. Группа веществ, изолируемых из объектов путём минерализации биологического материала
Вопросы:
1. Общая характеристика, методологические аспекты дробного метода анализа.
2. Исследование минерализата на наличие свинца и бария в осадке.
3. Исследование минерализата, после отделения осадка, на группу «металлических» ядов.
Слайд 2
Общая характеристика, методологические аспекты дробного метода анализа «металлических»
В химико-токсикологическом анализе «металлических» ядов совокупность методов анализа можно разделить (классифицировать) на 3 большие группы:
а) химические;
б) физико-химические;
в) физические.
Слайд 3 На современном этапе (с точки зрения методологии) при
На предварительном этапе химико-токсикологического анализа «металлических» ядов получили известность и практическое применение скрининговые исследования с помощью достаточно доступных химических тестов (реакций).
Слайд 4 История развития системных методов анализа «металлических» ядов.
Системный (сероводородный) метод включал 2 этапа:
а) Предварительное разделение катионов металлов на 5 аналитических групп (с использованием групповых осадителей – групповое обнаружение):
Слайд 5Аналитические группы (сероводородный метод анализа по Фрезениусу (1842 г)).
1 гр. K
2 гр. Mg , Ca , Ba , Sr (осаждение в виде карбонатов и фосфатов)
3 гр. Mn ,Cr ,Zn , Al , Fe , Ni , Co , Tl (осаждение сероводородом в щелочной среде)
4 гр. Cu , Cd , Ag , Bi , Hg , Pb (осаждение сероводородом в кислой среде)
5 гр. As , Sb , Sn (осаждение сероводородом в кислой среде, осадки растворимы (в отличие от сульфидов 4 аналитической группы) – в полисульфиде аммония).
+
+
+
+
2+
2+
2+
2+
2+
2+
2+
2+
2+
2+
2+
2+
2+
3+
3+
3+
3+
3+
3+
3+
Слайд 6б) Второй этап сероводородного метода включал дальнейшее разделение и идентификацию отдельных
Слайд 7 Сероводородный метод анализа соединений металлов длительное время использовался
Однако, имел недостатки:
1. Длительность исследования (несколько дней).
2. Применение многочисленных операций по осаждению, растворению, фильтрованию и др.
Это вызывало значительные потери соединений.
3. Невозможность совместить качественный анализ с количественным определением при использовании одной навески объекта.
4. Токсичность газообразного сероводорода.
Слайд 8 В связи с перечисленными недостатками, в настоящее время
Слайд 9 Дробный метод анализа «металлических» ядов (определение, характеристика).
Создателем (разработчиком) системного дробного метода анализа для целей химико-токсикологической практики является А.Н. Крылова (1975 г, НИИ судебной медицины).
Слайд 10Общее определение дробного метода анализа «металлических» ядов.
Дробный метод
Слайд 11Основные достоинства метода.
1. Максимальное применение специфических дробных реакций.
2. Большая чувствительность реакций
3. Сочетание качественного анализа с количественным определением при использовании одной навески объекта (минерализата).
Слайд 124. Простота и доступность дробного метода для химико-токсикологических лабораторий (в т.ч.
5. Максимальное сокращение времени на анализ (по сравнению с системным сероводородным методом).
Слайд 13Методологические аспекты дробного метода анализа.
Основные условия и приёмы, использованные
А. Условия (основные):
1. Максимальное применение специфических реакций, позволяющих обнаружить искомый металл в присутствии посторонних (фоновых) металлов.
2. Применение приёмов маскировки, с помощью которых устраняют влияние мешающих ионов.
Слайд 14Б. Основные приёмы маскировки мешающих ионов:
1. Применение для маскировки мешающих (фоновых)
а) цианидов:
Fe2(SO4)3 + 6 KCN → 2 Fe(CN)3 + 3 K2SO4
Fe(CN)3 + 3 KCN → K3[Fe(CN)6]
гексацианоферриат калия
Слайд 15б) фторидов:
Fe + 6 NaF → Na3[FeF6] + 3 Na
в) фосфатов:
Fe2(SO4)3 + 2 H3PO4 → 2 FePO4 + 3 H2SO4
фосфат железа
FePO4 + H3PO4 → H3[Fe(PO4)2]
дифосфоферриат водорода
г) тиосульфатов:
Fe2(SO4)3 + 3 Na2S2O3 → Fe2(S2O3)3 + 3 Na2SO4
Fe2(S2O3)3 + Na2S2O3 → 2 Na[Fe(S2O3)2]
дитиосульфоферриат натрия
3+
+
Слайд 162. Применение для маскировки мешающих (фоновых) металлов органических комплексообразователей (виннокаменная, лимонная
3. В целях маскировки мешающих ионов осуществляют разбавление минерализата до предела чувствительности химической реакции (на исследуемый металл), во избежание обнаружения естественно-содержащихся элементов.
4. В целях маскировки мешающих ионов, осуществляют варьирование рН среды или строгое соблюдение величин рН среды (особенно при комплексообразовании свинца, меди, кадмия и др.).
Слайд 17
5. В целях маскировки посторонних ионов используют малые объемы минерализата (особенно
6. Использование приёма селективной экстракции искомого металла в составе комплекса с органическими реагентами (дитизон, диэтилдитиокарбамат натрия).
Слайд 181)
S
C
N
N
N
N
H
H
C6H5
C6H5
рН > 7
рН < 7
C6H5
C6H5
N
N
N
N
H
C
SH
(кето-форма)
(енольная форма)
дитизон (дифенилтиокарбазон)
2)
C2H5
C2H5
N
C
S
S
Na
[ДДТК]Na (диэтилдитиокарбаминовой кислоты
натриевая соль)
Слайд 197. Применение определённой последовательности анализа отдельных «металлических» ядов:
а) Исследованию на ионы
б) Pb → Ba [PbSO4 – оказывают влияние на перекристаллизацию BaSO4↓]
в) Cu → Sb [оказывает влияние окрашенный осадок CuS↓]
г) Sb → As [оказывает влияние SbH3↑].
2+
3+
+
-
2+
2+
2+
3+
3+
3+
Слайд 20Пример селективной экстракции на примере свинца.
Сущность. Искомый металл
Приём состоит из 2х этапов:
1 этап – В основе первого этапа лежит селективная экстракция искомого металла из минерализата в слой органического растворителя в виде дитизоната свинца (при рН 7,5-8,0). Органическую фазу отделяют и используют для второго этапа.
Слайд 212 этап – На втором этапе производится реэкстрагирование свинца в водную
Слайд 22Приём селективной экстракции свинца из минерализата
1 этап – селективная экстракция
(СH3COO)2Pb
(водно-кислая фаза)
+
2
H5C6
N
N
C
SH
N
NH
C6H5
рН 8,0
дитизон (енольная форма, хлороформный раствор)
H5C6
N
N
C
S
N
NH
C6H5
¨
Pb/
2
+
2
СH3COOH
дитизонат свинца (хлороформный слой)
Слайд 232 этап – реэкстрагирование свинца в водную фазу:
N
N
C
N
NH
¨
Pb/
2
H5C6
C6H5
S
+
2 HNO3
Pb(NO3)2
+
2
N
N
C
H5C6
S
NH
NH
C6H5
(водная фаза)
дитизон (хлороформный слой)
Слайд 242. Исследование минерализата на наличие свинца и бария в осадке.
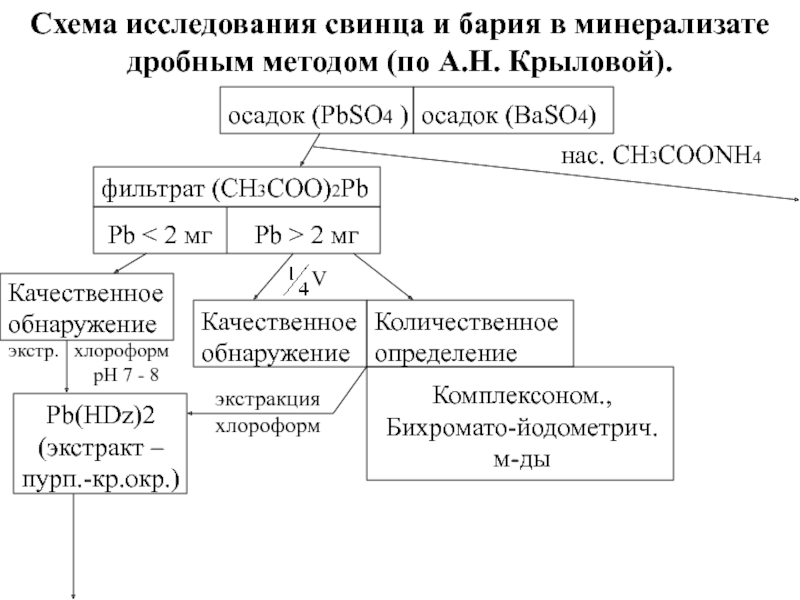
Слайд 26Схема исследования свинца и бария в минерализате дробным методом (по А.Н.
осадок (PbSO4 )
осадок (BaSO4)
нас. CH3COONH4
фильтрат (CH3COO)2Pb
Pb < 2 мг
Pb > 2 мг
Качественное
обнаружение
экстр. хлороформ
рН 7 - 8
Pb(HDz)2
(экстракт –
пурп.-кр.окр.)
Качественное
обнаружение
Количественное
определение
Комплексоном.,
Бихромато-йодометрич.
м-ды
V
экстракция
хлороформ
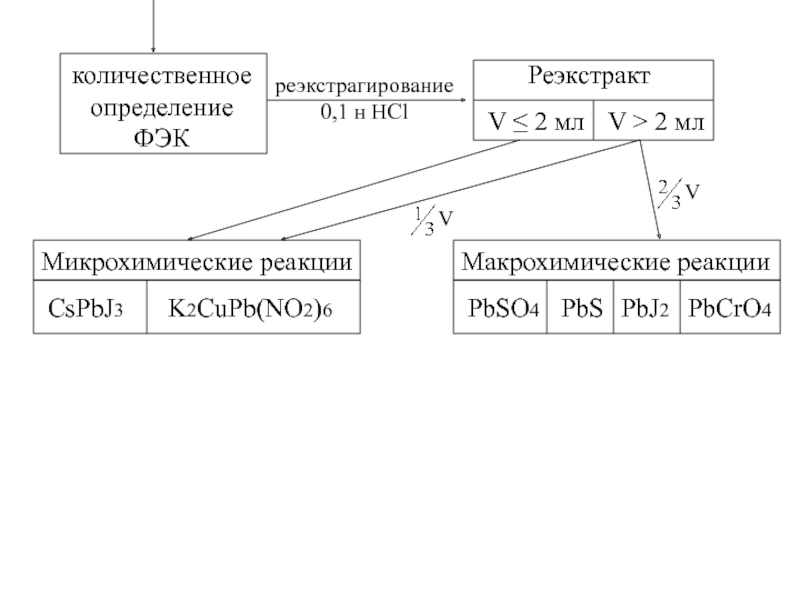
Слайд 27количественное
определение
ФЭК
реэкстрагирование
0,1 н HCl
Реэкстракт
V ≤ 2 мл
V > 2 мл
Микрохимические реакции
CsPbJ3
K2CuPb(NO2)6
V
Макрохимические реакции
PbSO4
PbS
PbJ2
PbCrO4
V
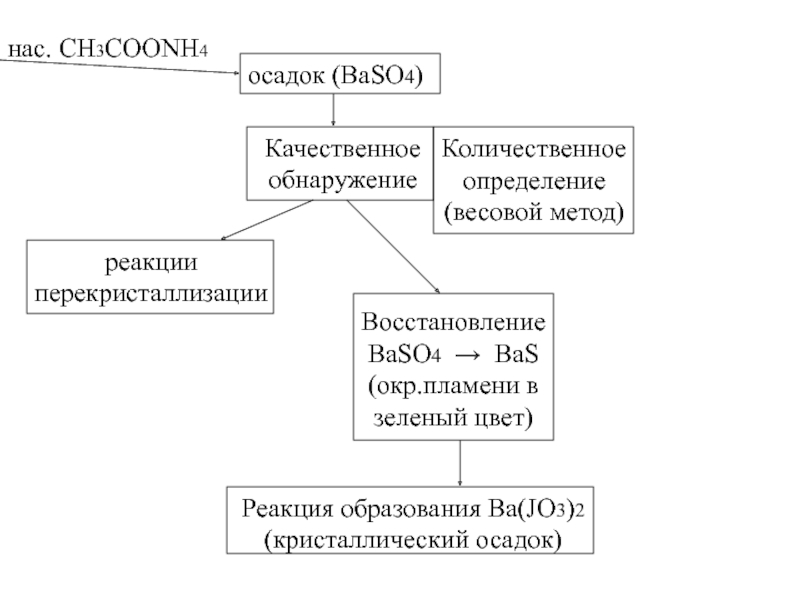
Слайд 28нас. CH3COONH4
осадок (BaSO4)
Качественное
обнаружение
Количественное
определение
(весовой метод)
реакции
перекристаллизации
Восстановление
BaSO4 → BaS
(окр.пламени в
зеленый
Реакция образования Ba(JO3)2
(кристаллический осадок)
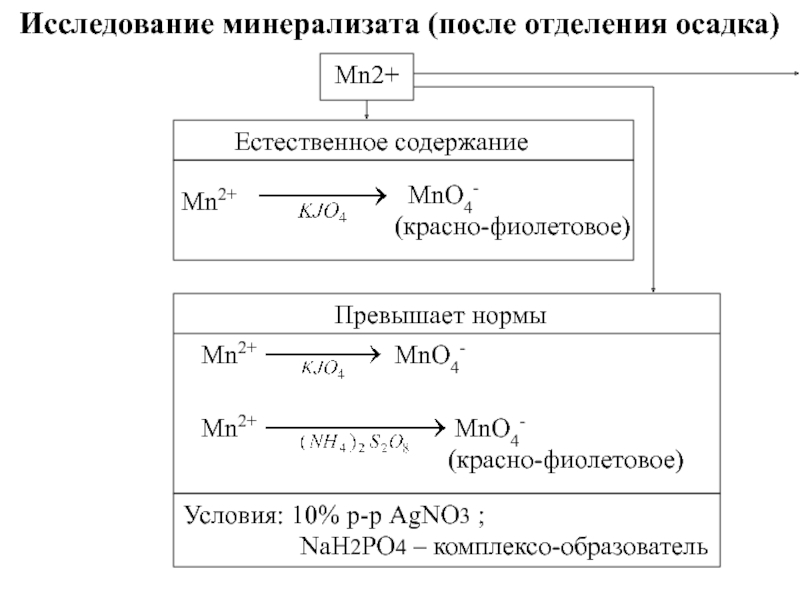
Слайд 29Исследование минерализата (после отделения осадка)
Mn2+
Естественное содержание
Mn2+
MnO4-
(красно-фиолетовое)
Превышает нормы
Mn2+
MnO4-
MnO4-
(красно-фиолетовое)
Mn2+
Условия: 10% р-р AgNO3 ;
NaH2PO4 – комплексо-образователь
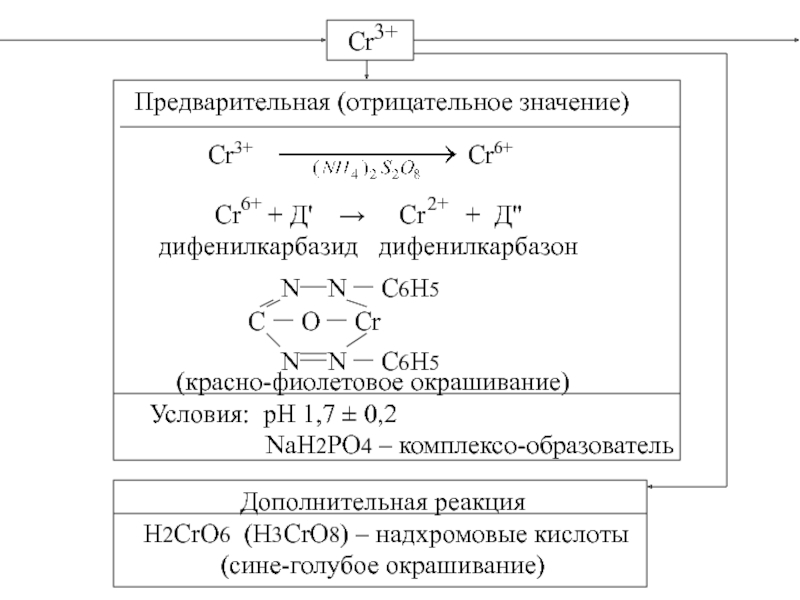
Слайд 30Cr
3+
Предварительная (отрицательное значение)
Cr3+
Cr6+
Cr + Д' →
дифенилкарбазид дифенилкарбазон
6+
2+
С
N
N
N
N
C6H5
C6H5
O
Cr
(красно-фиолетовое окрашивание)
Условия: рН 1,7 ± 0,2
NaH2PO4 – комплексо-образователь
Дополнительная реакция
H2CrO6 (H3CrO8) – надхромовые кислоты
(сине-голубое окрашивание)
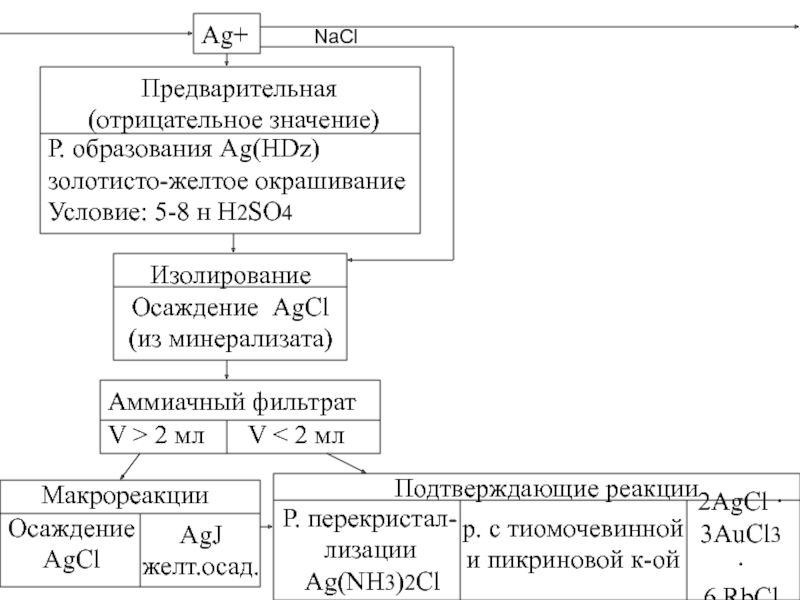
Слайд 31Ag+
Предварительная
(отрицательное
Р. образования Ag(HDz)
золотисто-желтое окрашивание
Условие: 5-8 н H2SO4
Изолирование
Осаждение AgCl
(из минерализата)
NaCl
Аммиачный фильтрат
V > 2 мл
V < 2 мл
Макрореакции
Осаждение
AgCl
AgJ
желт.осад.
Подтверждающие реакции
Р. перекристал-
лизации
Ag(NH3)2Cl
р. с тиомочевинной
и пикриновой к-ой
2AgCl ·
3AuCl3 ·
6 RbCl
Слайд 32Cu
2+
экстракция хлороформ (ДДТК)2Pb (рН – 3,0)
Изолирование, предварительное
желто-коричневое окрашивание
реэкстракция HgCl2 (рН – 5,0)
Реэкстракт CuCl2
Подтверждающие реакции
CuZn[Hg(SCN)4]2
розово-лиловый
осадок
CuCd[(FeCN)6]
лиловый осадок
Пиридин-роданидный
комплекс (зеленый цвет)
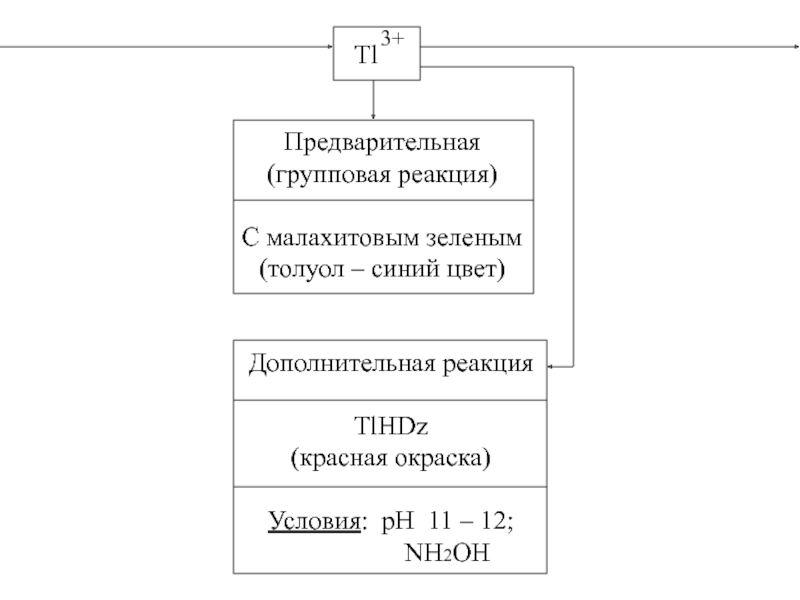
Слайд 33Tl
3+
Предварительная
(групповая реакция)
С малахитовым зеленым
(толуол – синий цвет)
Дополнительная реакция
TlHDz
(красная
Условия: рН 11 – 12;
NH2OH
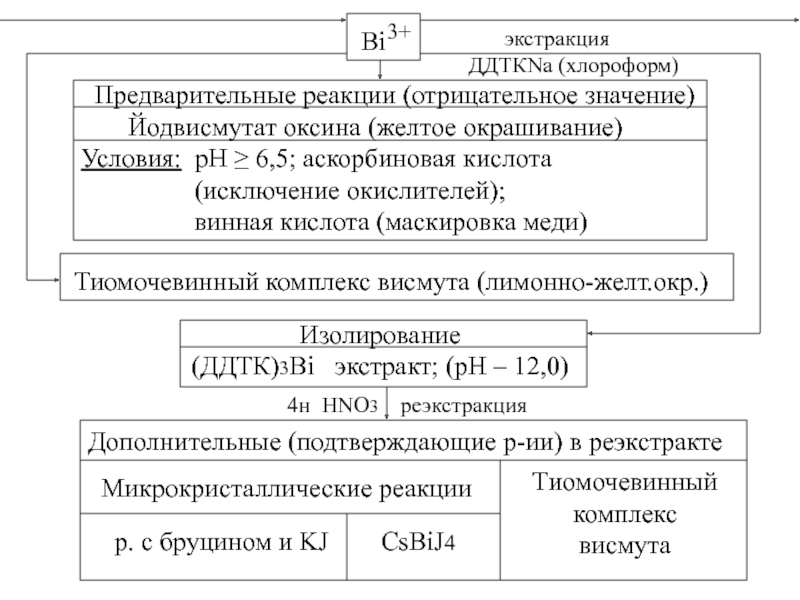
Слайд 34Bi
3+
Предварительные реакции (отрицательное значение)
Условия: рН ≥ 6,5; аскорбиновая кислота
(исключение окислителей);
винная кислота (маскировка меди)
Тиомочевинный комплекс висмута (лимонно-желт.окр.)
Изолирование
(ДДТК)3Bi экстракт; (рН – 12,0)
экстракция
ДДТКNa (хлороформ)
4н HNO3 реэкстракция
Дополнительные (подтверждающие р-ии) в реэкстракте
Микрокристаллические реакции
р. с бруцином и KJ
CsBiJ4
Тиомочевинный
комплекс
висмута
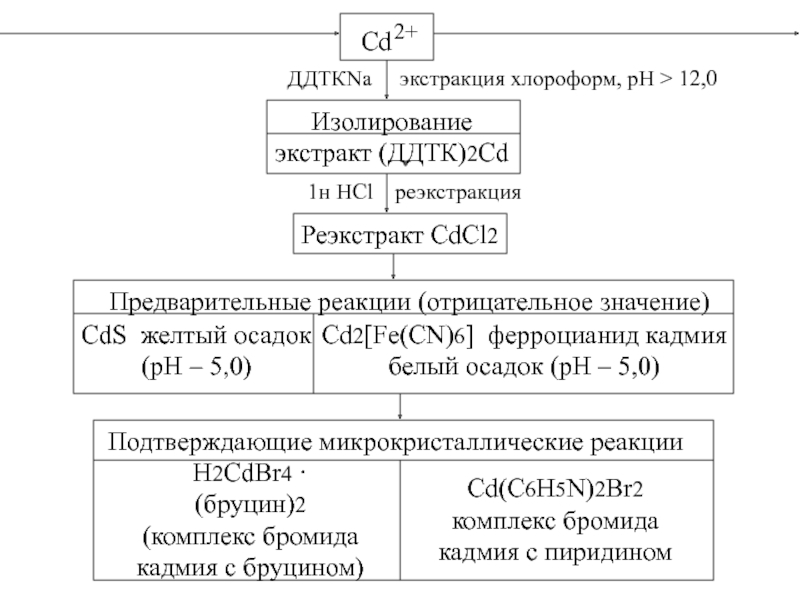
Слайд 35Cd
2+
ДДТКNa экстракция хлороформ, рН > 12,0
Изолирование
экстракт (ДДТК)2Cd
1н HCl
Реэкстракт CdCl2
Предварительные реакции (отрицательное значение)
CdS желтый осадок
(рН – 5,0)
Cd2[Fe(CN)6] ферроцианид кадмия
белый осадок (рН – 5,0)
Подтверждающие микрокристаллические реакции
H2CdBr4 · (бруцин)2
(комплекс бромида
кадмия с бруцином)
Cd(C6H5N)2Br2
комплекс бромида
кадмия с пиридином
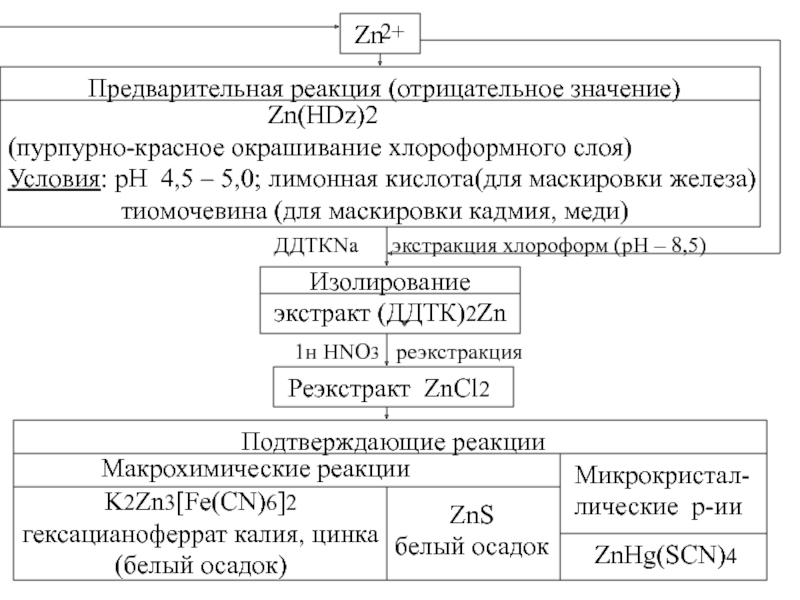
Слайд 36Zn
2+
Предварительная реакция (отрицательное значение)
(пурпурно-красное окрашивание хлороформного слоя)
Условия: рН 4,5 – 5,0; лимонная кислота(для маскировки железа)
тиомочевина (для маскировки кадмия, меди)
ДДТКNa экстракция хлороформ (рН – 8,5)
Изолирование
экстракт (ДДТК)2Zn
1н HNO3 реэкстракция
Реэкстракт ZnCl2
Подтверждающие реакции
Макрохимические реакции
Микрокристал-
лические р-ии
K2Zn3[Fe(CN)6]2
гексацианоферрат калия, цинка
(белый осадок)
ZnS
белый осадок
ZnHg(SCN)4














![б) фторидов:Fe + 6 NaF → Na3[FeF6] + 3 Na](/img/tmb/5/498509/b23aad179ce2a8265396490e291ea34f-800x.jpg)


![1)SCNNNNHHC6H5C6H5рН > 7рН < 7C6H5C6H5NNNNHCSH(кето-форма) (енольная форма) дитизон (дифенилтиокарбазон)2)C2H5C2H5NCSSNa[ДДТК]Na (диэтилдитиокарбаминовой кислоты](/img/tmb/5/498509/092909849fde21531b5a3ec636bda9db-800x.jpg)