- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Энергосиловое оборудование промышленных предприятий. Топливо и его виды презентация
Содержание
- 1. Энергосиловое оборудование промышленных предприятий. Топливо и его виды
- 2. Топливо и его виды Топливо – химическое
- 3. Элементарный состав топлива Топливо в том виде,
- 4. Сухая и горючая масса топлива Влажность и
- 5. Зольность, влажность, летучие Зольность – количество
- 6. Состав твердого топлива Примерный состав и теплотехнические
- 7. Состав жидких топлив Характеристики жидких топлив, получаемых
- 8. Состав горючих газов Состав и теплота сгорания
- 9. Теплота сгорания топлива Основная характеристика топлива –
- 10. Спасибо за внимание. Лектор: Кошарная Юлия Васильевна
Слайд 2Топливо и его виды
Топливо – химическое вещество, способное при горении (окислении)
Практическая целесообразность топлива определяется: количественным запасом, удобством добычи, скоростью горения, теплотворной способностью, возможностью длительного хранения и безопасностью продуктов сгорания.
Существуют естественные (природные) виды топлив и искусственные.
По агрегатному состоянию топливо бывает:
твердое: антрацит, каменный и бурый уголь, торф, дрова, сланцы, отходы деревообработки, сельхоз отходы (солома, костра, лузга, чинголак и др.)
жидкое: нефть и продукты ее переработки (бензин, керосин, лигроин, масла, дизельное топливо, мазут)
газообразное: природный газ, попутный нефтяной газ, коксовый и доменный газ, крекинговый газ, генераторный газ (искусственный).
Твердое, газообразное топливо и мазут в основном сжигают на ТЭС для получения электрической и тепловой энергии, а также используют для технологических нужд промышленности. Жидкое (до 70%) используется на транспорте (авиация, трактора …).
Слайд 3Элементарный состав топлива
Топливо в том виде, в каком оно поступает для
В общем случае в состав рабочего (твердого или жидкого) топлива входят: углерод С, водород Н, кислород О, азот N и летучая сера S, а также негорючие минеральные примеси – зола А и влага W.
Для рабочей массы топлива справедливо равенство:
Ср + Нр + Ор + Nр + Sр + Ар + Wр = 100%
где Ср, Нр, Ор и т.д. – элементы рабочего топлива в процентах от общей массы топлива
Влага W и зола А, содержащиеся в топливе, составляют балласт топлива. Он снижает теплоту сгорания топлива и затрудняет процесс горения в топке.
Сера S в естественных видах твердых топлив бывает трех видов:
органическая Sо, связанная с другими элементами топлива (С, Н, N, О) в виде сложных органических соединений;
колчеданная Sк в виде пирита, колчедана FeS2;
сульфатная Sсульф в виде солей серной кислоты (гипс, FeSO4 и др.)
Сера, содержащаяся в сульфатах, гореть не может и относится к балласту (зола). Органическая и колчеданная сера образуют летучую горючую серу Sл (при горении образует токсичный сернистый ангидрид SO2). Sобщ = Sо + Sк + Sсульф = Sл + Sсульф
Слайд 4Сухая и горючая масса топлива
Влажность и зольность твёрдого топлива в пределах
Для сухой массы топлива справедливо равенство:
Сс + Нс + Ос + Nс + Sс + Ас = 100%
где Сс, Нс, Ос и т.д. – элементы рабочего топлива в процентах от сухой массы топлива
Для горючей массы топлива (не содержащего золу и в абсолютно сухом состоянии):
Сг + Нг + Ог + Nг + Sгл = 100%
где Сс, Нс, Ос и т.д. – элементы рабочего топлива в процентах от сухой массы топлива
Формулы для пересчета процентного состава топлива
Слайд 5Зольность, влажность, летучие
Зольность – количество золы (твердый негорючий остаток), образующийся
Зола может быть в виде сыпучей массы плотностью 600 кг/м3 и шлака (сплавленных кусков) – 800 кг/м3. Процесс отделения золы называется обогащением топлива.
В состав золы входят: глинозем Al2O3, кремниевая кислота SiO2, известь CaO, магнезия MgO, щелочи Na2O и K2O, окислы железа FeO и Fe2O3.
Влажность – количество воды (влаги), присутствующее в топливе, и выраженное в процентах от массы топлива.
Влага бывает внешняя (капиллярная) и внутренняя (гигроскопическая и коллоидная). Для твердых топлив используют приведенную влажность (%, кг/МДж), отнесенную к Qрн – низшей рабочей теплоте сгорания топлива [МДж/кг]:
Wп = 1000Wр / Qрн
Влажность определяют высушиванием навески при 105 … 110 °С. Если Wп < 3% – топливо маловлажное, Wп = 3,89 … 8 % – топливо высоковлажное.
Летучие вещества – газы, водяные и смоляные пары, образующиеся в результате разлагания органической массы твердого топлива при нагревании без доступа воздуха.
Выход летучих веществ Vг в % на горючую массу, определяют путем прокаливания 1 г топлива в закрытом тигле при температуре (850 ± 10) °С в течение 7 мин.
Основной горючей составляющей частью является углерод С и водород Н.
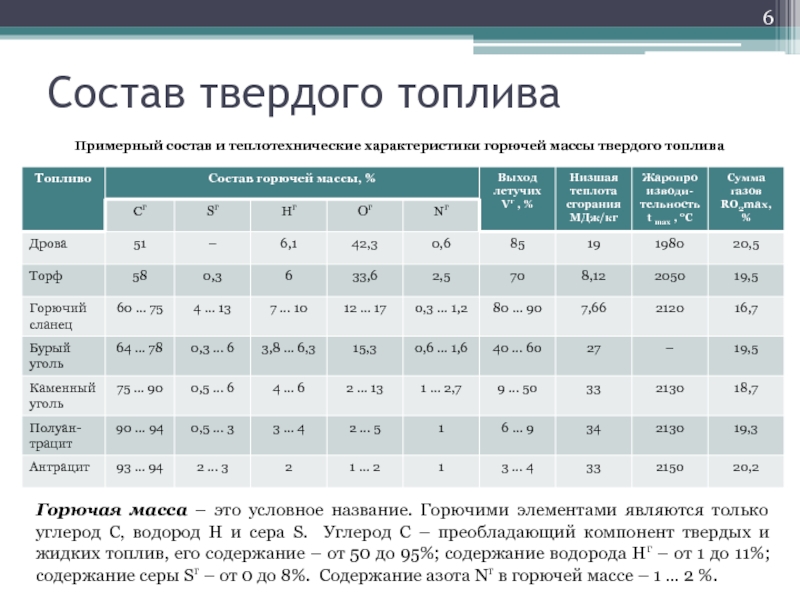
Слайд 6Состав твердого топлива
Примерный состав и теплотехнические характеристики горючей массы твердого топлива
Горючая
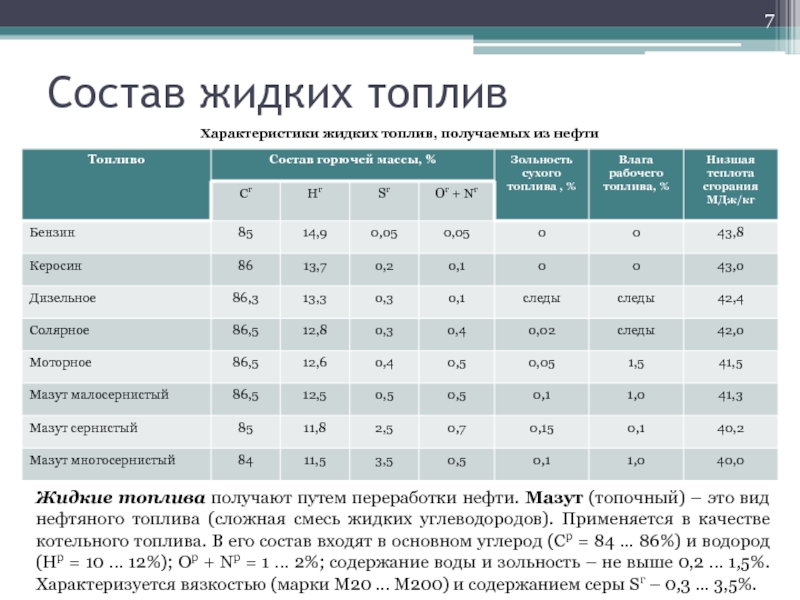
Слайд 7Состав жидких топлив
Характеристики жидких топлив, получаемых из нефти
Жидкие топлива получают путем
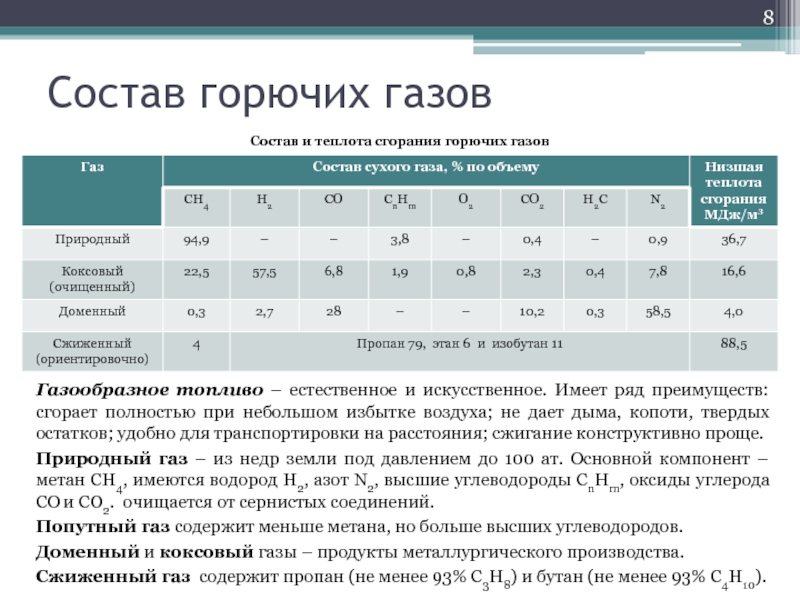
Слайд 8Состав горючих газов
Состав и теплота сгорания горючих газов
Газообразное топливо – естественное
Природный газ – из недр земли под давлением до 100 ат. Основной компонент – метан CH4, имеются водород Н2, азот N2, высшие углеводороды CnHm, оксиды углерода CO и CO2. очищается от сернистых соединений.
Попутный газ содержит меньше метана, но больше высших углеводородов.
Доменный и коксовый газы – продукты металлургического производства.
Сжиженный газ содержит пропан (не менее 93% C3H8) и бутан (не менее 93% C4H10).
Слайд 9Теплота сгорания топлива
Основная характеристика топлива – теплота сгорания Q – количество
Теплоту сгорания газообразного топлива относят к 1 м3 при нормальных условиях (температура 0 °С, давление 760 мм рт. ст.) – [кДж/м3].
Теплота сгорания зависит от химического состава топлива и может быть отнесена к органической, горючей и рабочей массе топлива. Влага (H2O), содержащаяся в продуктах сгорания, обладает энтальпией, равной примерно 2510 кДж/кг.
Высшая теплота сгорания рабочего топлива Qрв – теплота, выделяемая при полном сгорании 1 кг топлива, считая, что образующиеся при сгорании водяные пары конденсируются.
Низшая теплота сгорания рабочего топлива Qрн – теплота, выделяемая при полном сгорании 1 кг топлива, за вычетом теплоты, затраченной на испарение как влаги, содержащейся в топливе, так и влаги, образующейся от сгорания водорода.
Теплоту сгорания определяют 2-мя методами: калориметрическим и аналитическим.
Чаще – по формулам (Д.И. Менделеева):
для твердых и жидких топлив: Qрн = 338 Ср + 1025 Нр – 108,5 (Ор – Sрл) – 25 Wр
для сухого газообразного топлива:
Qсн = 127 СО + 108 Н2 + 358 CH4 + 591 C2H4 + 638 C2H6 + 911 C3H8 + 234 H2S