- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что изучает химия презентация
Содержание
- 2. Инструктаж по технике безопасности при работе в кабинете химии.
- 3. М.В. Ломоносов «Широко простирает химия руки свои в дела человеческие»
- 4. 1. Что изучает химия? Химия –
- 5. Что такое вещество? Дальше!
- 6. 2. Что называют атомом и молекулой?
- 7. Написание химических формул атомов и молекул Химический знак— Индекс— Коэффициент--
- 8. Что такое химический элемент?
- 9. Систематизировать понятия и составить схему Вещества простые-
- 12. Примеры атомов и молекул Атомы Водород-Н Кислород-
- 13. Массы атомов и молекул За единицу атомной
- 14. Что такое абсолютная и относительная атомная и молекулярная массы?
- 15. Расчет относительной молекулярной массы
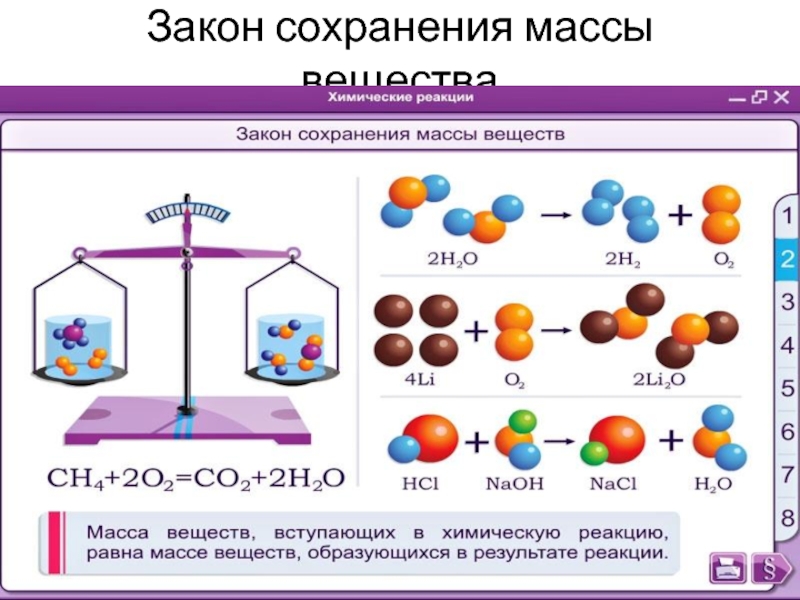
- 16. Закон сохранения массы Сколько атомов вступает в реакцию столько и получается
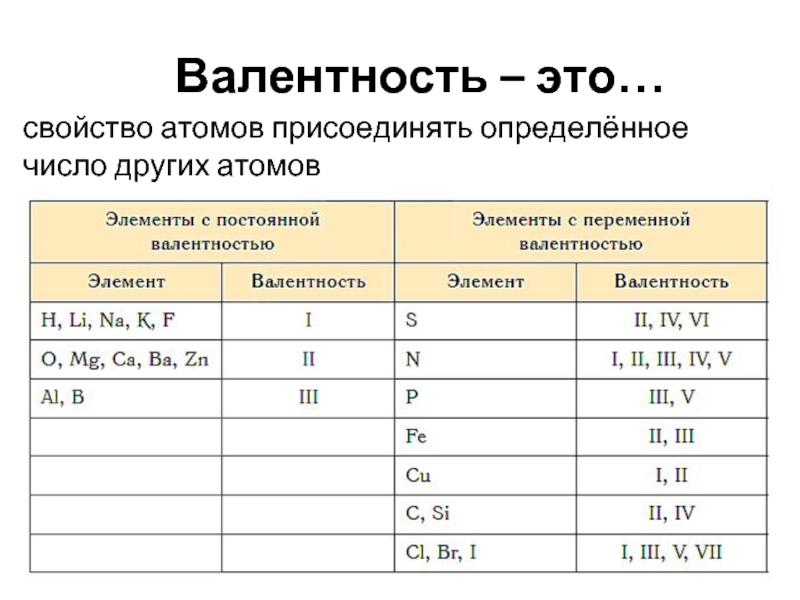
- 17. Валентность – это… свойство атомов присоединять определённое число других атомов
- 18. Алгоритм определения валентности, если известна валентность атома
- 19. Типы химических реакций Обмена АВ+СД=СВ+АД Замещения АВ+С=СВ+А Соединения А+В=АВ Разложения АВ=А+В АВС=АВ+С
- 20. Закончить фразы Валентность бывает постоянной и ……
- 21. Дать определение понятиям Атомная единица массы (а.е.м.)-
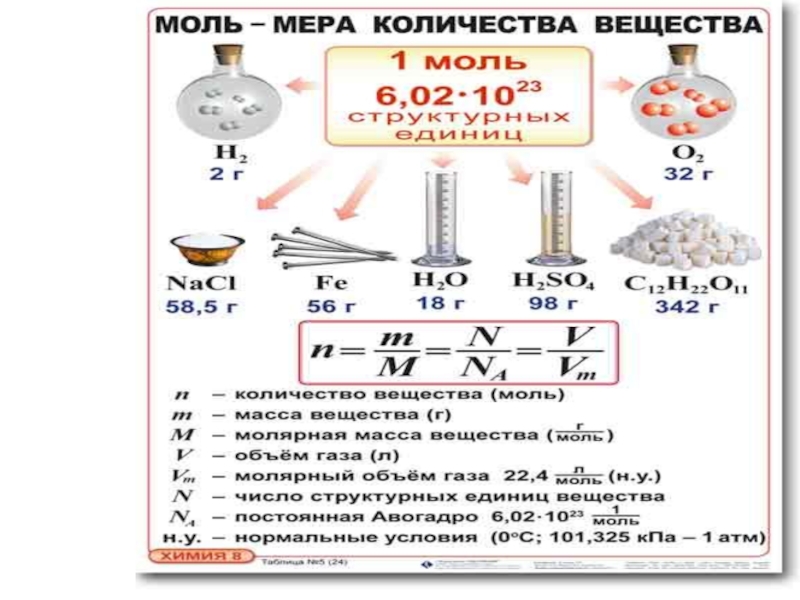
- 22. Количество вещества Количества вещества (V) – число
- 23. МОЛЬ Моль – это … Число Авогадро
- 24. синквейн – стихотворение из 5 строк
- 25. Относительная атомная масса (см. атомная масса химического
- 26. КОЛИЧЕСТВО ВЕЩЕСТВА – число атомов, молекул или
- 28. Количество вещества
- 30. Ответить на вопросы 1.Какое количество вещества (
- 31. 1. n = N/ Na = 12,
- 32. Основные положения атомно-молекулярного учения. Атомно-молекулярное теория
- 33. Закон Авогадро
- 34. Закон постоянства состава вещества Закон постоянства
- 36. Закон сохранения массы вещества Закон сохранения массы веществ в реакциях
- 38. Урок 1. 5.Строение атома. Ядро : протоны и нейтроны Электроны
- 39. Урок 1
- 40. Урок 1
- 41. Урок 1. 6. Химический элемент, изотопы. Химический
- 42. Урок 1 - Каков порядковый номер калия?
- 43. Урок 1 7.Вещество. Это вид материи; физическая субстанция со специфи- ческими химическими свойствами.
- 44. 8. Простые и сложные вещества
- 45. ТЕСТЫ мельчайшая химически неделимая электронейтраль- ная
- 46. ТЕСТЫ Найдите соответствие : Химический элемент
Слайд 6
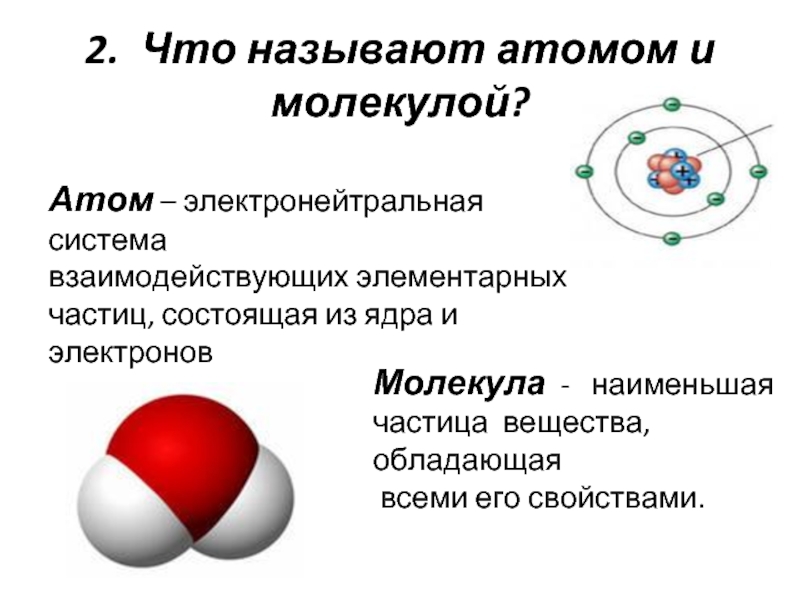
2. Что называют атомом и молекулой?
Атом – электронейтральная система
взаимодействующих элементарных
частиц, состоящая
Молекула - наименьшая
частица вещества, обладающая
всеми его свойствами.
Слайд 9Систематизировать понятия и составить схему
Вещества простые-
вещества сложные вещества, металлы, неметаллы,
Слайд 12Примеры атомов и молекул
Атомы
Водород-Н
Кислород- О
Молекулы
Водород Н2
Кислород О2
Вода Н2О
Спирт С2Н5ОН
Слайд 13Массы атомов и молекул
За единицу атомной массы в химии и физике
Слайд 18Алгоритм определения валентности, если известна валентность атома с постоянной валентностью
Правило валентности:
NaCL
Слайд 19Типы химических реакций
Обмена
АВ+СД=СВ+АД
Замещения
АВ+С=СВ+А
Соединения
А+В=АВ
Разложения
АВ=А+В
АВС=АВ+С
Слайд 20Закончить фразы
Валентность бывает постоянной и ……
За единицу валентности принято…..
Правило валентности: в
Определить валентность:
N2O 5 CaCL2 H2S
Слайд 21Дать определение понятиям
Атомная единица массы (а.е.м.)-
Относительная атомная масса (А r) –
Относительная
Найти относительную молекулярную массу молекулы:
серной кислоты, гидроксида натрия, оксида углерода -2
Слайд 22Количество вещества
Количества вещества (V) – число атомов, молекул или других структурных
За единицу измерения количества вещества принят МОЛЬ
1 Моль равен
Слайд 23МОЛЬ
Моль – это …
Число Авогадро – это…
Постоянная Авогадро- это …
Молярная масса
Слайд 24
синквейн – стихотворение из 5 строк по строгим правилам:
Тема, выраженная одним
Описание темы двумя прилагательными;
Описание действия в рамках темы 3 глаголами;
Фраза из 4 слов, выражающая суть или отношение автора к теме;
Одно слово – синоним к первому.
Слайд 25Относительная атомная масса (см. атомная масса химического элемента)
Относительная молекулярная масса ( сумма относительных атомных масс всех атомов, образующих молекулу вещества) Mr
Слайд 26КОЛИЧЕСТВО ВЕЩЕСТВА – число атомов, молекул или других структурных единиц вещества
Молярная масса – масса 1 моль вещества
(г /моль, кг/ моль) М
Молярный объем – объем 1 моль газа при н.у.
Vm = 22,4 л/моль
Слайд 30Ответить на вопросы
1.Какое количество вещества ( моль) содержит 12,04·10²³ атомов натрия?
2.Какова
3.Какой объем занимают 1,5 моль кислорода?
4.Какова масса 3 литров гелия?
Слайд 311. n = N/ Na = 12, 04 ·10²³ / 6,02
2. m = n · M(N₂) = 2 моль · 28 г/ моль = 56 г.
3. V= n · Vm = 1,5 моль · 22,4 л/моль = 33,6 л.
4. m= n· M = V/Vm · M(He)= 3л./22,4л/моль · 4г/моль =
= 0,54 г.
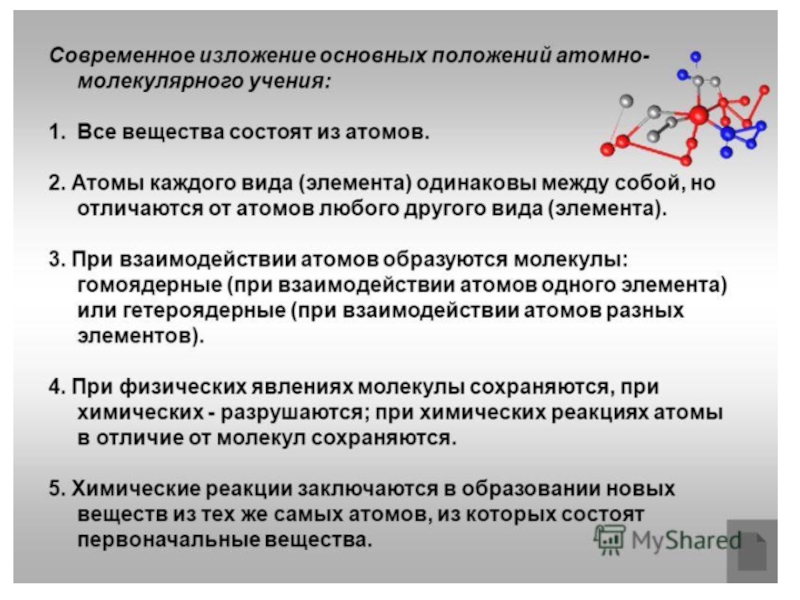
Слайд 32Основные положения атомно-молекулярного учения.
Атомно-молекулярное теория базируется на следующих законах и утверждениях:
Все
Атомы одного химического вещества (химический элемент) обладают одинаковыми свойствами, но отличаются от атомов другого вещества
При взаимодействии атомов образуются молекулы (гомоядерные — простые вещества, гетероядерные — сложные вещества)
При физических явлениях молекулы не изменяются, при химических происходит изменение их состава
Химические реакции заключаются в образовании новых веществ из тех же самых атомов, из которых состояли исходные вещества
Слайд 34Закон постоянства состава вещества
Закон постоянства состава вещества:
каждое химически чистое
Слайд 41Урок 1.
6. Химический элемент, изотопы.
Химический элемент – совокупность атомов с одинаковым
Изотопы - разновидность атомов одного
химического элемента с разным
числом нейтронов в ядре.
Слайд 42Урок 1
- Каков порядковый номер калия?
- Сколько протонов в его ядре?
-
- Сколько нейтронов в ядре калия?
- Чему равно массовое число атома калия?
№= 19
р = 19
е = 19
n = 20
Ar(K) = 39
Слайд 43Урок 1
7.Вещество.
Это вид материи; физическая субстанция со специфи-
ческими химическими свойствами.
Слайд 45ТЕСТЫ
мельчайшая химически неделимая электронейтраль-
ная частица вещества
виды элементарных частиц?
что называют массовым
вид атомов с одинаковым зарядом ядра?
разновидность атомов с одинаковым зарядом ядра,
но разной массой?
Слайд 46ТЕСТЫ
Найдите соответствие :
Химический элемент
2. Простое вещество постоянными физическими свойствами
3. Сложное вещество Б) состоит из атомов разных видов, имеет
4. Смесь постоянные свойства
В) состоит из разных веществ, которые
отличаются по свойствам
Г) один вид атомов, физические свойства
которого обычно не характеризуются
Только сложные вещества перечислены в ряду :
воздух, вода, кислород 2) серная кислота, водород, озон
3) поваренная соль, вода, сероводород 4) кислород, азот, хлор
Только простые вещества перечислены в ряду:
1) железо, кислород, соляная кислота 2) оксид натрия, вода, азот
3) фтор, кислород, сера 4) углерод, вода, сера
ОТВЕТ: 1 – Г; 2 - А;
3 – Б; 4 - В
ОТВЕТ: 1 - 3
ОТВЕТ: 3