- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Белоктар – биополимерлер презентация
Содержание
- 1. Белоктар – биополимерлер
- 2. жоспар: I. Кіріспе 1. Белоктар –
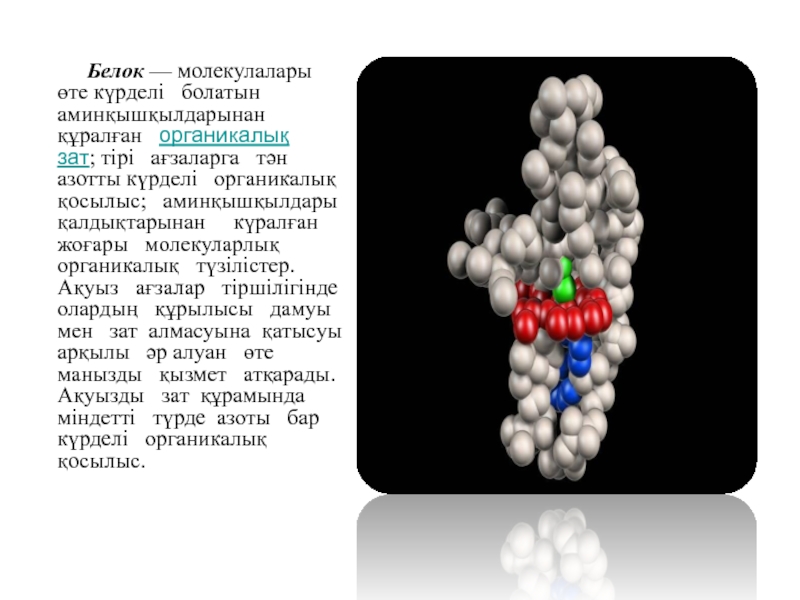
- 3. Белок —
- 4. Белоктар органикалық заттар дамуының ең жоғарғы сатысы
- 5. Ақуыздың құрылымының деңгейлерi: 1
- 6. Ақуыз
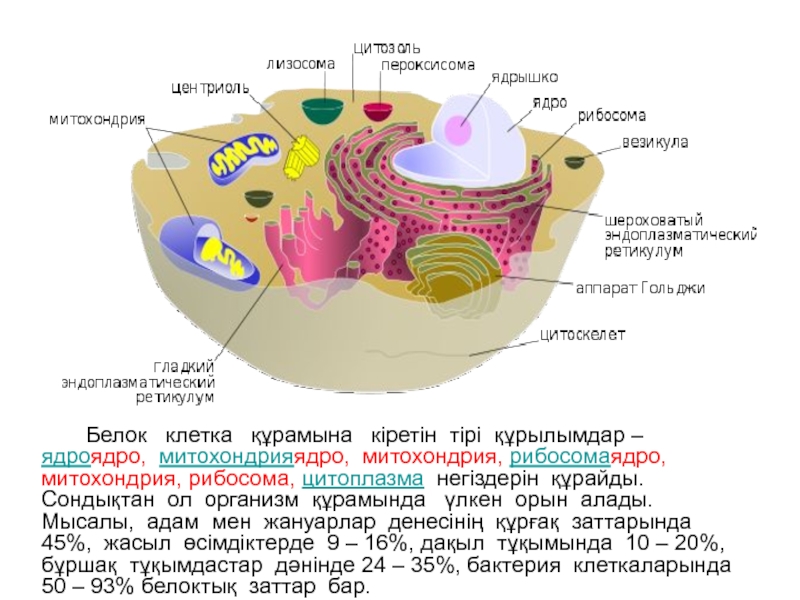
- 7. Белок клетка
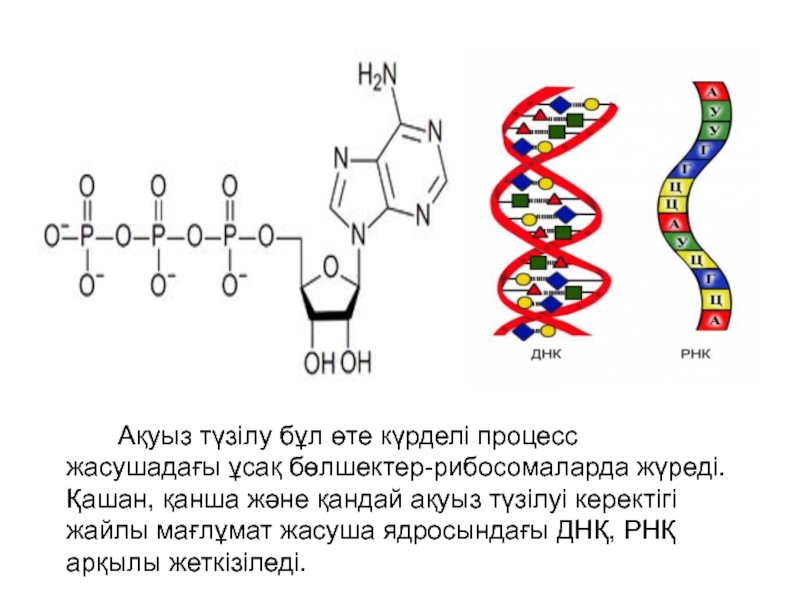
- 8. Ақуыз түзілу бұл
- 9. Белоктардың қасиеттерін
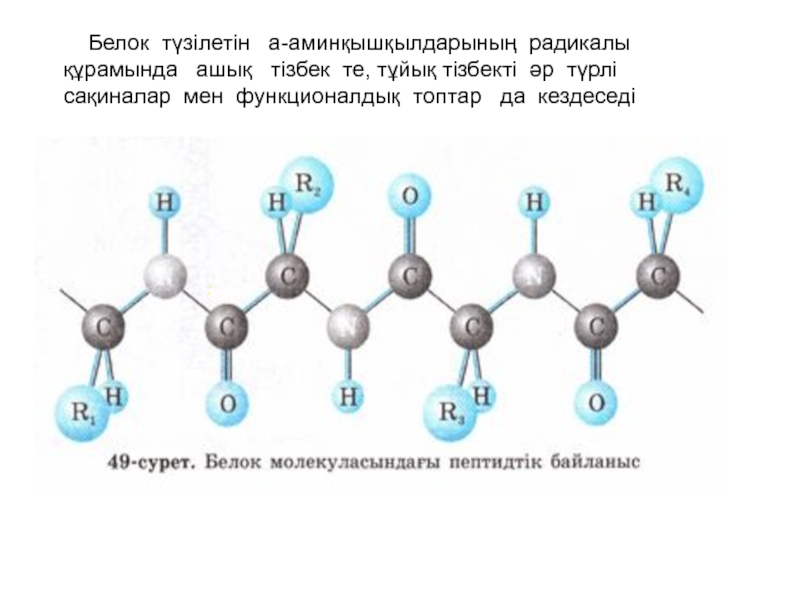
- 10. Белок түзілетін
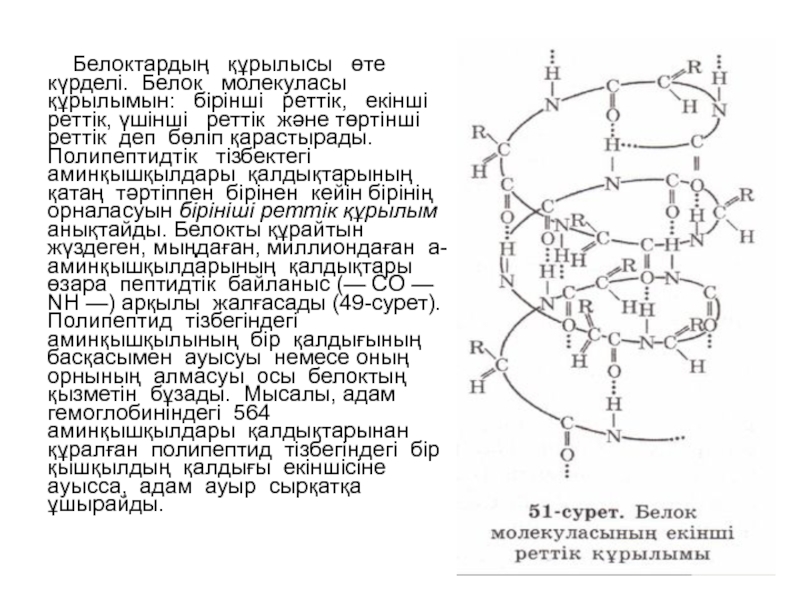
- 11. Белоктардың құрылысы өте
- 12. Белок молекуласы
- 13. Белоктарды, негізінен, мынадай белгілеріне қарап
- 14. Белоктардың екінші және үшінші
- 15. Химиялық қасиеттері Құрамы мен құрылысы күрделі
- 17. 1. О.Д.Дайырбеков, Б.Е.Алтынбеков, Б.К.Торғауытов,
- 18. Рахмет!!!
Слайд 2жоспар:
I. Кіріспе
1. Белоктар – биополимерлер
II. Негізгі бөлім
1.
2. Белоктардың құрамы
3. Белоктардың қызметі
4. Химиялық қасиеттері
5. Белок денатурациясы
III. Қорытынды
Слайд 3
Белок — молекулалары өте күрделі
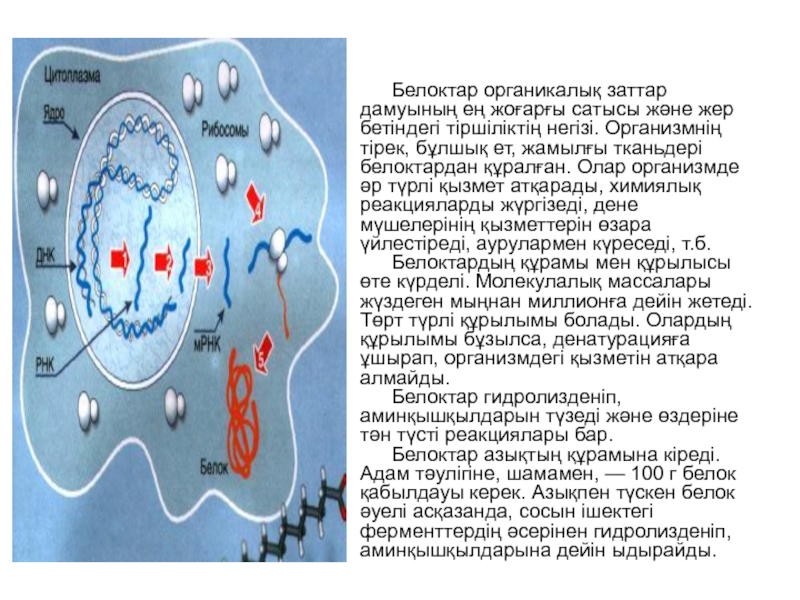
Слайд 4Белоктар органикалық заттар дамуының ең жоғарғы сатысы және жер бетіндегі тіршіліктің
Белоктардың құрамы мен құрылысы өте күрделі. Молекулалық массалары жүздеген мыңнан миллионға дейін жетеді. Төрт түрлі құрылымы болады. Олардың құрылымы бұзылса, денатурацияға ұшырап, организмдегі қызметін атқара алмайды.
Белоктар гидролизденіп, аминқышқылдарын түзеді және өздеріне тән түсті реакциялары бар.
Белоктар азықтың құрамына кіреді. Адам тәулігіне, шамамен, — 100 г белок қабылдауы керек. Азықпен түскен белок әуелі асқазанда, сосын ішектегі ферменттердің әсерінен гидролизденіп, аминқышқылдарына дейін ыдырайды.
Слайд 5
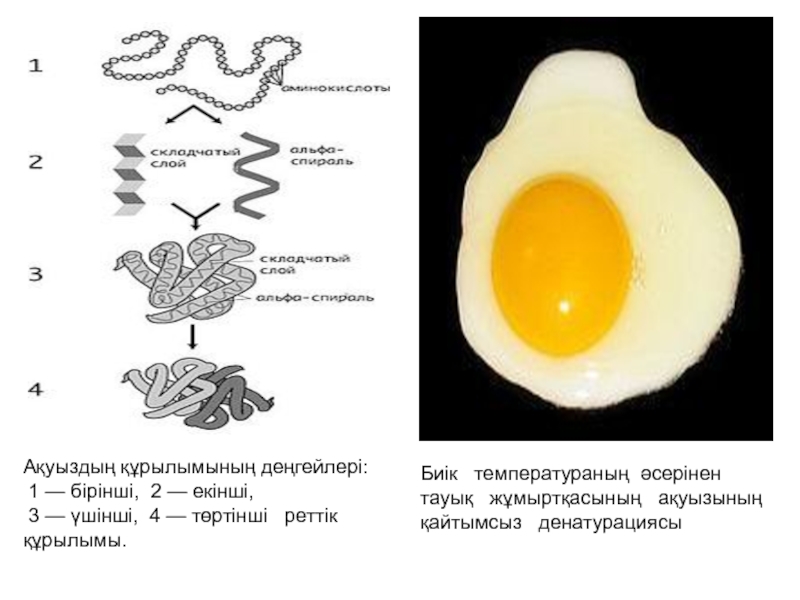
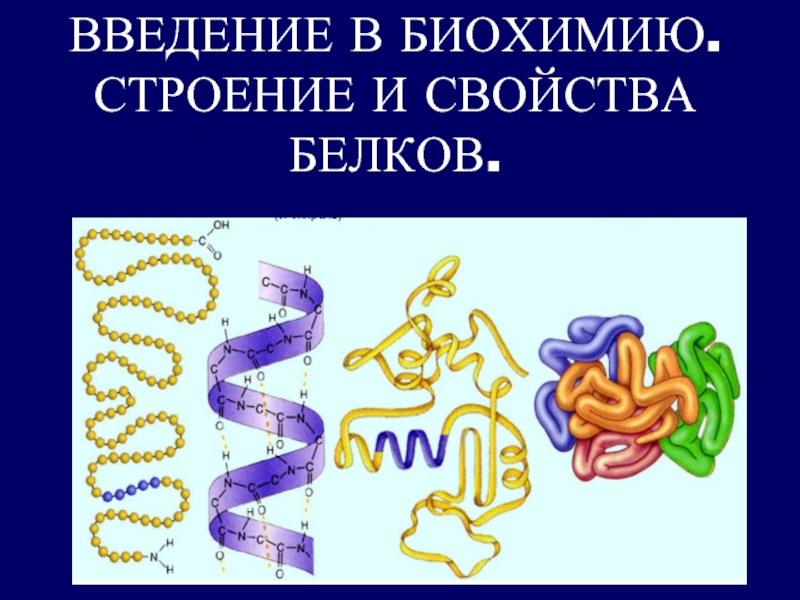
Ақуыздың құрылымының деңгейлерi:
1 — бірінші, 2 — екінші,
3
Биiк температураның әсерiнен тауық жұмыртқасының ақуызының қайтымсыз денатурациясы
Слайд 6
Ақуыз тірі организмнің негізін
Белок тек тірі организмдер құрамында ғана болады. Оның құрамында 50,6 – 54,5% көміртекБелок тек тірі организмдер құрамында ғана болады. Оның құрамында 50,6 – 54,5% көміртек, 21,5 – 23,5% оттекБелок тек тірі организмдер құрамында ғана болады. Оның құрамында 50,6 – 54,5% көміртек, 21,5 – 23,5% оттек, 6,5 – 7,3% сутекБелок тек тірі организмдер құрамында ғана болады. Оның құрамында 50,6 – 54,5% көміртек, 21,5 – 23,5% оттек, 6,5 – 7,3% сутек, 15 – 17,6% азотБелок тек тірі организмдер құрамында ғана болады. Оның құрамында 50,6 – 54,5% көміртек, 21,5 – 23,5% оттек, 6,5 – 7,3% сутек, 15 – 17,6% азот, 0,3 – 2,5% күкіртБелок тек тірі организмдер құрамында ғана болады. Оның құрамында 50,6 – 54,5% көміртек, 21,5 – 23,5% оттек, 6,5 – 7,3% сутек, 15 – 17,6% азот, 0,3 – 2,5% күкірт бар, кейде фосфор кездеседі. Осы элементтерден түзілетін амин кышқылдарының бір-бірімен байланысып қосылуы нәтижесінде белок молекуласы түзіледі. Белок молекуласының массасы өте үлкен, ол бірнеше мыңнан бірнеше миллионға дейін барады.
Слайд 7 Белок клетка құрамына кіретін
Слайд 8 Ақуыз түзілу бұл өте күрделі процесс жасушадағы
Слайд 9
Белоктардың қасиеттерін олардың құрамы мен
R—CHNH2—COOH
Слайд 10
Белок түзілетін a-аминқышқылдарының радикалы құрамында ашық
:
Слайд 11 Белоктардың құрылысы өте күрделі. Белок молекуласы
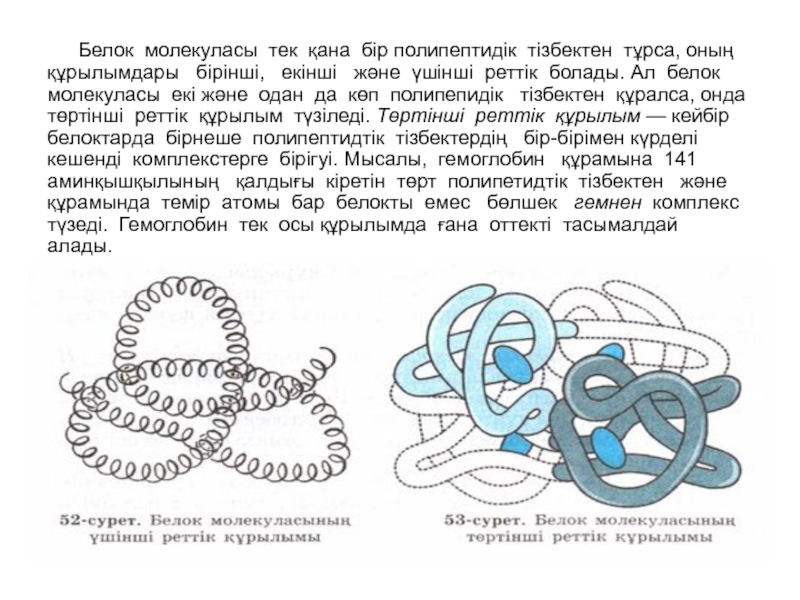
Полипептидтік тізбектегі аминқышқылдары қалдықтарының қатаң тәртіппен бірінен кейін бірінің орналасуын бірініші реттік құрылым анықтайды. Белокты құрайтын жүздеген, мыңдаған, миллиондаған а-аминқышқылдарының қалдықтары өзара пептидтік байланыс (— CO — NH —) арқылы жалғасады (49-сурет).
Полипептид тізбегіндегі аминқышқылының бір қалдығының басқасымен ауысуы немесе оның орнының алмасуы осы белоктың қызметін бұзады. Мысалы, адам гемоглобиніндегі 564 аминқышқылдары қалдықтарынан құралған полипептид тізбегіндегі бір қышқылдың қалдығы екіншісіне ауысса, адам ауыр сырқатқа ұшырайды.
Слайд 12
Белок молекуласы тек қана бір полипептидік тізбектен
Слайд 13
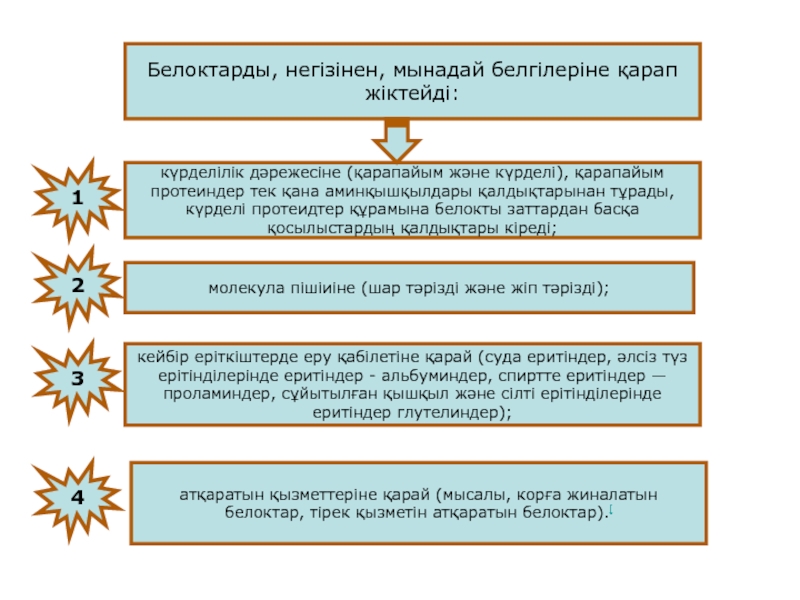
Белоктарды, негізінен, мынадай белгілеріне қарап жіктейді:
күрделілік дәрежесіне (қарапайым және күрделі),
молекула пішіиіне (шар тәрізді және жіп тәрізді);
кейбір еріткіштерде еру қабілетіне қарай (суда еритіндер, әлсіз түз ерітінділерінде еритіндер - альбуминдер, спиртте еритіндер — проламиндер, сұйытылған қышқыл және сілті ерітінділерінде еритіндер глутелиндер);
атқаратын қызметтеріне қарай (мысалы, корға жиналатын белоктар, тірек қызметін атқаратын белоктар).[
1
2
3
4
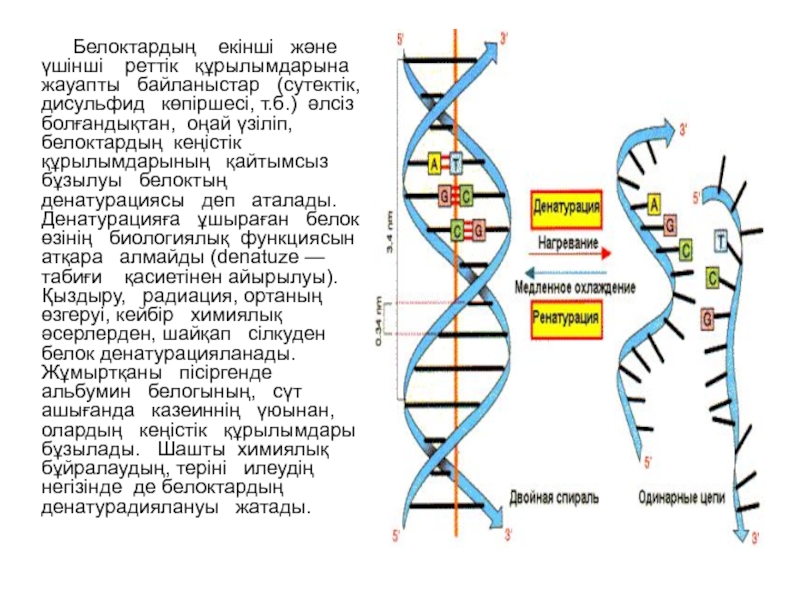
Слайд 14Белоктардың екінші және үшінші реттік құрылымдарына жауапты
Слайд 15Химиялық қасиеттері
Құрамы мен құрылысы күрделі болғандықтан, белоктардың қасиеттері де алуан түрлі.
Белоктар — екідайлы электролиттер. Ортаның белгілі бір рН мәнінде олардың молекулаларындағы оң және теріс зарядтар бірдей (изоэлектрлік нүкте деп аталады) болады. Бұл — белоктардың маңызды қасиеттерінің бірі. Бұл нүктеде белоктар электрбейтарап болып, суда еруі азаяды. Белоктардың осы қасиеті технологияда белокты өнімдер алуға қолданылады.
Белоктардың гидролизі. Сілті немесе қышқыл ерітінділерін қосып қыздырғанда, белоктар гидролизденіп, аминқышқылдарын түзеді:
Белоктардыц түсті реакциялары. Белоктарды сапалық анықтау үшін түсті реакциялар қолданылады.
а) Ксантопротеинреакциясымен (грек. ксанты — сары) құрамында бензол ядросы бар белоктар концентрлі азот қышқылымен сары түс береді.
ә) Биурет реакциясы. Мыс (II) гидроксидінің сілтідегі ерітіндісімен белоктарға әсер еткенде, ашық күлгін түс пайда болады. Бұл реакция белоктардың құрамындағы пептидтік байланыстарды анықтайды.
б) Құрамында күкірті бар белоктарға қорғасын ацетатын және сілті қосып қыздырғанда, қорғасын сульфидінің қара түнбасы түзіледі.
Слайд 16
Қорыта келгенде белоктар тірі организім
Белоктардың негізгі қызметтері: катализаторлық, энергетикалық, реттеуші, тасымалдаушы, ең бастысы құрылымдық.
Слайд 17 1. О.Д.Дайырбеков, Б.Е.Алтынбеков, Б.К.Торғауытов, У.И.Кенесариев, Т.С.Хайдарова Аурудың алдын
Пайдаланылған әдебиеттер