- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Белки, или протеины презентация
Содержание
- 2. Белки или протеины ( от греч. «протос»
- 3. Впервые белок был выделен (в виде клейковины)
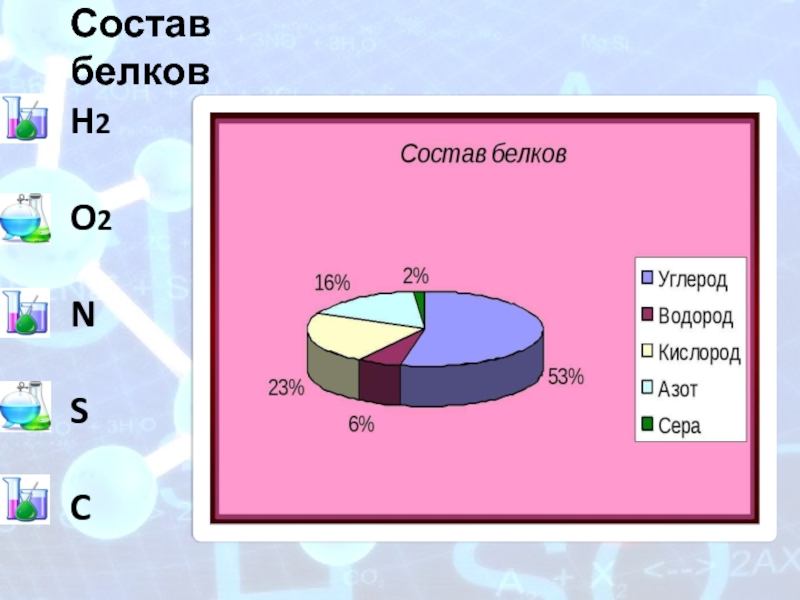
- 4. Состав белков H2 O2 N S C
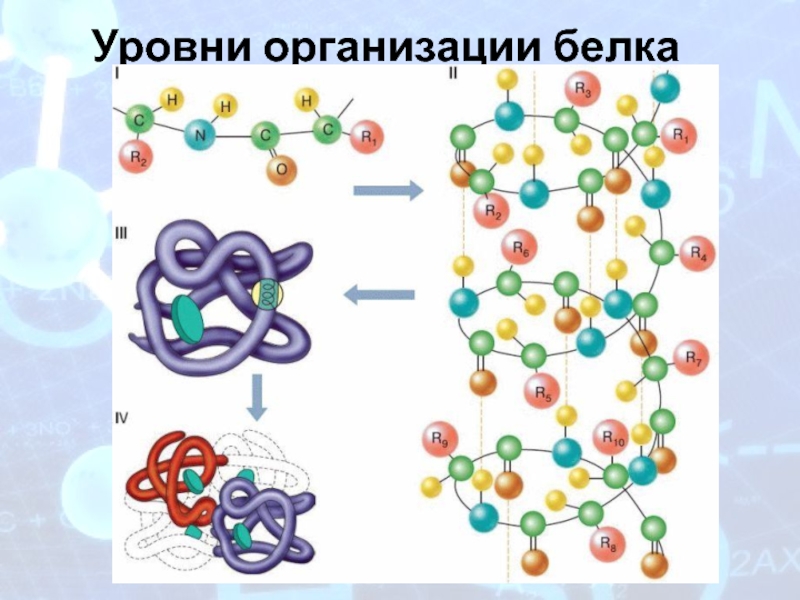
- 5. Уровни организации белка
- 6. Первичная структура Первичная структура – число и
- 7. Вторичная структура Путем образования водородных связей
- 8. Третичная структура Образуется благодаря взаимодействию радикалов, в
- 9. Четвретичная структура Она представляет собой функциональное объединение
- 10. Физические свойства Гемоглобин Белки в твердом состоянии
- 11. Биурентовая реакция Результат реакции Качественная на все
- 12. Ксантопротеиновая реакция Ксантопротеиновая реакция открывает наличие
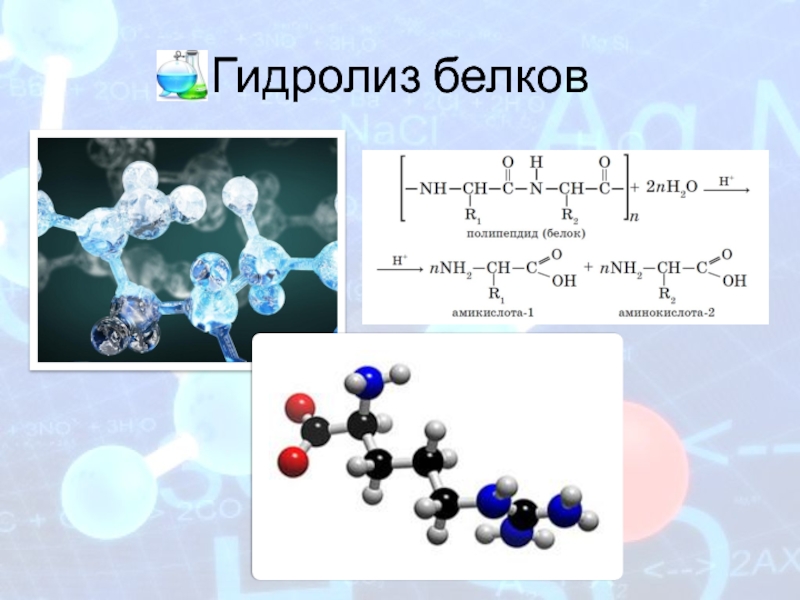
- 13. Гидролиз белков
- 14. Функции белков Каталитическая Транспортная Регуляторная Двигательная Гормональная Пластическая Защитная Структурная
- 15. Жиры, белки и углеводы – основа питания
- 16. Аминокислоты Всего аминокислот более 100 видов. Белки строятся только из 20 аминокислот.
- 17. Незаменимые аминокислоты Аминокислоты, которые организмы не синтезирует,
- 18. Необходимое количество белка Суточная норма потребления белка
- 19. Заключение Белки – обязательная составная часть
Слайд 2Белки или протеины ( от греч. «протос» - «первый»), - это
природные органические соединения, которые обеспечивают все жизнененные процессы любого организма
Слайд 3Впервые белок был выделен (в виде клейковины) в 1728 г. итальянцем
Якопо Бартоломео Беккари(1682-1766) из пшечничной муки. Это собитие принято считать рождением химии белка
Слайд 6Первичная структура
Первичная структура – число и последовательность аминокислот , соединенных друг
с другом пептидными связями в полипептидной цепи
Слайд 7Вторичная структура
Путем образования водородных связей между остатками карбоксильных и аминогрупп
разных аминокислот белковая молекула принимает вид
спирали.
спирали.
Слайд 8Третичная структура
Образуется благодаря взаимодействию радикалов, в частности радикалов аминокислоты цистеина, которые
содержат серу. Атомы серы двух аминокислот, находящихся на некотором расстоянии друг от друга в полипептидной цепи, соединяются, образуя так называемые дисульфидные связи.
Слайд 9Четвретичная структура
Она представляет собой функциональное объединение нескольких (двух, трех и более)молекул
белка, обладающих третичной структурной организацией.
Слайд 10Физические свойства
Гемоглобин
Белки в твердом состоянии белого цвета, а в растворе бесцветны,
если только они не несут какой-нибудь хромовой (окрашенной)группы, как, например, гемоглобин. Растворимость в воде у разных белков сильно варьирует. Малекулярная масса белков очень велика – от несколькихтысяч до многих миллионов дальтон. Благодаря присутствию в молекулах белков положительно и отрицательно заряженных групп они движутся с разной скоростьюи в электрическом поле.
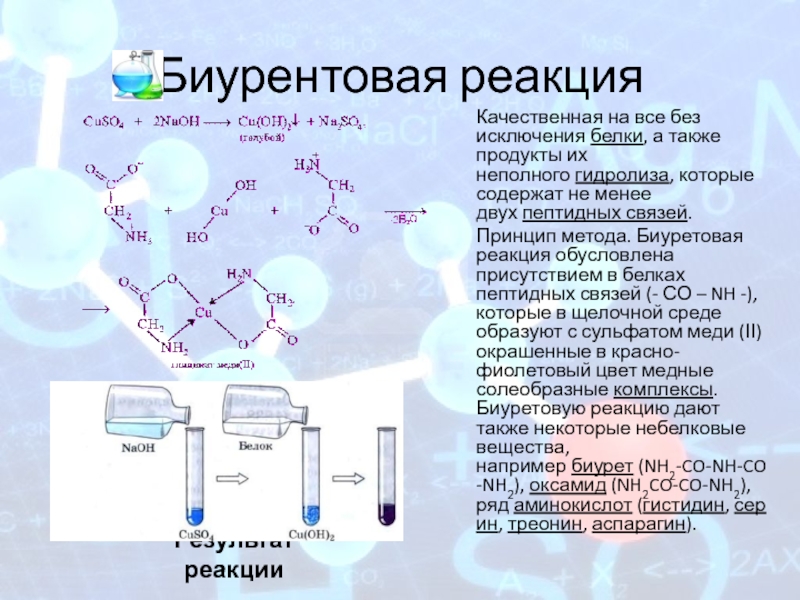
Слайд 11Биурентовая реакция
Результат реакции
Качественная на все без исключения белки, а также продукты их
неполного гидролиза, которые содержат не менее двух пептидных связей.
Принцип метода. Биуретовая реакция обусловлена присутствием в белках пептидных связей (- СО – NH -), которые в щелочной среде образуют с сульфатом меди (ІІ) окрашенные в красно-фиолетовый цвет медные солеобразные комплексы. Биуретовую реакцию дают также некоторые небелковые вещества, например биурет (NH2-CO-NH-CO-NH2), оксамид (NH2CO-CO-NH2), ряд аминокислот (гистидин, серин, треонин, аспарагин).
Принцип метода. Биуретовая реакция обусловлена присутствием в белках пептидных связей (- СО – NH -), которые в щелочной среде образуют с сульфатом меди (ІІ) окрашенные в красно-фиолетовый цвет медные солеобразные комплексы. Биуретовую реакцию дают также некоторые небелковые вещества, например биурет (NH2-CO-NH-CO-NH2), оксамид (NH2CO-CO-NH2), ряд аминокислот (гистидин, серин, треонин, аспарагин).
Слайд 12Ксантопротеиновая реакция
Ксантопротеиновая реакция открывает наличие в белках циклических аминокислот –
триптофана, фенилаланина, тирозина, содержащих в своем составе ароматическое ядро.
Реакция носит название от греч. слова Xanthos – желтый. Ряд белков при добавлении к ним концентрированной азотной кислоты при нагревании дают желтое окрашивание, которое может переходить в оранжевое в щелочной среде.
Реакция вызвана нитрованием бензольного ядра указанных циклических аминокислот и образованием нитросоединений желтого цвета.
Реакция носит название от греч. слова Xanthos – желтый. Ряд белков при добавлении к ним концентрированной азотной кислоты при нагревании дают желтое окрашивание, которое может переходить в оранжевое в щелочной среде.
Реакция вызвана нитрованием бензольного ядра указанных циклических аминокислот и образованием нитросоединений желтого цвета.
Слайд 14Функции белков
Каталитическая
Транспортная
Регуляторная
Двигательная
Гормональная
Пластическая
Защитная
Структурная
Слайд 17Незаменимые аминокислоты
Аминокислоты, которые организмы не синтезирует, называются незаменимыми. Всего их восемь:
лизин, метионин, триптофаг, лейцин, изолейцин, валин, треонин и фенилаланин.
Незаменимые аминокислоты долны поступать в организм с пищей.
Незаменимые аминокислоты долны поступать в организм с пищей.
Слайд 18Необходимое количество белка
Суточная норма потребления белка составляет 0.75-0.80 грамм на килограмм
веса для взрослого( около 56 грамм в сутки для среднего мужчины и 45 грамм для женщины)
Детям требуется больше белка – до 1.9 грамм на килограмм веса в сутки.
Детям требуется больше белка – до 1.9 грамм на килограмм веса в сутки.
Слайд 19Заключение
Белки – обязательная составная часть всех живых клеток, играют исключительно
важную роль в живой природе, являются главными, наиболее ценными и незаменимыми компонентами питания. Белки являются основной структурных элементов и тканей, поддерживают обмен веществ и энергии, учавствуют в процессах роста и размножения, обеспечивают механизмы движений, развитие иммунных реакция, необходимы для функционирования
Всех органов и систем организма.
Всех органов и систем организма.