- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Білки як високомолекулярні сполуки презентация
Содержание
- 1. Білки як високомолекулярні сполуки
- 2. Фронтальна робота 1) Я кі функціональні групи
- 3. Білки Білки (поліпептиди) — це природні високомолекулярні
- 4. У живих організмах амінокислотний склад білків визначається
- 5. Фізичні властивості білків Білки відрізняються за ступенем
- 6. Синтез білків Формальне утворення білкової макромолекули можна представити як реакцію поліконденсації α-амінокислот:
- 7. Виділяють чотири рівні структурної організації білків. Первинна
- 8. Третинна структура — форма закрученої в просторі
- 9. Хімічні властивості білків 1) Гідроліз білків є
- 10. Застосування одержаних знань 1) Яєчний білок поміщаємо
Слайд 2Фронтальна робота
1) Я кі функціональні групи входять до складу амінокислот?
2) Самостійно
виберіть із таблиці три амінокислоти та складіть формули утворених ними трипептидів.
Слайд 3Білки
Білки (поліпептиди) — це природні високомолекулярні нітрогеновмісні органічні сполуки (біополімери), побудовані
із залишків α-амінокислот, з’єднаних пептидними зв’язками.
Слайд 4 У живих організмах амінокислотний склад білків визначається генетичним кодом, у синтезі
в більшості випадків використовуються двадцять стандартних амінокислот. Безліч їхніх комбінацій дають велику розмаїтість властивостей молекул білків.
Слайд 5Фізичні властивості білків
Білки відрізняються за ступенем розчинності у воді, але більшість
із них у ній розчиняються. До нерозчинних належать, наприклад, кератин і фіброїн, який входить до складу шовку й павутиння. Білки також поділяються на гідрофільні й гідрофобні.
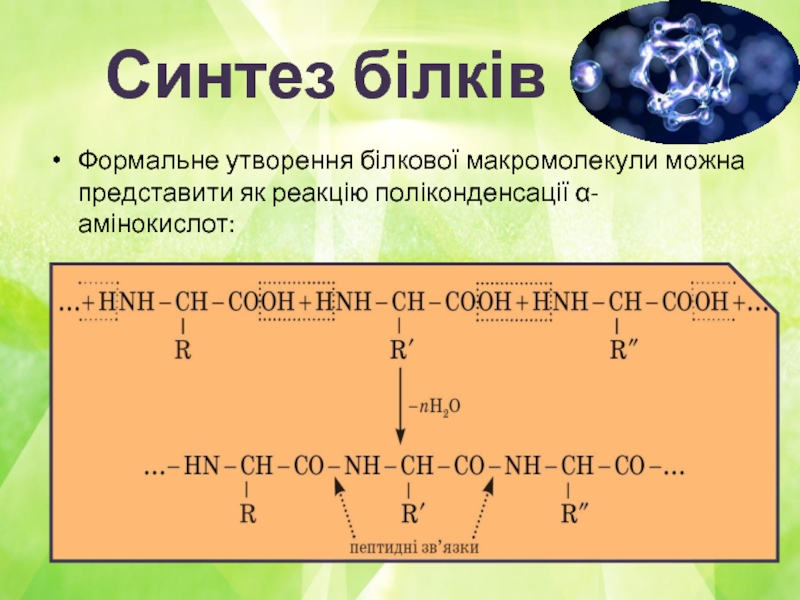
Слайд 6Синтез білків
Формальне утворення білкової макромолекули можна представити як реакцію поліконденсації α-амінокислот:
Слайд 7Виділяють чотири рівні структурної організації білків.
Первинна структура — певна послідовність α-амінокислотних
залишків у поліпептидному ланцюзі.
Вторинна структура (α-спіраль) — це конформація поліпептидного ланцюга, закріплена безліччю водневих зв’язків між групами N−H і C = O. Одна з моделей вторинної структури — α-спіраль.
Вторинна структура (α-спіраль) — це конформація поліпептидного ланцюга, закріплена безліччю водневих зв’язків між групами N−H і C = O. Одна з моделей вторинної структури — α-спіраль.
Слайд 8Третинна структура — форма закрученої в просторі спіралі, утворена головним чином
за рахунок дисульфідних містків −S − S−, водневих зв’язків, гідрофобних та йонних узаємодій.
Четвертинна структура — агрегати кількох білкових макромолекул (білкові комплекси), утворені за рахунок узаємодії різних поліпептидних ланцюгів.
Четвертинна структура — агрегати кількох білкових макромолекул (білкові комплекси), утворені за рахунок узаємодії різних поліпептидних ланцюгів.
Слайд 9Хімічні властивості білків
1) Гідроліз білків є гідролізом поліпептидного ланцюга з утворенням
набору амінокислот, що утворили цей поліпептидний ланцюг.
2) Денатурація — руйнування третинної та вторинної структур білкової молекули під дією нагрівання, сильних кислот, лугів, солей важких металів, спиртів, радіації.
2) Денатурація — руйнування третинної та вторинної структур білкової молекули під дією нагрівання, сильних кислот, лугів, солей важких металів, спиртів, радіації.
Слайд 10Застосування одержаних знань
1) Яєчний білок поміщаємо в хімічну склянку, додаємо води
(1:1), розмішуємо. Що спостерігаємо? Зробіть висновок про розчинність білка.
2) Наливаємо 1–2 мл одержаного розчину в пробірку. Дотримуючись правил техніки безпеки, нагріваємо до згортання білка.
3) Наливаємо 1–2 мл розчину білка в пробірку, доливаємо 1–2 мл спирту (98 %). Що спостерігаємо?
2) Наливаємо 1–2 мл одержаного розчину в пробірку. Дотримуючись правил техніки безпеки, нагріваємо до згортання білка.
3) Наливаємо 1–2 мл розчину білка в пробірку, доливаємо 1–2 мл спирту (98 %). Що спостерігаємо?