- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Амины. Азотсодержащие соединения презентация
Содержание
- 1. Амины. Азотсодержащие соединения
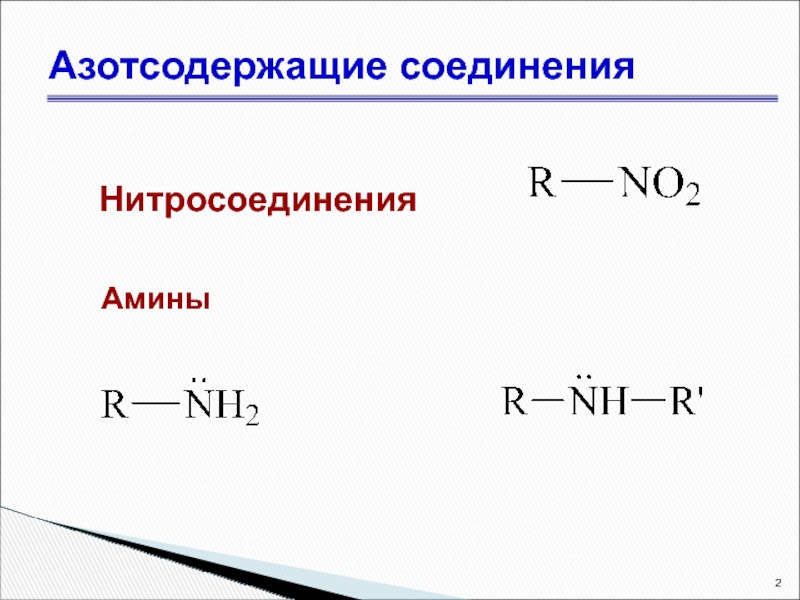
- 2. Азотсодержащие соединения Нитросоединения Амины
- 3. Амины – органические производные аммиака NH3,
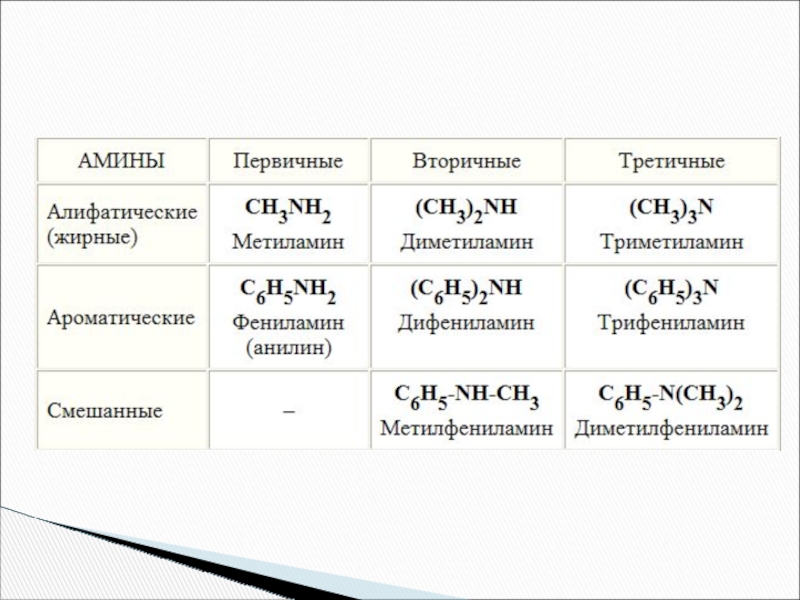
- 4. Амины
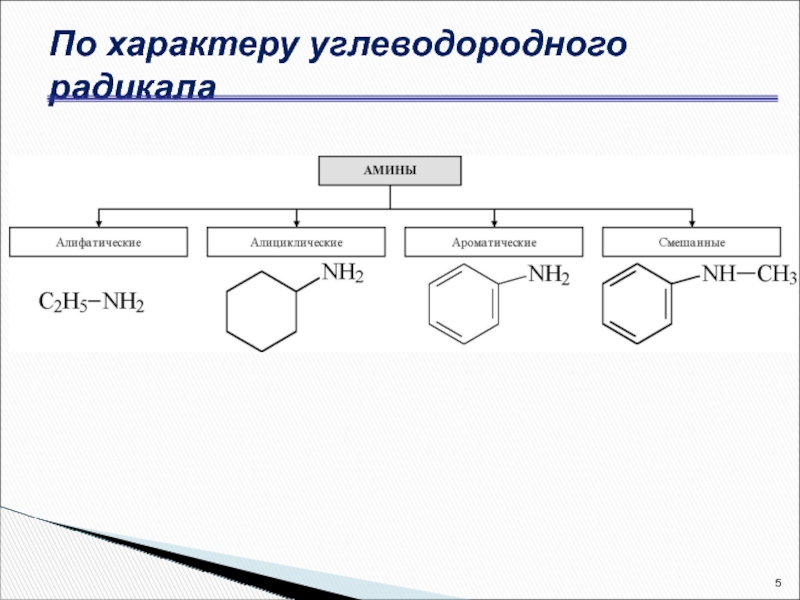
- 5. По характеру углеводородного радикала
- 7. В большинстве случаев названия аминов образуют из
- 8. Амины Номенклатура и изомерия 2-метилпропанамин (изобутиламин) (CH3)2CHCH2NH2
- 9. При наличии одинаковых радикалов используют приставки ди
- 10. Амины Номенклатура и изомерия
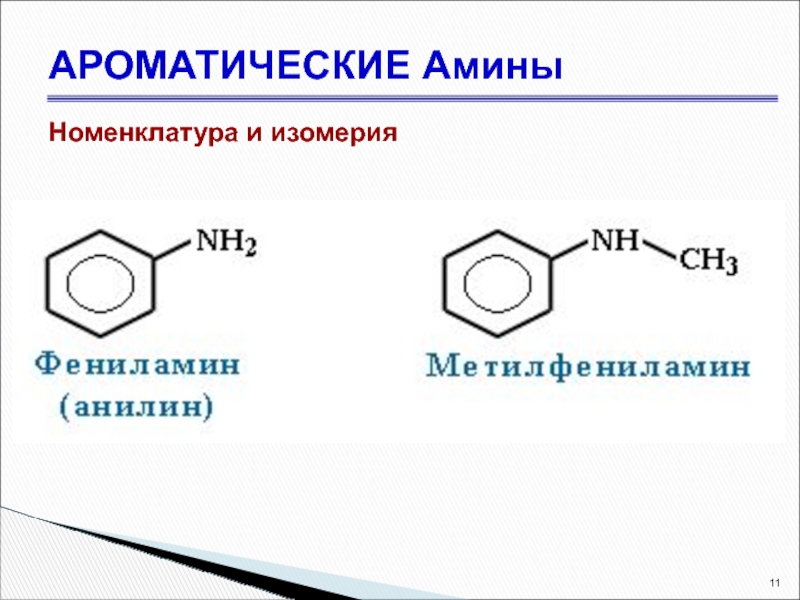
- 11. АРОМАТИЧЕСКИЕ Амины Номенклатура и изомерия
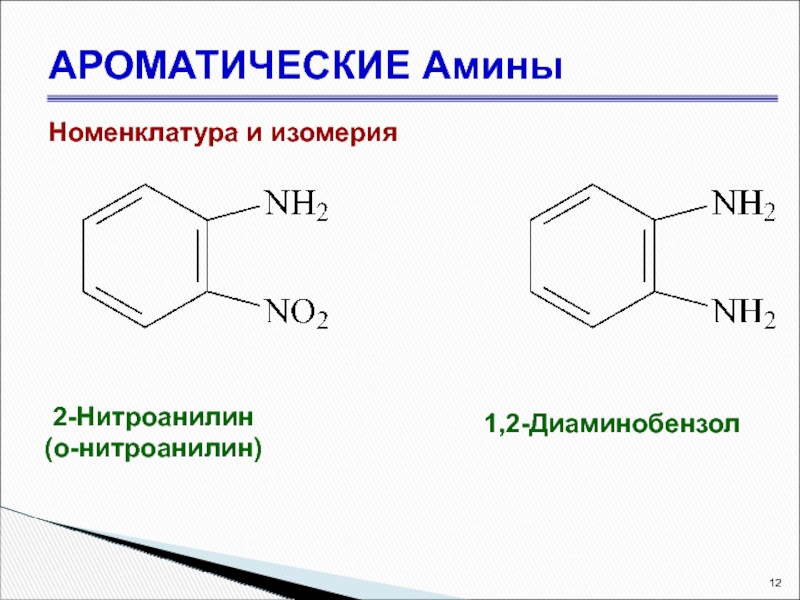
- 12. АРОМАТИЧЕСКИЕ Амины Номенклатура и изомерия 2-Нитроанилин (о-нитроанилин) 1,2-Диаминобензол
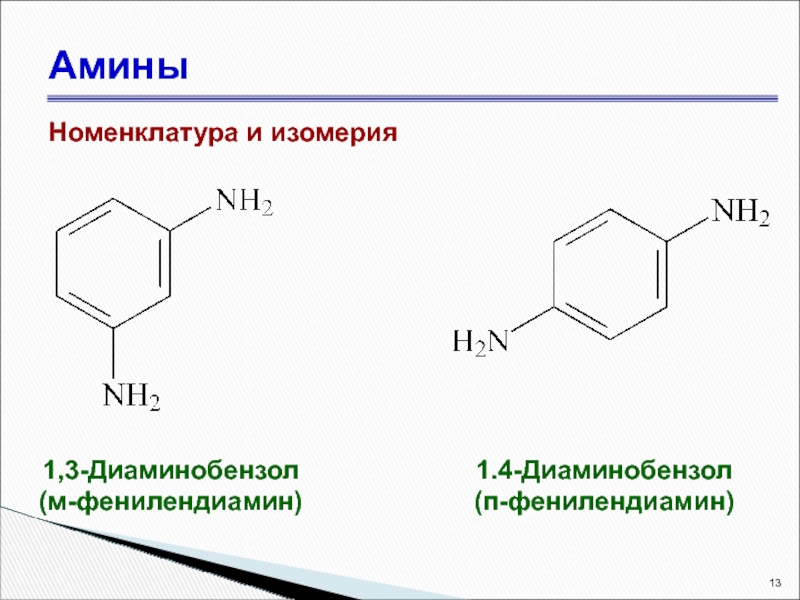
- 13. Амины Номенклатура и изомерия 1,3-Диаминобензол (м-фенилендиамин) 1.4-Диаминобензол (п-фенилендиамин)
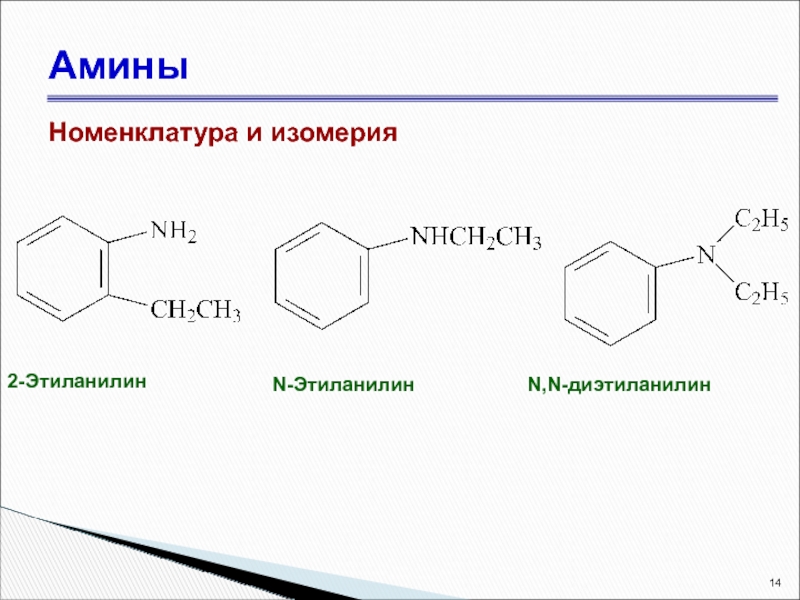
- 14. Амины Номенклатура и изомерия 2-Этиланилин N-Этиланилин N,N-диэтиланилин
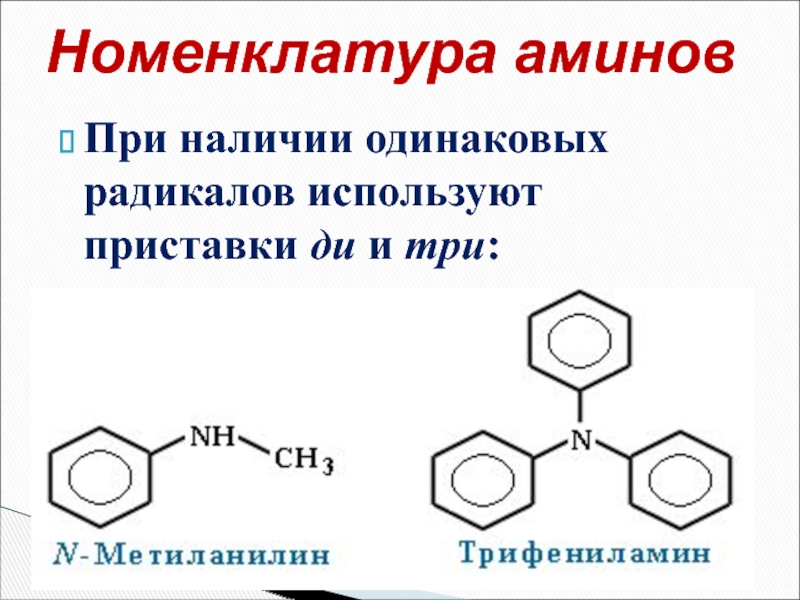
- 15. При наличии одинаковых радикалов используют приставки ди и три: Номенклатура аминов
- 16. 1. Структурная изомерия - углеродного скелета, начиная с С4H9NH2: Изомерия аминов
- 17. Структурная изомерия - положения аминогруппы, начиная с С3H7NH2: Изомерия аминов
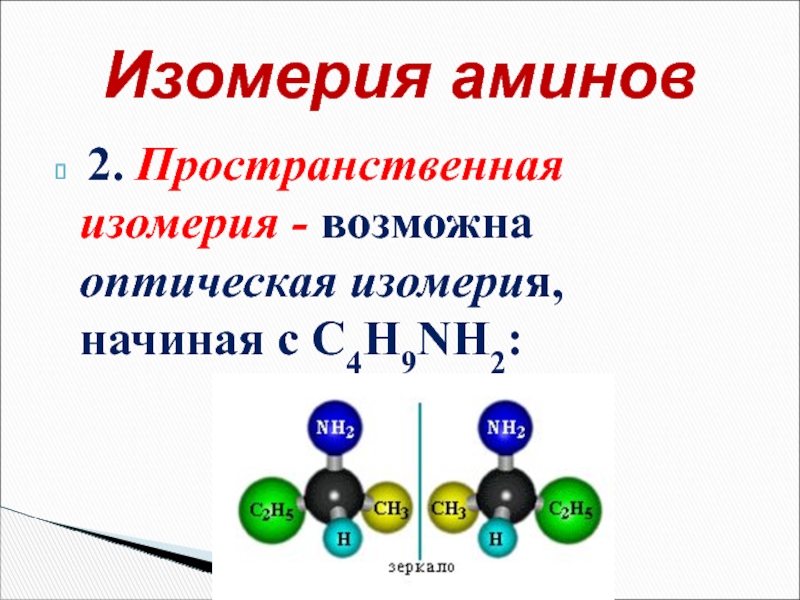
- 18. 2. Пространственная изомерия - возможна оптическая изомерия, начиная с С4H9NH2: Изомерия аминов
- 19. Связь N–H является полярной, поэтому первичные
- 20. Это объясняет относительно высокую температуру кипения
- 21. Третичные амины не образуют ассоциирующих водородных
- 22. При обычной температуре только низшие алифатические
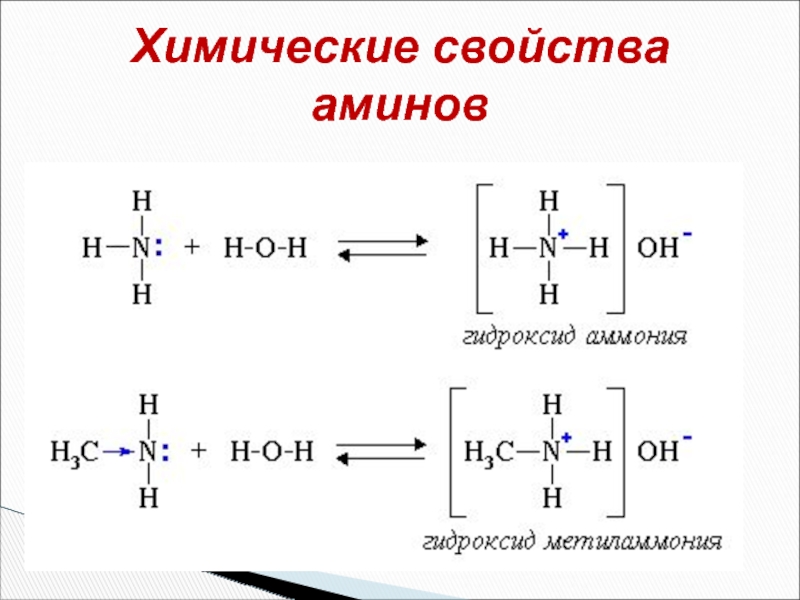
- 25. Химические свойства аминов
- 26. 2. Взаимодействуя с кислотами, амины образуют соли: Химические свойства аминов
- 27. Алкилирование (реакция Гофмана, 1850) 19.02.1660 - 12.11.1742 Гофман Фридрих
- 28. Амины Химические свойства Алкилирование
- 29. 3. В отличие от аммиака, низшие
- 30. Анилин (фениламин) С6H5NH2 – важнейший из ароматических аминов: Анилин
- 31. Анилин представляет собой бесцветную маслянистую жидкость
- 32. Для анилина характерны реакции как по
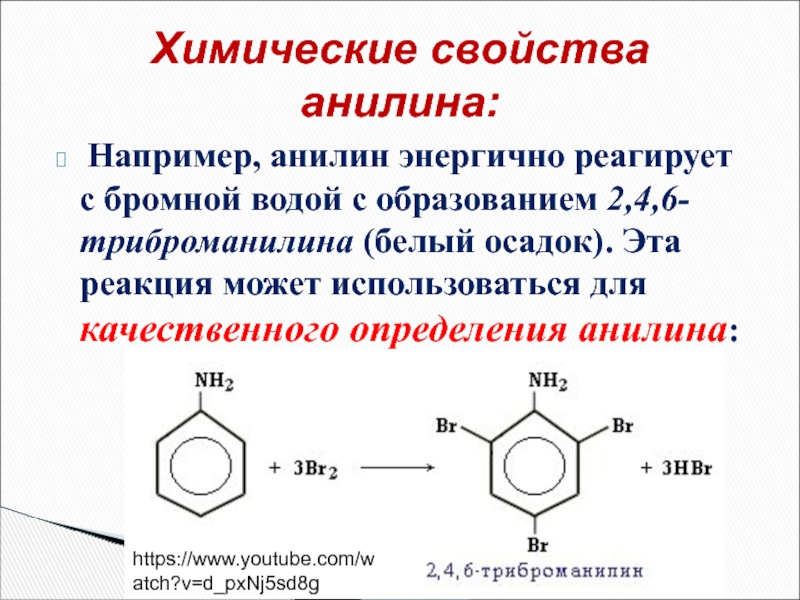
- 33. Например, анилин энергично реагирует с бромной
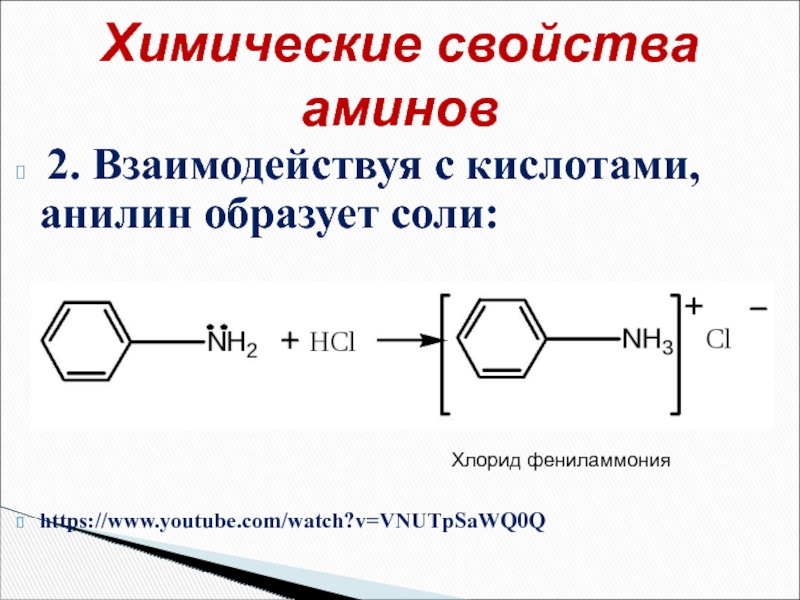
- 34. 2. Взаимодействуя с кислотами, анилин образует соли:
- 35. 1. Наиболее общим методом получения первичных аминов является восстановление нитросоединений: Получение аминов
- 36. Важнейший ароматический амин - анилин -
- 37. ЗИНИН Николай Николаевич
- 38. C6H5NH2 + O2 --> CO2 +
- 40. Широкое применение в качестве полупродукта в производстве витаминов и лекарственных средств (сульфаниламидные препараты). Применение анилина
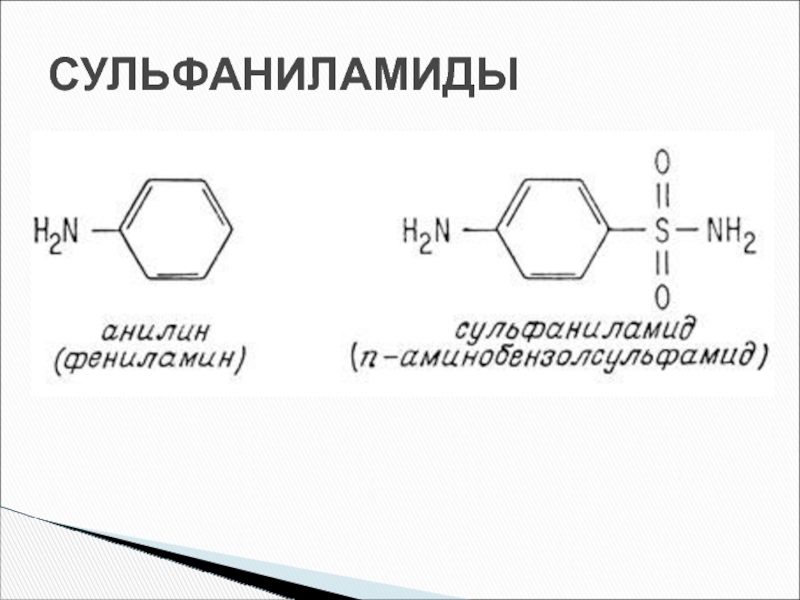
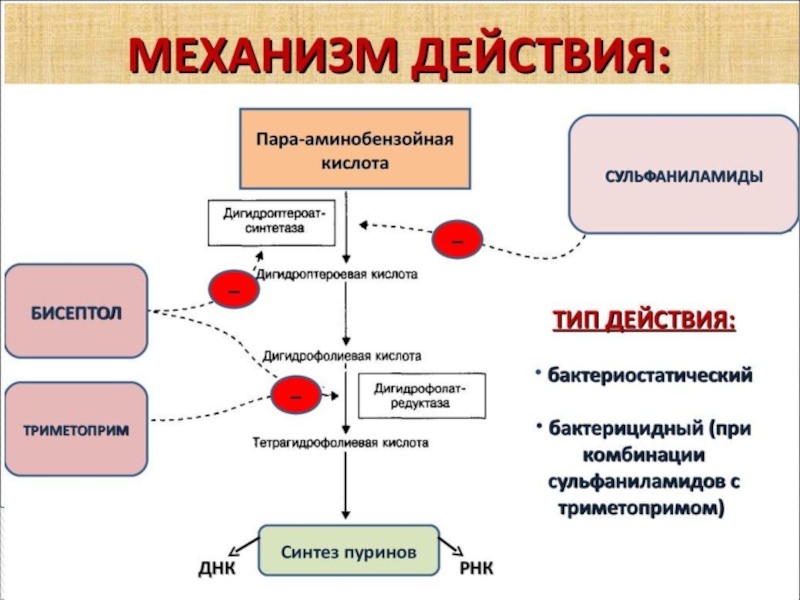
- 42. СУЛЬФАНИЛАМИДЫ
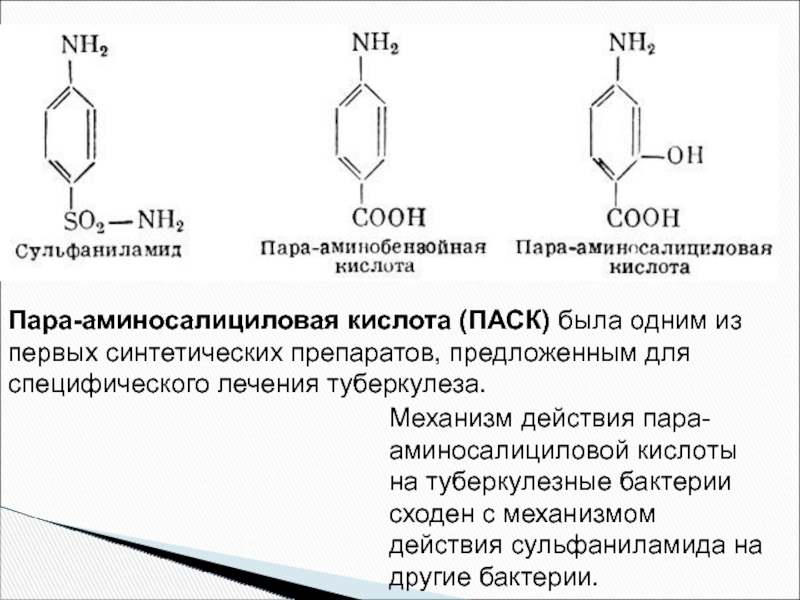
- 43. Пара-аминосалициловая кислота (ПАСК) была одним из первых
- 45. Назовите соединения:
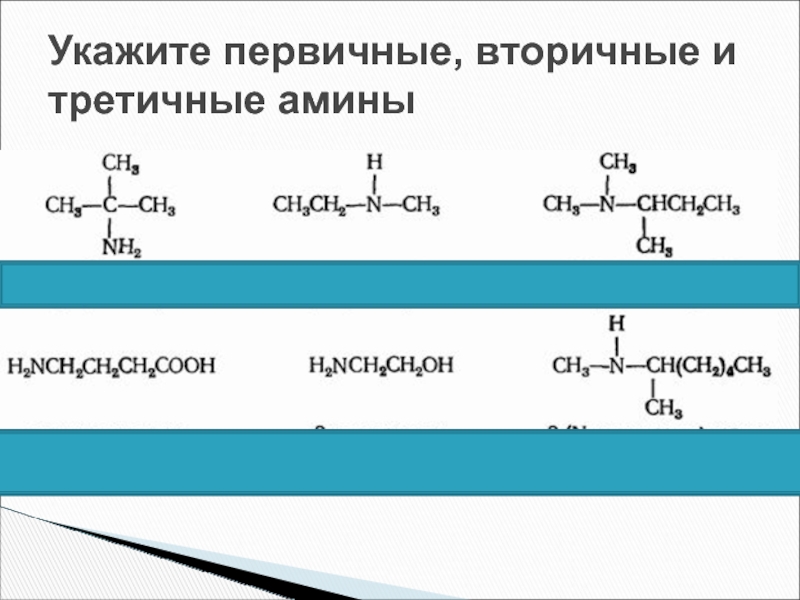
- 46. Укажите первичные, вторичные и третичные амины
Слайд 3 Амины – органические производные аммиака NH3, в молекуле которого один,
RNH2, R2NH, R3N
Простейший представитель – метиламин:
Слайд 7В большинстве случаев названия аминов образуют из названий углеводородных радикалов и
CH3-NH2 Метиламин
CH3-CH2-NH2 Этиламин
Различные радикалы перечисляются в алфавитном порядке:
CH3-CH2-NH-CH3 Метилэтиламин
Номенклатура аминов
Слайд 9При наличии одинаковых радикалов используют приставки ди и три:
Номенклатура аминов
(CH3)3N
(триметиламин)
Слайд 13Амины
Номенклатура и изомерия
1,3-Диаминобензол
(м-фенилендиамин)
1.4-Диаминобензол
(п-фенилендиамин)
Слайд 18 2. Пространственная изомерия - возможна оптическая изомерия, начиная с С4H9NH2:
Изомерия
Слайд 19 Связь N–H является полярной, поэтому первичные и вторичные амины образуют
Физические свойства аминов
Слайд 20 Это объясняет относительно высокую температуру кипения аминов по сравнению с
Физические свойства аминов
Слайд 21
Третичные амины не образуют ассоциирующих водородных связей (отсутствует группа N–H). Поэтому
а н-гексиламин – при 133 °С).
Физические свойства аминов
Слайд 22 При обычной температуре только низшие алифатические амины CH3NH2, (CH3)2NH и
средние гомологи – жидкости (с резким рыбным запахом),
высшие – твердые вещества без запаха.
Ароматические амины – бесцветные высококипящие жидкости или твердые вещества.
Физические свойства аминов
Слайд 29 3. В отличие от аммиака, низшие газообразные амины способны воспламеняться
Химические свойства аминов
Слайд 31 Анилин представляет собой бесцветную маслянистую жидкость с характерным запахом (т. кип.
Ядовит!
https://www.youtube.com/watch?v=2c6J-4sNGPc
Анилин
Слайд 32 Для анилина характерны реакции как по аминогруппе, так и по
С одной стороны, бензольное кольцо ослабляет основные свойства аминогруппы по сравнению алифатическими аминами и даже с аммиаком.
С другой стороны, под влиянием аминогруппы бензольное кольцо становится более активным в реакциях замещения, чем бензол.
Анилин
Слайд 33 Например, анилин энергично реагирует с бромной водой с образованием 2,4,6-триброманилина
Химические свойства анилина:
https://www.youtube.com/watch?v=d_pxNj5sd8g
Слайд 34 2. Взаимодействуя с кислотами, анилин образует соли:
https://www.youtube.com/watch?v=VNUTpSaWQ0Q
Химические свойства аминов
Хлорид фениламмония
Слайд 35 1. Наиболее общим методом получения первичных аминов является восстановление нитросоединений:
Получение аминов
Слайд 36 Важнейший ароматический амин - анилин - образуется при восстановлении нитробензола
Эта реакция носит имя русского химика Н.Н. Зинина, осуществившего ее впервые в 1842 г.
Получение аминов
Слайд 37
ЗИНИН
Николай Николаевич (25.VIII.1812–18.II.1880)
академик, возглавлял кафедру общей химии Медико-хирургической академии в
Слайд 38
C6H5NH2 + O2 --> CO2 + N2 + H2O
https://www.youtube.com/watch?v=cYtCWMczFFs
Реакция горения анилина
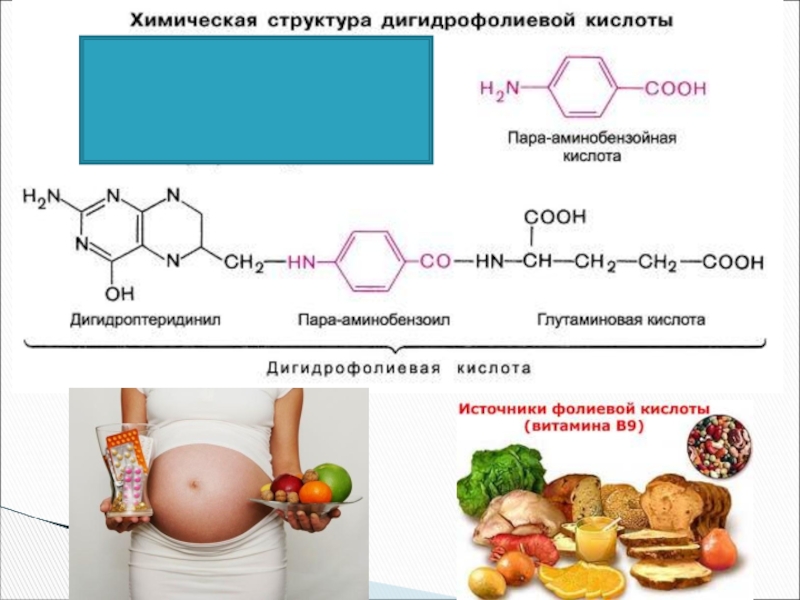
Слайд 40Широкое применение в качестве полупродукта в производстве витаминов и лекарственных средств
Применение анилина
Слайд 43
Пара-аминосалициловая кислота (ПАСК) была одним из первых синтетических препаратов, предложенным для специфического
Механизм действия пара-аминосалициловой кислоты на туберкулезные бактерии сходен с механизмом действия сульфаниламида на другие бактерии.