- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Алкіни (ацетиленові вуглеводні) презентация
Содержание
- 1. Алкіни (ацетиленові вуглеводні)
- 2. Відповідно до замісникової номенклатури (IUPAC) алкіни називають,
- 3. Промислові методи добування 1. Піроліз
- 4. 2. З кальцій карбіду (карбідний метод)
- 5. Лабораторні методи добування Відщеплення галогеноводню від
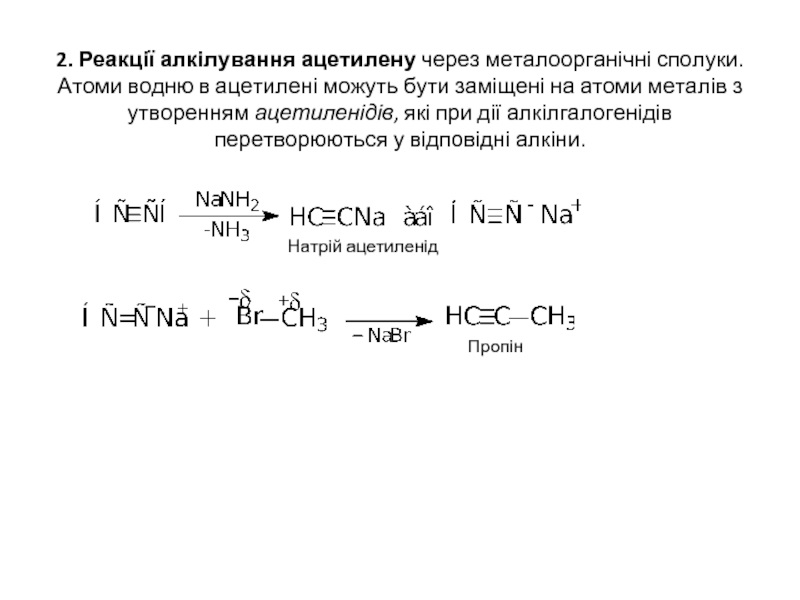
- 6. 2. Реакції алкілування ацетилену через металоорганічні сполуки.
- 7. ФІЗИЧНІ ВЛАСТИВОСТІ Алкіни С2-С4- це гази,
- 8. ХІМІЧНІ ВЛАСТИВОСТІ π-електронна густина отрійного зв’язку
- 9. В той же час, з боку атомів
- 10. Таким чином для алкінів характерні реакції
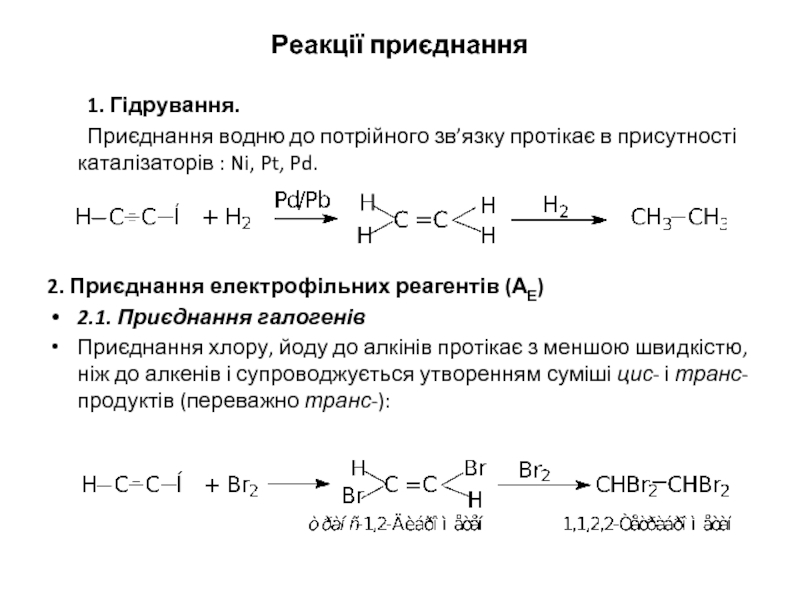
- 11. Реакції приєднання 1. Гідрування. Приєднання водню
- 12. 2.2. Приєднання галогеноводнів Електрофільне приєднання НСІ здійснюється
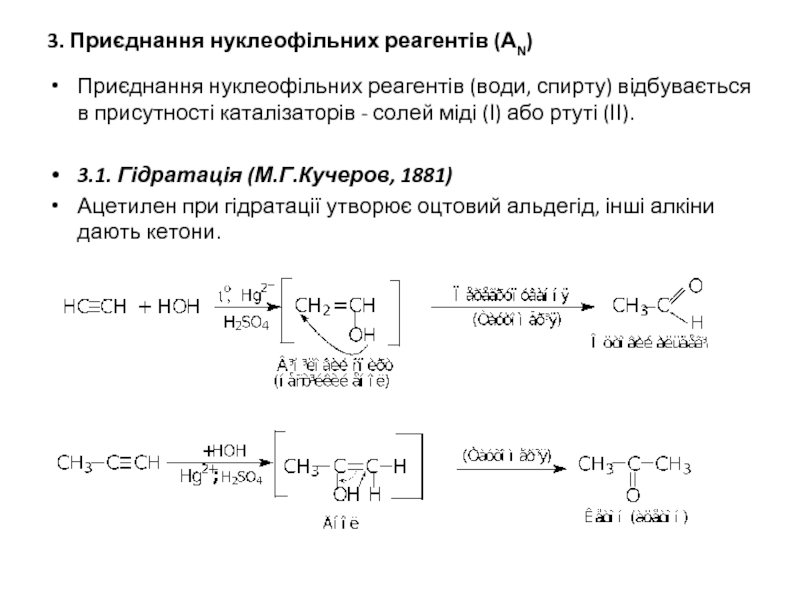
- 13. 3. Приєднання нуклеофільних реагентів (АN) Приєднання
- 14. Структура з НО-групою при подвійному зв’язку
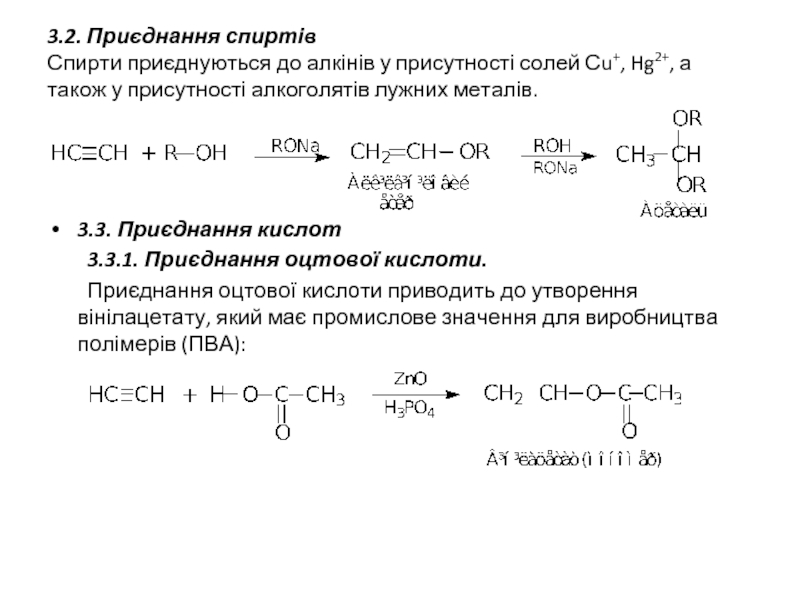
- 15. 3.2. Приєднання спиртів Спирти приєднуються до алкінів
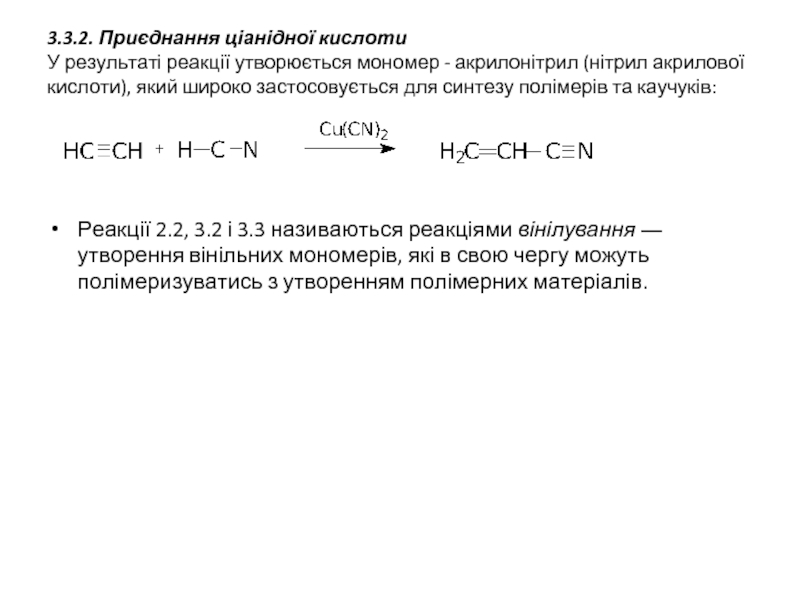
- 16. 3.3.2. Приєднання ціанідної кислоти У результаті реакції
- 17. 4. Карбонілування алкінів (В.Реппе, 1944-1949). Карбонілування –
- 18. 5. Приєднання альдегідів і кетонів Приєднання формальдегіду
- 19. Реакції полімеризації
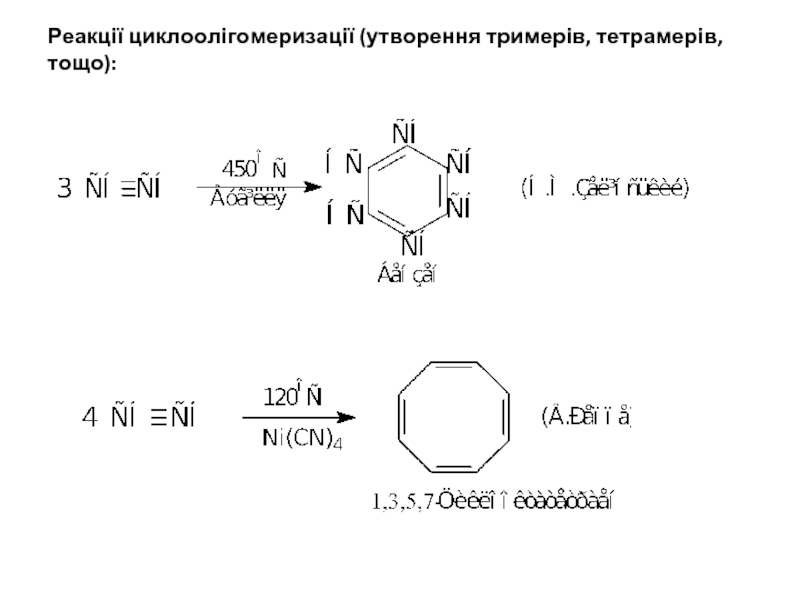
- 20. Реакції циклоолігомеризації (утворення тримерів, тетрамерів, тощо):
- 21. 3. Полімеризація У присутності ініціаторів або
- 22. Окиснення алкінів Сильні окиснювачі (КMnO4, K2Cr2O7 у
Слайд 1АЛКІНИ
Алкінами або ацетиленовими вуглеводнями називаються вуглеводні, які мають в молекулі один
Вони утворюють гомологічний ряд загальної формули СnН2n-2. Перший представник цього ряду – етин (ацетилен).
Слайд 2Відповідно до замісникової номенклатури (IUPAC) алкіни називають, змінюючи у відповідних алканах
Назви залишків алкінів утворюють додаванням суфікса –іл до назви вуглеводня:
У радикалів нумерація головного ланцюга починається з атома вуглецю, що має вільну валентність.
Слайд 3Промислові методи добування
1. Піроліз алканів (метану або нафтових фракцій)
При піролізі нафтових
Слайд 42. З кальцій карбіду (карбідний метод) При спіканні вапна з коксом при
При взаємодії з водою він легко гідролізує:
Карбід магнію (Мg2С3 )утворює пропін:
Слайд 5Лабораторні методи добування
Відщеплення галогеноводню від дигалогеналканів або галогеналкенів.
При підвищених температурах у
1,2-Дихлоретан Хлоретен Ацетилен
Слайд 62. Реакції алкілування ацетилену через металоорганічні сполуки. Атоми водню в ацетилені можуть
Натрій ацетиленід
Пропін
Слайд 7ФІЗИЧНІ ВЛАСТИВОСТІ
Алкіни С2-С4- це гази, починаючи з С5- і до С16-
Слайд 8ХІМІЧНІ ВЛАСТИВОСТІ
π-електронна густина отрійного зв’язку С≡С в ацетилені важче поляризується, ніж
Слайд 9В той же час, з боку атомів водню існує деякий дефіцит
В молекулі ацетилену зв’язок С-Н, утворений sp-гібридною орбіталлю атома С. Відомо, що електронегативність гібридної орбіталі зростає зі збільшенням у ній частки s-орбіталі: sp3 – 2,5; sp2 – 2,75; sp – 3,2 (за шкалою Л.Полінга).
Тому в цьому ж ряду зростає і полярніть зв’язку С⎯Н.
Це означає, що атоми вогдню в ацетилені протонізовані значно більше, ніж в етилені або в етані, про що свідчать значення констант іонізації цих сполук: рК(ацетилен) = 25; рК (етилен) = 44. Для порівняння рК (Н2О) = 15,7. Отже ацетилен проявляє кислотні властивості, хоча являється слабшою кислотою, ніж вода.
Слайд 10
Таким чином для алкінів характерні реакції приєднання (АЕ та АN), полімеризації,
Слайд 11Реакції приєднання
1. Гідрування.
Приєднання водню до потрійного зв’язку протікає в присутності каталізаторів
2. Приєднання електрофільних реагентів (АЕ)
2.1. Приєднання галогенів
Приєднання хлору, йоду до алкінів протікає з меншою швидкістю, ніж до алкенів і супроводжується утворенням суміші цис- і транс-продуктів (переважно транс-):
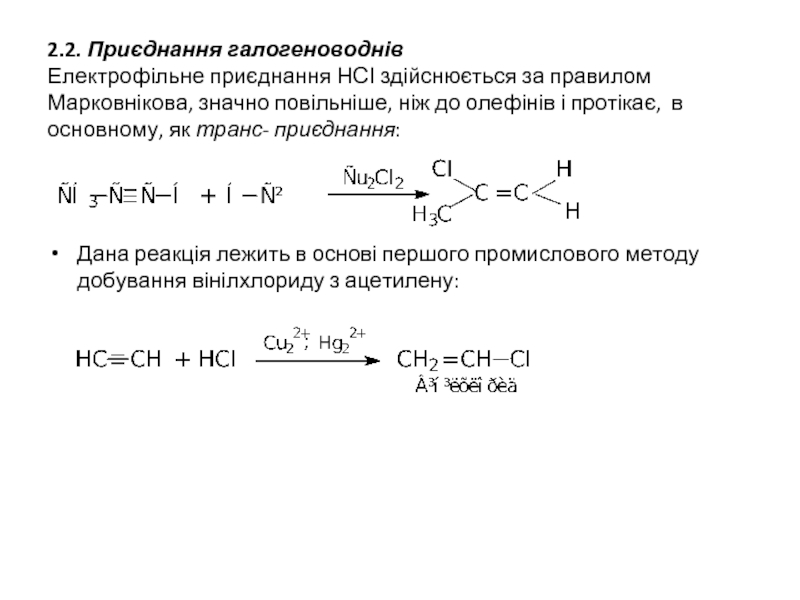
Слайд 122.2. Приєднання галогеноводнів Електрофільне приєднання НСІ здійснюється за правилом Марковнікова, значно повільніше,
Дана реакція лежить в основі першого промислового методу добування вінілхлориду з ацетилену:
Слайд 133. Приєднання нуклеофільних реагентів (АN)
Приєднання нуклеофільних реагентів (води, спирту) відбувається в
3.1. Гідратація (М.Г.Кучеров, 1881)
Ацетилен при гідратації утворює оцтовий альдегід, інші алкіни дають кетони.
Слайд 14 Структура з НО-групою при подвійному зв’язку називається енолом. Еноли, як правило,
Структурні ізомери, які можут легко переходити один в одного і існують у рівновазі називаються таутомерами, а така ізомерія - таутомерією. Даний різновид таутомерів називається кето-енольною таутомерією.
Слайд 153.2. Приєднання спиртів Спирти приєднуються до алкінів у присутності солей Сu+, Hg2+,
3.3. Приєднання кислот
3.3.1. Приєднання оцтової кислоти.
Приєднання оцтової кислоти приводить до утворення вінілацетату, який має промислове значення для виробництва полімерів (ПВА):
Слайд 163.3.2. Приєднання ціанідної кислоти У результаті реакції утворюється мономер - акрилонітрил (нітрил
Реакції 2.2, 3.2 і 3.3 називаються реакціями вінілування ― утворення вінільних мономерів, які в свою чергу можуть полімеризуватись з утворенням полімерних матеріалів.
Слайд 174. Карбонілування алкінів (В.Реппе, 1944-1949). Карбонілування – це введення карбонільної групи .
Якщо замість води взти спирт, то утворюється естер акрилової кислоти.
Такі естери є цінними мономерами для одержання прозорих пластиків.
Слайд 185. Приєднання альдегідів і кетонів Приєднання формальдегіду (Реппе) відбувається у присутності ацетиленіду
Приєднання ацетону протікає в присутності твердого КОН у середовищі абсолютного (повністю зневодненого ) етеру (реакція О.Фаворського):
Слайд 19
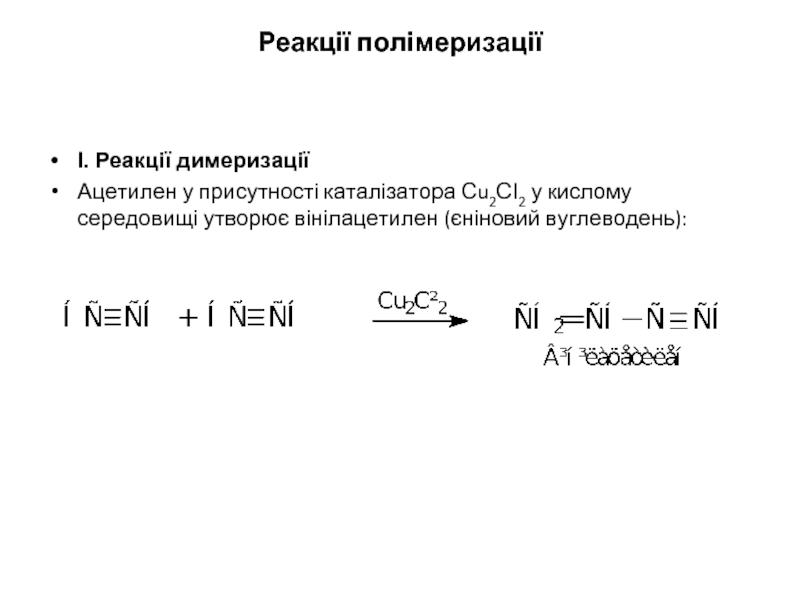
Реакції полімеризації
І. Реакції димеризації
Ацетилен у присутності каталізатора Сu2СІ2 у кислому середовищі
Слайд 213. Полімеризація
У присутності ініціаторів або металоорганічних каталізаторів утворюються спряжені полієни (від
Ацетилен полімеризується також у присутності солей Сu+ та окиснювача:
Вважають, що карбін є третьою алотропною видозміною вуглецю разом з алмазом та графітом. Причому, карбіну приписують ще і кумуленову будову макромолекули ...С=С=С=С=С...
Слайд 22Окиснення алкінів
Сильні окиснювачі (КMnO4, K2Cr2O7 у кислому середовищі, озон) окиснюють алкіни
Реакції заміщення
1. Реакції металування алкінів (заміщення водню на метали) - SE
Завдяки великій полярності зв’язку С—Н алкіни здатні реагувати з багатьма металами (заміщення «кислого» водню на метал) з утворенням ацетиленідів.