- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Алкены. Присоединение простых веществ презентация
Содержание
- 1. Алкены. Присоединение простых веществ
- 2. Реакции присоединения
- 3. Присоединение простых веществ Присоединение водорода – гидрирование,
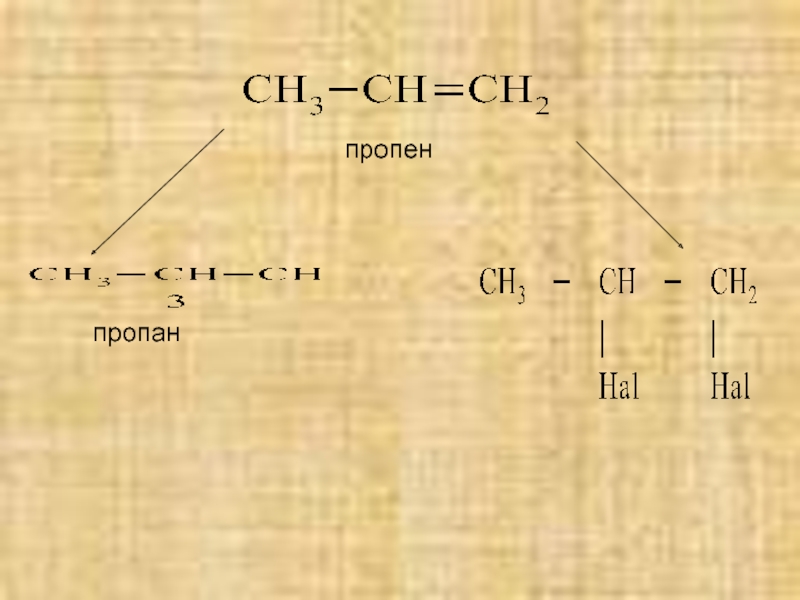
- 4. пропен пропан
- 5. Качественно реакцией на все непредельные углеводороды, в
- 6. Присоединение сложных веществ Присоединение галогеноводородов (+HHal) –
- 7. Присоединение веществ типа НХ (Х=Hal, OH и
- 8. Правило: В. В. Марковникова Атом водорода присоединяется
- 9. Реакции окисления
- 10. Реакция окисления В зависимости от условий непредельные углеводороды окисляются в различной степени.
- 11. Горение. Полное (избыток О2) Неполное (недостаток О2)
- 12. Неполное окисление под действием окислителей типа KMnO4,
- 13. Из KMnO4 1.2 – этандиол Раствор KMnO4
- 14. Реакции полимеризации
- 15. Реакции полимеризации. Процесс полимеризации алкенов открыт А
- 16. Способы получения алкенов. Дегидрирование алканов (- Н2)
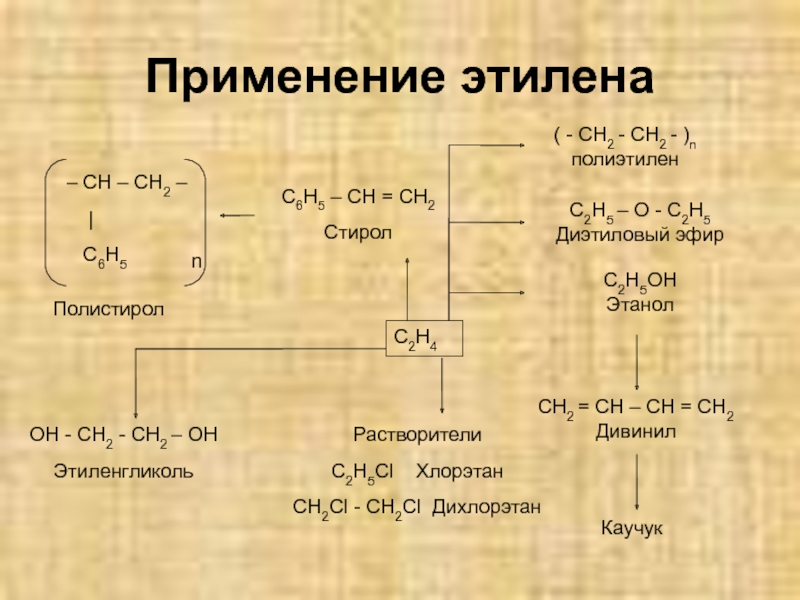
- 17. Применение этилена n
Слайд 3Присоединение простых веществ
Присоединение водорода – гидрирование, образуются алканы.
Присоединение галогенов (+F2, CL2,
Br2, I2) – галогенирование, образуются дигалогеналкины.
Слайд 5Качественно реакцией на все непредельные углеводороды, в том числе на алкены,
является реакция с бромной водой. Бромная вода при взаимодействии с алкенами обесцвечивается.
Слайд 6Присоединение сложных веществ
Присоединение галогеноводородов (+HHal) – гидрогалогенирование, образуются моногалогенфлканы (R-Hal).
Присоединение воды
(+H2O) – гидратация, образуются предельные одноатомные спирты (алканолы CnH2n+1OH).
Слайд 7Присоединение веществ типа НХ (Х=Hal, OH и так далее) к несимметричным
алкенам происходит по правилу: В. В. Марковникова:
Слайд 8Правило: В. В. Марковникова
Атом водорода присоединяется к атому углерода у кратной
связи, связанному с большим числом атомов водорода
Слайд 10Реакция окисления
В зависимости от условий непредельные углеводороды окисляются в различной степени.
Слайд 12Неполное окисление под действием окислителей типа KMnO4, K2Cr2O7.
Одной из наиболее характерных
реакций окисления является взаимодействие непредельных углеводородов (УВ) с раствором перманганата калия (KMnO4)
Слайд 13Из
KMnO4
1.2 – этандиол
Раствор KMnO4 обесцвечивается, происходит гидроксилирование алкенов (введение гидроксогруппы) с
образованием диолов (реакция Е. Е. Вагнера). Это качественная реакция на непредельных УВ, в том числе на алкены
Слайд 15Реакции полимеризации.
Процесс полимеризации алкенов открыт А М. Бутлеровым.
Полимеризацией называется процесс соединения
одинаковых молекул (мономеров), протекающий за счет разрыва кратных связей, с образованием высокомолекулярного соединения (полимера).
Слайд 16Способы получения алкенов.
Дегидрирование алканов (- Н2)
Гидрирование алкинов (+ Н2)
Дегидрирование спиртов (-
H2O)
Катализаторы: H2SO4, H3PO4, Al2O3, ZnCl2.
Катализаторы: H2SO4, H3PO4, Al2O3, ZnCl2.