- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Термодинамическая система презентация
Содержание
- 1. Термодинамическая система
- 2. Термодинамическая система Термодинамической системой называется совокупность макроскопических
- 3. Внутренняя энергия Внутренней энергией системы называется сумма
- 4. Работа в термодинамике Работой в термодинамике называется
- 5. V р V1 р1 1
- 6. Теплоотдача Теплоотдачей или теплообменом называется процесс обмена
- 7. Теплоемкость газов Теплоемкость газов зависит от характера
- 8. Теплоемкость жидкостей и твердых тел Жидкие
- 9. Следствия из первого начала термодинамики: 1) Изолированная
- 10. 4) Замкнутая система тел Замкнутой системой тел
- 11. Плавление / кристаллизация Плавлением называется переход
- 12. Теплоемкость при постоянном давлении При изобарном процессе:
- 13. Введем отношение теплопроводностей: При
- 14. Уравнение адиабатического процесса (Пуассона)
- 15. Политропа Зависимость
Слайд 1
Лекция 9
2. Молекулярная физика
2.3. Термодинамика
Равновесный процесс. Внутренняя энергия. Работа. Круговой процесс.
Слайд 2Термодинамическая система
Термодинамической системой называется совокупность макроскопических (состоящих из очень большого числа
Неравновесное состояние
Состояние, при котором хотя бы один из параметров системы не имеет определенного значения, называется неравновесным.
Равновесное состояние
Равновесное состояние – при котором все параметры системы имеют определенные значения, не изменяющиеся со временем.
Термодинамический процесс
Термодинамический процесс – переход системы из одного состояния в другое.
Равновесный процесс
Бесконечно медленный процесс состоит из последовательности равновесных состояний. Такой процесс можно считать равновесным (квазистатическим), так как параметры системы успевают выровняться по всей системе
Равновесные процессы обратимы!
Слайд 3Внутренняя энергия
Внутренней энергией системы называется сумма кинетических энергий хаотического движения всех
Внутренняя энергия идеального газа
Вся внутренняя энергия идеального газа представляет собой кинетическую энергию теплового движения (потенциальная энергия взаимодействия молекул для идеального газа равна нулю).
Внутренняя энергия одноатомного газа прямо пропорциональна его абсолютной температуре, массе газа, и обратно пропорциональна его молекулярному весу.
Круговой процесс (цикл)
Процесс, при котором система возвращается в исходное положение, называется круговым, или циклом.
Если система совершает круговой процесс (цикл), то
ее внутренняя энергия возвращается в исходное состояние.
Многоатомный газ:
Слайд 4Работа в термодинамике
Работой в термодинамике называется процесс обмена энергией между системой
если тела совершают работу над системой.
Изменение внутренней энергии
Изменение внутренней энергии системы в термодинамике может происходить двумя способами:
1) за счет передачи системе тепла от окружающих ее тел;
2) за счет совершения этими телами работы над системой.
Работа при расширении газа
Газ в сосуде с поршнем, расширившись и сдвинув
поршень, совершит работу:
Слайд 5
V
р
V1
р1
1
a
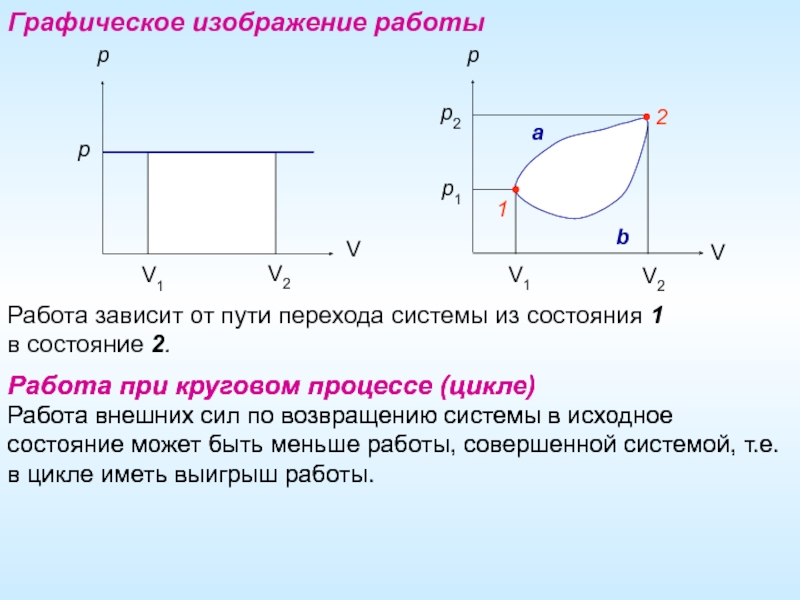
Графическое изображение работы
Работа зависит от пути перехода системы из состояния 1
V2
р
р2
2
V1
V2
b
р
V
Работа при круговом процессе (цикле)
Работа внешних сил по возвращению системы в исходное состояние может быть меньше работы, совершенной системой, т.е. в цикле иметь выигрыш работы.
Работа при круговом процессе (цикле)
Работа внешних сил по возвращению системы в исходное состояние может быть меньше работы, совершенной системой, т.е. в цикле иметь выигрыш работы.
Слайд 6Теплоотдача
Теплоотдачей или теплообменом называется процесс обмена энергией между системой и окружающими
Теплота
Энергия, отдаваемая или получаемая системой в процессе теплообмена, называется количеством тепла (теплотой).
если система получает тепло (нагревается), и
если система отдает тепло (охлаждается).
Калория
Калория — внесистемная единица тепла, численно равная количеству тепла, необходимого чтобы нагреть 1 г воды на 1 °С (от 19,5 °С до 20,5 °С). 1 кал = 4,18 Дж.
Теплоемкость
Теплоемкостью тела называют скалярную физическую величину, характеризующую связь между количеством сообщаемого системе тепла и изменением ее температуры.
Различают полную, удельную и молярную теплоемкость.
Слайд 7Теплоемкость газов
Теплоемкость газов зависит от характера процесса, при котором система получает
– теплоемкость при постоянном давлении
– теплоемкость при постоянном объеме
– теплоемкость при постоянной температуре
Полная теплоемкость
Полная теплоемкость тела численно равна количеству тепла, необходимого для повышения температуры тела на 1 градус.
Удельная теплоемкость
Удельная теплоемкость вещества численно равна количеству тепла, необходимого для повышения температуры единицы массы вещества на 1 градус.
Молярная теплоемкость
Молярная теплоемкость вещества численно равна количеству тепла, необходимого для повышения
температуры 1 моля вещества на 1 градус.
Слайд 8Теплоемкость жидкостей и твердых тел
Жидкие и твердые тела расширяются при
Первое начало термодинамики
Первым началом термодинамики называется закон сохранения энергии, распространенный на тепловые явления.
Изменение внутренней энергии системы при переходе ее из одного состояния в другое равно сумме работ внешних сил и количества теплоты, переданного системе.
(работа со знаком "–", потому что совершается над системой).
Или:
Количество теплоты, переданное системе, идет на изменение ее внутренней энергии и на совершение системой работы над внешними телами.
Слайд 9Следствия из первого начала термодинамики:
1) Изолированная система
Если система изолирована (теплота ей
2) Принцип эквивалентности тепла и работы
При круговом процессе система не может совершать работу без подвода тепла извне, или совершать работу большую, чем подводимое к ней тепло.
3) Вечный двигатель первого рода
Если тепло к системе не подводится, то работа может быть совершена только за счет убыли внутренней энергии.
Невозможен вечный двигатель первого рода, т.е. устройство, которое совершало бы работу без подвода энергии извне!
Первое начало термодинамики
Слайд 104) Замкнутая система тел
Замкнутой системой тел называется такая система, которая не
Внутренняя энергия замкнутой системы изменится не может!
Первое начало термодинамики
θ – температура, установившаяся после наступления теплового
равновесия.
Уравнение теплового баланса
Алгебраическая сумма количеств теплоты, отданных и полученных в замкнутой системе участвующими в теплообмене неподвижными телами, равна нулю.
Если никакой работы внутри системы не совершается (все тела неподвижны), то:
Слайд 11
Плавление / кристаллизация
Плавлением называется переход вещества из твердого в жидкое состояние.
Удельная теплота плавления / кристаллизации
Удельной теплотой плавления называется количество теплоты, необходимое для превращения при температуре плавления 1 кг кристаллического вещества в жидкость.
При кристаллизации жидкости такое же точно
количество теплоты выделяется.
Парообразование / конденсация
Парообразованием (испарением, кипением) называется переход вещества из жидкого состояния в газообразное. Обратный процесс называется конденсацией.
Удельная теплота парообразования / конденсации
Удельной теплотой парообразования называется количество теплоты, необходимое для превращения при постоянной температуре 1 кг жидкости в пар.
При конденсации пара такое же точно
количество теплоты выделяется.
Слайд 12Теплоемкость при постоянном давлении
При изобарном процессе:
Удельная теплота сгорания топлива
Удельной теплотой сгорания
Теплоемкость при постоянном объеме
При изохорном процессе:
Уравнение Майера
Универсальная газовая постоянная – физическая величина, численно равная работе расширения одного моля идеального газа в изобарном процессе при нагревании его на 1 градус.
Слайд 13
Введем отношение теплопроводностей:
При изохорном процессе:
Адиабатический процесс
Адиабатическим (адиабатным) называется процесс, при
При адиабатическом процессе газ совершает работу только за счет уменьшения своей внутренней энергии. К адиабатическим можно отнести все быстро протекающие процессы.
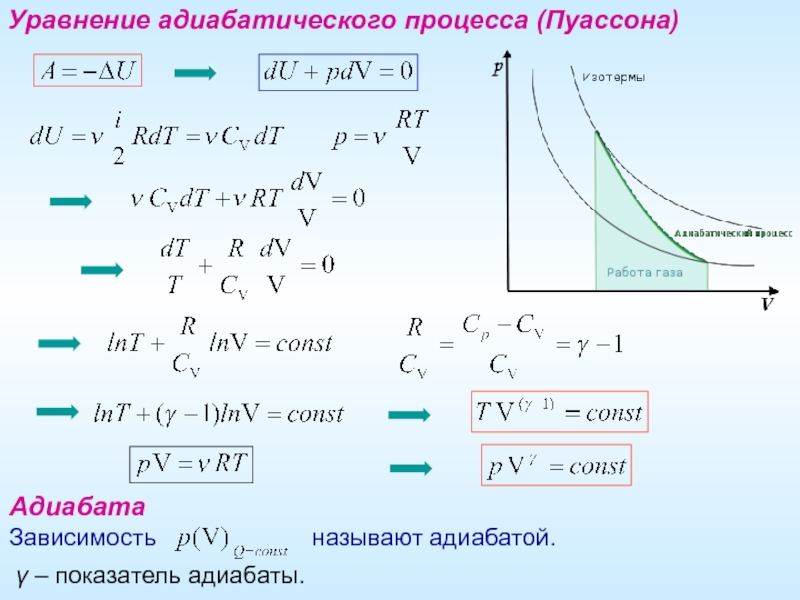
Слайд 14Уравнение адиабатического процесса (Пуассона)
Адиабата
Зависимость
γ – показатель адиабаты.
Слайд 15Политропа
Зависимость
n – показатель политропы.
Политропический процесс
Политропическими называются процессы, в ходе которых теплоемкость остается постоянной.